【人教版】化学九年级全一册 9.2.2 溶解度 习题课件
文档属性
| 名称 | 【人教版】化学九年级全一册 9.2.2 溶解度 习题课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 427.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-11 00:00:00 | ||
图片预览









文档简介
(共31张PPT)
课题2 溶 解 度
第2课时 溶解度
第九单元 溶 液
目录
学习目标
课堂导学
例题导学
课堂检测
化学用语天天练
请写出下列物质的化学式:
NaCl
NH4Cl
KNO3
NH4NO3
NaOH
Ca(OH)2
课程标准:1. 了解溶解度含义“四要素”;2. 初步学习绘制溶解度曲线和查阅溶解度曲线。
核心考点:利用溶解度曲线获得相关信息并进行数据分析和判断。
学习目标
课堂导学
【自主学习】阅读课本P35~36,了解固体的溶解度。
固体的溶解度
温度
1. 概念:在一定 下,某固态物质在________
溶剂里达到 状态时所溶解的 。(注:如果不指明溶剂,通常所说的溶解度是指物质在水里的溶解度)
100 g
饱和
质量
2. 四要素:(1)条件—— 。
(2)标准—— 。
(3)状态—— 。
(4)单位—— 。(定温、定量、定状态、定单位)
在一定温度下
在100 g溶剂里
达到饱和状态
克(g)
3. 影响因素
(1)内部因素:溶质、溶剂本身的性质。
(2)外部因素: 。(注:与溶剂量多少没有关系,因为概念已经规定在100 g溶剂里)
温度
4. 溶解度的相对大小(20 ℃)与溶解性的关系
溶解度/g <0. 01 0. 01~1 1~10 >10
一般称为
难溶
微溶
可溶
易溶
【自主学习】阅读课本P36~37,了解溶解度曲线及其应用。
溶解度曲线
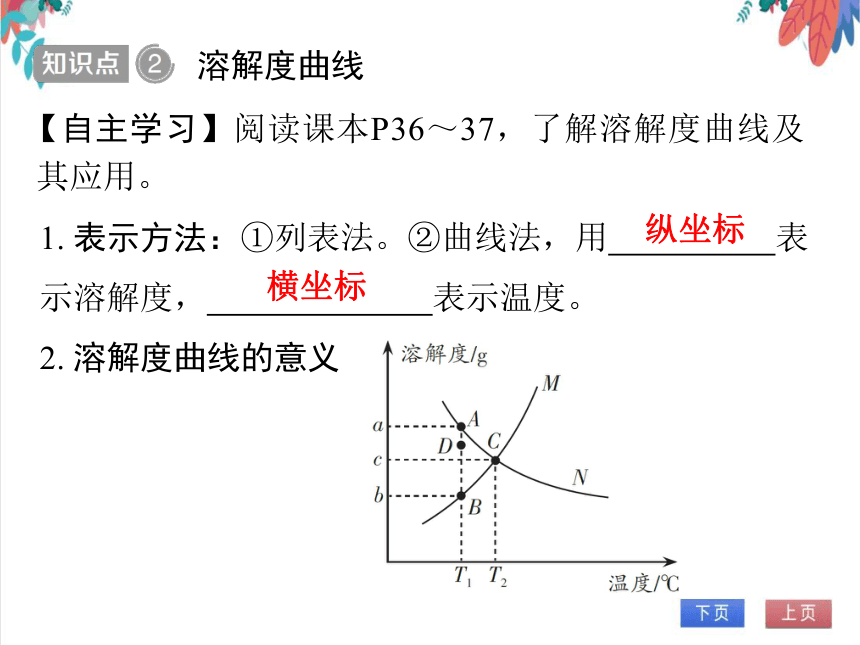
1. 表示方法:①列表法。②曲线法,用 表示溶解度, 表示温度。
2. 溶解度曲线的意义
纵坐标
横坐标
内容 表示意义
曲线 表示某物质在不同温度下的溶解度以及溶解度随温度变化的趋势
点 曲线上的点 表示某物质在对应温度下的溶解度
两曲线交点 表示两物质在该点对应温度下的溶解度相等
曲线下面的点 表示溶液是对应温度下该溶质的不饱和溶液
曲线上面的点 表示按此组成配制的溶液中溶质有剩余,得到的是对应温度下该溶质的饱和溶液
3. 溶解度曲线的变化规律
(1)多数固体的溶解度随温度的升高而 ,如 、 (填化学式,下同)。(陡升型)
(2)少数固体的溶解度受温度变化影响 ,如 。(缓升型)
(3)极少数固体的溶解度随温度的升高而 ,如 。(下降型)
增大
KNO3
NaNO3
很小
NaCl
减小
Ca(OH)2
【拓展延伸】结晶法提纯物质(适宜溶解度随温度变化趋势有差异的物质):①降温结晶法(蒸发浓缩→降温结晶→过滤),如提纯NaCl和KNO3混合溶液中的KNO3;②蒸发结晶法(蒸发结晶而不蒸干→趁热过滤),如提纯 NaCl和KNO3混合溶液中的NaCl。
4. 溶解度曲线的应用:
(1)可查出某物质在 时的溶解度。
(2)可以比较不同物质在 时溶解度的大小。(3)可以看出物质的溶解度随 变化的规律。
(4)可以比较不同物质的溶解度受 变化影响的大小。
不同温度
同一温度
温度
温度
气体的溶解度
【自主学习】阅读课本P38,了解气体的溶解度。
1. 概念:某气体的压强为 kPa和一定 时,在 体积水里溶解达到 状态时的气体 。
2. 影响因素
(1)内部因素:溶质、溶剂本身的性质。
(2)外部因素:①温度,随温度升高而 。②压强,随压强增大而 。
101
温度
1
饱和
体积
减小
增大
【拓展延伸】(1)标准状况通常是指温度为0 °C、压强为101 kPa。(2)打开汽水瓶盖会有气泡冒出,是因为汽水中溶有大量的二氧化碳,当打开瓶盖时,压强减小,二氧化碳的溶解度减小,因此大量的二氧化碳就会从水中逸出而冒出大量的气泡。(3)烧水时,刚开始会看到里面有许多小气泡不断上升,是因为溶解在水中的气体的溶解度随温度的升高而减小,因此会不断冒出气泡。
例题导学
【例1】 下列有关固体溶解度的说法正确的是( )
A. 在100 g水里溶解30 g硝酸钾刚好达到饱和状态,所以硝酸钾的溶解度是30 g
B. 20 ℃时,30 g硝酸钾能溶解在100 g水里,所以20 ℃时硝酸钾的溶解度是30 g
C. 20 ℃时,100 g硝酸钾饱和溶液里约有24 g硝酸钾,所以20 ℃时硝酸钾的溶解度为24 g
D. 20 ℃时,31. 6 g硝酸钾溶解在100 g水里恰好达到饱和状态,所以20 ℃时硝酸钾的溶解度是31.6 g
固体的溶解度
D
【点拨】解决本题要注意溶解度的四个要素:①条件:在一定温度下;②标准:在100 g溶剂里;③状态:达到饱和状态; ④单位:g。根据这四个要素进行解答。
【变式1】(2020·舟山)某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )
A. 变大 不变 B. 变大 变小
C. 不变 变大 D. 不变 不变
D
【例2】 (教材母题:九下人教版)甲、乙两种物质的溶解度曲线 如图所示。下列说法正确的是( )
A. a1 ℃时甲和乙的饱和溶液,升温到a2 ℃时仍是饱和溶液
B. 甲和乙的溶解度相等
C. a1 ℃时,甲和乙各30 g分别加入
100 g水中,均形成饱和溶液
D. a2 ℃时,在100 g水中加入60 g甲,
形成不饱和溶液
溶解度曲线
C
【点拨】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
【变式2】(教材母题:九下人教版)甲、乙、丙三种固体物质的溶解度曲线如图所示。回答下列问题:
甲>丙>乙
(1)a3℃时,三种物质的溶解度由大到小的顺序是 。
(2)a2℃时 和 的溶解度大小相等。
甲
丙
(3)三种物质中, 的溶解度受温度的影响最大,
的溶解度受温度的影响最小, 的溶解度随温度的升高而减小。
甲
乙
丙
【例3】 下列方法能增加气体物质的溶解度的是( )
A. 升高温度 B. 增加溶质
C. 减小压强 D. 加大压强
气体的溶解度
D
【点拨】利用气体的溶解度随温度的升高而减小,随着压强的增大而增大,结合事实进行分析解答。
【变式3】某汽水中含有二氧化碳、白砂糖、柠檬酸和水等多种物质,打开汽水瓶盖,有大量气泡逸出。下列说法正确的是( )
A. 白砂糖的溶解度减小
B. 二氧化碳的溶解度减小
C. 气泡逸出后的溶液为二氧化碳的不饱和溶液
D. 汽水溶液质量不变
B
课堂检测
1. 影响固体物质溶解度的操作是( )
A. 加热 B. 振荡
C. 搅拌 D. 加压
A
2. 下列关于溶解度说法正确的是( )
A. 硝酸钾的溶解度为222g/100g水
B. 溶解度随温度升高而升高
C. 难溶物质的溶解度为零
D. 溶解度可以定量的表示物质溶解性的大小
D
3. K2CO3、KNO3在不同温度时的溶解度及溶解度曲线如图。下列说法正确的是( )
温度/℃ 20 40 50 60 80
溶解度/g K2CO3 110 117 121 126 139
KNO3 31. 6 63. 9 85. 5 110 169
A. t2应在50 ℃~60 ℃之间
B. 乙代表K2CO3的溶解度曲线
C. K2CO3的溶解度大于KNO3
D. 将t2 ℃时甲、乙的饱和溶液降到t1 ℃,甲析出固体质量大
B
4. 不同温度时,NaCl固体的溶解度如表所示。20 ℃时,将50 g NaCl固体加入到盛有100 g水的烧杯中,充分溶解得到溶液。下列说法正确的是( )
A. 烧杯中溶液的质量为150 g
B. 烧杯中剩余固体的质量为14 g
C. 加入50 g水,搅拌后烧杯中仍有剩余固体
D. 升高温度能将烧杯中的饱和溶液变为不饱和溶液
温度/℃ 20 40 60 80 100
溶解度/g 36.0 36.6 37.3 38.4 39.8
B
5. 根据如图中的硝酸钾和氯化钠的溶解度曲线。回答下列问题:
(1)10 ℃时,将15 g硝酸钾加入到100 g水中,充分溶解后,得到硝酸钾的____________
(填“饱和”或“不饱和”)溶液。
(2)这两种物质中,溶解度受温度变
化影响较小的是 。
不饱和
氯化钠
(3)20 ℃时,将接近饱和的KNO3溶液转化为该温度下的KNO3饱和溶液,可使用的方法是________________
___________________________________(写一种即可)。
(4)提纯混有少量硝酸钾的氯化钠,采用的方法是
(填“蒸发结晶”或“降温结晶”)。
加溶质(或恒温蒸发溶剂)
蒸发结晶
谢谢!
课题2 溶 解 度
第2课时 溶解度
第九单元 溶 液
目录
学习目标
课堂导学
例题导学
课堂检测
化学用语天天练
请写出下列物质的化学式:
NaCl
NH4Cl
KNO3
NH4NO3
NaOH
Ca(OH)2
课程标准:1. 了解溶解度含义“四要素”;2. 初步学习绘制溶解度曲线和查阅溶解度曲线。
核心考点:利用溶解度曲线获得相关信息并进行数据分析和判断。
学习目标
课堂导学
【自主学习】阅读课本P35~36,了解固体的溶解度。
固体的溶解度
温度
1. 概念:在一定 下,某固态物质在________
溶剂里达到 状态时所溶解的 。(注:如果不指明溶剂,通常所说的溶解度是指物质在水里的溶解度)
100 g
饱和
质量
2. 四要素:(1)条件—— 。
(2)标准—— 。
(3)状态—— 。
(4)单位—— 。(定温、定量、定状态、定单位)
在一定温度下
在100 g溶剂里
达到饱和状态
克(g)
3. 影响因素
(1)内部因素:溶质、溶剂本身的性质。
(2)外部因素: 。(注:与溶剂量多少没有关系,因为概念已经规定在100 g溶剂里)
温度
4. 溶解度的相对大小(20 ℃)与溶解性的关系
溶解度/g <0. 01 0. 01~1 1~10 >10
一般称为
难溶
微溶
可溶
易溶
【自主学习】阅读课本P36~37,了解溶解度曲线及其应用。
溶解度曲线
1. 表示方法:①列表法。②曲线法,用 表示溶解度, 表示温度。
2. 溶解度曲线的意义
纵坐标
横坐标
内容 表示意义
曲线 表示某物质在不同温度下的溶解度以及溶解度随温度变化的趋势
点 曲线上的点 表示某物质在对应温度下的溶解度
两曲线交点 表示两物质在该点对应温度下的溶解度相等
曲线下面的点 表示溶液是对应温度下该溶质的不饱和溶液
曲线上面的点 表示按此组成配制的溶液中溶质有剩余,得到的是对应温度下该溶质的饱和溶液
3. 溶解度曲线的变化规律
(1)多数固体的溶解度随温度的升高而 ,如 、 (填化学式,下同)。(陡升型)
(2)少数固体的溶解度受温度变化影响 ,如 。(缓升型)
(3)极少数固体的溶解度随温度的升高而 ,如 。(下降型)
增大
KNO3
NaNO3
很小
NaCl
减小
Ca(OH)2
【拓展延伸】结晶法提纯物质(适宜溶解度随温度变化趋势有差异的物质):①降温结晶法(蒸发浓缩→降温结晶→过滤),如提纯NaCl和KNO3混合溶液中的KNO3;②蒸发结晶法(蒸发结晶而不蒸干→趁热过滤),如提纯 NaCl和KNO3混合溶液中的NaCl。
4. 溶解度曲线的应用:
(1)可查出某物质在 时的溶解度。
(2)可以比较不同物质在 时溶解度的大小。(3)可以看出物质的溶解度随 变化的规律。
(4)可以比较不同物质的溶解度受 变化影响的大小。
不同温度
同一温度
温度
温度
气体的溶解度
【自主学习】阅读课本P38,了解气体的溶解度。
1. 概念:某气体的压强为 kPa和一定 时,在 体积水里溶解达到 状态时的气体 。
2. 影响因素
(1)内部因素:溶质、溶剂本身的性质。
(2)外部因素:①温度,随温度升高而 。②压强,随压强增大而 。
101
温度
1
饱和
体积
减小
增大
【拓展延伸】(1)标准状况通常是指温度为0 °C、压强为101 kPa。(2)打开汽水瓶盖会有气泡冒出,是因为汽水中溶有大量的二氧化碳,当打开瓶盖时,压强减小,二氧化碳的溶解度减小,因此大量的二氧化碳就会从水中逸出而冒出大量的气泡。(3)烧水时,刚开始会看到里面有许多小气泡不断上升,是因为溶解在水中的气体的溶解度随温度的升高而减小,因此会不断冒出气泡。
例题导学
【例1】 下列有关固体溶解度的说法正确的是( )
A. 在100 g水里溶解30 g硝酸钾刚好达到饱和状态,所以硝酸钾的溶解度是30 g
B. 20 ℃时,30 g硝酸钾能溶解在100 g水里,所以20 ℃时硝酸钾的溶解度是30 g
C. 20 ℃时,100 g硝酸钾饱和溶液里约有24 g硝酸钾,所以20 ℃时硝酸钾的溶解度为24 g
D. 20 ℃时,31. 6 g硝酸钾溶解在100 g水里恰好达到饱和状态,所以20 ℃时硝酸钾的溶解度是31.6 g
固体的溶解度
D
【点拨】解决本题要注意溶解度的四个要素:①条件:在一定温度下;②标准:在100 g溶剂里;③状态:达到饱和状态; ④单位:g。根据这四个要素进行解答。
【变式1】(2020·舟山)某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )
A. 变大 不变 B. 变大 变小
C. 不变 变大 D. 不变 不变
D
【例2】 (教材母题:九下人教版)甲、乙两种物质的溶解度曲线 如图所示。下列说法正确的是( )
A. a1 ℃时甲和乙的饱和溶液,升温到a2 ℃时仍是饱和溶液
B. 甲和乙的溶解度相等
C. a1 ℃时,甲和乙各30 g分别加入
100 g水中,均形成饱和溶液
D. a2 ℃时,在100 g水中加入60 g甲,
形成不饱和溶液
溶解度曲线
C
【点拨】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
【变式2】(教材母题:九下人教版)甲、乙、丙三种固体物质的溶解度曲线如图所示。回答下列问题:
甲>丙>乙
(1)a3℃时,三种物质的溶解度由大到小的顺序是 。
(2)a2℃时 和 的溶解度大小相等。
甲
丙
(3)三种物质中, 的溶解度受温度的影响最大,
的溶解度受温度的影响最小, 的溶解度随温度的升高而减小。
甲
乙
丙
【例3】 下列方法能增加气体物质的溶解度的是( )
A. 升高温度 B. 增加溶质
C. 减小压强 D. 加大压强
气体的溶解度
D
【点拨】利用气体的溶解度随温度的升高而减小,随着压强的增大而增大,结合事实进行分析解答。
【变式3】某汽水中含有二氧化碳、白砂糖、柠檬酸和水等多种物质,打开汽水瓶盖,有大量气泡逸出。下列说法正确的是( )
A. 白砂糖的溶解度减小
B. 二氧化碳的溶解度减小
C. 气泡逸出后的溶液为二氧化碳的不饱和溶液
D. 汽水溶液质量不变
B
课堂检测
1. 影响固体物质溶解度的操作是( )
A. 加热 B. 振荡
C. 搅拌 D. 加压
A
2. 下列关于溶解度说法正确的是( )
A. 硝酸钾的溶解度为222g/100g水
B. 溶解度随温度升高而升高
C. 难溶物质的溶解度为零
D. 溶解度可以定量的表示物质溶解性的大小
D
3. K2CO3、KNO3在不同温度时的溶解度及溶解度曲线如图。下列说法正确的是( )
温度/℃ 20 40 50 60 80
溶解度/g K2CO3 110 117 121 126 139
KNO3 31. 6 63. 9 85. 5 110 169
A. t2应在50 ℃~60 ℃之间
B. 乙代表K2CO3的溶解度曲线
C. K2CO3的溶解度大于KNO3
D. 将t2 ℃时甲、乙的饱和溶液降到t1 ℃,甲析出固体质量大
B
4. 不同温度时,NaCl固体的溶解度如表所示。20 ℃时,将50 g NaCl固体加入到盛有100 g水的烧杯中,充分溶解得到溶液。下列说法正确的是( )
A. 烧杯中溶液的质量为150 g
B. 烧杯中剩余固体的质量为14 g
C. 加入50 g水,搅拌后烧杯中仍有剩余固体
D. 升高温度能将烧杯中的饱和溶液变为不饱和溶液
温度/℃ 20 40 60 80 100
溶解度/g 36.0 36.6 37.3 38.4 39.8
B
5. 根据如图中的硝酸钾和氯化钠的溶解度曲线。回答下列问题:
(1)10 ℃时,将15 g硝酸钾加入到100 g水中,充分溶解后,得到硝酸钾的____________
(填“饱和”或“不饱和”)溶液。
(2)这两种物质中,溶解度受温度变
化影响较小的是 。
不饱和
氯化钠
(3)20 ℃时,将接近饱和的KNO3溶液转化为该温度下的KNO3饱和溶液,可使用的方法是________________
___________________________________(写一种即可)。
(4)提纯混有少量硝酸钾的氯化钠,采用的方法是
(填“蒸发结晶”或“降温结晶”)。
加溶质(或恒温蒸发溶剂)
蒸发结晶
谢谢!
同课章节目录
