专题8金属和金属材料单元练习—2021-2022学年九年级化学仁爱版下册(word版有答案)
文档属性
| 名称 | 专题8金属和金属材料单元练习—2021-2022学年九年级化学仁爱版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 262.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-11 00:00:00 | ||
图片预览



文档简介
专题8金属和金属材料单元练习2021-2022学年九年级化学仁爱版下册
一、单选题
1.我国科学家研制出一种新型镁锂合金。该材料具有超轻等特性。下列说法正确的是
A.是一种新型化合物 B.合金中镁、锂原子不再运动
C.可以用于制造卫星、减轻卫星重量 D.该合金的熔点比镁高
2.下列环境中,铁钉表面最容易生锈的是( )
A.在稀盐酸中
B.在潮湿空气中
C.在干燥空气中
D.浸没在植物油中
3.下列通过丝绸之路传到国外的发明和技术中不涉及化学变化的是
A.使用火药 B.指南针用于航海
C.用泥土烧制陶瓷 D.治炼金属
4.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
5.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
6.5月15日,中国天问一号探测器成功着陆火星。火星上有峡谷山群、尘埃风暴,昼夜温差较大。安全着陆无需考虑的因素是
A.火星地形地貌 B.探测器金属硬度 C.火星岩石成分 D.探测器外壳熔点
7.进行下列对比实验,不需要控制变量的是
A.用红磷和白磷探究可燃物燃烧的条件
B.用铁钉探究钢铁生锈的条件
C.用足量稀盐酸区分氯化钾溶液和碳酸钾溶液
D.用镁、锌与稀硫酸反应,比较镁、锌的金属活动性强弱
8.向Cu(NO3)2、AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,再向滤渣中加入稀盐酸,发现没有气泡产生,则滤渣中一定含有的物质是
A.Fe、Cu B.Cu、Ag C.Cu D.Ag
9.如图是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )
A.丁中铁钉生锈最严重
B.丙中的铁钉不生锈
C.铁生锈的主要条件是与空气、水直接接触
D.甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊
10.将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混和溶液中,充分反应后过滤,得到滤液M和滤渣N,下列有关说法中,不合理的是
A.滤液M中一定存在Fe2+
B.滤渣N的质量一定小于加入铁粉的质量
C.滤渣N中一定没有单质镁
D.滤液M中至少含有两种金属阳离子
11.向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些铁粉,待完全反应后,再过滤。下列情况不可能存在的是
A.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Fe2+、Mg2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+
D.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+、Mg2+
二、简答题
12.请根据常见金属性质回答问题:
(1)将以下常见金属的活动顺序补充完整。
_______________________
(2)黄金首饰不易锈蚀的主要原因是 ______________________ 。
(3)从Mg、Zn、Cu、Fe中选出适当的物质与稀硫酸反应,写出反应的化学方程式 _____________ (写一个即可)。
(4)用CuSO4 配制农药波尔多液时不能在以下 _______ (填序号)中进行。
A.塑料桶 B.铁桶 C.木桶
13.学习化学知识的目的之一是分析和解决实际的问题。
(1)汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是_______。
(2)生石灰常用作食品干燥剂,用化学方程式表示其原因________。
(3)碳酸氢钠可用于治疗胃酸(主要成分是盐酸)过多,其原因是________(用化学方程式表示)。
(4)为减少煤燃烧产生的二氧化硫对大气的污染,可向煤中加入适量的石灰石,发生的反应为:2CaCO3+O2+2SO2 =2CaSO4+2CO2,该反应所涉及的物质中,属于氧化物的是_______。
(5)为维护食品安全,卫生部禁止在面粉中添加增白剂,如过氧化钙(CaO2)等。它和水反应能生成一种碱和氧气,反应的化学方程式是________。
14.高层建筑都采用铝合金门窗而不采用钢门钢窗,铁制的舰船外面需涂油漆而铝合金制的飞机却不用,解释两个事例的原因:①_________________;②______________________.
三、推断题
15.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
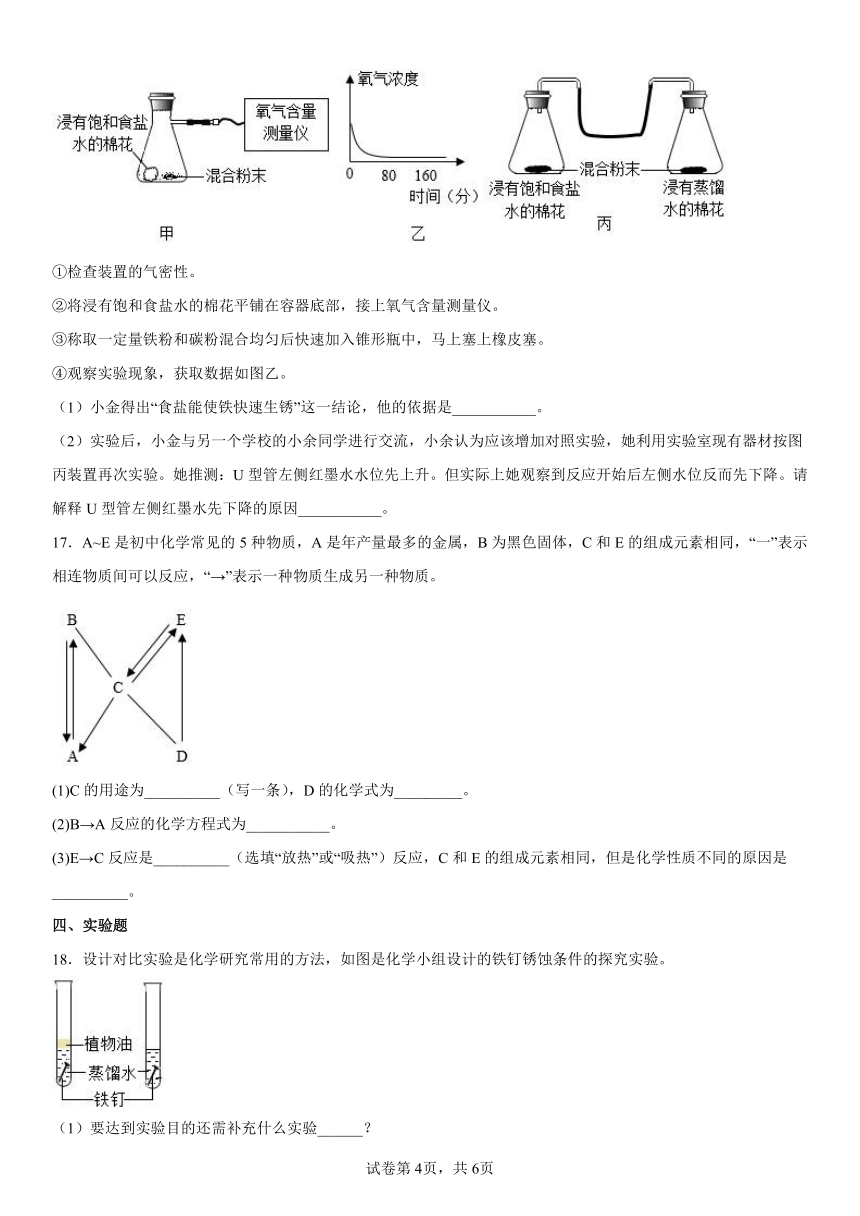
16.暖宝宝的主要成分是:铁粉、碳粉、水、食盐等,它的产热原理与铁生锈相同,但却能在短时间内产生大量的热。小金认为是食盐改变了反应的速度,为了验证自己的猜想,他按图甲装置进行如图实验。
①检查装置的气密性。
②将浸有饱和食盐水的棉花平铺在容器底部,接上氧气含量测量仪。
③称取一定量铁粉和碳粉混合均匀后快速加入锥形瓶中,马上塞上橡皮塞。
④观察实验现象,获取数据如图乙。
(1)小金得出“食盐能使铁快速生锈”这一结论,他的依据是___________。
(2)实验后,小金与另一个学校的小余同学进行交流,小余认为应该增加对照实验,她利用实验室现有器材按图丙装置再次实验。她推测:U型管左侧红墨水水位先上升。但实际上她观察到反应开始后左侧水位反而先下降。请解释U型管左侧红墨水先下降的原因___________。
17.A~E是初中化学常见的5种物质,A是年产量最多的金属,B为黑色固体,C和E的组成元素相同,“一”表示相连物质间可以反应,“→”表示一种物质生成另一种物质。
(1)C的用途为__________(写一条),D的化学式为_________。
(2)B→A反应的化学方程式为___________。
(3)E→C反应是__________(选填“放热”或“吸热”)反应,C和E的组成元素相同,但是化学性质不同的原因是__________。
四、实验题
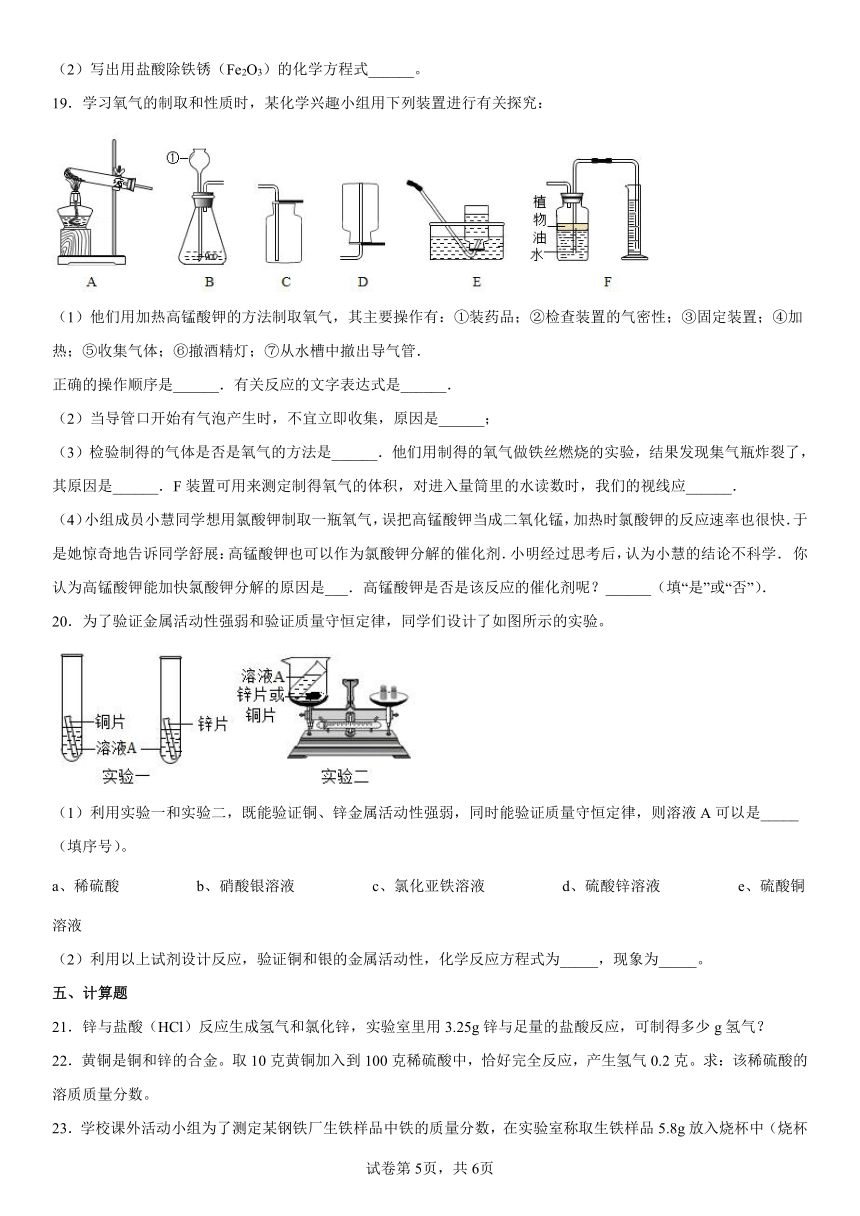
18.设计对比实验是化学研究常用的方法,如图是化学小组设计的铁钉锈蚀条件的探究实验。
(1)要达到实验目的还需补充什么实验______?
(2)写出用盐酸除铁锈(Fe2O3)的化学方程式______。
19.学习氧气的制取和性质时,某化学兴趣小组用下列装置进行有关探究:
(1)他们用加热高锰酸钾的方法制取氧气,其主要操作有:①装药品;②检查装置的气密性;③固定装置;④加热;⑤收集气体;⑥撤酒精灯;⑦从水槽中撤出导气管.
正确的操作顺序是______.有关反应的文字表达式是______.
(2)当导管口开始有气泡产生时,不宜立即收集,原因是______;
(3)检验制得的气体是否是氧气的方法是______.他们用制得的氧气做铁丝燃烧的实验,结果发现集气瓶炸裂了,其原因是______.F装置可用来测定制得氧气的体积,对进入量筒里的水读数时,我们的视线应______.
(4)小组成员小慧同学想用氯酸钾制取一瓶氧气,误把高锰酸钾当成二氧化锰,加热时氯酸钾的反应速率也很快.于是她惊奇地告诉同学舒展:高锰酸钾也可以作为氯酸钾分解的催化剂.小明经过思考后,认为小慧的结论不科学. 你认为高锰酸钾能加快氯酸钾分解的原因是___.高锰酸钾是否是该反应的催化剂呢?______(填“是”或“否”).
20.为了验证金属活动性强弱和验证质量守恒定律,同学们设计了如图所示的实验。
(1)利用实验一和实验二,既能验证铜、锌金属活动性强弱,同时能验证质量守恒定律,则溶液A可以是_____(填序号)。
a、稀硫酸 b、硝酸银溶液 c、氯化亚铁溶液 d、硫酸锌溶液 e、硫酸铜溶液
(2)利用以上试剂设计反应,验证铜和银的金属活动性,化学反应方程式为_____,现象为_____。
五、计算题
21.锌与盐酸(HCl)反应生成氢气和氯化锌,实验室里用3.25g锌与足量的盐酸反应,可制得多少g氢气?
22.黄铜是铜和锌的合金。取10克黄铜加入到100克稀硫酸中,恰好完全反应,产生氢气0.2克。求:该稀硫酸的溶质质量分数。
23.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室称取生铁样品5.8g放入烧杯中(烧杯的质量为30g).然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为85.6g(已知该反应中稀硫酸恰好完全反应,杂质不参与反应).请计算:
(1)产生氢气的质量是_____.
(2)该生铁样品中铁的质量分数?_____(精确到0.1%)
24.人类文明进步与金属材料发展关系十分密切。某课外兴趣小组探究金属的性质。
(1)用等质量相同表面积的镁条,等体积不同浓度的稀盐酸,在一定条件下反应,实验结果如图所示
对比a、b曲线,引起a曲线压强迅速增大的因素可能有______,______。
(2)将1g含镁48%的镁铝合金(不含其他元素)粉末在氧气中加热,至反应完全。
①该合金中镁消耗氧气的质量最多是多少 ______(写出计算过程)
②该合金与氧气反应后生成固体的质量最多是______(计算结果保留一位小数)。
试卷第1页,共3页
试卷第1页,共3页
学
参考答案:
1.C
2.B
3.B
4.B
5.D
6.C
7.C
8.D
9.A
10.B
11.A
12. Al Ag 黄金的金属活动性弱(或黄金的化学性质稳定;黄金不易跟氧气反应等) Zn+H2SO4=ZnSO4+H2↑(或Mg+H2SO4==MgSO4+H2↑;Fe+H2SO4=FeSO4+H2↑) B
13. 隔绝氧气和水 CaO + H2O=Ca(OH)2 NaHCO3 + HCl=NaCl + H2O + CO2↑ SO2 、CO2 2CaO2+ 2H2O=2Ca(OH)2+ O2↑
14. 铝的密度小而轻,钢的密度大而重 铁易生锈,需有一层保护膜,而铝表面有一层致密的氧化膜,可保护铝不再进一步氧化
15. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
16.在较短的时间内,氧气的含量迅速降低 铁粉在跟水、氧气的反应过程中,短时间内产生大量的热,使瓶内压强迅速增大
17.(1) 冶炼金属(作燃料) O2(合理即可)
(2)
(3) 吸热 它们的分子构成不同
18. 补充铁钉在干燥空气中不(或“是否”)生锈的实验 Fe2O3 + 6HCl ===2 FeCl 3+ 3H2O
19. ②①③④⑤⑦⑥ 高锰酸钾锰酸钾+二氧化锰+氧气 装置中有空气,会造成收集的氧气不纯 将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气 试管底部没有放入水或细沙 与量筒内凹液面的最低处保持平衡 高锰酸钾受热分解时生成了二氧化锰 否
20. c或e Cu+2AgNO3=Cu(NO3)2+2Ag 铜片表面有银白色固体析出,溶液由无色变为蓝色
21.解:设生成氢气质量为x
答:生成氢气质量为0.1g。
22.解:设参加反应的硫酸的质量为x
则稀硫酸的溶质质量分数为
答:稀硫酸的溶质质量分数为。
23. 0.2g 96.6%
24.(1)温度;盐酸的浓度
(2)解:①参加反应的镁的质量为1g×48%=0.48g
设该合金中镁消耗氧气的质量为x,生成的氧化镁的质量为y
48:32=0.48g:x x=0.32g
48:80=0.48g:y y=0.8g
②参加反应的铝的质量为1g 0.48g=0.52g
设生成的氧化铝的质量为z
108:204=0.52g:z z≈1.0g
则该合金与氧气反应后生成固体的质量最多是0.8g+1.0g=1.8g
答:①该合金中镁消耗氧气的质量最多是0.32g;
②该合金与氧气反应后生成固体的质量最多是1.8g。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.我国科学家研制出一种新型镁锂合金。该材料具有超轻等特性。下列说法正确的是
A.是一种新型化合物 B.合金中镁、锂原子不再运动
C.可以用于制造卫星、减轻卫星重量 D.该合金的熔点比镁高
2.下列环境中,铁钉表面最容易生锈的是( )
A.在稀盐酸中
B.在潮湿空气中
C.在干燥空气中
D.浸没在植物油中
3.下列通过丝绸之路传到国外的发明和技术中不涉及化学变化的是
A.使用火药 B.指南针用于航海
C.用泥土烧制陶瓷 D.治炼金属
4.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
5.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
6.5月15日,中国天问一号探测器成功着陆火星。火星上有峡谷山群、尘埃风暴,昼夜温差较大。安全着陆无需考虑的因素是
A.火星地形地貌 B.探测器金属硬度 C.火星岩石成分 D.探测器外壳熔点
7.进行下列对比实验,不需要控制变量的是
A.用红磷和白磷探究可燃物燃烧的条件
B.用铁钉探究钢铁生锈的条件
C.用足量稀盐酸区分氯化钾溶液和碳酸钾溶液
D.用镁、锌与稀硫酸反应,比较镁、锌的金属活动性强弱
8.向Cu(NO3)2、AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,再向滤渣中加入稀盐酸,发现没有气泡产生,则滤渣中一定含有的物质是
A.Fe、Cu B.Cu、Ag C.Cu D.Ag
9.如图是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )
A.丁中铁钉生锈最严重
B.丙中的铁钉不生锈
C.铁生锈的主要条件是与空气、水直接接触
D.甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊
10.将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混和溶液中,充分反应后过滤,得到滤液M和滤渣N,下列有关说法中,不合理的是
A.滤液M中一定存在Fe2+
B.滤渣N的质量一定小于加入铁粉的质量
C.滤渣N中一定没有单质镁
D.滤液M中至少含有两种金属阳离子
11.向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些铁粉,待完全反应后,再过滤。下列情况不可能存在的是
A.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Fe2+、Mg2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+
D.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+、Mg2+
二、简答题
12.请根据常见金属性质回答问题:
(1)将以下常见金属的活动顺序补充完整。
_______________________
(2)黄金首饰不易锈蚀的主要原因是 ______________________ 。
(3)从Mg、Zn、Cu、Fe中选出适当的物质与稀硫酸反应,写出反应的化学方程式 _____________ (写一个即可)。
(4)用CuSO4 配制农药波尔多液时不能在以下 _______ (填序号)中进行。
A.塑料桶 B.铁桶 C.木桶
13.学习化学知识的目的之一是分析和解决实际的问题。
(1)汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是_______。
(2)生石灰常用作食品干燥剂,用化学方程式表示其原因________。
(3)碳酸氢钠可用于治疗胃酸(主要成分是盐酸)过多,其原因是________(用化学方程式表示)。
(4)为减少煤燃烧产生的二氧化硫对大气的污染,可向煤中加入适量的石灰石,发生的反应为:2CaCO3+O2+2SO2 =2CaSO4+2CO2,该反应所涉及的物质中,属于氧化物的是_______。
(5)为维护食品安全,卫生部禁止在面粉中添加增白剂,如过氧化钙(CaO2)等。它和水反应能生成一种碱和氧气,反应的化学方程式是________。
14.高层建筑都采用铝合金门窗而不采用钢门钢窗,铁制的舰船外面需涂油漆而铝合金制的飞机却不用,解释两个事例的原因:①_________________;②______________________.
三、推断题
15.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
16.暖宝宝的主要成分是:铁粉、碳粉、水、食盐等,它的产热原理与铁生锈相同,但却能在短时间内产生大量的热。小金认为是食盐改变了反应的速度,为了验证自己的猜想,他按图甲装置进行如图实验。
①检查装置的气密性。
②将浸有饱和食盐水的棉花平铺在容器底部,接上氧气含量测量仪。
③称取一定量铁粉和碳粉混合均匀后快速加入锥形瓶中,马上塞上橡皮塞。
④观察实验现象,获取数据如图乙。
(1)小金得出“食盐能使铁快速生锈”这一结论,他的依据是___________。
(2)实验后,小金与另一个学校的小余同学进行交流,小余认为应该增加对照实验,她利用实验室现有器材按图丙装置再次实验。她推测:U型管左侧红墨水水位先上升。但实际上她观察到反应开始后左侧水位反而先下降。请解释U型管左侧红墨水先下降的原因___________。
17.A~E是初中化学常见的5种物质,A是年产量最多的金属,B为黑色固体,C和E的组成元素相同,“一”表示相连物质间可以反应,“→”表示一种物质生成另一种物质。
(1)C的用途为__________(写一条),D的化学式为_________。
(2)B→A反应的化学方程式为___________。
(3)E→C反应是__________(选填“放热”或“吸热”)反应,C和E的组成元素相同,但是化学性质不同的原因是__________。
四、实验题
18.设计对比实验是化学研究常用的方法,如图是化学小组设计的铁钉锈蚀条件的探究实验。
(1)要达到实验目的还需补充什么实验______?
(2)写出用盐酸除铁锈(Fe2O3)的化学方程式______。
19.学习氧气的制取和性质时,某化学兴趣小组用下列装置进行有关探究:
(1)他们用加热高锰酸钾的方法制取氧气,其主要操作有:①装药品;②检查装置的气密性;③固定装置;④加热;⑤收集气体;⑥撤酒精灯;⑦从水槽中撤出导气管.
正确的操作顺序是______.有关反应的文字表达式是______.
(2)当导管口开始有气泡产生时,不宜立即收集,原因是______;
(3)检验制得的气体是否是氧气的方法是______.他们用制得的氧气做铁丝燃烧的实验,结果发现集气瓶炸裂了,其原因是______.F装置可用来测定制得氧气的体积,对进入量筒里的水读数时,我们的视线应______.
(4)小组成员小慧同学想用氯酸钾制取一瓶氧气,误把高锰酸钾当成二氧化锰,加热时氯酸钾的反应速率也很快.于是她惊奇地告诉同学舒展:高锰酸钾也可以作为氯酸钾分解的催化剂.小明经过思考后,认为小慧的结论不科学. 你认为高锰酸钾能加快氯酸钾分解的原因是___.高锰酸钾是否是该反应的催化剂呢?______(填“是”或“否”).
20.为了验证金属活动性强弱和验证质量守恒定律,同学们设计了如图所示的实验。
(1)利用实验一和实验二,既能验证铜、锌金属活动性强弱,同时能验证质量守恒定律,则溶液A可以是_____(填序号)。
a、稀硫酸 b、硝酸银溶液 c、氯化亚铁溶液 d、硫酸锌溶液 e、硫酸铜溶液
(2)利用以上试剂设计反应,验证铜和银的金属活动性,化学反应方程式为_____,现象为_____。
五、计算题
21.锌与盐酸(HCl)反应生成氢气和氯化锌,实验室里用3.25g锌与足量的盐酸反应,可制得多少g氢气?
22.黄铜是铜和锌的合金。取10克黄铜加入到100克稀硫酸中,恰好完全反应,产生氢气0.2克。求:该稀硫酸的溶质质量分数。
23.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室称取生铁样品5.8g放入烧杯中(烧杯的质量为30g).然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为85.6g(已知该反应中稀硫酸恰好完全反应,杂质不参与反应).请计算:
(1)产生氢气的质量是_____.
(2)该生铁样品中铁的质量分数?_____(精确到0.1%)
24.人类文明进步与金属材料发展关系十分密切。某课外兴趣小组探究金属的性质。
(1)用等质量相同表面积的镁条,等体积不同浓度的稀盐酸,在一定条件下反应,实验结果如图所示
对比a、b曲线,引起a曲线压强迅速增大的因素可能有______,______。
(2)将1g含镁48%的镁铝合金(不含其他元素)粉末在氧气中加热,至反应完全。
①该合金中镁消耗氧气的质量最多是多少 ______(写出计算过程)
②该合金与氧气反应后生成固体的质量最多是______(计算结果保留一位小数)。
试卷第1页,共3页
试卷第1页,共3页
学
参考答案:
1.C
2.B
3.B
4.B
5.D
6.C
7.C
8.D
9.A
10.B
11.A
12. Al Ag 黄金的金属活动性弱(或黄金的化学性质稳定;黄金不易跟氧气反应等) Zn+H2SO4=ZnSO4+H2↑(或Mg+H2SO4==MgSO4+H2↑;Fe+H2SO4=FeSO4+H2↑) B
13. 隔绝氧气和水 CaO + H2O=Ca(OH)2 NaHCO3 + HCl=NaCl + H2O + CO2↑ SO2 、CO2 2CaO2+ 2H2O=2Ca(OH)2+ O2↑
14. 铝的密度小而轻,钢的密度大而重 铁易生锈,需有一层保护膜,而铝表面有一层致密的氧化膜,可保护铝不再进一步氧化
15. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
16.在较短的时间内,氧气的含量迅速降低 铁粉在跟水、氧气的反应过程中,短时间内产生大量的热,使瓶内压强迅速增大
17.(1) 冶炼金属(作燃料) O2(合理即可)
(2)
(3) 吸热 它们的分子构成不同
18. 补充铁钉在干燥空气中不(或“是否”)生锈的实验 Fe2O3 + 6HCl ===2 FeCl 3+ 3H2O
19. ②①③④⑤⑦⑥ 高锰酸钾锰酸钾+二氧化锰+氧气 装置中有空气,会造成收集的氧气不纯 将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气 试管底部没有放入水或细沙 与量筒内凹液面的最低处保持平衡 高锰酸钾受热分解时生成了二氧化锰 否
20. c或e Cu+2AgNO3=Cu(NO3)2+2Ag 铜片表面有银白色固体析出,溶液由无色变为蓝色
21.解:设生成氢气质量为x
答:生成氢气质量为0.1g。
22.解:设参加反应的硫酸的质量为x
则稀硫酸的溶质质量分数为
答:稀硫酸的溶质质量分数为。
23. 0.2g 96.6%
24.(1)温度;盐酸的浓度
(2)解:①参加反应的镁的质量为1g×48%=0.48g
设该合金中镁消耗氧气的质量为x,生成的氧化镁的质量为y
48:32=0.48g:x x=0.32g
48:80=0.48g:y y=0.8g
②参加反应的铝的质量为1g 0.48g=0.52g
设生成的氧化铝的质量为z
108:204=0.52g:z z≈1.0g
则该合金与氧气反应后生成固体的质量最多是0.8g+1.0g=1.8g
答:①该合金中镁消耗氧气的质量最多是0.32g;
②该合金与氧气反应后生成固体的质量最多是1.8g。
答案第1页,共2页
答案第1页,共2页
