第6章常用的金属和盐练习题—2021-2022学年九年级化学沪教版(上海)下册(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐练习题—2021-2022学年九年级化学沪教版(上海)下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 223.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-11 00:00:00 | ||
图片预览


文档简介
第6章常用的金属和盐练习题2021-2022学年九年级化学沪教版(上海)
一、单选题
1.小明用托盘天平称量6.5g白糖(1g以下的使用游码),称量完毕后发现砝码和白糖放反了,则小明称量的白糖实际是( )
A.6.5g B.6g C.5.5g D.0.5g
2.下列说法不正确的是( )
A.为减少“白色污染”,提倡自带购物布袋
B.煤、石油、天然气属于化石燃料,取之不尽,用之不竭
C.对铁制品进行防锈处理,可以有效减少金属资源的浪费
D.开发新能源汽车可减少汽油、柴油的使用,从而减少环境污染
3.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
4.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
5.下列化肥分别与熟石灰混合研磨后。能闻到刺激性气味的是
A.NH4Cl B.KNO3 C.NaNO3 D.Ca3(PO4)2
6.下列关于金属材料的说法中正确的是( )
A.铝制品表面应常用钢刷擦洗
B.可用铁桶盛装农药波尔多液
C.焊锡(锡铅合金)的熔点低,常用来焊接金属
D.钢因为比生铁的含碳量高,所以应用范围更广
7.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
8.物质的性质与用途密切相关。 下列做法不合理的是
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
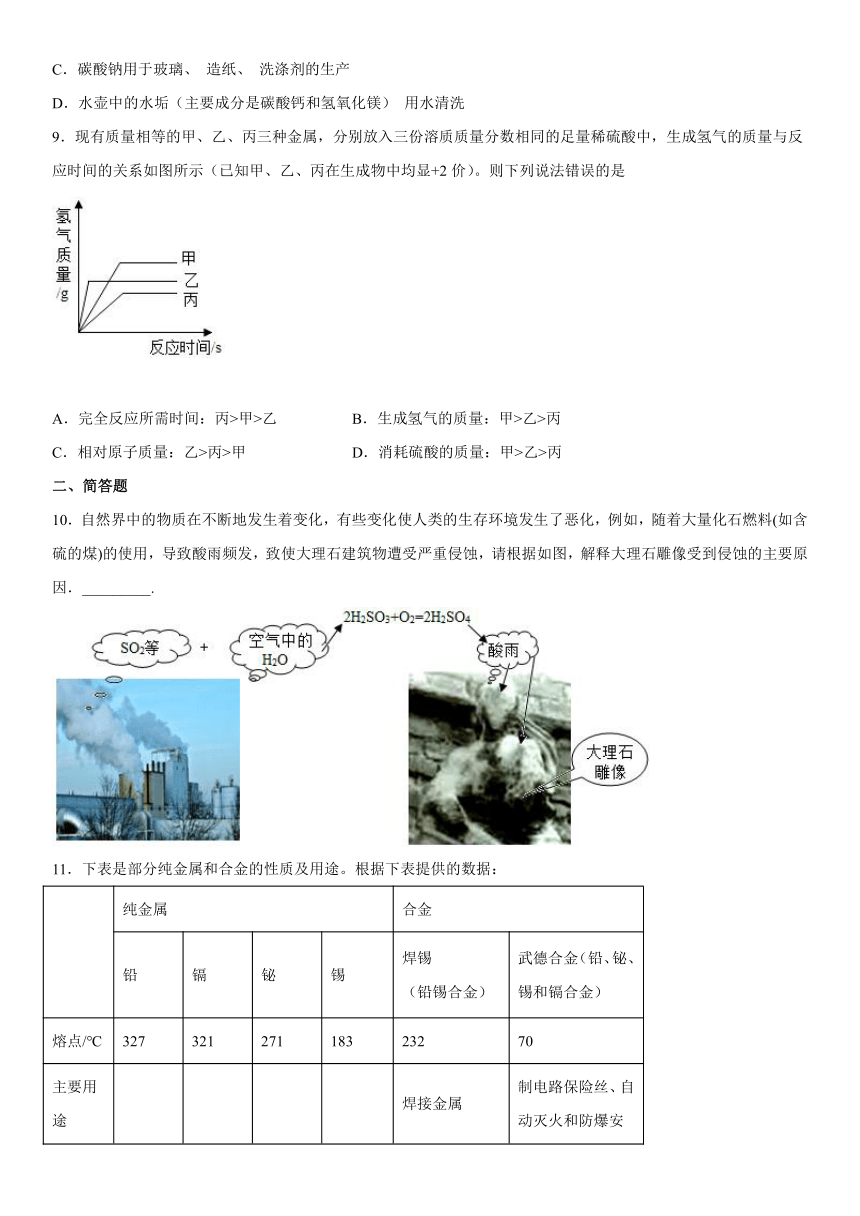
9.现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是
A.完全反应所需时间:丙>甲>乙 B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲 D.消耗硫酸的质量:甲>乙>丙
二、简答题
10.自然界中的物质在不断地发生着变化,有些变化使人类的生存环境发生了恶化,例如,随着大量化石燃料(如含硫的煤)的使用,导致酸雨频发,致使大理石建筑物遭受严重侵蚀,请根据如图,解释大理石雕像受到侵蚀的主要原因._________.
11.下表是部分纯金属和合金的性质及用途。根据下表提供的数据:
纯金属 合金
铅 镉 铋 锡 焊锡 (铅锡合金) 武德合金(铅、铋、锡和镉合金)
熔点/℃ 327 321 271 183 232 70
主要用途 焊接金属 制电路保险丝、自动灭火和防爆安全装置等
你能得到的启示是_________;生活中,王明家里的保险丝坏了,家里没有保险丝了,他找来铅丝代替保险丝。这种做法______(填“正确”或“不正确”)。
12.农民在大棚里种植蔬菜,为获得高产要开“碳吧”,实际上是向大棚内补充二氧化碳.具体操作是把稀硫酸放在塑料桶内息挂在高处,每天向桶内加适量的碳酸氢铵,则碳酸氢铵与硫酸反应生成硫酸铵、水和二氧化碳.
(1)请写出该反应的化学方程式:______.
(2)用塑料桶做反应容器,而不用铁桶,是因为______.
(3)把塑料桶悬挂在高处是因为______.
(4)反应生成的硫酸铵在农村可用做______.
三、推断题
13.向Fe(NO3)2和AgNO3的混合溶液中,加入一定量镁粉和锌粉的混合物,充分反应后过滤,滤液为浅绿色。
(1)写出一个一定发生的反应的化学方程式。
(2)请分析滤液中溶质的成分。
14.某同学以盖房子的方式总结出了如下物质间的关系,A、B、C均为初中常见的物质,且上下相邻的物质间均可发生反应。
(1)己知B是空气中含量较多且性质活泼的气体。
①若C与B反应时只有水生成,C物质的化学式为____________;
②若A是金属单质,与B反应的现象为紫红色固体逐渐变成黑色,则A物质是_______。
(2)己知B是一种产生温室效应的主要气体。
①若A是水,往A与B反应后的溶液滴加紫色石蕊试液,溶液变_______色。
②C物质常用来检验是否存在B物质,写出有关化学方程式___________。
15.推理和判断是学习化学的重要方法。
A、B、C为初中化学常见的三种物质,它们之间的转化关系如图所示(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物的反应条件已略去)请回答下列问题:
(1)若A、B、C均含有同一种元素,B、C组成元素相同,C的固体俗称“干冰”,则B的化学式是______________。
(2)若A、B、C是含相同金属元素的化合物,B、C的水溶液为蓝色,三种物质相互间发生的反应均为复分解反应,则A的化学式可能是____________(合理即可得分)。
(3)若A、B、C均为碱,其中B易溶于水,C难溶于水,写出一个由B转化为C的化学方程式_____________(合理即可得分)。
16.A~G表示初中化学常见物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,A和G均为红色,它们之间的转化关系如图所示(反应条件,部分反应物及生成物已略去),请回答下列问题:
(1)A的化学式为____________;
(2)B的一种用途是____________;
(3)反应③的化学方程式为:_________________;
(4)E、F、G三种金属的活动性由强到弱的顺序为_______________。(用元素符号表示)
四、实验题
17.化学兴趣小组的同学把铁钉和铁粉放在潮湿的环境中一段时间后,发现银白色的铁钉表面出现了一层黄色的物质。小组同学经查阅资料得知是铁锈。
(1)铁锈的主要成分是氧化铁___________(写化学式),铁锈属于___________(填“纯净物”或“混合物”)。在此过程中,铁粉温度明显升高,___________能变成___________能。
(2)小明将生锈的铁钉放入稀盐酸中。表面的铁锈很快消失,反应生成氯化铁和水,溶液变成黄色。铁离子___________(写出符号)使溶液显黄色。铁钉放在黄色的溶液中一段时间后溶液又变成了浅绿色:氯化铁和铁反应生成了氯化亚铁,该反应的符号表达式___________。基本反应类型是___________。
(3)小芳发现:等质量的铁钉和铁粉放入相同的稀盐酸中,都有气泡产生,但铁粉与稀盐酸产生气泡的速率明显更快,由此现象可得出反应速率与___________有关。
(4)铁元素是人体必须的___________(填“微量”或“常量”)元素。如果缺少铁元素,会导致___________。
18.化学是一门以实验为基础的科学,请结合图示回答问题:
(1)图中①仪器的名称是___________。
(2)实验室用高锰酸钾制取并收集较纯净的氧气,反应的化学方程式为___________,选择的装置组合是___________(填字母序号)。
(3)若用B装置制取氢气,分液漏斗代替长颈漏斗,优点是___________,若用D装置收集氢气,气体应该从___________进入(填“a”或“b”)。
19.现有一包固体粉末,可能含有Ba(OH)2、K2CO3、Na2SO4、MgCl2中的一种或几种,为确定其组成,进行如下实验:
步骤I:取少量样品于烧杯中,加入足量的水,充分搅拌,过滤得白色沉淀A和无色滤液B
步骤II:取步骤I所得白色沉淀A于试管中,加入足量稀盐酸,固体部分溶解且有气泡产生。
步骤III取步骤I所得无色滤液B于试管中,滴入少量Ba(OH)2溶液,无明显现象。
(1)白色沉淀A中一定存在的物质有________(填化学式);
(2)通过上述实验,可得到的实验结论是_______
(3)若只需一种试剂就能够进一步确定样品的组成,还需进行的实验操作是______
五、计算题
20.实验室用金属锌和稀硫酸制备氢气,若需要制备4.4g氢气,至少需要金属锌多少克?
21.现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合液过滤后得到溶液的质量为140g。(反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl)
(1)生成沉淀的质量是_______g。
(2)求碳酸钠溶液中溶质的质量分数是多少______?
22.我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为: 。
(1)求Fe2O3中铁元素的质量分数。
(2)根据化学方程式计算:用含Fe2O360%的赤铁矿石800 t,理论上可炼出纯铁多少吨?
试卷第1页,共3页
参考答案:
1.C
2.B
3.A
4.C
5.A
6.C
7.B
8.D
9.C
10.大理石的主要成分是碳酸钙,碳酸钙能和酸雨中的酸性物质反应,侵蚀大理石
11. 合金的熔点比其成分金属低 不正确
12. 稀硫酸能与铁反应而将铁桶腐蚀 二氧化碳密度比空气大,悬挂在高处有利于二氧化碳与蔬菜叶面充分接触 化肥(或氮肥)
13.(1)Mg + 2AgNO3=Mg(NO3)2+2Ag
(2)一定有硝酸镁、硝酸锌、硝酸亚铁,可能有硝酸银
14.(1) H2 Cu 铜
(2) 红
15. CO CuO或Cu(OH)2(合理均可)
16. Fe2O3 冶炼金属 Fe+CuSO4=FeSO4+Cu 铁>铜>银
17.(1) Fe2O3 混合物 化学 热
(2) Fe3+ 2FeCl3+Fe= 3FeCl2
化合反应
(3)反应物的接触面积
(4) 微量 贫血 缺铁性贫血
18. 锥形瓶 AE 控制反应速率 b
19. BaCO3、BaSO4 固体粉末一定含有Ba(OH)2、Na2SO4、K2CO3,可能含有MgCl2 向步骤Ⅱ的上层清液滴加足量的氢氧化钠溶液
20.143g
21.(1)10;(2)10.6%
22.(1)
(2)解:800 t矿石中Fe2O3的质量为800 t×60%=480 t
设理论上可炼出纯铁的质量为x
答:理论上可炼出纯铁336 t。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.小明用托盘天平称量6.5g白糖(1g以下的使用游码),称量完毕后发现砝码和白糖放反了,则小明称量的白糖实际是( )
A.6.5g B.6g C.5.5g D.0.5g
2.下列说法不正确的是( )
A.为减少“白色污染”,提倡自带购物布袋
B.煤、石油、天然气属于化石燃料,取之不尽,用之不竭
C.对铁制品进行防锈处理,可以有效减少金属资源的浪费
D.开发新能源汽车可减少汽油、柴油的使用,从而减少环境污染
3.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
4.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
5.下列化肥分别与熟石灰混合研磨后。能闻到刺激性气味的是
A.NH4Cl B.KNO3 C.NaNO3 D.Ca3(PO4)2
6.下列关于金属材料的说法中正确的是( )
A.铝制品表面应常用钢刷擦洗
B.可用铁桶盛装农药波尔多液
C.焊锡(锡铅合金)的熔点低,常用来焊接金属
D.钢因为比生铁的含碳量高,所以应用范围更广
7.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
8.物质的性质与用途密切相关。 下列做法不合理的是
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
9.现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是
A.完全反应所需时间:丙>甲>乙 B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲 D.消耗硫酸的质量:甲>乙>丙
二、简答题
10.自然界中的物质在不断地发生着变化,有些变化使人类的生存环境发生了恶化,例如,随着大量化石燃料(如含硫的煤)的使用,导致酸雨频发,致使大理石建筑物遭受严重侵蚀,请根据如图,解释大理石雕像受到侵蚀的主要原因._________.
11.下表是部分纯金属和合金的性质及用途。根据下表提供的数据:
纯金属 合金
铅 镉 铋 锡 焊锡 (铅锡合金) 武德合金(铅、铋、锡和镉合金)
熔点/℃ 327 321 271 183 232 70
主要用途 焊接金属 制电路保险丝、自动灭火和防爆安全装置等
你能得到的启示是_________;生活中,王明家里的保险丝坏了,家里没有保险丝了,他找来铅丝代替保险丝。这种做法______(填“正确”或“不正确”)。
12.农民在大棚里种植蔬菜,为获得高产要开“碳吧”,实际上是向大棚内补充二氧化碳.具体操作是把稀硫酸放在塑料桶内息挂在高处,每天向桶内加适量的碳酸氢铵,则碳酸氢铵与硫酸反应生成硫酸铵、水和二氧化碳.
(1)请写出该反应的化学方程式:______.
(2)用塑料桶做反应容器,而不用铁桶,是因为______.
(3)把塑料桶悬挂在高处是因为______.
(4)反应生成的硫酸铵在农村可用做______.
三、推断题
13.向Fe(NO3)2和AgNO3的混合溶液中,加入一定量镁粉和锌粉的混合物,充分反应后过滤,滤液为浅绿色。
(1)写出一个一定发生的反应的化学方程式。
(2)请分析滤液中溶质的成分。
14.某同学以盖房子的方式总结出了如下物质间的关系,A、B、C均为初中常见的物质,且上下相邻的物质间均可发生反应。
(1)己知B是空气中含量较多且性质活泼的气体。
①若C与B反应时只有水生成,C物质的化学式为____________;
②若A是金属单质,与B反应的现象为紫红色固体逐渐变成黑色,则A物质是_______。
(2)己知B是一种产生温室效应的主要气体。
①若A是水,往A与B反应后的溶液滴加紫色石蕊试液,溶液变_______色。
②C物质常用来检验是否存在B物质,写出有关化学方程式___________。
15.推理和判断是学习化学的重要方法。
A、B、C为初中化学常见的三种物质,它们之间的转化关系如图所示(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物的反应条件已略去)请回答下列问题:
(1)若A、B、C均含有同一种元素,B、C组成元素相同,C的固体俗称“干冰”,则B的化学式是______________。
(2)若A、B、C是含相同金属元素的化合物,B、C的水溶液为蓝色,三种物质相互间发生的反应均为复分解反应,则A的化学式可能是____________(合理即可得分)。
(3)若A、B、C均为碱,其中B易溶于水,C难溶于水,写出一个由B转化为C的化学方程式_____________(合理即可得分)。
16.A~G表示初中化学常见物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,A和G均为红色,它们之间的转化关系如图所示(反应条件,部分反应物及生成物已略去),请回答下列问题:
(1)A的化学式为____________;
(2)B的一种用途是____________;
(3)反应③的化学方程式为:_________________;
(4)E、F、G三种金属的活动性由强到弱的顺序为_______________。(用元素符号表示)
四、实验题
17.化学兴趣小组的同学把铁钉和铁粉放在潮湿的环境中一段时间后,发现银白色的铁钉表面出现了一层黄色的物质。小组同学经查阅资料得知是铁锈。
(1)铁锈的主要成分是氧化铁___________(写化学式),铁锈属于___________(填“纯净物”或“混合物”)。在此过程中,铁粉温度明显升高,___________能变成___________能。
(2)小明将生锈的铁钉放入稀盐酸中。表面的铁锈很快消失,反应生成氯化铁和水,溶液变成黄色。铁离子___________(写出符号)使溶液显黄色。铁钉放在黄色的溶液中一段时间后溶液又变成了浅绿色:氯化铁和铁反应生成了氯化亚铁,该反应的符号表达式___________。基本反应类型是___________。
(3)小芳发现:等质量的铁钉和铁粉放入相同的稀盐酸中,都有气泡产生,但铁粉与稀盐酸产生气泡的速率明显更快,由此现象可得出反应速率与___________有关。
(4)铁元素是人体必须的___________(填“微量”或“常量”)元素。如果缺少铁元素,会导致___________。
18.化学是一门以实验为基础的科学,请结合图示回答问题:
(1)图中①仪器的名称是___________。
(2)实验室用高锰酸钾制取并收集较纯净的氧气,反应的化学方程式为___________,选择的装置组合是___________(填字母序号)。
(3)若用B装置制取氢气,分液漏斗代替长颈漏斗,优点是___________,若用D装置收集氢气,气体应该从___________进入(填“a”或“b”)。
19.现有一包固体粉末,可能含有Ba(OH)2、K2CO3、Na2SO4、MgCl2中的一种或几种,为确定其组成,进行如下实验:
步骤I:取少量样品于烧杯中,加入足量的水,充分搅拌,过滤得白色沉淀A和无色滤液B
步骤II:取步骤I所得白色沉淀A于试管中,加入足量稀盐酸,固体部分溶解且有气泡产生。
步骤III取步骤I所得无色滤液B于试管中,滴入少量Ba(OH)2溶液,无明显现象。
(1)白色沉淀A中一定存在的物质有________(填化学式);
(2)通过上述实验,可得到的实验结论是_______
(3)若只需一种试剂就能够进一步确定样品的组成,还需进行的实验操作是______
五、计算题
20.实验室用金属锌和稀硫酸制备氢气,若需要制备4.4g氢气,至少需要金属锌多少克?
21.现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合液过滤后得到溶液的质量为140g。(反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl)
(1)生成沉淀的质量是_______g。
(2)求碳酸钠溶液中溶质的质量分数是多少______?
22.我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为: 。
(1)求Fe2O3中铁元素的质量分数。
(2)根据化学方程式计算:用含Fe2O360%的赤铁矿石800 t,理论上可炼出纯铁多少吨?
试卷第1页,共3页
参考答案:
1.C
2.B
3.A
4.C
5.A
6.C
7.B
8.D
9.C
10.大理石的主要成分是碳酸钙,碳酸钙能和酸雨中的酸性物质反应,侵蚀大理石
11. 合金的熔点比其成分金属低 不正确
12. 稀硫酸能与铁反应而将铁桶腐蚀 二氧化碳密度比空气大,悬挂在高处有利于二氧化碳与蔬菜叶面充分接触 化肥(或氮肥)
13.(1)Mg + 2AgNO3=Mg(NO3)2+2Ag
(2)一定有硝酸镁、硝酸锌、硝酸亚铁,可能有硝酸银
14.(1) H2 Cu 铜
(2) 红
15. CO CuO或Cu(OH)2(合理均可)
16. Fe2O3 冶炼金属 Fe+CuSO4=FeSO4+Cu 铁>铜>银
17.(1) Fe2O3 混合物 化学 热
(2) Fe3+ 2FeCl3+Fe= 3FeCl2
化合反应
(3)反应物的接触面积
(4) 微量 贫血 缺铁性贫血
18. 锥形瓶 AE 控制反应速率 b
19. BaCO3、BaSO4 固体粉末一定含有Ba(OH)2、Na2SO4、K2CO3,可能含有MgCl2 向步骤Ⅱ的上层清液滴加足量的氢氧化钠溶液
20.143g
21.(1)10;(2)10.6%
22.(1)
(2)解:800 t矿石中Fe2O3的质量为800 t×60%=480 t
设理论上可炼出纯铁的质量为x
答:理论上可炼出纯铁336 t。
答案第1页,共2页
答案第1页,共2页
