第6章常用的金属和盐章节练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐章节练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 159.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-12 00:00:00 | ||
图片预览




文档简介
第6章常用的金属和盐章节练习2021-2022学年九年级化学沪教版(上海)
一、单选题
1.我们伟大祖国的发展日新月异,化学发挥着重要作用.请用已经学过的知识辨析下列说法中不正确的是
A.陕北建成了世界领先大型煤化工基地,提高能源利用率,解决直接燃煤的环境污染问题
B.2016年6月,我国在世界上首次量产高性能石墨烯锂电池.石墨烯属于碳单质,化学式为C
C.2016年6月,长征七号首飞成功,采用新型液氧煤汕发动机,使我国的空间运载能力达到国际先进水平.液氧和煤油都属于非金属单质
D.贵州北盘江大桥建成通车,桥面到谷底垂直高度达565米,成 为世界第一高桥!钢桁架梁采用高强度的钢材.这种钢材和纯铁相比,硬度增大很多
2.下列是常见的金属活动性顺序
以下判断不正确的是( )
A.X可与Y(NO3)2溶液反应 B.X可与盐酸反应
C.Y可与AgNO3溶液反应 D.Y可与稀H2SO4反应
3.将A、B、C、D四种物质放入一密闭容器中,在一定条件下充分反应,测得反应前后有关数据如下表所示,下列有关此反应的说法中正确的是
物质 A B C D
反应前质量(g) 20 50 80 30
反应后质量(g) 0 100 20 x
A.反应后D的质量x为50 g
B.参加反应的A、C的质量比为1∶4
C.若B、D的相对分子质量之比为5∶6,则其化学计量数之比为2∶1
D.该反应一定为复分解反应
4.下列化学方程式所表示的化学反应能发生的是 ( )
A.Cu+H2SO4=CuSO4+H2↑ B.Fe+ Zn( NO3)2=Fe(NO3)2+Zn↓
C.CuCl2+2NaOH=Cu(OH)2↓+2NaCl D.Na2CO3+2KNO3=K2CO3+ 2NaNO3
5.工业炼铁中会发生一氧化碳与氧化铁的反应,该反应中发生还原反应的物质是
A.CO B.Fe2O3 C.CO2 D.Fe
6.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
7.下列除去物质中所含少量杂质的方法错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B CaSO4溶液 稀硫酸 过量CaCO3 粉末、过滤
C FeCl2溶液 CuCl2 过量铁粉、过滤
D 二氧化碳 一氧化碳 点燃
A.A B.B C.C D.D
8.下列各组物质在溶液中能大量共存且形成无色溶液的是
A.NaCl BaCl2Na2CO3 B.KNO3HCl CaCl2
C.H2SO4 FeCl3NaNO3 D.NaOH HNO3NH4NO3
9.两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是
A.该图反映出镁比锌的金属活动性强
B.a点时,两个烧杯中的酸都恰好完全反应
C.b点时,两个烧杯中产生氢气的质量相等
D.c点时,两个烧杯中都有金属剩余
10.现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是( )
A.金属活动性:乙>甲>丙 B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲 D.消耗硫酸的质量:甲>乙>丙
11.某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是
A.定期用清水冲洗,除去灰尘 B.放于体验区,让观众触摸
C.用盐水除去铁剑上的锈斑 D.放在充满氮气的展览柜中
二、简答题
12.探究金属化学性质时,发现铝与硫酸的实验,刚开始几乎没有气泡,过一段才产生大量气泡,为什么
13.全世界每年因生锈损失的钢铁,约占世界年产量的四分之一。 铁与氧气、水等反应生成铁锈,铁锈的主要成分是_________;请你谈谈生活中观察到的保护钢铁制品的两条有效措施:______;_____________。
14.自行车作为常用的代步工具,既轻便灵活,又符合环保要求。下图是一款自行车的示意图。
(1)所标物质中,属于有机合成材料的是______(填一种即可,下同);属于合金的是____;含有的金属元素是______。
(2)车架表面刷油漆主要是为了防锈,其原理是_________________;
请再提出一条可延长自行车使用寿命的建议______________________。
(3)当今自行车外形美观,材质轻便.牢固,除了代步,还可作为健身工具。由此你对化学与人类生活的关系有何感想?__________________________。
三、推断题
15.有A,B,C,D四种可溶性的物质,每种由以下两组中的离子构成。(每种离子只能选用一次)
阳离子
阴离子
四种物质之间的反应有如下现象:
(1)A+B→白色沉淀,不溶于稀硝酸。
(2)B+D→蓝色沉淀。
(3)C+B→白色沉淀,再加稀硝酸沉淀溶解并生成C。
由此可推知:A为_____,B为_____,C为_____,D为_____。(写化学式)
16.现有 A~E 五种初中化学常见物质,其中 A 是红色固体,B 是人体胃液中常见的酸,E 常用于除油污。它们的转化关系如下图。请回答:
(1)C 的一种用途是______;
(2)A 转化为C:反应的化学方程式为______。
(3)D 转化为 E:反应的化学方程式为______。
17.某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。
(1)向固体乙上滴加盐酸时____________(填“有”或“没有”)气泡产生。
(2)溶液甲中一定含有哪些溶质?(写化学式)__________________
(3)请写出该实验过程中所发生反应的化学方程式。______________________
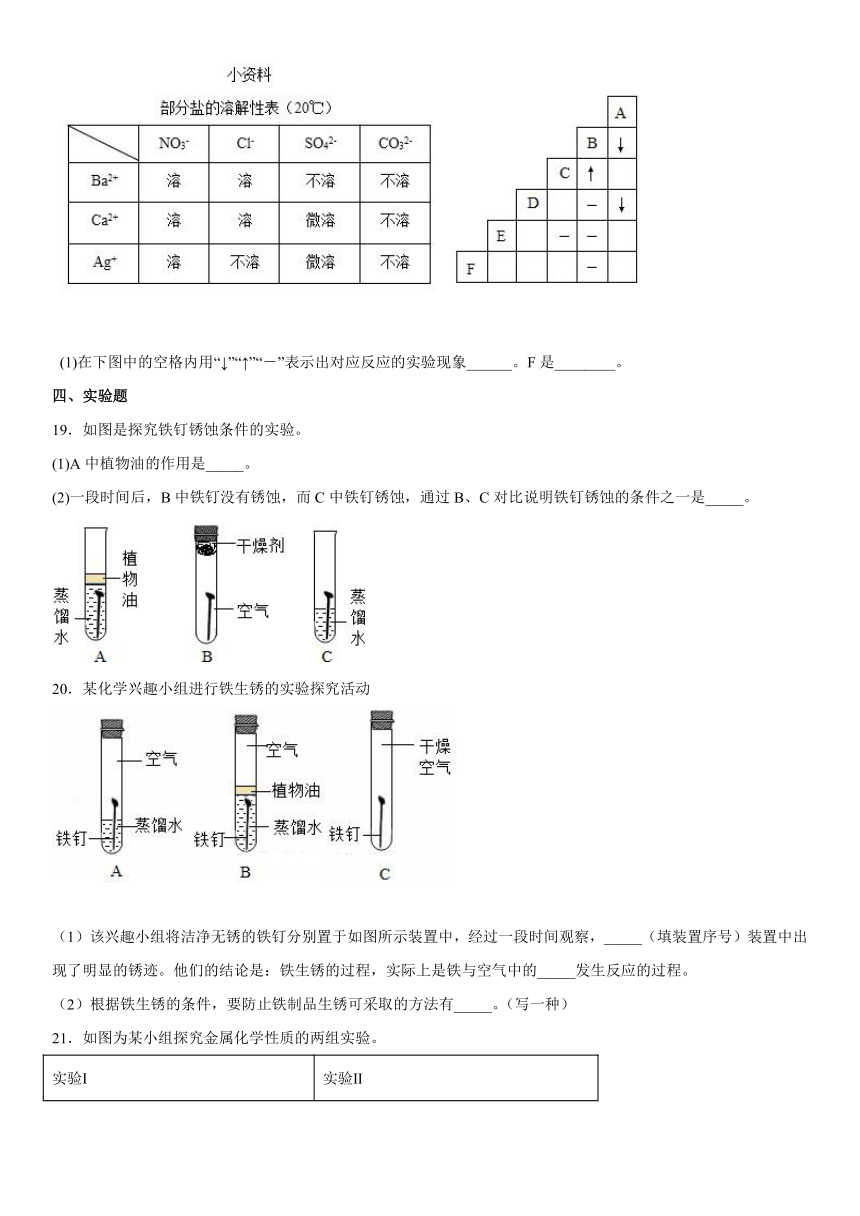
18.有A、B、C、D、E、F六种物质的溶已知它们分别是K2CO3、BaCl2、Ca(NO3)2、NaCl、H2SO4、AgNO3中的某一种溶液。下图为常温时上述溶液两两混合的部分实验现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物。请回答下列问题
(1)在下图中的空格内用“↓”“↑”“-”表示出对应反应的实验现象______。F是________。
四、实验题
19.如图是探究铁钉锈蚀条件的实验。
(1)A中植物油的作用是_____。
(2)一段时间后,B中铁钉没有锈蚀,而C中铁钉锈蚀,通过B、C对比说明铁钉锈蚀的条件之一是_____。
20.某化学兴趣小组进行铁生锈的实验探究活动
(1)该兴趣小组将洁净无锈的铁钉分别置于如图所示装置中,经过一段时间观察,_____(填装置序号)装置中出现了明显的锈迹。他们的结论是:铁生锈的过程,实际上是铁与空气中的_____发生反应的过程。
(2)根据铁生锈的条件,要防止铁制品生锈可采取的方法有_____。(写一种)
21.如图为某小组探究金属化学性质的两组实验。
实验Ⅰ 实验Ⅱ
(1) 实验Ⅰ,通过观察金属表面产生气泡的快慢,___________(填“能”或“不能”)说明Zn的活动性比Fe强。
(2) 实验Ⅱ,试管D中反应的化学方程式是___________;要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是___________(填字母序号)。
五、计算题
22.草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为______。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是______?
23.某同学欲测定生铁中铁的质量分数,他称取样品11.5g,加入足量溶质质量分数为10%的稀硫酸充分反应(杂质不溶于水,也不与稀硫酸反应),产生气体的质量与所加稀硫酸的质量关系如图所示,请回答:
(1)恰好完全反应时生成氢气的质量为 g。
(2)该样品中铁的质量分数?(精确到0.1%)。
(3)图中m的值。
24.我国高铁建设走在世界前列,修建高铁需要大量铁矿石来炼铁,进而炼钢。
(1)下列三种铁矿石的主要成分Fe2O3、Fe3O4、FeCO3中,含铁量最高的是______。高炉炼铁需要的原料有铁矿石、______、______和石灰石。
(2)要炼出含铁96%的生铁1000 t,至少需要含氧化铁80%的赤铁矿多少吨?若高炉气体不加处理,理论上会向大气中排放CO2多少吨?(无计算过程不给分,计算结果保留整数。)
25.某兴趣小组为测定镁铝合金中各成分的质量分数,现做如下实验。取两份等质量的合金,一份与足量稀HCl反应产生0.6gH2;另一份与足量的NaOH溶液反应产生0.2gH2。已知:Mg与NaOH溶液不反应,Al与NaOH溶液反应的方程式为:。
试计算(写出计算过程):
(1)求Mg与稀HCl反应产生H2的质量;
(2)求合金中Al的质量分数(计算结果精确到0.1%)。
试卷第1页,共3页
参考答案:
1.C
2.D
3.C
4.C
5.B
6.C
7.D
8.B
9.D
10.C
11.D
12.铝表面有一层致密氧化膜,与 H2 SO4 反应无气体产生;过一段时间,铝与 H2 SO4 反应产生大量气泡。
13. Fe2O3 在表面刷漆或喷漆 在表面涂上机油;在表面镀上一层其他金属;使其表面氧化生成致密的氧化膜
14. 塑料(橡胶) 不锈钢(或钢) 铁 使铁与水和氧气隔绝 雨淋后及时清洗擦干后涂上油(合理即可) 化学能够开发新的材料,以改善人类的生存条件,使我们的生活变得更美好
15. Na2SO4 Ba(OH)2 Mg(NO3)2 CuCl2
16.(1)灭火等
(2)等
(3)
17. 没有 Al( NO3) 3、Zn( NO3)2、Cu(NO3 ) 2 Cu + 2 AgNO3 = Cu (NO3) 2 + 2 Ag Zn +2AgNO3 = Zn(NO3)2 +2Ag[或 Zn + Cu(NO3)2= Zn(NO3)2 +Cu]
18. 硝酸钙[或Ca(NO3)2]
19. 隔绝空气 与水接触
20. A 氧气和水蒸气(或氧气和水分)(没答全不给分) 刷漆(涂油、表面洁净干燥、镀金属等)(答案合理即可)
21. 不能 Fe+CuSO4=Cu+FeSO4 CD
22.(1)39:6:24;(2)8.8g;(3)14.6%
23.(1)0.4;
(2)解:设该样品中铁的质量分数为x,消耗硫酸的质量为y
x≈97.4%
y=19.6g;
(3)图中m=19.6g÷10%=196g。
答:该样品中铁的质量分数为97.4%,m=196g。
24.(1) Fe3O4 焦炭 空气
(2)解:设至少需要赤铁矿的质量为x,反应产生CO2的质量为y
=
x=1714 t
=
y =1131 t
答:至少需要含氧化铁80%的赤铁矿1714 t,理论上会向大气中排放CO2 1131 t。
25.(1)解:设Al的质量为x
x=1.8g
设Al与HC1反应产生的H2质量为y
y=0.2g
所以:Mg与盐酸反应产生的H2质量为
(2)设Mg的质量为z
z=4.8g
合金中铝的质量分数为。
答:镁与盐酸产生氢气的质量是0.4g,铝的质量分数为27.3%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.我们伟大祖国的发展日新月异,化学发挥着重要作用.请用已经学过的知识辨析下列说法中不正确的是
A.陕北建成了世界领先大型煤化工基地,提高能源利用率,解决直接燃煤的环境污染问题
B.2016年6月,我国在世界上首次量产高性能石墨烯锂电池.石墨烯属于碳单质,化学式为C
C.2016年6月,长征七号首飞成功,采用新型液氧煤汕发动机,使我国的空间运载能力达到国际先进水平.液氧和煤油都属于非金属单质
D.贵州北盘江大桥建成通车,桥面到谷底垂直高度达565米,成 为世界第一高桥!钢桁架梁采用高强度的钢材.这种钢材和纯铁相比,硬度增大很多
2.下列是常见的金属活动性顺序
以下判断不正确的是( )
A.X可与Y(NO3)2溶液反应 B.X可与盐酸反应
C.Y可与AgNO3溶液反应 D.Y可与稀H2SO4反应
3.将A、B、C、D四种物质放入一密闭容器中,在一定条件下充分反应,测得反应前后有关数据如下表所示,下列有关此反应的说法中正确的是
物质 A B C D
反应前质量(g) 20 50 80 30
反应后质量(g) 0 100 20 x
A.反应后D的质量x为50 g
B.参加反应的A、C的质量比为1∶4
C.若B、D的相对分子质量之比为5∶6,则其化学计量数之比为2∶1
D.该反应一定为复分解反应
4.下列化学方程式所表示的化学反应能发生的是 ( )
A.Cu+H2SO4=CuSO4+H2↑ B.Fe+ Zn( NO3)2=Fe(NO3)2+Zn↓
C.CuCl2+2NaOH=Cu(OH)2↓+2NaCl D.Na2CO3+2KNO3=K2CO3+ 2NaNO3
5.工业炼铁中会发生一氧化碳与氧化铁的反应,该反应中发生还原反应的物质是
A.CO B.Fe2O3 C.CO2 D.Fe
6.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
7.下列除去物质中所含少量杂质的方法错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B CaSO4溶液 稀硫酸 过量CaCO3 粉末、过滤
C FeCl2溶液 CuCl2 过量铁粉、过滤
D 二氧化碳 一氧化碳 点燃
A.A B.B C.C D.D
8.下列各组物质在溶液中能大量共存且形成无色溶液的是
A.NaCl BaCl2Na2CO3 B.KNO3HCl CaCl2
C.H2SO4 FeCl3NaNO3 D.NaOH HNO3NH4NO3
9.两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是
A.该图反映出镁比锌的金属活动性强
B.a点时,两个烧杯中的酸都恰好完全反应
C.b点时,两个烧杯中产生氢气的质量相等
D.c点时,两个烧杯中都有金属剩余
10.现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是( )
A.金属活动性:乙>甲>丙 B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲 D.消耗硫酸的质量:甲>乙>丙
11.某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是
A.定期用清水冲洗,除去灰尘 B.放于体验区,让观众触摸
C.用盐水除去铁剑上的锈斑 D.放在充满氮气的展览柜中
二、简答题
12.探究金属化学性质时,发现铝与硫酸的实验,刚开始几乎没有气泡,过一段才产生大量气泡,为什么
13.全世界每年因生锈损失的钢铁,约占世界年产量的四分之一。 铁与氧气、水等反应生成铁锈,铁锈的主要成分是_________;请你谈谈生活中观察到的保护钢铁制品的两条有效措施:______;_____________。
14.自行车作为常用的代步工具,既轻便灵活,又符合环保要求。下图是一款自行车的示意图。
(1)所标物质中,属于有机合成材料的是______(填一种即可,下同);属于合金的是____;含有的金属元素是______。
(2)车架表面刷油漆主要是为了防锈,其原理是_________________;
请再提出一条可延长自行车使用寿命的建议______________________。
(3)当今自行车外形美观,材质轻便.牢固,除了代步,还可作为健身工具。由此你对化学与人类生活的关系有何感想?__________________________。
三、推断题
15.有A,B,C,D四种可溶性的物质,每种由以下两组中的离子构成。(每种离子只能选用一次)
阳离子
阴离子
四种物质之间的反应有如下现象:
(1)A+B→白色沉淀,不溶于稀硝酸。
(2)B+D→蓝色沉淀。
(3)C+B→白色沉淀,再加稀硝酸沉淀溶解并生成C。
由此可推知:A为_____,B为_____,C为_____,D为_____。(写化学式)
16.现有 A~E 五种初中化学常见物质,其中 A 是红色固体,B 是人体胃液中常见的酸,E 常用于除油污。它们的转化关系如下图。请回答:
(1)C 的一种用途是______;
(2)A 转化为C:反应的化学方程式为______。
(3)D 转化为 E:反应的化学方程式为______。
17.某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。
(1)向固体乙上滴加盐酸时____________(填“有”或“没有”)气泡产生。
(2)溶液甲中一定含有哪些溶质?(写化学式)__________________
(3)请写出该实验过程中所发生反应的化学方程式。______________________
18.有A、B、C、D、E、F六种物质的溶已知它们分别是K2CO3、BaCl2、Ca(NO3)2、NaCl、H2SO4、AgNO3中的某一种溶液。下图为常温时上述溶液两两混合的部分实验现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物。请回答下列问题
(1)在下图中的空格内用“↓”“↑”“-”表示出对应反应的实验现象______。F是________。
四、实验题
19.如图是探究铁钉锈蚀条件的实验。
(1)A中植物油的作用是_____。
(2)一段时间后,B中铁钉没有锈蚀,而C中铁钉锈蚀,通过B、C对比说明铁钉锈蚀的条件之一是_____。
20.某化学兴趣小组进行铁生锈的实验探究活动
(1)该兴趣小组将洁净无锈的铁钉分别置于如图所示装置中,经过一段时间观察,_____(填装置序号)装置中出现了明显的锈迹。他们的结论是:铁生锈的过程,实际上是铁与空气中的_____发生反应的过程。
(2)根据铁生锈的条件,要防止铁制品生锈可采取的方法有_____。(写一种)
21.如图为某小组探究金属化学性质的两组实验。
实验Ⅰ 实验Ⅱ
(1) 实验Ⅰ,通过观察金属表面产生气泡的快慢,___________(填“能”或“不能”)说明Zn的活动性比Fe强。
(2) 实验Ⅱ,试管D中反应的化学方程式是___________;要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是___________(填字母序号)。
五、计算题
22.草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为______。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是______?
23.某同学欲测定生铁中铁的质量分数,他称取样品11.5g,加入足量溶质质量分数为10%的稀硫酸充分反应(杂质不溶于水,也不与稀硫酸反应),产生气体的质量与所加稀硫酸的质量关系如图所示,请回答:
(1)恰好完全反应时生成氢气的质量为 g。
(2)该样品中铁的质量分数?(精确到0.1%)。
(3)图中m的值。
24.我国高铁建设走在世界前列,修建高铁需要大量铁矿石来炼铁,进而炼钢。
(1)下列三种铁矿石的主要成分Fe2O3、Fe3O4、FeCO3中,含铁量最高的是______。高炉炼铁需要的原料有铁矿石、______、______和石灰石。
(2)要炼出含铁96%的生铁1000 t,至少需要含氧化铁80%的赤铁矿多少吨?若高炉气体不加处理,理论上会向大气中排放CO2多少吨?(无计算过程不给分,计算结果保留整数。)
25.某兴趣小组为测定镁铝合金中各成分的质量分数,现做如下实验。取两份等质量的合金,一份与足量稀HCl反应产生0.6gH2;另一份与足量的NaOH溶液反应产生0.2gH2。已知:Mg与NaOH溶液不反应,Al与NaOH溶液反应的方程式为:。
试计算(写出计算过程):
(1)求Mg与稀HCl反应产生H2的质量;
(2)求合金中Al的质量分数(计算结果精确到0.1%)。
试卷第1页,共3页
参考答案:
1.C
2.D
3.C
4.C
5.B
6.C
7.D
8.B
9.D
10.C
11.D
12.铝表面有一层致密氧化膜,与 H2 SO4 反应无气体产生;过一段时间,铝与 H2 SO4 反应产生大量气泡。
13. Fe2O3 在表面刷漆或喷漆 在表面涂上机油;在表面镀上一层其他金属;使其表面氧化生成致密的氧化膜
14. 塑料(橡胶) 不锈钢(或钢) 铁 使铁与水和氧气隔绝 雨淋后及时清洗擦干后涂上油(合理即可) 化学能够开发新的材料,以改善人类的生存条件,使我们的生活变得更美好
15. Na2SO4 Ba(OH)2 Mg(NO3)2 CuCl2
16.(1)灭火等
(2)等
(3)
17. 没有 Al( NO3) 3、Zn( NO3)2、Cu(NO3 ) 2 Cu + 2 AgNO3 = Cu (NO3) 2 + 2 Ag Zn +2AgNO3 = Zn(NO3)2 +2Ag[或 Zn + Cu(NO3)2= Zn(NO3)2 +Cu]
18. 硝酸钙[或Ca(NO3)2]
19. 隔绝空气 与水接触
20. A 氧气和水蒸气(或氧气和水分)(没答全不给分) 刷漆(涂油、表面洁净干燥、镀金属等)(答案合理即可)
21. 不能 Fe+CuSO4=Cu+FeSO4 CD
22.(1)39:6:24;(2)8.8g;(3)14.6%
23.(1)0.4;
(2)解:设该样品中铁的质量分数为x,消耗硫酸的质量为y
x≈97.4%
y=19.6g;
(3)图中m=19.6g÷10%=196g。
答:该样品中铁的质量分数为97.4%,m=196g。
24.(1) Fe3O4 焦炭 空气
(2)解:设至少需要赤铁矿的质量为x,反应产生CO2的质量为y
=
x=1714 t
=
y =1131 t
答:至少需要含氧化铁80%的赤铁矿1714 t,理论上会向大气中排放CO2 1131 t。
25.(1)解:设Al的质量为x
x=1.8g
设Al与HC1反应产生的H2质量为y
y=0.2g
所以:Mg与盐酸反应产生的H2质量为
(2)设Mg的质量为z
z=4.8g
合金中铝的质量分数为。
答:镁与盐酸产生氢气的质量是0.4g,铝的质量分数为27.3%。
答案第1页,共2页
答案第1页,共2页
