富集在海水中得元素—氯.
图片预览










文档简介
课件37张PPT。1富集在海水中得元素—氯若将海水中的盐结晶后平铺于陆地上,可使陆地平均升高150米2
3在第一次世界大战期间,一次德军与英、法军战士在比利时的伊普尔对峙,黎明时,英、法军前线战壕的士兵突然看到一股阴森森的黄绿色气体逐渐向前袭来,很快数百名英、法军战士窒息而死,数千名士兵双目失明。这是1915年4月22日发生的令人发指的事件——德国军队向英、法军队施用了惨无人道的毒气战。
这种黄绿色的气体是什么气体?它为什么很快就毒死了那么多的军人呢?你想知道谜底吗?你想了解它还有哪些性质和用途吗?4反对战争,维护世界和平!!5 2005年3月19日在京沪高速公路江苏淮安段两车相撞,导致氯气大量泄漏。6一、氯元素
1.存在:在海水中主要以NaCl的形式存在。Cl2.原子结构性质:最外层有7e-,易得到1个电子形成Cl-,性质很活泼,表现为典型的非金属性。请根据氯元素的原
子结构示意图,
推测其化学性质?自然界中有没有游离态的氯?如果没有,人们是怎样制得氯气的呢? 3、化合价:-1,0, +1,+3,+5,+7
4、性 质: 得电子能力强,氧化性强7舍勒 (1742~1786)瑞典化学家。1774年舍勒 发现氯气他将这种元素命名为Chlorine,这个名称来自希腊文,有“绿色”的意思。我国早年译文将其译成“绿气”,后改为氯气。氯气化学式:Cl28思
考
与
交
流阅读书本P82科学史话,思考
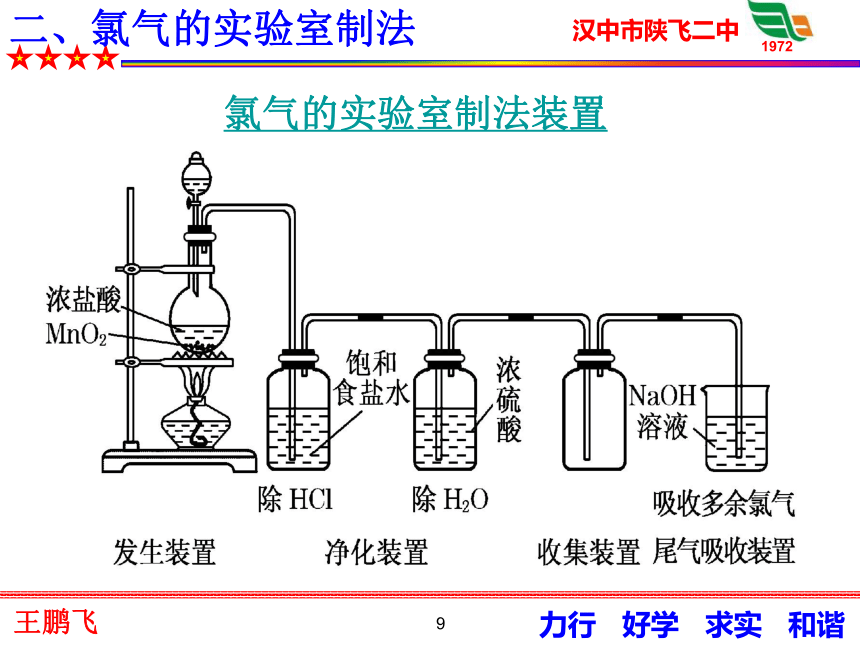
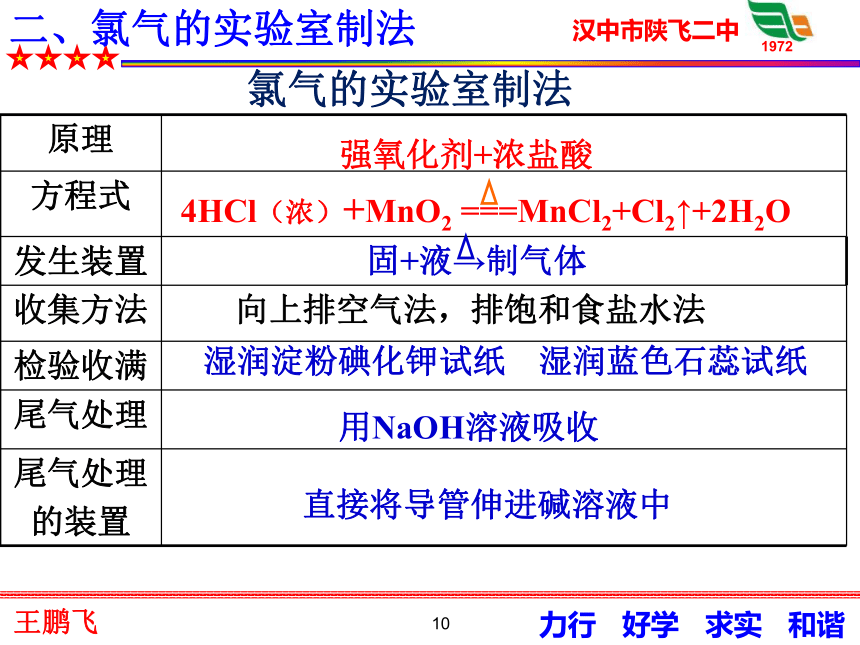
1、从氯气的发现到确认为一种新的元素,时间长达三十多年。分组讨论你从这一史实中得到什么启示?2、舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出舍勒发现氯气的化学反应方程式。 9二、氯气的实验室制法氯气的实验室制法装置10氯气的实验室制法强氧化剂+浓盐酸湿润淀粉碘化钾试纸湿润蓝色石蕊试纸用NaOH溶液吸收直接将导管伸进碱溶液中二、氯气的实验室制法11(1)为了减少制得的Cl2中HCl的含量,所以加热温度不宜过高,以减少HCl的挥发.
(2)盐酸的作用是酸性和还原性,必须使用浓盐酸,稀盐酸不反应.
(3)实验结束后,先使反应停止并排出残留的Cl2,再拆卸装置,避免污染空气.
(4)尾气吸收时,不能用澄清石灰水吸收Cl2,因为溶液中Ca(OH)2含量少,吸收不完全.应该用谁呢?温馨提示二、氯气的实验室制法12三、氯气的物理性质物理性质黄绿色
气体密度比
空气大在水中溶解度不大(1:2)有刺激
性气味有毒 较低(易液化)在实验室里闻氯气时,必须十分小心,应该用手在瓶口轻轻地扇动,仅使极少量的氯气飘入鼻孔。当闻其它的气体气味时,也应该采用这种方法。13请观察放一瓶氯气,回答氯气有何 物理性质 ?不能用排水集气法
收集氯气黄绿色气体有刺激性气味有毒密度比空气大可溶于水三、氯气的物理性质:14四、氯气的化学性质具有强氧化性:容易得到电子,做氧化剂金属氢气易与有还原性的物质发生氧化还原反应15四、氯气的化学性质:1、Cl2与金属的反应:2Na + Cl2 === 2 NaCl2Fe + 3Cl2 === 2FeCl3Cl2 + Cu === CuCl2(有黄色火焰,形成白烟)(棕黄色烟,蓝绿色溶液)(发红热,形成棕褐色烟;溶于水后溶液呈棕黄色 )点燃点燃点燃小结:大多数金属都能在一定条件下与氯气化合生成相应的金属氯化物(盐) ,在反应中氯气均作氧化剂,体现出强氧化性 。162、 Cl2与氢气反应现象:
反应式:H2在Cl2中安静燃烧,发出苍白色火焰,产生白雾。实验4-3 Cl2与氢气反应的实验,注意观察现象17 通过对H2在Cl2中燃烧的实验,你对燃烧的条件及本质有什么新的认识? (1)燃烧不一定有氧气参加。
(2)任何发光发热的剧烈的化学反应都叫做燃烧。
(3)燃烧的本质是发生了氧化还原反应.思考与交流18南昌儿童游泳集体氯气中毒中新网南昌6月6日消息:南昌发生一起儿童游泳集体氯气中毒事件,11名症状较重的儿童被立刻送往医院抢救。
原因是馆内一工作人员操作失误,在泳池内还有队员的情 况下,将净 化水质用的氯气管道 打开消毒,当即导致靠近管道附近的多名小选手出现呕吐、头晕、四肢无力等氯气中毒症状。氯气有毒为什么游泳池还要通入它?19 你是否试过打开自来水,会闻到一股刺激性的气味?这是什么原因?203、氯气与水反应Cl2 + H2O = HCl + HClOHClO是比碳酸还弱的酸,易分解,具有强氧化性,漂白性和杀菌能力。①一元弱酸 (酸性比碳酸还弱)
②强氧化性 (杀菌、消毒)
③漂白性 (强氧化性的表现)
④不稳定易分解21新制的氯水有什么性质?
能与那些物质发生反应?方案一:检验Cl-( )
方案二:检验H+ ( )酸化的硝酸银酸碱指示剂?如何验证氯气与水发生了反应?新制氯水与久置氯水有何区别?关于氯水的成分,新制氯水与久置的氯水相比,成分相同吗?
干燥的氯气与湿润的氯气在性质上有区别吗?
液氯与氯水是否相同?22液氯与氯水的区别?新制氯水与久置氯水的区别?纯净物混合物分子:离子:Cl2 ,HClO,H2OH+,Cl-,ClO-分子:H2O离子:H+,Cl-新制有氧化性,无酸性和漂白性有酸性,强氧化性,能漂白,消毒,光照时HClO分解久置只有Cl2分子实验室使用的氯水只能现配现用,并盛放在棕色试剂瓶中只有酸性
酸性增强23氯水的性质氯水的成分
Cl2
HClO
H+
Cl-氧化性:2KI + Cl2 = 2KCl + I2
2Fe2+ + Cl2 = 2Fe3+ + 2Cl-漂白性:使有色布条、品红褪色酸性:使石蕊变红
Zn + 2H+ = Zn2+ + H2Cl- + Ag+ = AgCl↓教材84页实验4-4,4-5氯水的漂白性24氯水性质小结:1、氯水:氯气的水溶液;黄绿色。2、氯水的强氧化性—次氯酸具有强氧化性。3、氯水的不稳定性—次氯酸不稳定。4、氯水的酸性—盐酸、次氯酸电离出H+。5、氯水的成份:分子(H2O Cl2 HCl0)
离子(H+ Cl- ClO- )25 漂白性的比较名称原理实质程度范围过氧化钠氯 水将有色的色素
氧化为稳定的
无色物质 氯水中的次氯酸将有色物质氧化成无色物质氧化作用 氧化作用永久性 永久性 漂白大多数有色物质 漂白大多数有色物质,能使紫色石蕊试液褪色活性炭吸附有色
色素物理吸附261、下列关于氯水的说法中正确的是:
A、新制氯水中只含有Cl2和H2O分子
B、新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
C、光照氯水有气泡逸出,该气体是Cl2
D、氯水放置数天后酸性增强
2、下列物质能使红墨水褪色的是
A、活性炭 B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液
3、氯气能使湿润的蓝色石蕊试纸
A、褪色 B、变成红色
C、先褪色后变红 D、先变红后褪色
课堂练习DADD27想一想根据氯气与水的反应原理,推测氯气与NaOH能否发生反应?若反应,其产物是什么?4、氯气与碱反应2NaOH+Cl2=NaClO+NaCl+H2O有效成分:NaClO2 Ca(OH)2+2Cl2==Ca(ClO)2+CaCl2+2H2O漂白粉、漂粉精漂白液有效成分:Ca(ClO)2以上充分反应可得较多的Ca(ClO) 2 (制漂粉精)有毒的氯气尾气用NaOH溶液进行尾气吸收处理氯气与熟石灰反应的化学方程式:282Fe2+ + Cl2 == 2Fe3+ + 2Cl-
Cl2 + 2Br- == 2Cl- + Br2
Cl2 + 2 I- == 2Cl- + I2 2 == 2NaCl + Br2
2 == 2NaCl + I25、与盐溶液的反应与FeCl2 、NaBr、KI等盐溶液反应 2FeCl2 + Cl2 == 2FeCl3--- 氯气的强氧化性Cl2+ NaBr
Cl2+ NaI思考:根据上述实验,排出Cl2、Br2、I2的氧化性强弱顺序及Cl-、Br-、I-的还原性强弱顺序结论:氧化性:Cl2>Br2>I2
还原性:I->Br->Cl-29卤素单质的化学性质(见课本86页科学视野)①对比Cl2,写出Br2与 Na 、Fe 反应的化学方程式。 ②对比Cl2,写出F2 、Br2、I2与 H2 反应的化学方程式。 它们发生反应的条件相同吗? ③对比Cl2,写出Br2与 H2O 反应的化学方程式。 I2 +Fe=FeI2Br2+2Na=2NaBr
3Br2+2Fe=2FeBr330F2 冷暗处爆炸 H2+F2====2HF HF很稳定 Cl2 光照或点燃 H2+Cl2=====2HCl HCl稳定Br2 高温 H2+Br2======2HBr HBr较不稳定I2 高温、持续加热 H2+I2======2HI HI很不稳定
缓慢进行 卤素单质与氢气的反应结论: F Cl Br I 随核电荷数的增多,原子半径的增大
(1)卤素单质与H2化合的难易关系:F2 >Cl2> Br2> I 2(2)卤化氢的稳定性关系:HF > HCl > HBr > HI?还原性呢 314.已知常温下氯酸钾与浓盐酸反应放出氯气(卤素单质在溶液中的置换能力为:Cl2>Br2>I2,碘遇淀粉变蓝色,溴水显橙色),现按右图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )32解析:生成的氯气为黄绿色气体,氯气置换出的溴为橙色,置换出的碘遇淀粉变蓝色,氢氧化钠吸收氯气生成无色物质,而棉球还是显白色。
答案:A33Br2+ H2O=====HBr+HBrO反应越来越难以发生2F2+2H2O=====4HF+O2 (特例)Cl2 +H2O=====HCl+HClO卤素单质与水反应通式:X2 + H2O=====HX+HXO(X: Cl、Br、I)I2 +H2O=====HI+HIO34五、氯离子的检验实验:P85实验4-6无Cl-35(2)方法和结论:
在被检验的溶液中加入稀硝酸酸化,再滴入AgNO3溶液,若产生白色沉淀,则被检液中含有Cl-。
或 在被检验的溶液中滴入AgNO3溶液,若产生白色沉淀,再加入稀硝酸,沉淀不溶,则被检液中含有Cl-。(1)试剂AgNO3溶液、稀硝酸 稀硝酸—排除干扰离子CO32-等小结:氯离子(Cl-)的检验361、氯的原子结构和性质谢谢37
3在第一次世界大战期间,一次德军与英、法军战士在比利时的伊普尔对峙,黎明时,英、法军前线战壕的士兵突然看到一股阴森森的黄绿色气体逐渐向前袭来,很快数百名英、法军战士窒息而死,数千名士兵双目失明。这是1915年4月22日发生的令人发指的事件——德国军队向英、法军队施用了惨无人道的毒气战。
这种黄绿色的气体是什么气体?它为什么很快就毒死了那么多的军人呢?你想知道谜底吗?你想了解它还有哪些性质和用途吗?4反对战争,维护世界和平!!5 2005年3月19日在京沪高速公路江苏淮安段两车相撞,导致氯气大量泄漏。6一、氯元素
1.存在:在海水中主要以NaCl的形式存在。Cl2.原子结构性质:最外层有7e-,易得到1个电子形成Cl-,性质很活泼,表现为典型的非金属性。请根据氯元素的原
子结构示意图,
推测其化学性质?自然界中有没有游离态的氯?如果没有,人们是怎样制得氯气的呢? 3、化合价:-1,0, +1,+3,+5,+7
4、性 质: 得电子能力强,氧化性强7舍勒 (1742~1786)瑞典化学家。1774年舍勒 发现氯气他将这种元素命名为Chlorine,这个名称来自希腊文,有“绿色”的意思。我国早年译文将其译成“绿气”,后改为氯气。氯气化学式:Cl28思
考
与
交
流阅读书本P82科学史话,思考
1、从氯气的发现到确认为一种新的元素,时间长达三十多年。分组讨论你从这一史实中得到什么启示?2、舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出舍勒发现氯气的化学反应方程式。 9二、氯气的实验室制法氯气的实验室制法装置10氯气的实验室制法强氧化剂+浓盐酸湿润淀粉碘化钾试纸湿润蓝色石蕊试纸用NaOH溶液吸收直接将导管伸进碱溶液中二、氯气的实验室制法11(1)为了减少制得的Cl2中HCl的含量,所以加热温度不宜过高,以减少HCl的挥发.
(2)盐酸的作用是酸性和还原性,必须使用浓盐酸,稀盐酸不反应.
(3)实验结束后,先使反应停止并排出残留的Cl2,再拆卸装置,避免污染空气.
(4)尾气吸收时,不能用澄清石灰水吸收Cl2,因为溶液中Ca(OH)2含量少,吸收不完全.应该用谁呢?温馨提示二、氯气的实验室制法12三、氯气的物理性质物理性质黄绿色
气体密度比
空气大在水中溶解度不大(1:2)有刺激
性气味有毒 较低(易液化)在实验室里闻氯气时,必须十分小心,应该用手在瓶口轻轻地扇动,仅使极少量的氯气飘入鼻孔。当闻其它的气体气味时,也应该采用这种方法。13请观察放一瓶氯气,回答氯气有何 物理性质 ?不能用排水集气法
收集氯气黄绿色气体有刺激性气味有毒密度比空气大可溶于水三、氯气的物理性质:14四、氯气的化学性质具有强氧化性:容易得到电子,做氧化剂金属氢气易与有还原性的物质发生氧化还原反应15四、氯气的化学性质:1、Cl2与金属的反应:2Na + Cl2 === 2 NaCl2Fe + 3Cl2 === 2FeCl3Cl2 + Cu === CuCl2(有黄色火焰,形成白烟)(棕黄色烟,蓝绿色溶液)(发红热,形成棕褐色烟;溶于水后溶液呈棕黄色 )点燃点燃点燃小结:大多数金属都能在一定条件下与氯气化合生成相应的金属氯化物(盐) ,在反应中氯气均作氧化剂,体现出强氧化性 。162、 Cl2与氢气反应现象:
反应式:H2在Cl2中安静燃烧,发出苍白色火焰,产生白雾。实验4-3 Cl2与氢气反应的实验,注意观察现象17 通过对H2在Cl2中燃烧的实验,你对燃烧的条件及本质有什么新的认识? (1)燃烧不一定有氧气参加。
(2)任何发光发热的剧烈的化学反应都叫做燃烧。
(3)燃烧的本质是发生了氧化还原反应.思考与交流18南昌儿童游泳集体氯气中毒中新网南昌6月6日消息:南昌发生一起儿童游泳集体氯气中毒事件,11名症状较重的儿童被立刻送往医院抢救。
原因是馆内一工作人员操作失误,在泳池内还有队员的情 况下,将净 化水质用的氯气管道 打开消毒,当即导致靠近管道附近的多名小选手出现呕吐、头晕、四肢无力等氯气中毒症状。氯气有毒为什么游泳池还要通入它?19 你是否试过打开自来水,会闻到一股刺激性的气味?这是什么原因?203、氯气与水反应Cl2 + H2O = HCl + HClOHClO是比碳酸还弱的酸,易分解,具有强氧化性,漂白性和杀菌能力。①一元弱酸 (酸性比碳酸还弱)
②强氧化性 (杀菌、消毒)
③漂白性 (强氧化性的表现)
④不稳定易分解21新制的氯水有什么性质?
能与那些物质发生反应?方案一:检验Cl-( )
方案二:检验H+ ( )酸化的硝酸银酸碱指示剂?如何验证氯气与水发生了反应?新制氯水与久置氯水有何区别?关于氯水的成分,新制氯水与久置的氯水相比,成分相同吗?
干燥的氯气与湿润的氯气在性质上有区别吗?
液氯与氯水是否相同?22液氯与氯水的区别?新制氯水与久置氯水的区别?纯净物混合物分子:离子:Cl2 ,HClO,H2OH+,Cl-,ClO-分子:H2O离子:H+,Cl-新制有氧化性,无酸性和漂白性有酸性,强氧化性,能漂白,消毒,光照时HClO分解久置只有Cl2分子实验室使用的氯水只能现配现用,并盛放在棕色试剂瓶中只有酸性
酸性增强23氯水的性质氯水的成分
Cl2
HClO
H+
Cl-氧化性:2KI + Cl2 = 2KCl + I2
2Fe2+ + Cl2 = 2Fe3+ + 2Cl-漂白性:使有色布条、品红褪色酸性:使石蕊变红
Zn + 2H+ = Zn2+ + H2Cl- + Ag+ = AgCl↓教材84页实验4-4,4-5氯水的漂白性24氯水性质小结:1、氯水:氯气的水溶液;黄绿色。2、氯水的强氧化性—次氯酸具有强氧化性。3、氯水的不稳定性—次氯酸不稳定。4、氯水的酸性—盐酸、次氯酸电离出H+。5、氯水的成份:分子(H2O Cl2 HCl0)
离子(H+ Cl- ClO- )25 漂白性的比较名称原理实质程度范围过氧化钠氯 水将有色的色素
氧化为稳定的
无色物质 氯水中的次氯酸将有色物质氧化成无色物质氧化作用 氧化作用永久性 永久性 漂白大多数有色物质 漂白大多数有色物质,能使紫色石蕊试液褪色活性炭吸附有色
色素物理吸附261、下列关于氯水的说法中正确的是:
A、新制氯水中只含有Cl2和H2O分子
B、新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
C、光照氯水有气泡逸出,该气体是Cl2
D、氯水放置数天后酸性增强
2、下列物质能使红墨水褪色的是
A、活性炭 B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液
3、氯气能使湿润的蓝色石蕊试纸
A、褪色 B、变成红色
C、先褪色后变红 D、先变红后褪色
课堂练习DADD27想一想根据氯气与水的反应原理,推测氯气与NaOH能否发生反应?若反应,其产物是什么?4、氯气与碱反应2NaOH+Cl2=NaClO+NaCl+H2O有效成分:NaClO2 Ca(OH)2+2Cl2==Ca(ClO)2+CaCl2+2H2O漂白粉、漂粉精漂白液有效成分:Ca(ClO)2以上充分反应可得较多的Ca(ClO) 2 (制漂粉精)有毒的氯气尾气用NaOH溶液进行尾气吸收处理氯气与熟石灰反应的化学方程式:282Fe2+ + Cl2 == 2Fe3+ + 2Cl-
Cl2 + 2Br- == 2Cl- + Br2
Cl2 + 2 I- == 2Cl- + I2 2 == 2NaCl + Br2
2 == 2NaCl + I25、与盐溶液的反应与FeCl2 、NaBr、KI等盐溶液反应 2FeCl2 + Cl2 == 2FeCl3--- 氯气的强氧化性Cl2+ NaBr
Cl2+ NaI思考:根据上述实验,排出Cl2、Br2、I2的氧化性强弱顺序及Cl-、Br-、I-的还原性强弱顺序结论:氧化性:Cl2>Br2>I2
还原性:I->Br->Cl-29卤素单质的化学性质(见课本86页科学视野)①对比Cl2,写出Br2与 Na 、Fe 反应的化学方程式。 ②对比Cl2,写出F2 、Br2、I2与 H2 反应的化学方程式。 它们发生反应的条件相同吗? ③对比Cl2,写出Br2与 H2O 反应的化学方程式。 I2 +Fe=FeI2Br2+2Na=2NaBr
3Br2+2Fe=2FeBr330F2 冷暗处爆炸 H2+F2====2HF HF很稳定 Cl2 光照或点燃 H2+Cl2=====2HCl HCl稳定Br2 高温 H2+Br2======2HBr HBr较不稳定I2 高温、持续加热 H2+I2======2HI HI很不稳定
缓慢进行 卤素单质与氢气的反应结论: F Cl Br I 随核电荷数的增多,原子半径的增大
(1)卤素单质与H2化合的难易关系:F2 >Cl2> Br2> I 2(2)卤化氢的稳定性关系:HF > HCl > HBr > HI?还原性呢 314.已知常温下氯酸钾与浓盐酸反应放出氯气(卤素单质在溶液中的置换能力为:Cl2>Br2>I2,碘遇淀粉变蓝色,溴水显橙色),现按右图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )32解析:生成的氯气为黄绿色气体,氯气置换出的溴为橙色,置换出的碘遇淀粉变蓝色,氢氧化钠吸收氯气生成无色物质,而棉球还是显白色。
答案:A33Br2+ H2O=====HBr+HBrO反应越来越难以发生2F2+2H2O=====4HF+O2 (特例)Cl2 +H2O=====HCl+HClO卤素单质与水反应通式:X2 + H2O=====HX+HXO(X: Cl、Br、I)I2 +H2O=====HI+HIO34五、氯离子的检验实验:P85实验4-6无Cl-35(2)方法和结论:
在被检验的溶液中加入稀硝酸酸化,再滴入AgNO3溶液,若产生白色沉淀,则被检液中含有Cl-。
或 在被检验的溶液中滴入AgNO3溶液,若产生白色沉淀,再加入稀硝酸,沉淀不溶,则被检液中含有Cl-。(1)试剂AgNO3溶液、稀硝酸 稀硝酸—排除干扰离子CO32-等小结:氯离子(Cl-)的检验361、氯的原子结构和性质谢谢37
