第八章常见的酸碱盐基础练习—2021—2022学年九年级化学科粤版(2012)下册(word版有答案)
文档属性
| 名称 | 第八章常见的酸碱盐基础练习—2021—2022学年九年级化学科粤版(2012)下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 113.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-14 00:00:00 | ||
图片预览



文档简介
第八章常见的酸碱盐基础练习2021—2022学年九年级化学科粤版(2012)下册
一、单选题
1.小玲家的水稻出现了倒伏现象,急需施用的化肥是( )
A.CO(NH2)2 B.Ca3(PO4)2 C.K2SO4 D.NH4Cl
2.下列化学肥料中能促进植物生长,增强抗病虫害和抗倒伏能力的是
A.K2SO4 B.CO(NH2)2
C.NaNO3 D.NH4H2PO4
3.小深同学用思维导图梳理了Na2CO3 的相关知识,其中描述错误的是( )
A.A B.B C.C D.D
4.下列物质的用途,一定涉及化学变化的是
A.金具有黄色金属光泽 制作饰品
B.活性炭具有吸附性 作除味剂
C.生石灰吸收空气中的水分 作干燥剂
D.干冰升华吸收大量的热 作制冷剂
5.下列有关溶液的说法正确的是( )
A.均一、稳定的液体一定是溶液
B.稀释浓硫酸时,会放出大量的热
C.降低温度,不饱和溶液一定能变成饱和溶液
D.实验室利用氯化钠固体和水配制50g质量分数为6%的氯化钠溶液的步骤是:计算、量取、溶解、贮存
6.利用推理、归纳的方法得出以下结论,其中正确的是
A.金刚石、石墨是组成元素相同的单质,所以化学性质相似
B.氧化物中一定含有氧元素,所以含氧元素的化合物一定是氧化物
C.碱溶液pH>7,所以pH>7的溶液均为碱溶液
D.铁的金属活动性比铝弱,所以铁制品比铝制品更耐腐蚀
7.根据下列实验现象可以判断某溶液一定呈碱性的是( )
A.溶液中滴入石蕊仍为紫色
B.溶液中滴入酚酞显红色
C.溶液中滴入石蕊显红色
D.溶液中滴入酚酞不显色
8.室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
9.“庄稼一枝花,全靠肥当家”。下列关于农作物和化肥的说法正确的是( )
A.(NH4)2SO4属于复合肥料
B.农作物所必需的营养元素只有氮、磷和钾三种
C.磷肥能使作物根系发达,耐寒耐旱
D.铵态氮肥与熟石灰混合施用可以明显提高肥效
10.某固体可能含有,,,,中的一种或几种,现对其进行如下实验:
①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液;
②取少量上述溶液,加过量稀硫酸,有气泡产生;
③取②所得溶液少量,滴加溶液,产生白色沉淀.
分析以上实验现象,对原固体组成的推断正确的是( )
A.肯定有,;无,
B.肯定有;无,
C.肯定有,;无
D.肯定有;无,
二、简答题
11.自制汽水时,需要的原料有白糖、碳酸氢钠、柠檬酸、凉开水等。制作时会有大量气泡冒出,原因是 __________________________。
12.人体胃液的pH 通常在 0.9-1.5 之间,胃酸过多或过少,都会引起胃部不适根据所学知识回答下列问题。
(1)写出一个利用中和反应治疗人体内胃酸过多的化学方程式。
(2)有一些人因胃酸过少影响消化,你建议他应该多吃哪些食物?
13.工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:
(1)在① ③三个过程中,发生分解反应的是_____(填序号)。
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:
①在t1℃时,Na2CO3的溶解度是____g。
②t2℃时,NaCl的溶解度___Na2CO3的溶解度(填“大于”“等于”“小于”之一)。
③要从海水中提取NaCl,应采用的方法是___(填“蒸发结晶”或“降温结晶”)。
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是__g。
三、推断题
14.有A,B,C,D四种可溶性的物质,每种由以下两组中的离子构成。(每种离子只能选用一次)
阳离子
阴离子
四种物质之间的反应有如下现象:
(1)A+B→白色沉淀,不溶于稀硝酸。
(2)B+D→蓝色沉淀。
(3)C+B→白色沉淀,再加稀硝酸沉淀溶解并生成C。
由此可推知:A为_____,B为_____,C为_____,D为_____。(写化学式)
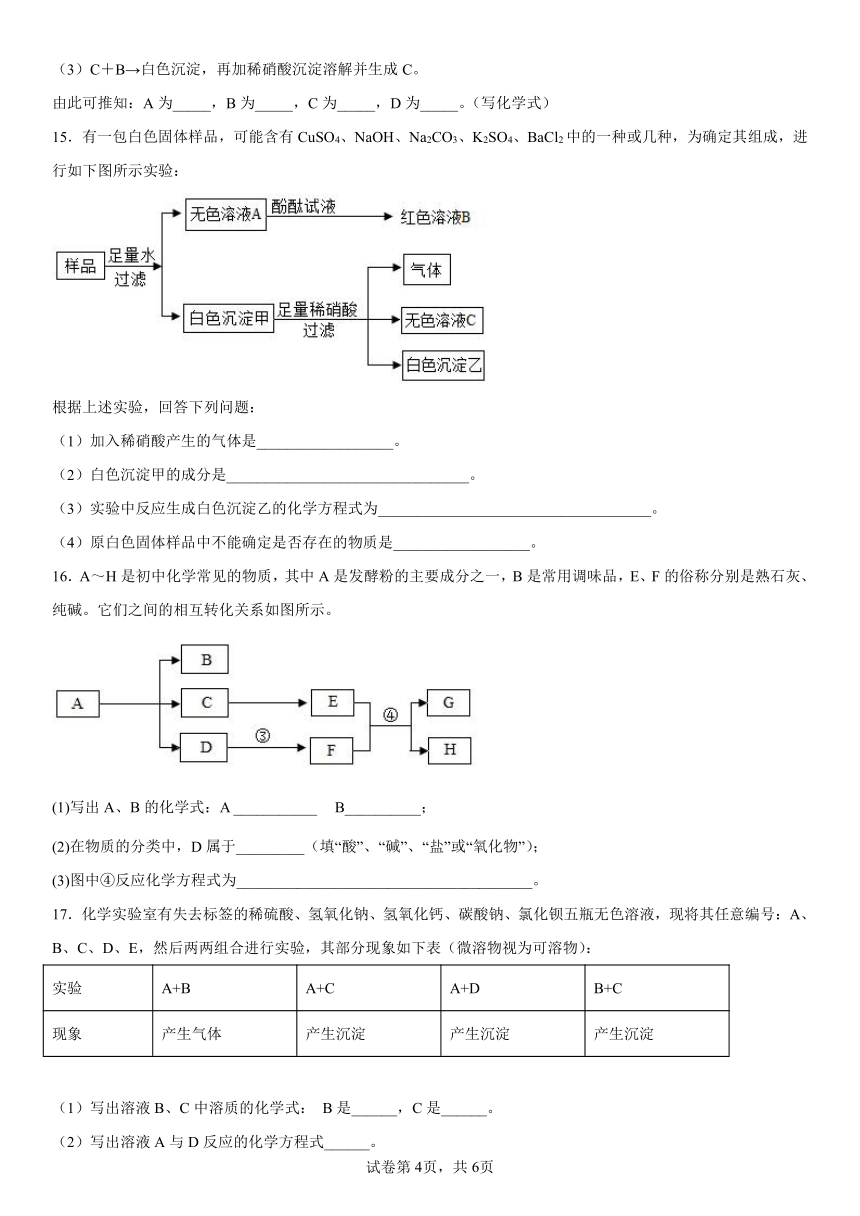
15.有一包白色固体样品,可能含有CuSO4、NaOH、Na2CO3、K2SO4、BaCl2中的一种或几种,为确定其组成,进行如下图所示实验:
根据上述实验,回答下列问题:
(1)加入稀硝酸产生的气体是__________________。
(2)白色沉淀甲的成分是________________________________。
(3)实验中反应生成白色沉淀乙的化学方程式为____________________________________。
(4)原白色固体样品中不能确定是否存在的物质是__________________。
16.A~H是初中化学常见的物质,其中A是发酵粉的主要成分之一,B是常用调味品,E、F的俗称分别是熟石灰、纯碱。它们之间的相互转化关系如图所示。
(1)写出A、B的化学式:A ___________ B__________;
(2)在物质的分类中,D属于_________(填“酸”、“碱”、“盐”或“氧化物”);
(3)图中④反应化学方程式为_______________________________________。
17.化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可溶物):
实验 A+B A+C A+D B+C
现象 产生气体 产生沉淀 产生沉淀 产生沉淀
(1)写出溶液B、C中溶质的化学式: B是______,C是______。
(2)写出溶液A与D反应的化学方程式______。
四、实验题
18.某兴趣小组的同学探究分子的运动,实验如图所示。图中试管A和装置D的试管中装有体积和浓度相同的浓氨水,试管B和C中装有体积和浓度相同的酚酞溶液。
(1)实验前,另取少量酚酞溶液,向其中滴加浓氨水,观察到酚酞溶液变红。这一操作的目的是 ________________________ 。
(2)实验①和实验②都会出现的现象是 _________ ,但出现此现象的快慢不同。
(3)从微观的角度解释产生上述现象快慢不同的原因是 __________________ 。
19.小林在凉拌紫卷心菜时,加入一些食醋,发现紫卷心菜变红了,激发了他的探究欲望,特邀你协助完成下列活动与探究。
[提出问题] 紫卷心菜等植物的汁液能作酸碱指示剂吗?
[实验探究] 取紫卷心菜、牵牛花的花瓣、胡萝卜,分别在研钵中捣烂,加入酒精(乙醇与水的体积比为1:1)浸泡,用纱布将浸泡出的汁液挤出,分别加入到蒸馏水、稀酸溶液和稀碱溶液中,有关颜色变化情况如下:
汁液 在不同液体中的颜色变化
蒸馏水 稀酸溶液 稀碱溶液
紫卷心菜 蓝紫色 红色 绿色
牵牛花 紫色 红色 蓝色
胡萝卜 橙色 橙色 橙色
[得出结论] ________、_______的汁液能做酸碱指示剂,_________的汁液不能做酸碱指示剂。
[拓展应用] 小林用上述的牵牛花汁液来测定某雨水样品的酸碱性,发现牵牛花汁液呈红色。
则该雨水呈_______性(选填“酸”或“碱”或“中”)。
[反思与评价] 小林发现,上述汁液无法测出溶液的酸碱度,请你告诉他,在实验室测定溶
液的酸碱度常用________________________。
五、计算题
20.如图是某化肥厂生产的碳酸氢铵的包装袋上的部分说明。
(1)避免高温天气施用的原因是___________(用化学方程式表示)。
(2)一袋该化肥中至少含有纯净的NH4HCO3的质量为______Kg(直接写出计算结果)。
21.实验室常用氢氧化钠溶液来吸收SO2,则吸收3.2g二氧化硫至少需要10%的氢氧化钠溶液的质量是多少?(写出计算过程)
22.常见的化肥的①尿素〔CO(NH2)2〕、②硝酸钾(KNO3)、③碳酸氢铵(NH4HCO3)、④硫酸钾(K2SO4)、⑤磷酸二氢钾(KH2PO4)等。
(1)以上五种肥料中属于复合肥的是_______(填数字序号)。
(2)工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应方程式为: ;要合成 90 吨尿素,需要二氧化碳多少吨?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.A
4.C
5.B
6.A
7.B
8.C
9.C
10.B
11.碳酸氢钠与柠檬酸在水中反应生成二氧化碳
12.(1)
(2)酸性食物,如橘子、酸奶等
13. ③ 18 小于 蒸发结晶 59
14. Na2SO4 Ba(OH)2 Mg(NO3)2 CuCl2
15. CO2 BaSO4、BaCO3 (写对一种得1分,多写不得分) NaOH
16. NaHCO3 NaCl 氧化物 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
17. H2SO4 BaCl2
18. 探究浓氨水和酚酞溶液接触是否有变化(变红) 酚酞溶液变红 D中氨水温度比B高,D中氨气分子运动速率比B快,所以C中酚酞溶液先变红。
19. 紫卷心菜 牵牛花 胡萝卜 酸 pH试纸或pH计
20.(1)
(2)39.5
21.40g
22.(1)②⑤
(2)设要合成 90 吨尿素,需要二氧化碳的质量为x,
x=66t
答:要合成 90 吨尿素,需要二氧化碳的质量为66t。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.小玲家的水稻出现了倒伏现象,急需施用的化肥是( )
A.CO(NH2)2 B.Ca3(PO4)2 C.K2SO4 D.NH4Cl
2.下列化学肥料中能促进植物生长,增强抗病虫害和抗倒伏能力的是
A.K2SO4 B.CO(NH2)2
C.NaNO3 D.NH4H2PO4
3.小深同学用思维导图梳理了Na2CO3 的相关知识,其中描述错误的是( )
A.A B.B C.C D.D
4.下列物质的用途,一定涉及化学变化的是
A.金具有黄色金属光泽 制作饰品
B.活性炭具有吸附性 作除味剂
C.生石灰吸收空气中的水分 作干燥剂
D.干冰升华吸收大量的热 作制冷剂
5.下列有关溶液的说法正确的是( )
A.均一、稳定的液体一定是溶液
B.稀释浓硫酸时,会放出大量的热
C.降低温度,不饱和溶液一定能变成饱和溶液
D.实验室利用氯化钠固体和水配制50g质量分数为6%的氯化钠溶液的步骤是:计算、量取、溶解、贮存
6.利用推理、归纳的方法得出以下结论,其中正确的是
A.金刚石、石墨是组成元素相同的单质,所以化学性质相似
B.氧化物中一定含有氧元素,所以含氧元素的化合物一定是氧化物
C.碱溶液pH>7,所以pH>7的溶液均为碱溶液
D.铁的金属活动性比铝弱,所以铁制品比铝制品更耐腐蚀
7.根据下列实验现象可以判断某溶液一定呈碱性的是( )
A.溶液中滴入石蕊仍为紫色
B.溶液中滴入酚酞显红色
C.溶液中滴入石蕊显红色
D.溶液中滴入酚酞不显色
8.室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
9.“庄稼一枝花,全靠肥当家”。下列关于农作物和化肥的说法正确的是( )
A.(NH4)2SO4属于复合肥料
B.农作物所必需的营养元素只有氮、磷和钾三种
C.磷肥能使作物根系发达,耐寒耐旱
D.铵态氮肥与熟石灰混合施用可以明显提高肥效
10.某固体可能含有,,,,中的一种或几种,现对其进行如下实验:
①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液;
②取少量上述溶液,加过量稀硫酸,有气泡产生;
③取②所得溶液少量,滴加溶液,产生白色沉淀.
分析以上实验现象,对原固体组成的推断正确的是( )
A.肯定有,;无,
B.肯定有;无,
C.肯定有,;无
D.肯定有;无,
二、简答题
11.自制汽水时,需要的原料有白糖、碳酸氢钠、柠檬酸、凉开水等。制作时会有大量气泡冒出,原因是 __________________________。
12.人体胃液的pH 通常在 0.9-1.5 之间,胃酸过多或过少,都会引起胃部不适根据所学知识回答下列问题。
(1)写出一个利用中和反应治疗人体内胃酸过多的化学方程式。
(2)有一些人因胃酸过少影响消化,你建议他应该多吃哪些食物?
13.工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:
(1)在① ③三个过程中,发生分解反应的是_____(填序号)。
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:
①在t1℃时,Na2CO3的溶解度是____g。
②t2℃时,NaCl的溶解度___Na2CO3的溶解度(填“大于”“等于”“小于”之一)。
③要从海水中提取NaCl,应采用的方法是___(填“蒸发结晶”或“降温结晶”)。
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是__g。
三、推断题
14.有A,B,C,D四种可溶性的物质,每种由以下两组中的离子构成。(每种离子只能选用一次)
阳离子
阴离子
四种物质之间的反应有如下现象:
(1)A+B→白色沉淀,不溶于稀硝酸。
(2)B+D→蓝色沉淀。
(3)C+B→白色沉淀,再加稀硝酸沉淀溶解并生成C。
由此可推知:A为_____,B为_____,C为_____,D为_____。(写化学式)
15.有一包白色固体样品,可能含有CuSO4、NaOH、Na2CO3、K2SO4、BaCl2中的一种或几种,为确定其组成,进行如下图所示实验:
根据上述实验,回答下列问题:
(1)加入稀硝酸产生的气体是__________________。
(2)白色沉淀甲的成分是________________________________。
(3)实验中反应生成白色沉淀乙的化学方程式为____________________________________。
(4)原白色固体样品中不能确定是否存在的物质是__________________。
16.A~H是初中化学常见的物质,其中A是发酵粉的主要成分之一,B是常用调味品,E、F的俗称分别是熟石灰、纯碱。它们之间的相互转化关系如图所示。
(1)写出A、B的化学式:A ___________ B__________;
(2)在物质的分类中,D属于_________(填“酸”、“碱”、“盐”或“氧化物”);
(3)图中④反应化学方程式为_______________________________________。
17.化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可溶物):
实验 A+B A+C A+D B+C
现象 产生气体 产生沉淀 产生沉淀 产生沉淀
(1)写出溶液B、C中溶质的化学式: B是______,C是______。
(2)写出溶液A与D反应的化学方程式______。
四、实验题
18.某兴趣小组的同学探究分子的运动,实验如图所示。图中试管A和装置D的试管中装有体积和浓度相同的浓氨水,试管B和C中装有体积和浓度相同的酚酞溶液。
(1)实验前,另取少量酚酞溶液,向其中滴加浓氨水,观察到酚酞溶液变红。这一操作的目的是 ________________________ 。
(2)实验①和实验②都会出现的现象是 _________ ,但出现此现象的快慢不同。
(3)从微观的角度解释产生上述现象快慢不同的原因是 __________________ 。
19.小林在凉拌紫卷心菜时,加入一些食醋,发现紫卷心菜变红了,激发了他的探究欲望,特邀你协助完成下列活动与探究。
[提出问题] 紫卷心菜等植物的汁液能作酸碱指示剂吗?
[实验探究] 取紫卷心菜、牵牛花的花瓣、胡萝卜,分别在研钵中捣烂,加入酒精(乙醇与水的体积比为1:1)浸泡,用纱布将浸泡出的汁液挤出,分别加入到蒸馏水、稀酸溶液和稀碱溶液中,有关颜色变化情况如下:
汁液 在不同液体中的颜色变化
蒸馏水 稀酸溶液 稀碱溶液
紫卷心菜 蓝紫色 红色 绿色
牵牛花 紫色 红色 蓝色
胡萝卜 橙色 橙色 橙色
[得出结论] ________、_______的汁液能做酸碱指示剂,_________的汁液不能做酸碱指示剂。
[拓展应用] 小林用上述的牵牛花汁液来测定某雨水样品的酸碱性,发现牵牛花汁液呈红色。
则该雨水呈_______性(选填“酸”或“碱”或“中”)。
[反思与评价] 小林发现,上述汁液无法测出溶液的酸碱度,请你告诉他,在实验室测定溶
液的酸碱度常用________________________。
五、计算题
20.如图是某化肥厂生产的碳酸氢铵的包装袋上的部分说明。
(1)避免高温天气施用的原因是___________(用化学方程式表示)。
(2)一袋该化肥中至少含有纯净的NH4HCO3的质量为______Kg(直接写出计算结果)。
21.实验室常用氢氧化钠溶液来吸收SO2,则吸收3.2g二氧化硫至少需要10%的氢氧化钠溶液的质量是多少?(写出计算过程)
22.常见的化肥的①尿素〔CO(NH2)2〕、②硝酸钾(KNO3)、③碳酸氢铵(NH4HCO3)、④硫酸钾(K2SO4)、⑤磷酸二氢钾(KH2PO4)等。
(1)以上五种肥料中属于复合肥的是_______(填数字序号)。
(2)工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应方程式为: ;要合成 90 吨尿素,需要二氧化碳多少吨?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.A
4.C
5.B
6.A
7.B
8.C
9.C
10.B
11.碳酸氢钠与柠檬酸在水中反应生成二氧化碳
12.(1)
(2)酸性食物,如橘子、酸奶等
13. ③ 18 小于 蒸发结晶 59
14. Na2SO4 Ba(OH)2 Mg(NO3)2 CuCl2
15. CO2 BaSO4、BaCO3 (写对一种得1分,多写不得分) NaOH
16. NaHCO3 NaCl 氧化物 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
17. H2SO4 BaCl2
18. 探究浓氨水和酚酞溶液接触是否有变化(变红) 酚酞溶液变红 D中氨水温度比B高,D中氨气分子运动速率比B快,所以C中酚酞溶液先变红。
19. 紫卷心菜 牵牛花 胡萝卜 酸 pH试纸或pH计
20.(1)
(2)39.5
21.40g
22.(1)②⑤
(2)设要合成 90 吨尿素,需要二氧化碳的质量为x,
x=66t
答:要合成 90 吨尿素,需要二氧化碳的质量为66t。
答案第1页,共2页
答案第1页,共2页
