【人教版】化学九年级全一册 第十一单元 盐 化肥 达标测试卷(课件版)
文档属性
| 名称 | 【人教版】化学九年级全一册 第十一单元 盐 化肥 达标测试卷(课件版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-15 00:00:00 | ||
图片预览










文档简介
(共37张PPT)
第十一单元达标测试卷
(时间:60分钟 满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Ca-40 Cu-64
Zn-65
一、 选择题(本大题包括15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一个是正确的)
1. 下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )
A. NaCl B. NaOH C. NaHCO3 D. Na2SO4
C
2. 李阿姨种植的盆栽近期叶片发黄,查询后发现是缺氮所致。李阿姨可在盆栽中适量施用 ( )
A. Ca(H2PO4)2
B. K2SO4
C. NH4NO3
D. KH2PO4
C
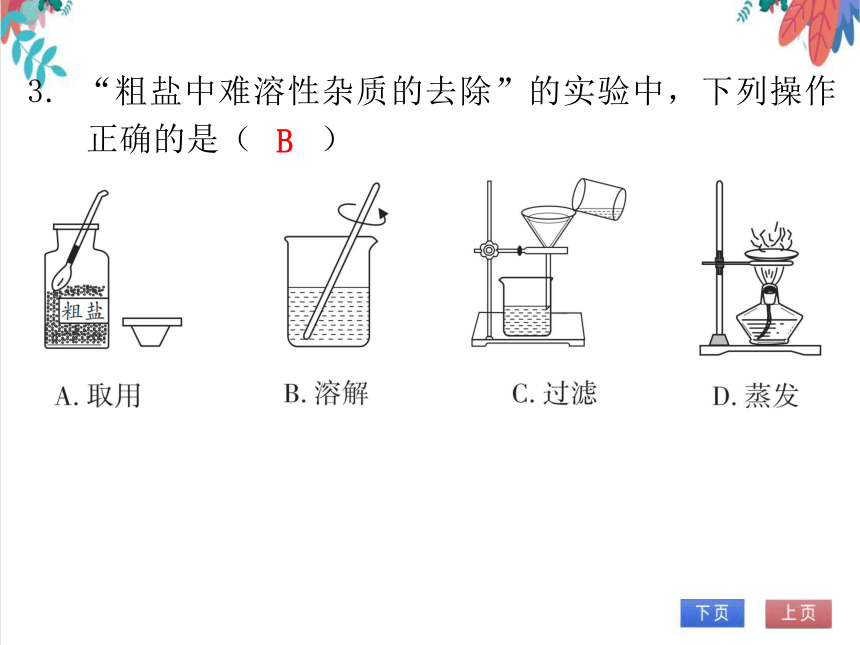
3. “粗盐中难溶性杂质的去除”的实验中,下列操作正确的是( )
B
4. 下列说法正确的是( )
A. NaHCO3俗称苏打
B. CaCO3可用作补钙剂
C. Na2CO3俗称火碱
D. K2CO3属于复合肥
D
5. 下列关于物质用途的说法中,错误的是( )
A. 亚硝酸钠用于烹调
B. 盐酸用于金属表面除锈
C. 碳酸氢钠用于焙制糕点
D. 熟石灰用于改良酸性土壤
A
6. 下列有关粗盐提纯实验说法错误的是( )
A. 溶解粗盐时,应加入适量的水,以提高实验效率
B. 过滤时,为加快过滤速度,可用玻璃棒在漏斗内搅拌
C. 蒸发滤液时,待蒸发皿中出现较多固体时,停止加热
D. 蒸发结束后,用玻璃棒将固体转移到指定的容器中
B
7. 下列各组物质在水溶液中能大量共存,且溶液为无色的是( )
A. Na2CO3、KNO3、NaCl
B. Na2SO4、KCl、Fe(NO3)3
C. Na2CO3、BaCl2、NaNO3
D. AgNO3、NaCl、CuSO4
A
8. 下列各组物质的水溶液,不用其他试剂就能鉴别出来的是( )
A. KNO3、HCl、Na2SO4、BaCl2
B. NaNO3、KCl、CuSO4、Ba(OH)2
C. HCl、Ca(OH)2、NaOH、HNO3
D. Ba(NO3)2、H2SO4、NaOH、MgSO4
D
9. 下列各组物质鉴别方案的描述,错误的是( )
A. KNO3、Na2SO4、Ba(OH)2、MgCl2四种溶液,需另加试剂方可鉴别
B. MgCl2、HCl、KOH、NaCl四种溶液,利用组内物质即可鉴别
C. Na2CO3、NH4NO3、NaOH、NaCl四种固体,利用水及组内物质都无法鉴别
D . NaCl、NaOH、CaO、CuSO4四种固体,只用适量水即可鉴别
B
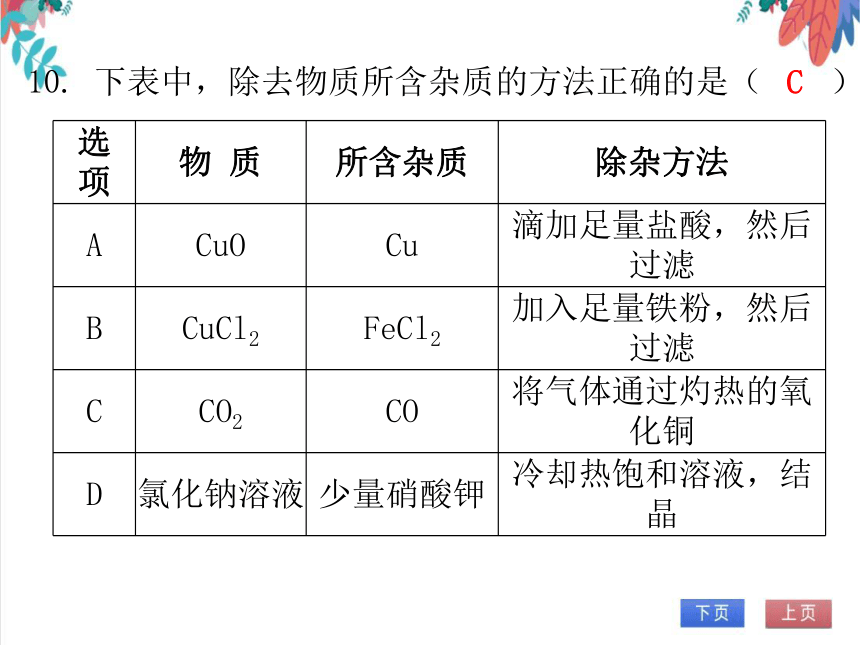
10. 下表中,除去物质所含杂质的方法正确的是( )
C
选 项 物 质 所含杂质 除杂方法
A CuO Cu 滴加足量盐酸,然后过滤
B CuCl2 FeCl2 加入足量铁粉,然后过滤
C CO2 CO 将气体通过灼热的氧化铜
D 氯化钠溶液 少量硝酸钾 冷却热饱和溶液,结晶
11. 归纳推理是一种重要的化学思维方法。下列归纳推理正确的是( )
A. 碱溶液能使酚酞溶液变红,那么能使酚酞溶液变红的溶液一定是碱溶液
B. 复分解反应只是两种化合物相互交换成分,则复分解反应一定没有化合价的改变
C. 氢氧化铜和氢氧化钠都含有氢氧根离子,故它们都能使无色酚酞试液变红色
D. 一氧化碳和二氧化碳的组成元素相同,所以CO与NaOH溶液反应也能生成盐和水
B
12. 某同学为除去食盐水中的Na2SO4杂质,进行了以下实验:
下列有关说法错误的是( )
A. X为BaCl2溶液 B. Y为Na2CO3
C. Z为稀盐酸 D. 步骤②与④可交换
D
13. 化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
C
选 项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
14. 向一定量盐酸和氯化钙混合溶液中逐滴加入碳酸钠溶液,用数字化实验设备测得溶液pH变化情况如图。下列有关说法错误的是( )
A. AB段反应现象为有气泡产生
B. BC段反应现象为有白色沉淀生成
C. CD段溶液中含有的溶质为碳酸钠和氯化钙
D. CD段溶液pH大于7是因碳酸钠溶液显碱性
C
15. 下列各图象中有关量的变化趋势与选项要求相符合的是( )
A. 向含有NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量
B. 向等质量的锌粉、镁粉中分别加入少量的相同浓度相同质量的稀硫酸
C. 向一定浓度的NaOH溶液中加入水
D. 向一定质量的镁粉和银粉固体混合物中逐滴加入Cu(NO3)2溶液
B
二、 填空题(本大题包括2小题,共15分)
16. (7分)(1)尿素[CO(NH2)2]是农业生产中常用的一种优质肥料。它由____________种元素组成;其中氢、氧元素的质量比为____________;它属于化学肥料中的____________肥。
(2)如图是某化肥包装袋上的部分说明:
①碳酸氢铵属于化学肥料中的____________(填字母);
A. 钾肥 B. 氮肥
C. 磷肥 D. 复合肥
四
1∶4
氮
B
②碳酸氢铵应具有的性质是_______(填字母);
A. 易溶于水 B. 有挥发性 C. 受热易分解
③碳酸氢铵与熟石灰反应的化学方程式为NH4HCO3+Ca(OH)2 === CaCO3+2X+NH3↑,则X的化学式是_______;施用该类肥料时,要避免与_______(填“酸”或“碱”)性物质混用,否则会减低肥效。
AC
H2O
碱
17. (8分)向Ba(OH)2溶液中滴入Na2CO3溶液至恰好完全反应。
(1)反应的化学方程式是
____________________________________________。
(2)可以观察到的实验现象是_____________________。
(3)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。__________;__________;___________。(填离子符号)
Ba(OH)2+Na2CO3=== BaCO3↓+2NaOH
产生白色沉淀
OH-
Ba2+
Na+
(4)下列物质中能与Ba(OH)2溶液反应产生沉淀的是___________和___________。
A. NaNO3 B. HCl
C. MgCl2 D. (NH4)2SO4
C
D
三、 实验题(本大题包括2小题,共20分)
18. (10分)在日常生活和工农业生产中,溶液有着广泛的应用。
Ⅰ. 在农业上通常用12%的氯化钠溶液选种。实验室欲配制该质量分数的溶液60 g,操作如图,请回答下列问题:
(1)请用图中的序号表示配制溶液的正确操作顺序_________________。
(2)认真观察②,其中的错误操作是_______________。若不进行改正,其他操作步骤正确,则所配溶液的溶质的质量分数___________(填“大于”“小于”或“等于”)10%。
(3)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应___________。
A. 增加适量氯化钠固体
B. 减少适量氯化钠固体
C. 调节平衡螺母
④②①⑤③
药品和砝码放反了
小于
B
(4)若配制所得的氯化钠溶液溶质质量分数偏小,可能的原因是___________。
A. 用量筒量取水时俯视读数
B. 烧杯用蒸馏水润洗后未等晾干就配制溶液
C. 天平指针偏右就开始称量
D. 转移已配好的溶液时,有少量溶液溅出
E. 转移已称好的氯化钠固体时,部分洒落在烧杯外
BE
Ⅱ. 如图是粗盐提纯实验的部分操作,请回答相关问题。
(1)如图所示操作中,有错误的是___________(填字母)。
(2)改正错误后,粗盐提纯的正确操作顺序为___________(填字母)。
C
DACB
(3)操作B中,玻璃棒的作用是____________________
_______________________________,当_________________时,即停止加热。
(4)步骤D中称取10. 0 g粗盐,将该粗盐逐渐加入盛有10 mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐为2. 0 g,最终得到NaCl晶体6. 4 g,该实验精盐的产率是____________。
搅拌,使溶液均匀受热,防止局部温度过热造成液滴飞溅
出现大量固体
80%
19. (10分)小芳对复分解反应发生的条件产生兴趣,于是她和小组内同学仅用以下药品展开了探究。
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、氯化钠溶液、酚酞试液。
【提出问题】复分解反应发生的条件是什么?
【查阅资料】硝酸钡溶液显中性,且Ba2+有毒。
【实验探究】小芳用上述物质做了下列几组实验:
组合序号 ① ② ③ ④ ⑤ ⑥
组合物质 稀盐酸氯化钠 稀盐酸氢氧化钠 稀盐酸碳酸钠 稀硫酸硝酸钡 氯化钠硝酸钡 硝酸钡碳酸钠
【记录和解释】
(1)组合①②⑤均无明显现象,其中组合___________与另外两组的实质不同。为证明该不同之处,小芳在实验过程中使用了酚酞试液。
(2)请写出组合⑥的化学方程式
____________________________________________。
【实验结论】他们通过实验探究并请教老师后知道,只有当两种化合物互相交换成分,生成物中有________________生成时,复分解反应才可以发生。
②
Na2CO3+Ba(NO3)2=== BaCO3↓+2NaNO3
沉淀或气体或水
【拓展延伸】实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。为了确定沉淀和清液的成分,继续展开探究。
【实验1】探究沉淀的成分。
【提出猜想】Ⅰ. 沉淀只有硫酸钡;Ⅱ._____________;Ⅲ. 沉淀中含有硫酸钡和碳酸钡。
【实验探究】小莲取少量沉淀于试管中,滴加过量的_________________________________(请补充完整实验操作和观察到的现象),证明了猜想Ⅲ是正确的。
沉淀只有碳酸钡
稀盐酸,沉淀部分溶解,有气泡产生
【实验2】探究清液的成分。①取少量清液于试管中,向其中滴加硝酸钡溶液,无明显现象。②另取少量清液于另一只试管中,滴加____________________
_______,有白色沉淀产生。
【解释与结论】探究活动结束后,小组内成员通过讨论分析,一致认为清液中一定没有的离子是_______________________________(指示剂除外,且不考虑水的电离)。
【处理废液】为了防止污染环境,小芳对废液进行处理,将固体回收进一步处理,溶液排放。
稀硫酸(或Na2CO3溶液)
OH-、 CO32-、 SO42-、 H+
【交流与反思】根据你对复分解反应发生条件的了解,请写出一个题中实验药品间除①~⑥组合之外,能发生复分解反应的化学方程式______________________________________________________________________________________。
H2SO4+2NaOH=== Na2SO4+2H2O(或H2SO4+Na2CO3=== Na2SO4+H2O+CO2↑)
四、 综合能力题(本大题包括1小题,共10分)
20. (10分)现有一瓶NaCl样品(杂质为CaCl2、MgSO4),实验兴趣小组按如图流程进行得到精盐(纯氯化钠晶体)。
(1)操作Ⅰ和操作Ⅱ的名称为___________。
(2)加入过量Ba(OH)2溶液的目的是
____________________________________________(用化学方程式表示)。
(3)加入过量Na2CO3溶液的目的是__________________
_______________。
(4)小组成员猜测滤液Ⅱ的成分,认为除了氯化钠外还一定含有两种杂质__________________(填化学式),请你设计合理的实验方案,通过实验步骤与现象验证他们的猜测是正确的。
过滤
MgSO4+Ba(OH)2=== BaSO4↓+Mg(OH)2↓
除去CaCl2和过量的Ba(OH)2
Na2CO3、 NaOH
(5)加入盐酸发生反应的化学方程式为
________________________________________________________________________________________(写一个即可)。
(6)提纯后得到的精盐质量_________(填“>”“<”或“=”)样品中氯化钠的质量。
实验步骤 实验现象 实验结论
①取滤液Ⅱ少量于试管中,向其中加入过量_________________溶液 有白色沉淀产生 结论正确
②向步骤①所得上层清液中加酚酞试液 _____________ NaOH+HCl=== NaCl+H2O(或Na2CO3+2HCl=== 2NaCl+H2O+CO2↑)
>
溶液变红
CaCl2(或BaCl2)
五、 计算题(本大题包括1小题,共10分)
21. (10分)现有 H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计了如图实验方案:(注:硫酸铜溶液略显酸性)
(1) c点混合溶液与NaOH恰好反应完全,此点溶液中的溶质为___________(写化学式)。
(2) 与硫酸铜溶液反应的氢氧化钠溶液的质量为___________g;请计算该混合溶液中 CuSO4的溶质质量分数(写出计算过程)。
Na2SO4
50
解:设该混合溶液中的 CuSO4的溶质质量分数为x。
CuSO4+2NaOH=== Na2SO4+Cu(OH)2↓
160 80
100 gx 50 g×16%
x=16%
答:该混合溶液中的 CuSO4的溶质质量分数为16%。
(3) 若在100 g混合溶液中不断加入上述氢氧化钠的溶液,请你画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图。
(4) 该实验方案能证明硫酸和氢氧化钠发生了中和反应的原因是_________________________________。
开始加入氢氧化钠没有沉淀生成
谢谢!
第十一单元达标测试卷
(时间:60分钟 满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Ca-40 Cu-64
Zn-65
一、 选择题(本大题包括15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一个是正确的)
1. 下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )
A. NaCl B. NaOH C. NaHCO3 D. Na2SO4
C
2. 李阿姨种植的盆栽近期叶片发黄,查询后发现是缺氮所致。李阿姨可在盆栽中适量施用 ( )
A. Ca(H2PO4)2
B. K2SO4
C. NH4NO3
D. KH2PO4
C
3. “粗盐中难溶性杂质的去除”的实验中,下列操作正确的是( )
B
4. 下列说法正确的是( )
A. NaHCO3俗称苏打
B. CaCO3可用作补钙剂
C. Na2CO3俗称火碱
D. K2CO3属于复合肥
D
5. 下列关于物质用途的说法中,错误的是( )
A. 亚硝酸钠用于烹调
B. 盐酸用于金属表面除锈
C. 碳酸氢钠用于焙制糕点
D. 熟石灰用于改良酸性土壤
A
6. 下列有关粗盐提纯实验说法错误的是( )
A. 溶解粗盐时,应加入适量的水,以提高实验效率
B. 过滤时,为加快过滤速度,可用玻璃棒在漏斗内搅拌
C. 蒸发滤液时,待蒸发皿中出现较多固体时,停止加热
D. 蒸发结束后,用玻璃棒将固体转移到指定的容器中
B
7. 下列各组物质在水溶液中能大量共存,且溶液为无色的是( )
A. Na2CO3、KNO3、NaCl
B. Na2SO4、KCl、Fe(NO3)3
C. Na2CO3、BaCl2、NaNO3
D. AgNO3、NaCl、CuSO4
A
8. 下列各组物质的水溶液,不用其他试剂就能鉴别出来的是( )
A. KNO3、HCl、Na2SO4、BaCl2
B. NaNO3、KCl、CuSO4、Ba(OH)2
C. HCl、Ca(OH)2、NaOH、HNO3
D. Ba(NO3)2、H2SO4、NaOH、MgSO4
D
9. 下列各组物质鉴别方案的描述,错误的是( )
A. KNO3、Na2SO4、Ba(OH)2、MgCl2四种溶液,需另加试剂方可鉴别
B. MgCl2、HCl、KOH、NaCl四种溶液,利用组内物质即可鉴别
C. Na2CO3、NH4NO3、NaOH、NaCl四种固体,利用水及组内物质都无法鉴别
D . NaCl、NaOH、CaO、CuSO4四种固体,只用适量水即可鉴别
B
10. 下表中,除去物质所含杂质的方法正确的是( )
C
选 项 物 质 所含杂质 除杂方法
A CuO Cu 滴加足量盐酸,然后过滤
B CuCl2 FeCl2 加入足量铁粉,然后过滤
C CO2 CO 将气体通过灼热的氧化铜
D 氯化钠溶液 少量硝酸钾 冷却热饱和溶液,结晶
11. 归纳推理是一种重要的化学思维方法。下列归纳推理正确的是( )
A. 碱溶液能使酚酞溶液变红,那么能使酚酞溶液变红的溶液一定是碱溶液
B. 复分解反应只是两种化合物相互交换成分,则复分解反应一定没有化合价的改变
C. 氢氧化铜和氢氧化钠都含有氢氧根离子,故它们都能使无色酚酞试液变红色
D. 一氧化碳和二氧化碳的组成元素相同,所以CO与NaOH溶液反应也能生成盐和水
B
12. 某同学为除去食盐水中的Na2SO4杂质,进行了以下实验:
下列有关说法错误的是( )
A. X为BaCl2溶液 B. Y为Na2CO3
C. Z为稀盐酸 D. 步骤②与④可交换
D
13. 化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
C
选 项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
14. 向一定量盐酸和氯化钙混合溶液中逐滴加入碳酸钠溶液,用数字化实验设备测得溶液pH变化情况如图。下列有关说法错误的是( )
A. AB段反应现象为有气泡产生
B. BC段反应现象为有白色沉淀生成
C. CD段溶液中含有的溶质为碳酸钠和氯化钙
D. CD段溶液pH大于7是因碳酸钠溶液显碱性
C
15. 下列各图象中有关量的变化趋势与选项要求相符合的是( )
A. 向含有NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量
B. 向等质量的锌粉、镁粉中分别加入少量的相同浓度相同质量的稀硫酸
C. 向一定浓度的NaOH溶液中加入水
D. 向一定质量的镁粉和银粉固体混合物中逐滴加入Cu(NO3)2溶液
B
二、 填空题(本大题包括2小题,共15分)
16. (7分)(1)尿素[CO(NH2)2]是农业生产中常用的一种优质肥料。它由____________种元素组成;其中氢、氧元素的质量比为____________;它属于化学肥料中的____________肥。
(2)如图是某化肥包装袋上的部分说明:
①碳酸氢铵属于化学肥料中的____________(填字母);
A. 钾肥 B. 氮肥
C. 磷肥 D. 复合肥
四
1∶4
氮
B
②碳酸氢铵应具有的性质是_______(填字母);
A. 易溶于水 B. 有挥发性 C. 受热易分解
③碳酸氢铵与熟石灰反应的化学方程式为NH4HCO3+Ca(OH)2 === CaCO3+2X+NH3↑,则X的化学式是_______;施用该类肥料时,要避免与_______(填“酸”或“碱”)性物质混用,否则会减低肥效。
AC
H2O
碱
17. (8分)向Ba(OH)2溶液中滴入Na2CO3溶液至恰好完全反应。
(1)反应的化学方程式是
____________________________________________。
(2)可以观察到的实验现象是_____________________。
(3)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。__________;__________;___________。(填离子符号)
Ba(OH)2+Na2CO3=== BaCO3↓+2NaOH
产生白色沉淀
OH-
Ba2+
Na+
(4)下列物质中能与Ba(OH)2溶液反应产生沉淀的是___________和___________。
A. NaNO3 B. HCl
C. MgCl2 D. (NH4)2SO4
C
D
三、 实验题(本大题包括2小题,共20分)
18. (10分)在日常生活和工农业生产中,溶液有着广泛的应用。
Ⅰ. 在农业上通常用12%的氯化钠溶液选种。实验室欲配制该质量分数的溶液60 g,操作如图,请回答下列问题:
(1)请用图中的序号表示配制溶液的正确操作顺序_________________。
(2)认真观察②,其中的错误操作是_______________。若不进行改正,其他操作步骤正确,则所配溶液的溶质的质量分数___________(填“大于”“小于”或“等于”)10%。
(3)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应___________。
A. 增加适量氯化钠固体
B. 减少适量氯化钠固体
C. 调节平衡螺母
④②①⑤③
药品和砝码放反了
小于
B
(4)若配制所得的氯化钠溶液溶质质量分数偏小,可能的原因是___________。
A. 用量筒量取水时俯视读数
B. 烧杯用蒸馏水润洗后未等晾干就配制溶液
C. 天平指针偏右就开始称量
D. 转移已配好的溶液时,有少量溶液溅出
E. 转移已称好的氯化钠固体时,部分洒落在烧杯外
BE
Ⅱ. 如图是粗盐提纯实验的部分操作,请回答相关问题。
(1)如图所示操作中,有错误的是___________(填字母)。
(2)改正错误后,粗盐提纯的正确操作顺序为___________(填字母)。
C
DACB
(3)操作B中,玻璃棒的作用是____________________
_______________________________,当_________________时,即停止加热。
(4)步骤D中称取10. 0 g粗盐,将该粗盐逐渐加入盛有10 mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐为2. 0 g,最终得到NaCl晶体6. 4 g,该实验精盐的产率是____________。
搅拌,使溶液均匀受热,防止局部温度过热造成液滴飞溅
出现大量固体
80%
19. (10分)小芳对复分解反应发生的条件产生兴趣,于是她和小组内同学仅用以下药品展开了探究。
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、氯化钠溶液、酚酞试液。
【提出问题】复分解反应发生的条件是什么?
【查阅资料】硝酸钡溶液显中性,且Ba2+有毒。
【实验探究】小芳用上述物质做了下列几组实验:
组合序号 ① ② ③ ④ ⑤ ⑥
组合物质 稀盐酸氯化钠 稀盐酸氢氧化钠 稀盐酸碳酸钠 稀硫酸硝酸钡 氯化钠硝酸钡 硝酸钡碳酸钠
【记录和解释】
(1)组合①②⑤均无明显现象,其中组合___________与另外两组的实质不同。为证明该不同之处,小芳在实验过程中使用了酚酞试液。
(2)请写出组合⑥的化学方程式
____________________________________________。
【实验结论】他们通过实验探究并请教老师后知道,只有当两种化合物互相交换成分,生成物中有________________生成时,复分解反应才可以发生。
②
Na2CO3+Ba(NO3)2=== BaCO3↓+2NaNO3
沉淀或气体或水
【拓展延伸】实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。为了确定沉淀和清液的成分,继续展开探究。
【实验1】探究沉淀的成分。
【提出猜想】Ⅰ. 沉淀只有硫酸钡;Ⅱ._____________;Ⅲ. 沉淀中含有硫酸钡和碳酸钡。
【实验探究】小莲取少量沉淀于试管中,滴加过量的_________________________________(请补充完整实验操作和观察到的现象),证明了猜想Ⅲ是正确的。
沉淀只有碳酸钡
稀盐酸,沉淀部分溶解,有气泡产生
【实验2】探究清液的成分。①取少量清液于试管中,向其中滴加硝酸钡溶液,无明显现象。②另取少量清液于另一只试管中,滴加____________________
_______,有白色沉淀产生。
【解释与结论】探究活动结束后,小组内成员通过讨论分析,一致认为清液中一定没有的离子是_______________________________(指示剂除外,且不考虑水的电离)。
【处理废液】为了防止污染环境,小芳对废液进行处理,将固体回收进一步处理,溶液排放。
稀硫酸(或Na2CO3溶液)
OH-、 CO32-、 SO42-、 H+
【交流与反思】根据你对复分解反应发生条件的了解,请写出一个题中实验药品间除①~⑥组合之外,能发生复分解反应的化学方程式______________________________________________________________________________________。
H2SO4+2NaOH=== Na2SO4+2H2O(或H2SO4+Na2CO3=== Na2SO4+H2O+CO2↑)
四、 综合能力题(本大题包括1小题,共10分)
20. (10分)现有一瓶NaCl样品(杂质为CaCl2、MgSO4),实验兴趣小组按如图流程进行得到精盐(纯氯化钠晶体)。
(1)操作Ⅰ和操作Ⅱ的名称为___________。
(2)加入过量Ba(OH)2溶液的目的是
____________________________________________(用化学方程式表示)。
(3)加入过量Na2CO3溶液的目的是__________________
_______________。
(4)小组成员猜测滤液Ⅱ的成分,认为除了氯化钠外还一定含有两种杂质__________________(填化学式),请你设计合理的实验方案,通过实验步骤与现象验证他们的猜测是正确的。
过滤
MgSO4+Ba(OH)2=== BaSO4↓+Mg(OH)2↓
除去CaCl2和过量的Ba(OH)2
Na2CO3、 NaOH
(5)加入盐酸发生反应的化学方程式为
________________________________________________________________________________________(写一个即可)。
(6)提纯后得到的精盐质量_________(填“>”“<”或“=”)样品中氯化钠的质量。
实验步骤 实验现象 实验结论
①取滤液Ⅱ少量于试管中,向其中加入过量_________________溶液 有白色沉淀产生 结论正确
②向步骤①所得上层清液中加酚酞试液 _____________ NaOH+HCl=== NaCl+H2O(或Na2CO3+2HCl=== 2NaCl+H2O+CO2↑)
>
溶液变红
CaCl2(或BaCl2)
五、 计算题(本大题包括1小题,共10分)
21. (10分)现有 H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计了如图实验方案:(注:硫酸铜溶液略显酸性)
(1) c点混合溶液与NaOH恰好反应完全,此点溶液中的溶质为___________(写化学式)。
(2) 与硫酸铜溶液反应的氢氧化钠溶液的质量为___________g;请计算该混合溶液中 CuSO4的溶质质量分数(写出计算过程)。
Na2SO4
50
解:设该混合溶液中的 CuSO4的溶质质量分数为x。
CuSO4+2NaOH=== Na2SO4+Cu(OH)2↓
160 80
100 gx 50 g×16%
x=16%
答:该混合溶液中的 CuSO4的溶质质量分数为16%。
(3) 若在100 g混合溶液中不断加入上述氢氧化钠的溶液,请你画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图。
(4) 该实验方案能证明硫酸和氢氧化钠发生了中和反应的原因是_________________________________。
开始加入氢氧化钠没有沉淀生成
谢谢!
同课章节目录
