【人教版】化学九年级全一册 第五单元 化学方程式 达标测试卷(课件版)
文档属性
| 名称 | 【人教版】化学九年级全一册 第五单元 化学方程式 达标测试卷(课件版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-15 00:00:00 | ||
图片预览










文档简介
(共35张PPT)
第五单元达标测试卷
(时间:60分钟 满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Ca-40
一、选择题(本大题包括15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一个是正确的)
1. 化学反应前后,可能发生变化的是( )
A. 分子数目
B. 质子数
C. 原子种类
D. 物质的总质量
A
2. 下列现象,能用质量守恒定律解释的是( )
A. 10 g蔗糖溶于水,总质量变大
B. 镁条燃烧后,生成白色固体的质量比原来镁条的质量增加了
C. 湿衣服晒干后,质量减小
D. 100 mL水与100 mL酒精混合后,总体积小于200 mL
B
3. 下列关于化学方程式2H2O 2H2↑+O2↑的叙述中,正确的是( )
A. 水等于氢气和氧气
B. 2个水分子生成2个氢气和1个氧气
C. 水在通电条件下分解生成氢气和氧气
D. 每2份质量的水在通电条件下生成2份质量的氢气和1份质量的氧气
C
4. 在A+3B=== 2C+2D中,已知1.4 g A跟4.8 g B恰好完全反应生成4.4 g C。又知D的相对分子质量为18,则A的相对分子质量为( )
A. 44
B. 28
C. 23
D. 14
B
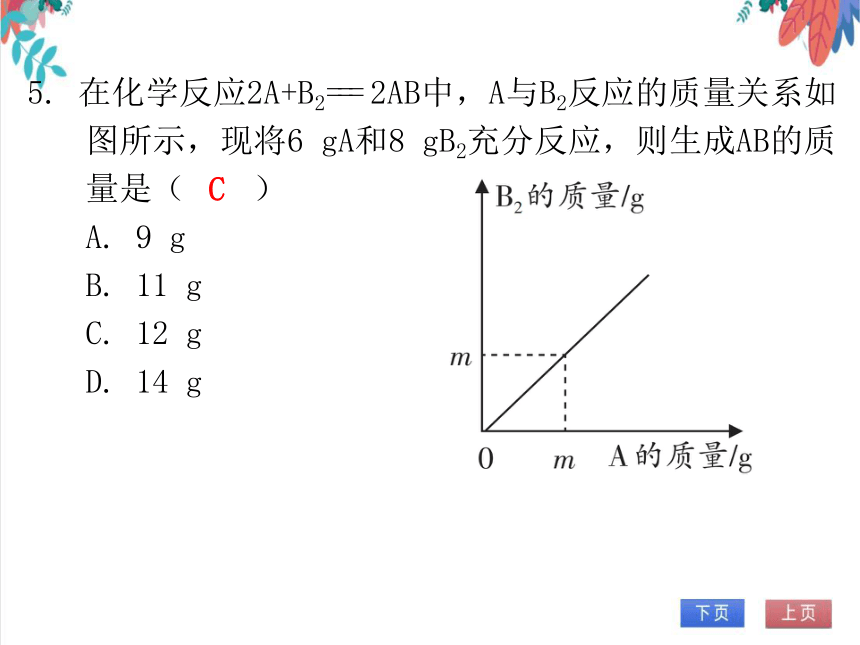
5. 在化学反应2A+B2=== 2AB中,A与B2反应的质量关系如图所示,现将6 gA和8 gB2充分反应,则生成AB的质量是( )
A. 9 g
B. 11 g
C. 12 g
D. 14 g
C
6. 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,具有强氧化性,可发生反应:6ClO2+16NH3=== 5N2+6NH4Cl+12X。则X的化学式为( )
A. H2
B. O2
C. H2O
D. H2O2
C
7. 下列说法正确的是( )
A. 化学方程式的配平是为了遵守质量守恒定律
B. 配平化学方程式,有时也可改变化学式中各组成元素右下角的数字
C. 原子团在化学反应中是不可以拆分的
D. 化学方程式中的↑表示生成物是气体,所以生成物中只要有气体必须标↑
A
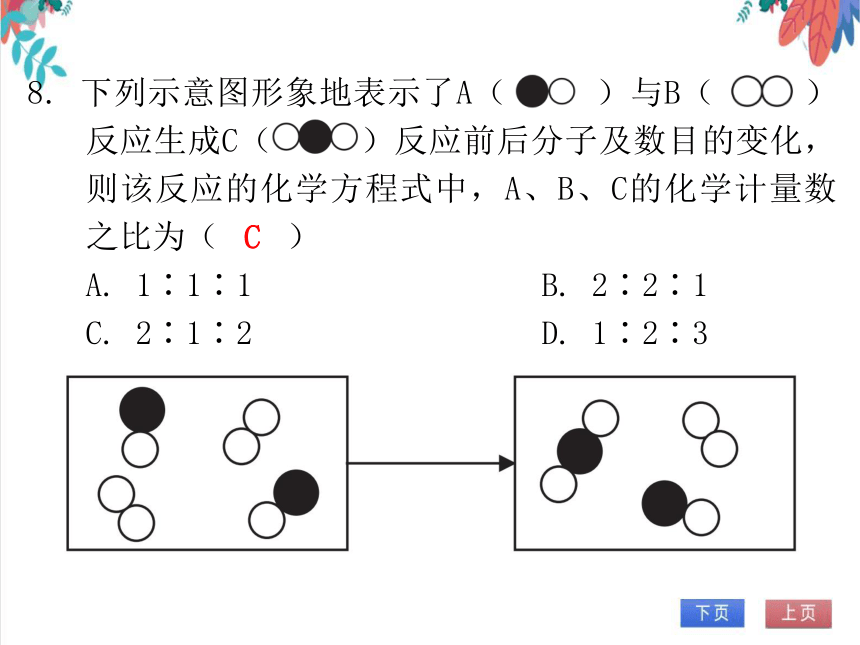
8. 下列示意图形象地表示了A( )与B( )反应生成C( )反应前后分子及数目的变化,则该反应的化学方程式中,A、B、C的化学计量数之比为( )
A. 1∶1∶1 B. 2∶2∶1
C. 2∶1∶2 D. 1∶2∶3
C
9. 下列化学方程式书写正确的是( )
A. 铜丝在氧气中加热生成氧化铜:Cu+O2 CuO
B. 磷在氧气中燃烧:2P2O5 4P+5O2
C. 硫在氧气中燃烧:S+O2 SO2↑
D. 氢气在氧气中燃烧生成水:2H2+O2 2H2O
D
10. 某化合物A在氧气中完全燃烧。消耗4. 8克氧气,生成4. 4克二氧化碳和2. 7克水,则A中( )
A. 只含有碳、氢元素
B. 只含有碳、氧元素
C. 含有碳、氢、氧三种元素
D. 一定含有碳、氢元素,可能含氧元素
C
11. 下列关于化学反应2X+Y2=== Z的叙述,不正确的是( )
A. Z一定是化合物
B. 若a g X与b g Y充分反应,生成Z的质量可能为(a+b) g
C. 若X和Y的相对分子质量分别为m和n,则Z的相对分子质量为(m+n)
D. 在反应中X、Y、Z三种物质的粒子数目比为2∶1∶2
C
12. 如图是某反应的微观示意图。下列说法不正确的是( )
A. 甲中氢、硫元素的质量比为1∶16
B. 反应后硫元素的化合价为+4
C. 参加反应的甲、乙分子个数比为1∶2
D. 反应后分子总数减少
C
13. 在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图。下列说法正确的是( )
A. 该反应前后分子总数保持不变
B. 丙一定是该反应的催化剂
C. 丁的相对分子质量是甲的2倍
D. 参加反应的乙和生成的丁质量比为3∶2
D
14. 在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表,下列说法正确的是( )
A. M、N、Y都是反应物
B. x的值为22
C. 该反应是化合反应
D. 反应中X、Y、M、N四种物质的质量比为22∶9∶111∶80
D
物 质 X Y M N
反应前质量(g) 4 6 111 4
反应后质量(g) x 15 0 84
15. 下列图象能正确反映对应变化关系的是( )
A. 表示加热KClO3(含少量MnO2)固体制取氧气时剩余固体的质量
B. 表示加热KClO3(含少量MnO2)固体制取氧气时固体中氧元素的质量
C. 表示双氧水(含少量MnO2)分解时溶剂的质量
D. 表示双氧水(含少量MnO2)分解时氢元素的质量分数
B
二、 填空题(本大题包括2小题,共15分)
16. (7分)请根据要求回答下列问题。
(1)电解水制取氧气,反应的化学方程式为 _________________________________。
(2)下列气体不宜做小包装糕点类食品填充气的是_____________(填字母)。
A. 氧气 B. 氮气 C. 水蒸气 D. 二氧化碳
(3)“氧烛”能快速提供氧气。氧烛中含有氯酸钠(NaClO3)、金属粉末(Al、Fe、Mg等)和催化剂。氧烛放出的氧气来自于上述物质中的___________,
判断的依据是________________________________。
AC
氯酸钠
2H2O 2H2↑+O2↑
化学反应前后元素种类不变
(4)氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜沉淀与硫酸钠,反应的化学方程式为____________________________________________。
2NaOH+CuSO4=== Cu(OH)2↓+Na2SO4
17. (8分)(1)氯化钠(俗称食盐)是生活常见的物质,也是重要的化工原料。电解熔融氯化钠(NaCl),可以得到金属钠和氯气。其微观变化过程如图所示。
①请根据化学反应的微观原理将图乙补充完整。
②请写出以上反应的化学方程式:______________
____________________________________________。(2)如图所示是某密闭容器中物质变化过程的微观示意图。
①A、B、C中表示化合物的是___________。
2NaCl(熔融) 2Na+Cl2↑
BC
②上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是___________,该化学变化中发生改变的粒子是一氧化碳分子和___________(填具体粒子名称),一定不变的粒子是______________________(填具体粒子名称),该反应属于___________(填基本反应类型)。
变化Ⅰ
氧分子
碳原子和氧原子
化合反应
三、 实验题(本大题包括2小题,共20分)
18. (10分)某课外兴趣小组的同学设计了如图实验来验证质量守恒定律。
(1)图1实验中,发生反应的化学方程式为________________________,图1实验过程中小气球的作用是_________________________________,变化现象为________________。
平衡装置内外压强,防止瓶塞飞出
先膨胀后缩小
4P+5O2 2P2O5
(2)图2实验________(填“能”或“不能”)验证质量守恒定律,原因是___________________________。
(3)请从微观的角度解释反应前后质量相等的原因:_____________________________________________
________。
(4)将图2装置改成图3装置(气密性良好),将充分反应后的锥形瓶放回左盘,发现指针没有停在中间,而是___________(填“偏右”或“偏左”),你认为可能的原因是______________________。
不能
反应生成的二氧化碳逸出装置
化学反应前后原子的种类、 数目和质量没有发生改变
偏右
气球膨胀,浮力增大
(5)小华将图3改成图4装置,已知氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,该装置 ___________(填“能”或“不能”)验证质量守恒定律。
不能
19. (10分)某化学兴趣小组利用镁条在空气中燃烧的实验验证质量守恒定律。
(1)请写出镁条与氧气反应的化学方程式:____________________________________________。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律。我 ___________(填“同意”或“不同意”)小明的观点,因为_____________________________________
____________________________________________。
2Mg+O2 2MgO
不同意
镁燃烧是镁与氧气发生的反应,生成氧化镁的质量等于参加反应的镁和氧气的质量之和
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】
①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【作出猜想】黄色固体为Mg3N2。
【实验探究】请设计实验,验证猜想。
实验操作 实验现象 实验结论
取少量 __于试管中,加入少量_________ ,将湿润的红色石蕊试纸放在试管口 、 _________________________________ 黄色固体为氮化镁
黄色固体
蒸馏水
有气泡产生
红色的石蕊试纸变成蓝色
【反思交流】
①若用镁条代替红磷完成测定空气中氧气含量的实验,不考虑其他因素的影响,进入水的体积会 ___________(填“大于”“小于”或“等于”)瓶内空气总体积的1/5。
②空气中的氮气的含量远大于氧气的含量,可是镁条在空气中燃烧的产物氧化镁却远多于氮化镁,合理的解释是___________________________________
_______________________________________。
大于
氧气的化学性质比氮气更活泼,镁条更容易和氧气发生反应
四、 综合能力题(本大题包括1小题,共10分)
20. (10分)A、B、C、D、E、F、G和X是初中化学常见的物质,它们之间的转化关系如图1所示,部分反应条件、反应物及生成物已略去。已知A、C组成元素相同,且常温下为液体,G在B中剧烈燃烧,火星四射。图2所示的是D、E的相关信息(重叠部分表示两种物质的共同点)。
请回答下列问题:
(1)物质E是氧化铜,则物质D是_________,物质X在反应①中起的作用是___________。
(2)物质C→B的反应条件为___________;该反应属于___________反应(填基本反应类型)。写出一条有关物质B的用途是___________。
(3)请写出下列反应的化学方程式:
B+D→E:_________________________;
B+G→F:_________________________________。
(4)实验室检验气体B的方法为_____________________________________________________________。
Cu
催化作用
通电
分解
供呼吸
2Cu+O2 2CuO
3Fe+2O2 Fe3O4
将带火星的木条伸入气体B中,若木条复燃,则该气体为氧气
五、 计算题(本大题包括1小题,共10分)
21. (10分)若空间站的宇航员每人每天平均需消耗960 g氧气,排出110 g二氧化碳。
(1)空间站解决氧气供给的方法是电解水。则为一名宇航员每天提供氧气需要电解水的质量是多少?(写出计算过程)
解:设需要电解水的质量是x。
答:需要电解水的质量是
1 080 g。
(2)空间站解决二氧化碳的方法是将空间站的空气分离出二氧化碳,在一定条件下将二氧化碳与氢气反应生成甲烷和水:CO2+4H2 CH4+2H2O,处理一名宇航员呼出的二氧化碳,请在如图坐标中画出相应的曲线图(纵坐标为氧化物的质量,请设定具体物质;并标出曲线中必要的数据)。
(3)除了用上述方法处理二氧化碳,空间站还常用另外一种处理办法,是利用氢氧化锂来将二氧化碳反应掉,写出该反应的化学方程式________________
____________________________________________。
谢谢!
第五单元达标测试卷
(时间:60分钟 满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Ca-40
一、选择题(本大题包括15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一个是正确的)
1. 化学反应前后,可能发生变化的是( )
A. 分子数目
B. 质子数
C. 原子种类
D. 物质的总质量
A
2. 下列现象,能用质量守恒定律解释的是( )
A. 10 g蔗糖溶于水,总质量变大
B. 镁条燃烧后,生成白色固体的质量比原来镁条的质量增加了
C. 湿衣服晒干后,质量减小
D. 100 mL水与100 mL酒精混合后,总体积小于200 mL
B
3. 下列关于化学方程式2H2O 2H2↑+O2↑的叙述中,正确的是( )
A. 水等于氢气和氧气
B. 2个水分子生成2个氢气和1个氧气
C. 水在通电条件下分解生成氢气和氧气
D. 每2份质量的水在通电条件下生成2份质量的氢气和1份质量的氧气
C
4. 在A+3B=== 2C+2D中,已知1.4 g A跟4.8 g B恰好完全反应生成4.4 g C。又知D的相对分子质量为18,则A的相对分子质量为( )
A. 44
B. 28
C. 23
D. 14
B
5. 在化学反应2A+B2=== 2AB中,A与B2反应的质量关系如图所示,现将6 gA和8 gB2充分反应,则生成AB的质量是( )
A. 9 g
B. 11 g
C. 12 g
D. 14 g
C
6. 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,具有强氧化性,可发生反应:6ClO2+16NH3=== 5N2+6NH4Cl+12X。则X的化学式为( )
A. H2
B. O2
C. H2O
D. H2O2
C
7. 下列说法正确的是( )
A. 化学方程式的配平是为了遵守质量守恒定律
B. 配平化学方程式,有时也可改变化学式中各组成元素右下角的数字
C. 原子团在化学反应中是不可以拆分的
D. 化学方程式中的↑表示生成物是气体,所以生成物中只要有气体必须标↑
A
8. 下列示意图形象地表示了A( )与B( )反应生成C( )反应前后分子及数目的变化,则该反应的化学方程式中,A、B、C的化学计量数之比为( )
A. 1∶1∶1 B. 2∶2∶1
C. 2∶1∶2 D. 1∶2∶3
C
9. 下列化学方程式书写正确的是( )
A. 铜丝在氧气中加热生成氧化铜:Cu+O2 CuO
B. 磷在氧气中燃烧:2P2O5 4P+5O2
C. 硫在氧气中燃烧:S+O2 SO2↑
D. 氢气在氧气中燃烧生成水:2H2+O2 2H2O
D
10. 某化合物A在氧气中完全燃烧。消耗4. 8克氧气,生成4. 4克二氧化碳和2. 7克水,则A中( )
A. 只含有碳、氢元素
B. 只含有碳、氧元素
C. 含有碳、氢、氧三种元素
D. 一定含有碳、氢元素,可能含氧元素
C
11. 下列关于化学反应2X+Y2=== Z的叙述,不正确的是( )
A. Z一定是化合物
B. 若a g X与b g Y充分反应,生成Z的质量可能为(a+b) g
C. 若X和Y的相对分子质量分别为m和n,则Z的相对分子质量为(m+n)
D. 在反应中X、Y、Z三种物质的粒子数目比为2∶1∶2
C
12. 如图是某反应的微观示意图。下列说法不正确的是( )
A. 甲中氢、硫元素的质量比为1∶16
B. 反应后硫元素的化合价为+4
C. 参加反应的甲、乙分子个数比为1∶2
D. 反应后分子总数减少
C
13. 在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图。下列说法正确的是( )
A. 该反应前后分子总数保持不变
B. 丙一定是该反应的催化剂
C. 丁的相对分子质量是甲的2倍
D. 参加反应的乙和生成的丁质量比为3∶2
D
14. 在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表,下列说法正确的是( )
A. M、N、Y都是反应物
B. x的值为22
C. 该反应是化合反应
D. 反应中X、Y、M、N四种物质的质量比为22∶9∶111∶80
D
物 质 X Y M N
反应前质量(g) 4 6 111 4
反应后质量(g) x 15 0 84
15. 下列图象能正确反映对应变化关系的是( )
A. 表示加热KClO3(含少量MnO2)固体制取氧气时剩余固体的质量
B. 表示加热KClO3(含少量MnO2)固体制取氧气时固体中氧元素的质量
C. 表示双氧水(含少量MnO2)分解时溶剂的质量
D. 表示双氧水(含少量MnO2)分解时氢元素的质量分数
B
二、 填空题(本大题包括2小题,共15分)
16. (7分)请根据要求回答下列问题。
(1)电解水制取氧气,反应的化学方程式为 _________________________________。
(2)下列气体不宜做小包装糕点类食品填充气的是_____________(填字母)。
A. 氧气 B. 氮气 C. 水蒸气 D. 二氧化碳
(3)“氧烛”能快速提供氧气。氧烛中含有氯酸钠(NaClO3)、金属粉末(Al、Fe、Mg等)和催化剂。氧烛放出的氧气来自于上述物质中的___________,
判断的依据是________________________________。
AC
氯酸钠
2H2O 2H2↑+O2↑
化学反应前后元素种类不变
(4)氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜沉淀与硫酸钠,反应的化学方程式为____________________________________________。
2NaOH+CuSO4=== Cu(OH)2↓+Na2SO4
17. (8分)(1)氯化钠(俗称食盐)是生活常见的物质,也是重要的化工原料。电解熔融氯化钠(NaCl),可以得到金属钠和氯气。其微观变化过程如图所示。
①请根据化学反应的微观原理将图乙补充完整。
②请写出以上反应的化学方程式:______________
____________________________________________。(2)如图所示是某密闭容器中物质变化过程的微观示意图。
①A、B、C中表示化合物的是___________。
2NaCl(熔融) 2Na+Cl2↑
BC
②上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是___________,该化学变化中发生改变的粒子是一氧化碳分子和___________(填具体粒子名称),一定不变的粒子是______________________(填具体粒子名称),该反应属于___________(填基本反应类型)。
变化Ⅰ
氧分子
碳原子和氧原子
化合反应
三、 实验题(本大题包括2小题,共20分)
18. (10分)某课外兴趣小组的同学设计了如图实验来验证质量守恒定律。
(1)图1实验中,发生反应的化学方程式为________________________,图1实验过程中小气球的作用是_________________________________,变化现象为________________。
平衡装置内外压强,防止瓶塞飞出
先膨胀后缩小
4P+5O2 2P2O5
(2)图2实验________(填“能”或“不能”)验证质量守恒定律,原因是___________________________。
(3)请从微观的角度解释反应前后质量相等的原因:_____________________________________________
________。
(4)将图2装置改成图3装置(气密性良好),将充分反应后的锥形瓶放回左盘,发现指针没有停在中间,而是___________(填“偏右”或“偏左”),你认为可能的原因是______________________。
不能
反应生成的二氧化碳逸出装置
化学反应前后原子的种类、 数目和质量没有发生改变
偏右
气球膨胀,浮力增大
(5)小华将图3改成图4装置,已知氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,该装置 ___________(填“能”或“不能”)验证质量守恒定律。
不能
19. (10分)某化学兴趣小组利用镁条在空气中燃烧的实验验证质量守恒定律。
(1)请写出镁条与氧气反应的化学方程式:____________________________________________。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律。我 ___________(填“同意”或“不同意”)小明的观点,因为_____________________________________
____________________________________________。
2Mg+O2 2MgO
不同意
镁燃烧是镁与氧气发生的反应,生成氧化镁的质量等于参加反应的镁和氧气的质量之和
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】
①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【作出猜想】黄色固体为Mg3N2。
【实验探究】请设计实验,验证猜想。
实验操作 实验现象 实验结论
取少量 __于试管中,加入少量_________ ,将湿润的红色石蕊试纸放在试管口 、 _________________________________ 黄色固体为氮化镁
黄色固体
蒸馏水
有气泡产生
红色的石蕊试纸变成蓝色
【反思交流】
①若用镁条代替红磷完成测定空气中氧气含量的实验,不考虑其他因素的影响,进入水的体积会 ___________(填“大于”“小于”或“等于”)瓶内空气总体积的1/5。
②空气中的氮气的含量远大于氧气的含量,可是镁条在空气中燃烧的产物氧化镁却远多于氮化镁,合理的解释是___________________________________
_______________________________________。
大于
氧气的化学性质比氮气更活泼,镁条更容易和氧气发生反应
四、 综合能力题(本大题包括1小题,共10分)
20. (10分)A、B、C、D、E、F、G和X是初中化学常见的物质,它们之间的转化关系如图1所示,部分反应条件、反应物及生成物已略去。已知A、C组成元素相同,且常温下为液体,G在B中剧烈燃烧,火星四射。图2所示的是D、E的相关信息(重叠部分表示两种物质的共同点)。
请回答下列问题:
(1)物质E是氧化铜,则物质D是_________,物质X在反应①中起的作用是___________。
(2)物质C→B的反应条件为___________;该反应属于___________反应(填基本反应类型)。写出一条有关物质B的用途是___________。
(3)请写出下列反应的化学方程式:
B+D→E:_________________________;
B+G→F:_________________________________。
(4)实验室检验气体B的方法为_____________________________________________________________。
Cu
催化作用
通电
分解
供呼吸
2Cu+O2 2CuO
3Fe+2O2 Fe3O4
将带火星的木条伸入气体B中,若木条复燃,则该气体为氧气
五、 计算题(本大题包括1小题,共10分)
21. (10分)若空间站的宇航员每人每天平均需消耗960 g氧气,排出110 g二氧化碳。
(1)空间站解决氧气供给的方法是电解水。则为一名宇航员每天提供氧气需要电解水的质量是多少?(写出计算过程)
解:设需要电解水的质量是x。
答:需要电解水的质量是
1 080 g。
(2)空间站解决二氧化碳的方法是将空间站的空气分离出二氧化碳,在一定条件下将二氧化碳与氢气反应生成甲烷和水:CO2+4H2 CH4+2H2O,处理一名宇航员呼出的二氧化碳,请在如图坐标中画出相应的曲线图(纵坐标为氧化物的质量,请设定具体物质;并标出曲线中必要的数据)。
(3)除了用上述方法处理二氧化碳,空间站还常用另外一种处理办法,是利用氢氧化锂来将二氧化碳反应掉,写出该反应的化学方程式________________
____________________________________________。
谢谢!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
