第6章常用的金属和盐同步练习—2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案)
文档属性
| 名称 | 第6章常用的金属和盐同步练习—2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 221.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-15 00:00:00 | ||
图片预览



文档简介
第6章常用的金属和盐同步练习021-2022学年九年级化学沪教版(上海)下册
一、单选题
1.下列说法正确的是
A.NaHCO3俗称苏打
B.CaCO3可用作补钙剂
C.Na2CO3俗称火碱
D.K2CO3属于复合肥
2.Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于
A.氧化物
B.盐
C.有机物
D.混合物
3.工业上利用赤铁矿石(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如图所示,下列说法不正确的是
A.CaSiO3中硅元素显+4价
B.高炉气体中SO2会形成酸雨,不能直接排放到空气中
C.原料中焦炭的作用之一是生成具有还原性的物质CO
D.高炉炼铁的原理是,该反应属于置换反应
4.化肥碳酸铵、硫酸钾均为白色固体。分别取少量固体进行下列实验,不能将两者区别出来的是
A.与熟石灰粉末混合研磨 B.加入稀盐酸中
C.加入溶液中 D.加入溶液中
5.将一定质量的Zn放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到滤渣和滤液,下列说法错误的是
A.滤渣中只含有Ag时,滤液一定呈蓝色
B.滤渣中含有Cu和Ag时,滤液一定呈无色
C.滤渣中含有Zn时,滤液中的溶质只有Zn(NO3)2
D.滤渣中含有Cu时,滤液中的溶质一定没有AgNO3
6.氯化铵(NH4Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化铵的说法正确的是
A.氯化铵属于酸 B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效 D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
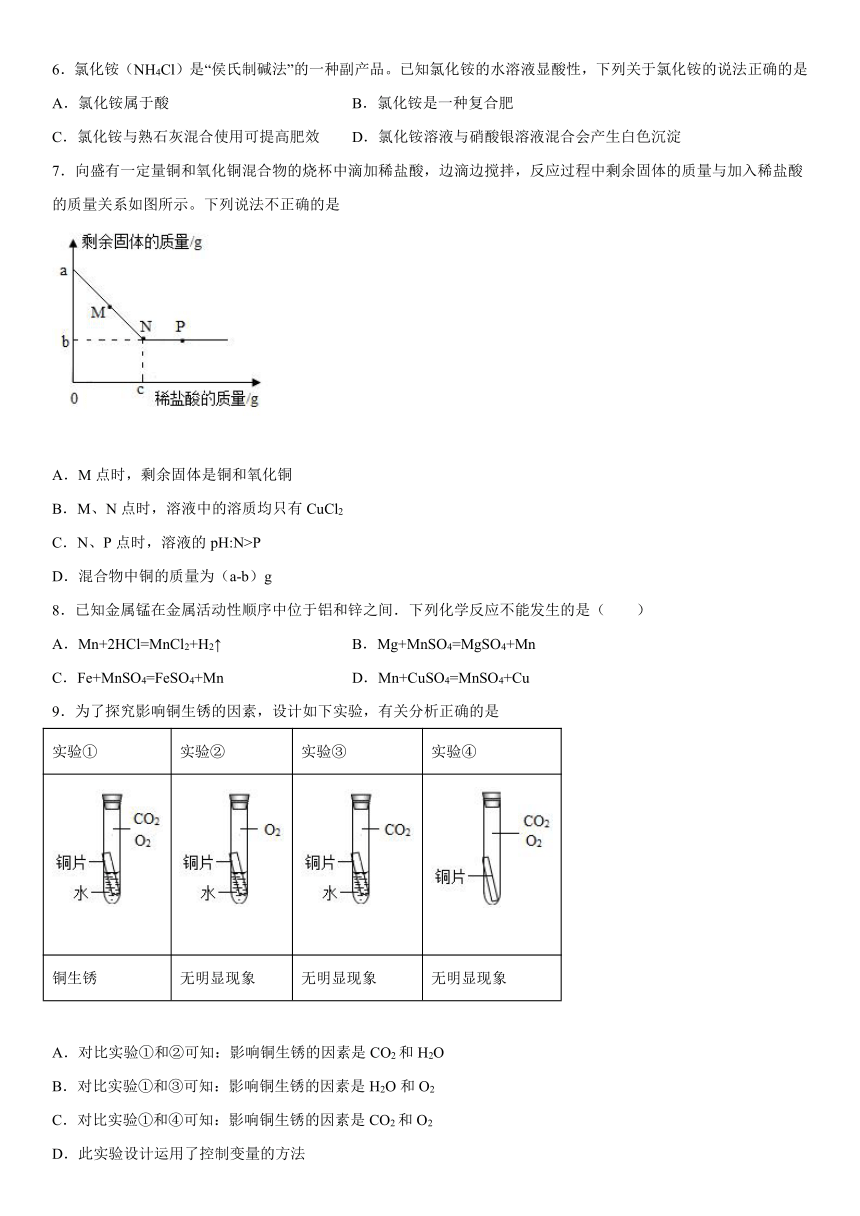
7.向盛有一定量铜和氧化铜混合物的烧杯中滴加稀盐酸,边滴边搅拌,反应过程中剩余固体的质量与加入稀盐酸的质量关系如图所示。下列说法不正确的是
A.M点时,剩余固体是铜和氧化铜
B.M、N点时,溶液中的溶质均只有CuCl2
C.N、P点时,溶液的pH:N>P
D.混合物中铜的质量为(a-b)g
8.已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )
A.Mn+2HCl=MnCl2+H2↑ B.Mg+MnSO4=MgSO4+Mn
C.Fe+MnSO4=FeSO4+Mn D.Mn+CuSO4=MnSO4+Cu
9.为了探究影响铜生锈的因素,设计如下实验,有关分析正确的是
实验① 实验② 实验③ 实验④
铜生锈 无明显现象 无明显现象 无明显现象
A.对比实验①和②可知:影响铜生锈的因素是CO2和H2O
B.对比实验①和③可知:影响铜生锈的因素是H2O和O2
C.对比实验①和④可知:影响铜生锈的因素是CO2和O2
D.此实验设计运用了控制变量的方法
10.现有盐酸和CaCl2的混合溶液,向其中加入过量某物质X,溶液的pH随加入X的量的变化关系如图所示。则X是
A.石灰石 B.熟石灰 C.纯碱 D.烧碱
二、简答题
11.中央台《国家宝藏》节目中展示了清乾隆金瓯永固杯。
(1)金杯历经近300年,仍然金光灿灿,从物质性质的角度解释其原因_____。
(2)现今市场上存在一种假冒黄金饰品(主要成分是锌和铜),在实验室中要鉴定出一枚戒指为假黄金,可选用的试剂是_____(填一种即可)。写出相应的化学反应的方程式_____。
12.许多家庭开始使用“扫地机器人”,它不仅可以帮助我们扫地,而且简单实用。如图是某品牌扫地机器人内部的结构示意图,请回答下列问题:
(1)机身外壳材料的主要成分是铝合金,它属于 _____ (填“纯净物”或“混合物”),与单质铝相比,它的硬度更 _____ (填“大”或“小”),写出铝离子的结构示意图: _____ 。
(2)请用化学方程式表示金属铁、铝的活动性顺序 _____ 。
(3)根据扫地机器人的制造、使用情况,谈一谈化学与生活的关系 _____ 。
13.当你漫步阿根廷的布宜诺斯艾丽斯时,会被这里精美绝伦的雕塑所吸引,“花之魂”就是世界10大奇异雕塑之一(图甲),它是由钢和铝(6% ~16%)加工而成的巨型“花朵”。傍晚时分“花朵”霓虹闪烁,将城市的夜晚打扮得流光溢彩,美轮美奂。
(1)钢铝加工而成的“花之魂”比铁雕塑性能优良之处_____________(写一条)。
(2)目前金属耗速过快,替代材料越来越多。列举生活中常用的一种合成材料________。
(3)图乙是铝的原子结构示意图,铝原子在化学反应中易_________电子(填“得”或“失”)。
三、推断题
14.某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍)等金属,如下是某工厂从该手机电路板中回收部分金属的流程示意图。已知:
(1)操作①的名称是_______。
(2)滤液②中金属阳离子的符号是_______。
(3)用实际参加反应的离子来表示滤液③和铁粉的反应方程式是_______。
(4)Cu、Ag、Ni在溶液中的活动性由强到弱的顺序是_______。
15.已知是初中化学常见的物质,B与人体血红蛋白结合会引起煤气中毒,C是赤铁矿的主要成分,H是胃酸的主要成分,它们之间的关系如下图所示。(图中“”表示物质间转化关系,“—”两端物质间能相互反应。)请回答下列问题:
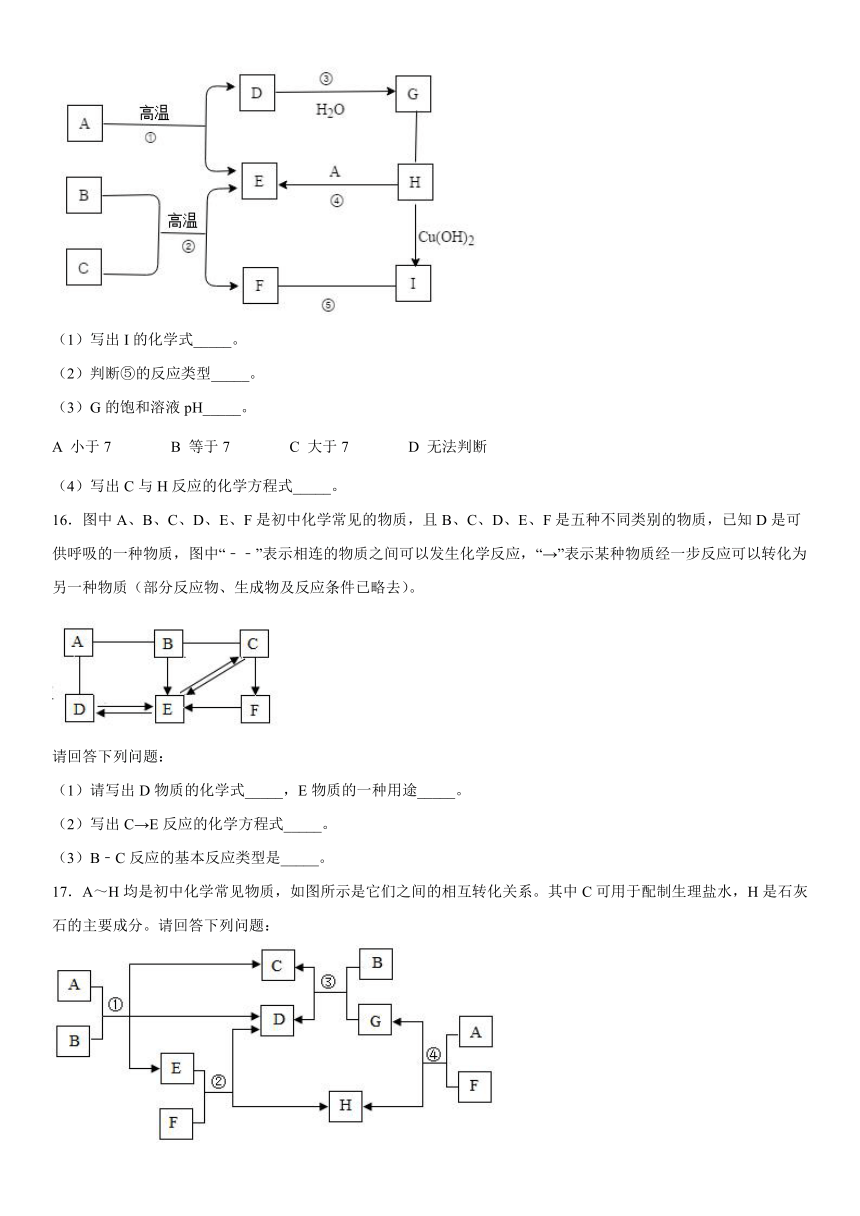
(1)写出I的化学式_____。
(2)判断⑤的反应类型_____。
(3)G的饱和溶液pH_____。
A 小于7 B 等于7 C 大于7 D 无法判断
(4)写出C与H反应的化学方程式_____。
16.图中A、B、C、D、E、F是初中化学常见的物质,且B、C、D、E、F是五种不同类别的物质,已知D是可供呼吸的一种物质,图中“﹣﹣”表示相连的物质之间可以发生化学反应,“→”表示某种物质经一步反应可以转化为另一种物质(部分反应物、生成物及反应条件已略去)。
请回答下列问题:
(1)请写出D物质的化学式_____,E物质的一种用途_____。
(2)写出C→E反应的化学方程式_____。
(3)B﹣C反应的基本反应类型是_____。
17.A~H均是初中化学常见物质,如图所示是它们之间的相互转化关系。其中C可用于配制生理盐水,H是石灰石的主要成分。请回答下列问题:
(1)H的化学式为______。
(2)反应③的基本反应类型为______。
(3)反应①的化学方程式为______。
四、实验题
18.某化学小组用下图装置制取氧气。
(1)写出仪器a的名称_____。
(2)用AE装置制取氧气,写出反应的化学方程式_____。
(3)实验室用BC装置制取二氧化碳时,若用铁丝网代替铜网,会有什么后果?_____
19.为了探究相关金属的活动性,设计了如下图所示的实验。
(1)实验①的目的是_____。
(2)实验②中发生反应的反应方程式为_____。
(3)该探究得到的实验结论是_____。
20.某化学兴趣小组利用“化学喷泉”设计了如下实验:20 ℃时,用 250 mL 圆底烧瓶收集一瓶纯净的 CO2,按下图组装装置。用注射器缓缓注入 3 mL NaOH 溶液,轻轻振荡烧瓶,打开止水夹,玻璃导管尖嘴处很快产生“喷泉”,与此同时,C、E 装置中发生连锁反应。回答下列问题:
(1)图中仪器 X 的名称是_______。
(2)注入 NaOH 溶液后,烧瓶内发生反应的化学方程式是________。
(3)“连锁反应”后,C 试管中溶液的颜色变化为_________;E 试管中的现象为_____,反应的化学方程式为________。
(4)实验结束后,同学们发现圆底烧瓶中溶液呈红色,由此认为烧瓶中一定还有 NaOH剩余,你认为是否正确?______,说明原因:_________。
五、计算题
21.锌和稀硫酸反应生成硫酸锌和氢气,实验室里用6.5g锌与足量稀硫酸反应,可制得氢气的质量是多少?
22.现有11 g含有少量氯化钠的某纯碱样品,为了测定该样品中的碳酸钠的质量分数,将该纯碱样品全部溶解在100 g水中,再加入氯化钙溶液141 g,恰好完全反应,经过滤后测得所得溶液质量为242 g,请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留到0.1%)。
(2)所得溶液中溶质的质量分数。
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.C
5.B
6.D
7.D
8.C
9.D
10.C
11. 金的化学性质不活泼 稀盐酸 Zn+2HCl═ZnCl2+H2↑
12. 混合物 大 2Al+3FeSO 4 ==3Fe+2Al2(SO4) 化学的发展提高了人们的生活质量
13. 耐腐蚀(或不易生锈/硬度大/经久耐用) 塑料(或合成纤维/合成橡胶/聚乙烯) 失
14. 过滤 Fe2+ Ni、Cu、Ag
15. 置换反应 C
16. O2 洗涤或做溶剂 CO2+Ca(OH)2=CaCO3↓+H2O 复分解反应
17. CaCO3 复分解反应
18. 酒精灯 2KClO32KCl+3O2↑ 制取的二氧化碳中会混有氢气
19. 比较Cu与Ag的活动性强弱 Fe+2HCl=FeCl2+H2↑ 活动性排列:Fe>Cu>Ag
20. 锥形瓶 红色变浅或褪去 出现蓝色絮状沉淀 不正确 生成碳酸钠的水溶液也呈碱性,也可使酚酞变红
21.解:可制得氢气的质量为 x
x=0.2g
答:可制得氢气的质量为 0.2g。
22.解:碳酸钙的质量为:11g + 100g + 141g - 242g =10g
设原混合物中Na2CO3的质量为x ,生成NaCl的质量为y
(1)纯碱样品中碳酸钠的质量分数=
(2)反应后所得滤液中氯化钠的质量=11.7g +(11g – 10.6g)= 12.1g
所得滤液的溶质质量分数=
答:纯碱样品中碳酸钠的质量分数为96.4%,所得溶液中溶质质量分数为5%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列说法正确的是
A.NaHCO3俗称苏打
B.CaCO3可用作补钙剂
C.Na2CO3俗称火碱
D.K2CO3属于复合肥
2.Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于
A.氧化物
B.盐
C.有机物
D.混合物
3.工业上利用赤铁矿石(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如图所示,下列说法不正确的是
A.CaSiO3中硅元素显+4价
B.高炉气体中SO2会形成酸雨,不能直接排放到空气中
C.原料中焦炭的作用之一是生成具有还原性的物质CO
D.高炉炼铁的原理是,该反应属于置换反应
4.化肥碳酸铵、硫酸钾均为白色固体。分别取少量固体进行下列实验,不能将两者区别出来的是
A.与熟石灰粉末混合研磨 B.加入稀盐酸中
C.加入溶液中 D.加入溶液中
5.将一定质量的Zn放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到滤渣和滤液,下列说法错误的是
A.滤渣中只含有Ag时,滤液一定呈蓝色
B.滤渣中含有Cu和Ag时,滤液一定呈无色
C.滤渣中含有Zn时,滤液中的溶质只有Zn(NO3)2
D.滤渣中含有Cu时,滤液中的溶质一定没有AgNO3
6.氯化铵(NH4Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化铵的说法正确的是
A.氯化铵属于酸 B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效 D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
7.向盛有一定量铜和氧化铜混合物的烧杯中滴加稀盐酸,边滴边搅拌,反应过程中剩余固体的质量与加入稀盐酸的质量关系如图所示。下列说法不正确的是
A.M点时,剩余固体是铜和氧化铜
B.M、N点时,溶液中的溶质均只有CuCl2
C.N、P点时,溶液的pH:N>P
D.混合物中铜的质量为(a-b)g
8.已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )
A.Mn+2HCl=MnCl2+H2↑ B.Mg+MnSO4=MgSO4+Mn
C.Fe+MnSO4=FeSO4+Mn D.Mn+CuSO4=MnSO4+Cu
9.为了探究影响铜生锈的因素,设计如下实验,有关分析正确的是
实验① 实验② 实验③ 实验④
铜生锈 无明显现象 无明显现象 无明显现象
A.对比实验①和②可知:影响铜生锈的因素是CO2和H2O
B.对比实验①和③可知:影响铜生锈的因素是H2O和O2
C.对比实验①和④可知:影响铜生锈的因素是CO2和O2
D.此实验设计运用了控制变量的方法
10.现有盐酸和CaCl2的混合溶液,向其中加入过量某物质X,溶液的pH随加入X的量的变化关系如图所示。则X是
A.石灰石 B.熟石灰 C.纯碱 D.烧碱
二、简答题
11.中央台《国家宝藏》节目中展示了清乾隆金瓯永固杯。
(1)金杯历经近300年,仍然金光灿灿,从物质性质的角度解释其原因_____。
(2)现今市场上存在一种假冒黄金饰品(主要成分是锌和铜),在实验室中要鉴定出一枚戒指为假黄金,可选用的试剂是_____(填一种即可)。写出相应的化学反应的方程式_____。
12.许多家庭开始使用“扫地机器人”,它不仅可以帮助我们扫地,而且简单实用。如图是某品牌扫地机器人内部的结构示意图,请回答下列问题:
(1)机身外壳材料的主要成分是铝合金,它属于 _____ (填“纯净物”或“混合物”),与单质铝相比,它的硬度更 _____ (填“大”或“小”),写出铝离子的结构示意图: _____ 。
(2)请用化学方程式表示金属铁、铝的活动性顺序 _____ 。
(3)根据扫地机器人的制造、使用情况,谈一谈化学与生活的关系 _____ 。
13.当你漫步阿根廷的布宜诺斯艾丽斯时,会被这里精美绝伦的雕塑所吸引,“花之魂”就是世界10大奇异雕塑之一(图甲),它是由钢和铝(6% ~16%)加工而成的巨型“花朵”。傍晚时分“花朵”霓虹闪烁,将城市的夜晚打扮得流光溢彩,美轮美奂。
(1)钢铝加工而成的“花之魂”比铁雕塑性能优良之处_____________(写一条)。
(2)目前金属耗速过快,替代材料越来越多。列举生活中常用的一种合成材料________。
(3)图乙是铝的原子结构示意图,铝原子在化学反应中易_________电子(填“得”或“失”)。
三、推断题
14.某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍)等金属,如下是某工厂从该手机电路板中回收部分金属的流程示意图。已知:
(1)操作①的名称是_______。
(2)滤液②中金属阳离子的符号是_______。
(3)用实际参加反应的离子来表示滤液③和铁粉的反应方程式是_______。
(4)Cu、Ag、Ni在溶液中的活动性由强到弱的顺序是_______。
15.已知是初中化学常见的物质,B与人体血红蛋白结合会引起煤气中毒,C是赤铁矿的主要成分,H是胃酸的主要成分,它们之间的关系如下图所示。(图中“”表示物质间转化关系,“—”两端物质间能相互反应。)请回答下列问题:
(1)写出I的化学式_____。
(2)判断⑤的反应类型_____。
(3)G的饱和溶液pH_____。
A 小于7 B 等于7 C 大于7 D 无法判断
(4)写出C与H反应的化学方程式_____。
16.图中A、B、C、D、E、F是初中化学常见的物质,且B、C、D、E、F是五种不同类别的物质,已知D是可供呼吸的一种物质,图中“﹣﹣”表示相连的物质之间可以发生化学反应,“→”表示某种物质经一步反应可以转化为另一种物质(部分反应物、生成物及反应条件已略去)。
请回答下列问题:
(1)请写出D物质的化学式_____,E物质的一种用途_____。
(2)写出C→E反应的化学方程式_____。
(3)B﹣C反应的基本反应类型是_____。
17.A~H均是初中化学常见物质,如图所示是它们之间的相互转化关系。其中C可用于配制生理盐水,H是石灰石的主要成分。请回答下列问题:
(1)H的化学式为______。
(2)反应③的基本反应类型为______。
(3)反应①的化学方程式为______。
四、实验题
18.某化学小组用下图装置制取氧气。
(1)写出仪器a的名称_____。
(2)用AE装置制取氧气,写出反应的化学方程式_____。
(3)实验室用BC装置制取二氧化碳时,若用铁丝网代替铜网,会有什么后果?_____
19.为了探究相关金属的活动性,设计了如下图所示的实验。
(1)实验①的目的是_____。
(2)实验②中发生反应的反应方程式为_____。
(3)该探究得到的实验结论是_____。
20.某化学兴趣小组利用“化学喷泉”设计了如下实验:20 ℃时,用 250 mL 圆底烧瓶收集一瓶纯净的 CO2,按下图组装装置。用注射器缓缓注入 3 mL NaOH 溶液,轻轻振荡烧瓶,打开止水夹,玻璃导管尖嘴处很快产生“喷泉”,与此同时,C、E 装置中发生连锁反应。回答下列问题:
(1)图中仪器 X 的名称是_______。
(2)注入 NaOH 溶液后,烧瓶内发生反应的化学方程式是________。
(3)“连锁反应”后,C 试管中溶液的颜色变化为_________;E 试管中的现象为_____,反应的化学方程式为________。
(4)实验结束后,同学们发现圆底烧瓶中溶液呈红色,由此认为烧瓶中一定还有 NaOH剩余,你认为是否正确?______,说明原因:_________。
五、计算题
21.锌和稀硫酸反应生成硫酸锌和氢气,实验室里用6.5g锌与足量稀硫酸反应,可制得氢气的质量是多少?
22.现有11 g含有少量氯化钠的某纯碱样品,为了测定该样品中的碳酸钠的质量分数,将该纯碱样品全部溶解在100 g水中,再加入氯化钙溶液141 g,恰好完全反应,经过滤后测得所得溶液质量为242 g,请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留到0.1%)。
(2)所得溶液中溶质的质量分数。
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.C
5.B
6.D
7.D
8.C
9.D
10.C
11. 金的化学性质不活泼 稀盐酸 Zn+2HCl═ZnCl2+H2↑
12. 混合物 大 2Al+3FeSO 4 ==3Fe+2Al2(SO4) 化学的发展提高了人们的生活质量
13. 耐腐蚀(或不易生锈/硬度大/经久耐用) 塑料(或合成纤维/合成橡胶/聚乙烯) 失
14. 过滤 Fe2+ Ni、Cu、Ag
15. 置换反应 C
16. O2 洗涤或做溶剂 CO2+Ca(OH)2=CaCO3↓+H2O 复分解反应
17. CaCO3 复分解反应
18. 酒精灯 2KClO32KCl+3O2↑ 制取的二氧化碳中会混有氢气
19. 比较Cu与Ag的活动性强弱 Fe+2HCl=FeCl2+H2↑ 活动性排列:Fe>Cu>Ag
20. 锥形瓶 红色变浅或褪去 出现蓝色絮状沉淀 不正确 生成碳酸钠的水溶液也呈碱性,也可使酚酞变红
21.解:可制得氢气的质量为 x
x=0.2g
答:可制得氢气的质量为 0.2g。
22.解:碳酸钙的质量为:11g + 100g + 141g - 242g =10g
设原混合物中Na2CO3的质量为x ,生成NaCl的质量为y
(1)纯碱样品中碳酸钠的质量分数=
(2)反应后所得滤液中氯化钠的质量=11.7g +(11g – 10.6g)= 12.1g
所得滤液的溶质质量分数=
答:纯碱样品中碳酸钠的质量分数为96.4%,所得溶液中溶质质量分数为5%。
答案第1页,共2页
答案第1页,共2页
