第12章盐单元巩固—2021-2022学年九年级化学京改版(2013)下册(word版 含答案)
文档属性
| 名称 | 第12章盐单元巩固—2021-2022学年九年级化学京改版(2013)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 118.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-16 00:00:00 | ||
图片预览



文档简介
第12章盐单元巩固2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.氢氧化钠的俗称是
A.纯碱 B.小苏打 C.熟石灰 D.烧碱
2.分类是化学学习和研究的重要方法之一,下列分类中不正确的是
A.纯净物:氧气、干冰、水银 B.肥料:二氧化碳、硫酸铵、硝酸钾
C.单质:金刚石、铁粉、黄铜 D.盐:氯化钠、硝酸钠、碳酸钙
3.下列各组物质的溶液中,不另加试剂则无法鉴别出来的是
A.H2SO4 NaOH CuSO4
B.HCl NaOH NaCl
C.H2SO4 Ca(OH)2 FeCl3
D.HCl Ca(OH)2 Na2CO3
4.如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是
A.水、硝酸铵
B.水、烧碱
C.稀硫酸、铁粉
D.稀盐酸、小苏打
5.小明家的甘蔗茎杆细弱,需要追施钾肥,应选择( )
A.KOH B.Ca3(PO4)2 C.K2CO3 D.CO(NH2)2
6.草木灰是一种碱性农家肥,下列肥料不能与草木灰混合使用的是
A.KNO3 B.NH4HCO3 C.KCl D.Ca3(PO4)2
7.下列做法不能达到目的是( )
A.用洗涤剂去除油污 B.用白酒去除水垢
C.用小苏打发酵面粉 D.用煮沸的方法软化硬水
8.下列除杂方法正确的是
选项 物质(括号内为杂质) 方法
A K2CO3溶液(K2SO4) 加BaCl2溶液,过滤
B N2(O2) 将气体通过灼热的铜网
C NaOH溶液(Na2CO3) 加入稀硫酸
D ZnSO4溶液(CuSO4) 加入过量的铁粉,过滤
A.A B.B C.C D.D
9.下列各组物质在溶液中能大量共存且形成无色溶液的是
A.NaCl BaCl2Na2CO3 B.KNO3HCl CaCl2
C.H2SO4 FeCl3NaNO3 D.NaOH HNO3NH4NO3
10.把、、、、五种无色溶液鉴别开来,实验方案中所加试剂和先后顺序最合理的是( )
A.石蕊试液、稀、溶液 B.溶液、稀、石蕊试液
C.稀、石蕊试液、溶液 D.稀、酚酞试液、溶液
11.不使用其它试剂,利用物质间两两混合反应将物质区别开(提供的物质可重复使用),也是物质鉴别的常用方法。下面四组物质利用上述方法可鉴别开的是
A.H2SO4、Na2SO4、BaCl2、FeCl3 B.BaCl2、HCl、NaNO3、AgNO3
C.Na2CO3、HNO3、NaNO3、BaCl2 D.H2SO4、NaOH、MgCl2、Ba(NO3)2
二、简答题
12.(1)生活中处处有化学.请按要求将下列各组物质的序号填到横线上;①尿素、磷铵、硫酸钾;②塑料、合成纤维、合成橡胶;③铜、钢材、铝合金;④无机盐、糖类、维生素;⑤天然气、汽油、煤.
常用作燃料的是_____;常见的金属材料是_____;常见的有机合成材料是_____;人类重要的营养素是_____;常用的化学肥料是_____.
(2)锂(Li)电池因质量轻、能量密度高、充电快被广泛应用.锂原子核内有_____个质子,在反应中容易_____(填“得到”或“失去”)1个电子,锂离子符号为_____.
13.碳铵是农业上一种常见的氮肥,如图是包装袋上的文字说明,使用时,施加在农作物根部附近,盖土或用水灌溉,切忌暴晒,它在碱性土壤中会失效(放出NH3、生成水和正盐)。据此:
(1)碳铵的性质是 _____________________________________________________________ 。
(2)若改良酸性土壤时,向土壤中施加了熟石灰,当向土壤中施加碳铵,造成肥分流失的化学反应是 __________________________________ 。
14.溶液对于自然界中的生命活动和人类生产活动具有重要的意义,多角度认识溶液有助于指导我们的生活。
(1)关于溶液的说法,正确的是_________(填写标号)
A.溶液中各部分的性质相同B.均一、稳定的液体一定是溶液
C.浓溶液不一定是饱和溶液D.溶液加水稀释后溶质的质量变小
(2)表1是部分物质在20℃时的溶解性;表Ⅱ是氯化钠、碳酸钠在不同温度时的溶解度。
离子 OH- Cl- CO32- SO42-
K+ 溶 溶 溶 溶
Mg2+ 不 溶 微 溶
.Ba2+. 溶 溶 不
温度 (℃) 0 10 20 30 40
氯化钠(g) 35 35.5 36 36.5 37
碳酸钠(g) 6 10 18 36.5 50
表1空格中应填写________;分析表Ⅱ可知,氯化钠和碳酸钠的饱和溶液溶质质量分数相同时的温度是___。
(3)简单解释“夏天晒盐、冬天捞碱”的科学原理__________。
三、推断题
15.有A,B,C,D四种化合物,A是硝酸盐,B是酸,C是碱,D是含+3价元素的氯化物,发生以下反应:
(1)A,B的溶液混合后,出现不溶于稀硝酸的白色沉淀。
(2)B,C的溶液完全反应后,得到氯化钠溶液。
(3)C,D的溶液混合后,出现红褐色沉淀。试推断A,B,C,D的化学式。
A._____;B._____;C._____;D._____。
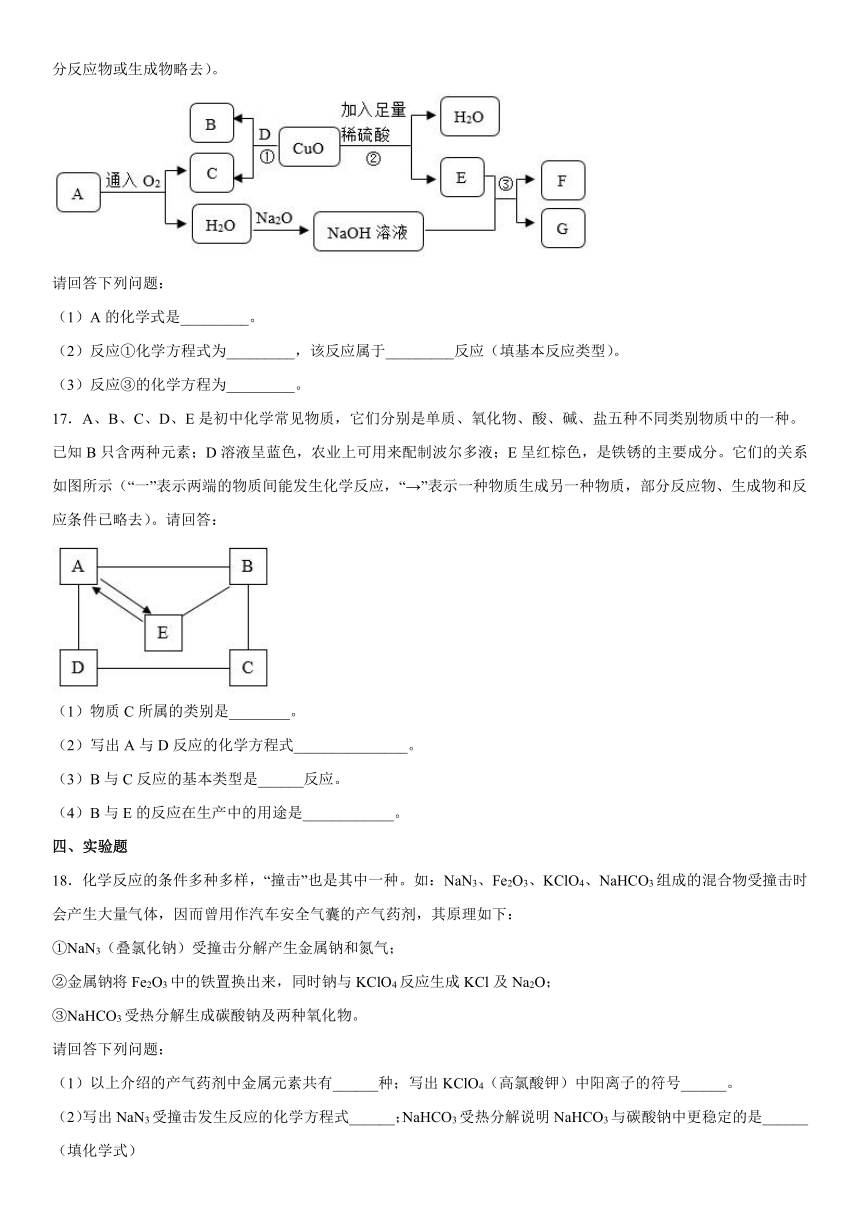
16.A~G为初中常见的七种物质,其中A是天然气的主要成分,D为单质,他们之间的相互关系如下图所示(部分反应物或生成物略去)。
请回答下列问题:
(1)A的化学式是_________。
(2)反应①化学方程式为_________,该反应属于_________反应(填基本反应类型)。
(3)反应③的化学方程为_________。
17.A、B、C、D、E是初中化学常见物质,它们分别是单质、氧化物、酸、碱、盐五种不同类别物质中的一种。已知B只含两种元素;D溶液呈蓝色,农业上可用来配制波尔多液;E呈红棕色,是铁锈的主要成分。它们的关系如图所示(“一”表示两端的物质间能发生化学反应,“→”表示一种物质生成另一种物质,部分反应物、生成物和反应条件已略去)。请回答:
(1)物质C所属的类别是________。
(2)写出A与D反应的化学方程式_______________。
(3)B与C反应的基本类型是______反应。
(4)B与E的反应在生产中的用途是____________。
四、实验题
18.化学反应的条件多种多样,“撞击”也是其中一种。如:NaN3、Fe2O3、KClO4、NaHCO3组成的混合物受撞击时会产生大量气体,因而曾用作汽车安全气囊的产气药剂,其原理如下:
①NaN3(叠氯化钠)受撞击分解产生金属钠和氮气;
②金属钠将Fe2O3中的铁置换出来,同时钠与KClO4反应生成KCl及Na2O;
③NaHCO3受热分解生成碳酸钠及两种氧化物。
请回答下列问题:
(1)以上介绍的产气药剂中金属元素共有______种;写出KClO4(高氯酸钾)中阳离子的符号______。
(2)写出NaN3受撞击发生反应的化学方程式______;NaHCO3受热分解说明NaHCO3与碳酸钠中更稳定的是______(填化学式)
(3)若取100g上述产气药剂进行撞击反应实验(假设各物质均反应完全);
资料1:碱石灰能吸收水和二氧化碳;
资料2:标准状况下,气体的体积与质量有如下关系:
22.4L气体 水蒸气 氮气 氧气 二氧化碳
相应的质量(克) 18 28 32 44
①产气药剂撞击后产生的气体成分有氮气、______及水蒸气。
②将以上气体全部通过足量的碱石灰后体积为33.6L(标准状况),则产气药剂中NaN3的质量分数为______。
(4)已知相关物质的溶解度随温度变化的曲线如图。
①由此可知NaClO4属于______(选填“易溶”或“微溶”或“难溶”)物质。
②实验室称取一定质量的KCl、NaClO4溶解后加热反应、降温结晶、蒸馏水洗涤、真空干燥得到KClO4晶体。检验洗涤是否干净的方法是取最后一次洗涤液______,若观察到______证明还未洗净。
19.小华爷爷去年购买化肥,由于外包装上字迹模糊,无法辨认,只记得该化肥成分是KNO3、NH4HCO3和中(NH4)2SO4一种。小华为帮助爷爷鉴别化肥,设计如下方案:
(1)取该化肥少量于研钵中,加入少量熟石灰粉末混合研磨,闻到氨味,推断该化肥成分一定不是______。
(2)为进一步鉴别该化肥的成分,小华设计了以下实验:
实验步骤 实验现象 实验结论
取少量化肥于试管中,加水溶解后,再滴加稀盐酸 无气泡产生 该化肥成分是______(填写物质名称)
(3)实验室需要用固体(NH4)2SO4和蒸馏水配制50g溶质质量分数为6%的(NH4)2SO4溶液,配制该溶液的过程中,所需要的玻璃仪器除量筒、玻璃棒、托盘天平、药匙和胶头滴管外,还需要______(填写仪器名称),需要(NH4)2SO4的质量为______g。若用已配好的25g溶质质量分数为6%的(NH4)2SO4溶液加水(水的密度为1g/cm3)配制溶质质量分数为3%的(NH4)2SO4溶液,配制时应选用______mL的量筒量取水(填“10”或“50”)。
20.工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中含有一种杂质碳酸钠。某科学学习小组同学围绕工业“烧碱”样品纯度测定问题,展开了讨论与探究。
【原理思路】利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算工业“烧碱”样品纯度。
【实验方案】根据以上思路,小科设计的方案是:利用如图甲的装置(固定装置省略),通过测定反应前后整套装置和药品的总质量的减少量确定CO2质量。
(1)小科按该方案进行测定,加入足量稀硫酸充分反应后,发现最终测得碳酸钠的质量明显偏低。你认为导致测得的“碳酸钠”的质量明显偏低的原因是______;
【方案改进】为减少误差,小组同学经讨论,对小科方案进行改进,设计了如图乙的实验方案(固定装置省略)。通过测定反应前后D质量的变化。
(2)图乙B装置中样品在与足量稀硫酸反应前和停止反应后,都要鼓入足量的空气,在反应前通空气时,a、b、c三个弹簧夹的控制方法是______。
(3)若撤去图乙中的A和E装置,则测得工业“烧碱”的纯度将______(选填“偏高”“偏低”或“无影响”)。
(4)按改进后的图乙实验方案进行实验,发现测得的工业“烧碱”的纯度明显偏高,从实验操作上分析产生上述结果的原因是______(写出一种即可)。
五、计算题
21.草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为______。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是______?
22.向盛有28g氯化钡和氯化钠固体混合物的烧杯中加入273.3g水,固体完全溶解。再逐滴加入一定质量分数的硫酸钠溶液,反应过程中生成沉淀的质量与所加硫酸钠溶液的质量关系如图所示。请计算:
(1)反应过程中生成沉淀的质量__________g;
(2)固体混合物中氯化钡的质量____;
(3)恰好完全反应时,所得溶液中溶质的质量分数。
23.同学们从山上采集到一种石灰石,他们取80g该样品进行煅烧实验(反应的化学方程为:,杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
反应时间t/s t0 t1 t2 t3 t4 t5 t6
反应后固体的质量m/g 80 75 70 66 62 58 58
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为______g。
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
试卷第1页,共3页
参考答案:
1.D
2.C
3.B
4.A
5.C
6.B
7.B
8.B
9.B
10.B
11.C
12. ⑤ ③ ② ④ ① 3 失去 Li+
13. 易溶于水,受热易分解,能和显碱性的物质反应 NH4HCO3+Ca(OH)2=CaCO3+2H2O+NH3↑
14. A、C 不 30 “夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出.“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出
15. AgNO3 HCl NaOH FeCl3
16. CH4 置换
17. 碱 Fe+CuSO4=Cu+FeSO4 复分解 除锈
18. 三 K+ Na2CO3 二氧化碳 65% 易溶 加入硝酸银溶液 有白色沉淀
19.(1)KNO3
(2)硫酸铵
(3) 烧杯 3 50
20.(1)反应生成的二氧化碳部分留在装置中
(2)打开ab,关闭c
(3)偏低
(4)反应后没有鼓入足量的空气
21.(1)39:6:24;(2)8.8g;(3)14.6%
22.(1)23.3;(2)20.8g;(3)5%
23.(1)22
(2)解:设该石灰石中碳酸钙的质量分数为x
x=62.5%
答:石灰石中碳酸钙的质量分数为62.5%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.氢氧化钠的俗称是
A.纯碱 B.小苏打 C.熟石灰 D.烧碱
2.分类是化学学习和研究的重要方法之一,下列分类中不正确的是
A.纯净物:氧气、干冰、水银 B.肥料:二氧化碳、硫酸铵、硝酸钾
C.单质:金刚石、铁粉、黄铜 D.盐:氯化钠、硝酸钠、碳酸钙
3.下列各组物质的溶液中,不另加试剂则无法鉴别出来的是
A.H2SO4 NaOH CuSO4
B.HCl NaOH NaCl
C.H2SO4 Ca(OH)2 FeCl3
D.HCl Ca(OH)2 Na2CO3
4.如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是
A.水、硝酸铵
B.水、烧碱
C.稀硫酸、铁粉
D.稀盐酸、小苏打
5.小明家的甘蔗茎杆细弱,需要追施钾肥,应选择( )
A.KOH B.Ca3(PO4)2 C.K2CO3 D.CO(NH2)2
6.草木灰是一种碱性农家肥,下列肥料不能与草木灰混合使用的是
A.KNO3 B.NH4HCO3 C.KCl D.Ca3(PO4)2
7.下列做法不能达到目的是( )
A.用洗涤剂去除油污 B.用白酒去除水垢
C.用小苏打发酵面粉 D.用煮沸的方法软化硬水
8.下列除杂方法正确的是
选项 物质(括号内为杂质) 方法
A K2CO3溶液(K2SO4) 加BaCl2溶液,过滤
B N2(O2) 将气体通过灼热的铜网
C NaOH溶液(Na2CO3) 加入稀硫酸
D ZnSO4溶液(CuSO4) 加入过量的铁粉,过滤
A.A B.B C.C D.D
9.下列各组物质在溶液中能大量共存且形成无色溶液的是
A.NaCl BaCl2Na2CO3 B.KNO3HCl CaCl2
C.H2SO4 FeCl3NaNO3 D.NaOH HNO3NH4NO3
10.把、、、、五种无色溶液鉴别开来,实验方案中所加试剂和先后顺序最合理的是( )
A.石蕊试液、稀、溶液 B.溶液、稀、石蕊试液
C.稀、石蕊试液、溶液 D.稀、酚酞试液、溶液
11.不使用其它试剂,利用物质间两两混合反应将物质区别开(提供的物质可重复使用),也是物质鉴别的常用方法。下面四组物质利用上述方法可鉴别开的是
A.H2SO4、Na2SO4、BaCl2、FeCl3 B.BaCl2、HCl、NaNO3、AgNO3
C.Na2CO3、HNO3、NaNO3、BaCl2 D.H2SO4、NaOH、MgCl2、Ba(NO3)2
二、简答题
12.(1)生活中处处有化学.请按要求将下列各组物质的序号填到横线上;①尿素、磷铵、硫酸钾;②塑料、合成纤维、合成橡胶;③铜、钢材、铝合金;④无机盐、糖类、维生素;⑤天然气、汽油、煤.
常用作燃料的是_____;常见的金属材料是_____;常见的有机合成材料是_____;人类重要的营养素是_____;常用的化学肥料是_____.
(2)锂(Li)电池因质量轻、能量密度高、充电快被广泛应用.锂原子核内有_____个质子,在反应中容易_____(填“得到”或“失去”)1个电子,锂离子符号为_____.
13.碳铵是农业上一种常见的氮肥,如图是包装袋上的文字说明,使用时,施加在农作物根部附近,盖土或用水灌溉,切忌暴晒,它在碱性土壤中会失效(放出NH3、生成水和正盐)。据此:
(1)碳铵的性质是 _____________________________________________________________ 。
(2)若改良酸性土壤时,向土壤中施加了熟石灰,当向土壤中施加碳铵,造成肥分流失的化学反应是 __________________________________ 。
14.溶液对于自然界中的生命活动和人类生产活动具有重要的意义,多角度认识溶液有助于指导我们的生活。
(1)关于溶液的说法,正确的是_________(填写标号)
A.溶液中各部分的性质相同B.均一、稳定的液体一定是溶液
C.浓溶液不一定是饱和溶液D.溶液加水稀释后溶质的质量变小
(2)表1是部分物质在20℃时的溶解性;表Ⅱ是氯化钠、碳酸钠在不同温度时的溶解度。
离子 OH- Cl- CO32- SO42-
K+ 溶 溶 溶 溶
Mg2+ 不 溶 微 溶
.Ba2+. 溶 溶 不
温度 (℃) 0 10 20 30 40
氯化钠(g) 35 35.5 36 36.5 37
碳酸钠(g) 6 10 18 36.5 50
表1空格中应填写________;分析表Ⅱ可知,氯化钠和碳酸钠的饱和溶液溶质质量分数相同时的温度是___。
(3)简单解释“夏天晒盐、冬天捞碱”的科学原理__________。
三、推断题
15.有A,B,C,D四种化合物,A是硝酸盐,B是酸,C是碱,D是含+3价元素的氯化物,发生以下反应:
(1)A,B的溶液混合后,出现不溶于稀硝酸的白色沉淀。
(2)B,C的溶液完全反应后,得到氯化钠溶液。
(3)C,D的溶液混合后,出现红褐色沉淀。试推断A,B,C,D的化学式。
A._____;B._____;C._____;D._____。
16.A~G为初中常见的七种物质,其中A是天然气的主要成分,D为单质,他们之间的相互关系如下图所示(部分反应物或生成物略去)。
请回答下列问题:
(1)A的化学式是_________。
(2)反应①化学方程式为_________,该反应属于_________反应(填基本反应类型)。
(3)反应③的化学方程为_________。
17.A、B、C、D、E是初中化学常见物质,它们分别是单质、氧化物、酸、碱、盐五种不同类别物质中的一种。已知B只含两种元素;D溶液呈蓝色,农业上可用来配制波尔多液;E呈红棕色,是铁锈的主要成分。它们的关系如图所示(“一”表示两端的物质间能发生化学反应,“→”表示一种物质生成另一种物质,部分反应物、生成物和反应条件已略去)。请回答:
(1)物质C所属的类别是________。
(2)写出A与D反应的化学方程式_______________。
(3)B与C反应的基本类型是______反应。
(4)B与E的反应在生产中的用途是____________。
四、实验题
18.化学反应的条件多种多样,“撞击”也是其中一种。如:NaN3、Fe2O3、KClO4、NaHCO3组成的混合物受撞击时会产生大量气体,因而曾用作汽车安全气囊的产气药剂,其原理如下:
①NaN3(叠氯化钠)受撞击分解产生金属钠和氮气;
②金属钠将Fe2O3中的铁置换出来,同时钠与KClO4反应生成KCl及Na2O;
③NaHCO3受热分解生成碳酸钠及两种氧化物。
请回答下列问题:
(1)以上介绍的产气药剂中金属元素共有______种;写出KClO4(高氯酸钾)中阳离子的符号______。
(2)写出NaN3受撞击发生反应的化学方程式______;NaHCO3受热分解说明NaHCO3与碳酸钠中更稳定的是______(填化学式)
(3)若取100g上述产气药剂进行撞击反应实验(假设各物质均反应完全);
资料1:碱石灰能吸收水和二氧化碳;
资料2:标准状况下,气体的体积与质量有如下关系:
22.4L气体 水蒸气 氮气 氧气 二氧化碳
相应的质量(克) 18 28 32 44
①产气药剂撞击后产生的气体成分有氮气、______及水蒸气。
②将以上气体全部通过足量的碱石灰后体积为33.6L(标准状况),则产气药剂中NaN3的质量分数为______。
(4)已知相关物质的溶解度随温度变化的曲线如图。
①由此可知NaClO4属于______(选填“易溶”或“微溶”或“难溶”)物质。
②实验室称取一定质量的KCl、NaClO4溶解后加热反应、降温结晶、蒸馏水洗涤、真空干燥得到KClO4晶体。检验洗涤是否干净的方法是取最后一次洗涤液______,若观察到______证明还未洗净。
19.小华爷爷去年购买化肥,由于外包装上字迹模糊,无法辨认,只记得该化肥成分是KNO3、NH4HCO3和中(NH4)2SO4一种。小华为帮助爷爷鉴别化肥,设计如下方案:
(1)取该化肥少量于研钵中,加入少量熟石灰粉末混合研磨,闻到氨味,推断该化肥成分一定不是______。
(2)为进一步鉴别该化肥的成分,小华设计了以下实验:
实验步骤 实验现象 实验结论
取少量化肥于试管中,加水溶解后,再滴加稀盐酸 无气泡产生 该化肥成分是______(填写物质名称)
(3)实验室需要用固体(NH4)2SO4和蒸馏水配制50g溶质质量分数为6%的(NH4)2SO4溶液,配制该溶液的过程中,所需要的玻璃仪器除量筒、玻璃棒、托盘天平、药匙和胶头滴管外,还需要______(填写仪器名称),需要(NH4)2SO4的质量为______g。若用已配好的25g溶质质量分数为6%的(NH4)2SO4溶液加水(水的密度为1g/cm3)配制溶质质量分数为3%的(NH4)2SO4溶液,配制时应选用______mL的量筒量取水(填“10”或“50”)。
20.工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中含有一种杂质碳酸钠。某科学学习小组同学围绕工业“烧碱”样品纯度测定问题,展开了讨论与探究。
【原理思路】利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算工业“烧碱”样品纯度。
【实验方案】根据以上思路,小科设计的方案是:利用如图甲的装置(固定装置省略),通过测定反应前后整套装置和药品的总质量的减少量确定CO2质量。
(1)小科按该方案进行测定,加入足量稀硫酸充分反应后,发现最终测得碳酸钠的质量明显偏低。你认为导致测得的“碳酸钠”的质量明显偏低的原因是______;
【方案改进】为减少误差,小组同学经讨论,对小科方案进行改进,设计了如图乙的实验方案(固定装置省略)。通过测定反应前后D质量的变化。
(2)图乙B装置中样品在与足量稀硫酸反应前和停止反应后,都要鼓入足量的空气,在反应前通空气时,a、b、c三个弹簧夹的控制方法是______。
(3)若撤去图乙中的A和E装置,则测得工业“烧碱”的纯度将______(选填“偏高”“偏低”或“无影响”)。
(4)按改进后的图乙实验方案进行实验,发现测得的工业“烧碱”的纯度明显偏高,从实验操作上分析产生上述结果的原因是______(写出一种即可)。
五、计算题
21.草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为______。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是______?
22.向盛有28g氯化钡和氯化钠固体混合物的烧杯中加入273.3g水,固体完全溶解。再逐滴加入一定质量分数的硫酸钠溶液,反应过程中生成沉淀的质量与所加硫酸钠溶液的质量关系如图所示。请计算:
(1)反应过程中生成沉淀的质量__________g;
(2)固体混合物中氯化钡的质量____;
(3)恰好完全反应时,所得溶液中溶质的质量分数。
23.同学们从山上采集到一种石灰石,他们取80g该样品进行煅烧实验(反应的化学方程为:,杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
反应时间t/s t0 t1 t2 t3 t4 t5 t6
反应后固体的质量m/g 80 75 70 66 62 58 58
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为______g。
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
试卷第1页,共3页
参考答案:
1.D
2.C
3.B
4.A
5.C
6.B
7.B
8.B
9.B
10.B
11.C
12. ⑤ ③ ② ④ ① 3 失去 Li+
13. 易溶于水,受热易分解,能和显碱性的物质反应 NH4HCO3+Ca(OH)2=CaCO3+2H2O+NH3↑
14. A、C 不 30 “夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出.“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出
15. AgNO3 HCl NaOH FeCl3
16. CH4 置换
17. 碱 Fe+CuSO4=Cu+FeSO4 复分解 除锈
18. 三 K+ Na2CO3 二氧化碳 65% 易溶 加入硝酸银溶液 有白色沉淀
19.(1)KNO3
(2)硫酸铵
(3) 烧杯 3 50
20.(1)反应生成的二氧化碳部分留在装置中
(2)打开ab,关闭c
(3)偏低
(4)反应后没有鼓入足量的空气
21.(1)39:6:24;(2)8.8g;(3)14.6%
22.(1)23.3;(2)20.8g;(3)5%
23.(1)22
(2)解:设该石灰石中碳酸钙的质量分数为x
x=62.5%
答:石灰石中碳酸钙的质量分数为62.5%
答案第1页,共2页
答案第1页,共2页
