第12章 盐 测试题-2021-2022学年九年级化学京改版(2013)下册(word版 含答案)
文档属性
| 名称 | 第12章 盐 测试题-2021-2022学年九年级化学京改版(2013)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 111.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-16 00:00:00 | ||
图片预览



文档简介
第12章《盐》测试题
一、单选题
1.下列化肥属于氮肥的是
A.KCl
B.CO(NH2)2
C.K2SO4
D.Ca3(PO4)2
2.下列化肥中,从外观即可与其他化肥相区别的是
A.磷矿粉 B.硝酸铵 C.硫酸钾 D.氯化钾
3.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
4.小美发现荔枝园旁边的水稻叶子发黄,并倒下了一片,你认为应该向稻田施用的复合肥是( )
A.CO(NH2)2 B.KCl C.Ca3(PO4)2 D.KNO3
5.下列关于氯化钠的认识,正确的是
A.组成:含有钠和氯两种单质 B.性质:与盐酸类似,能与碳酸盐反应
C.用途:可用于生产金属钠 D.生产:常用钠与氯气通过化合反应获得
6.下表用甲试剂鉴别乙中的两种化肥,难以实现的是
甲 乙 甲 乙
A Ca(OH)2 CO(NH2)2、NH4HCO3 B Ba(NO3)2 KCl、(NH4)2SO4
C AgNO3 NH4Cl、NH4NO3 D NaCl K2SO4、KNO3
A.A
B.B
C.C
D.D
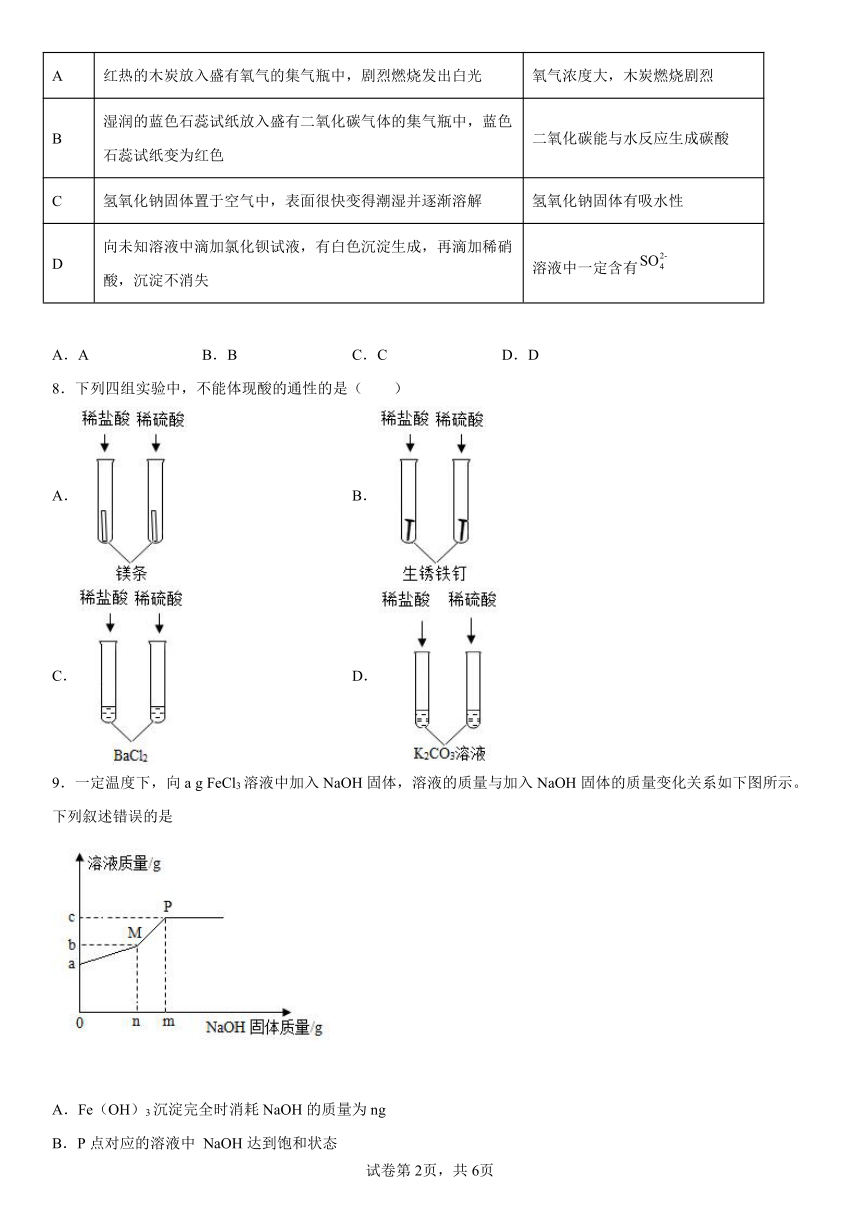
7.根据下面实验过程得出的结论,不正确的是
选项 实验过程 实验结论
A 红热的木炭放入盛有氧气的集气瓶中,剧烈燃烧发出白光 氧气浓度大,木炭燃烧剧烈
B 湿润的蓝色石蕊试纸放入盛有二氧化碳气体的集气瓶中,蓝色石蕊试纸变为红色 二氧化碳能与水反应生成碳酸
C 氢氧化钠固体置于空气中,表面很快变得潮湿并逐渐溶解 氢氧化钠固体有吸水性
D 向未知溶液中滴加氯化钡试液,有白色沉淀生成,再滴加稀硝酸,沉淀不消失 溶液中一定含有
A.A B.B C.C D.D
8.下列四组实验中,不能体现酸的通性的是( )
A. B.
C. D.
9.一定温度下,向a g FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如下图所示。下列叙述错误的是
A.Fe(OH)3沉淀完全时消耗NaOH的质量为ng
B.P点对应的溶液中 NaOH达到饱和状态
C.m=c-a
D.生成Fe(OH)3的质量为(n-b+a)g
二、简答题
10.(1)生活中处处有化学.请按要求将下列各组物质的序号填到横线上;①尿素、磷铵、硫酸钾;②塑料、合成纤维、合成橡胶;③铜、钢材、铝合金;④无机盐、糖类、维生素;⑤天然气、汽油、煤.
常用作燃料的是_____;常见的金属材料是_____;常见的有机合成材料是_____;人类重要的营养素是_____;常用的化学肥料是_____.
(2)锂(Li)电池因质量轻、能量密度高、充电快被广泛应用.锂原子核内有_____个质子,在反应中容易_____(填“得到”或“失去”)1个电子,锂离子符号为_____.
11.用珍珠(主要成分CaCO3)加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假.为了向消费者提供鉴别方法,需找出真假“珍珠粉”理化性质上的差异,工商局提供了真、假“珍珠粉”样品,请你展开探究:(主要写出猜想、方案,不需要说出方案实施的具体结果)
猜想一:_____.
方案一:_____.
猜想二:_____.
方案二:_____.
猜想三:_____.
方案三:_____.
12.根据实验回答:
(1)图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现象为:浑浊→变红→红色消失。根据现象判断氢氧化钙的性质有___________、___________(物理和化学性质,各填一条)。
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是___________,可能有的溶质是___________。
(3)图2装置气密性良好。取0.5g碳酸氢钠于甲中,加入2mL盐酸,___________(填操作),并将导管伸入澄清石灰水中,观察到___________。乙中反应的化学方程式为___________。
(4)图2中甲作为发生装置还可制得的气体是___________(填一种)。
三、推断题
13.推理和判断是学习化学的重要方法。
A、B、C为初中化学常见的三种物质,它们之间的转化关系如图所示(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物的反应条件已略去)请回答下列问题:
(1)若A、B、C均含有同一种元素,B、C组成元素相同,C的固体俗称“干冰”,则B的化学式是______________。
(2)若A、B、C是含相同金属元素的化合物,B、C的水溶液为蓝色,三种物质相互间发生的反应均为复分解反应,则A的化学式可能是____________(合理即可得分)。
(3)若A、B、C均为碱,其中B易溶于水,C难溶于水,写出一个由B转化为C的化学方程式_____________(合理即可得分)。
14.在下图有关物质间转化关系中,涉及物质均为初中化学常见的物质。其中A、B、C 均为氧化物,A为黑色固体,C可用作蔬菜大棚中的气体肥料;D、E、F为不同类型的化合物,F俗称纯碱,E和G按照一定比例混合可制备波尔多液(图中部分反应物、生成物已略)。
(1)固态C的俗称为________。
(2)写出D的一点用途________。
(3)写出A→C的化学方程式________。
(4)写出E与F发生反应的化学方程式_______。
15.已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种化合物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的 ____________ (填化学式)有关。
(2)E物质的化学式是 _______ 。
(3)在①~⑥反应中属于化合反应的是 _______ (填数字序号)。
(4)反应⑤的化学方程式 ___________________________________________________ 。
四、实验题
16.甲、乙两同学想了解碳酸钠溶液的酸碱性。他们做了以下研究:
实 验 操 作 检测结果
甲同学 取pH试纸放在玻璃片上;用玻璃棒蘸取碳酸钠溶液沾在pH试纸上;将试纸显示的颜色与标准比色卡比较。 pH>7
乙同学 将pH试纸直接浸入碳酸钠溶液中,把试纸显示的颜色与标准比色卡比较。 pH>7
(1)碳酸钠的化学式为__________,它属于________(填酸、碱、盐、氧化物)
(2)根据两位同学的实验可得出碳酸钠溶液酸碱性的结论:__________________
(3)根据两位同学的实验操作,你认为_________同学操作不规范。为什么 _____________。
(4)如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用__________试液来进行实验。
17.将硝酸钠和硝酸钡的混合物进行分离,实验方法如下;
1、向混合物溶液里加入过量的碳酸钠溶液,有白色沉淀生成;
2、过滤,滤出沉淀并进行洗涤;
3、向沉淀中加入硝酸,至沉淀完全溶解后,蒸发溶液得到晶体;
4、向滤液中加入硝酸,到不再产生气泡为止;
5、蒸发中所得溶液,得到晶体;
请回答下列问题:
(1)得到的沉淀是________,实验得到的晶体是________,实验得到的晶体是________,
(2)实验为什么要加入过量的溶液________?
(3)实验中为什么要向滤液中加入硝酸________?
(4)写出实验1,3,4中的化学方程式________、________、________.
五、计算题
18.某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取6g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题:
(1)该样品中碳酸钠的质量分数是多少?(写出计算步骤,计算结果精确到0.1%)
(2)如果反应开始前,向烧杯中滴加几滴无色酚酞试液,在整个测定过程中可观察到的现象是: 。
19.某纯碱样品中含有少量氯化钠杂质。称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。试回答:
(1)生成CO2的质量_____。
(2)22.8g样品中氯化钠的质量为_____。
(3)计算所得溶液中溶质的质量分数_________。(写出解题过程,计算结果精确到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.B
4.D
5.C
6.D
7.D
8.C
9.C
10. ⑤ ③ ② ④ ① 3 失去 Li+
11. 真假“珍珠粉”灼烧后可能有不同现象 取样,在酒精灯火焰上灼烧片刻,观察颜色、状态变化 真、假“珍珠粉”的溶解性可能不同 取样,分别将它们的放入足量的水中,分辨溶解性有无差异 真、假“珍珠粉”的是否与盐酸反应冒气泡 取样,分别将它们的放入装有盐酸的试管中,观察气泡有无差异
12. 微溶于水 能和盐酸反应 氯化钙 氯化氢 塞紧橡皮塞 澄清石灰水变浑浊 氧气等
13. CO CuO或Cu(OH)2(合理均可)
14. 干冰 除铁锈(合理即可) (合理即可)
15. CO2 CuSO4 ③
16. 盐 碳酸钠溶液显碱性 乙 使用pH试纸测定溶液酸碱度时,不能把pH试纸直接放入被测液中,这样会污染试剂 紫色石蕊试液
17. 碳酸钡 硝酸钡 硝酸钠 让硝酸钡完全反应变成碳酸钡 把过量的碳酸钠除去,变为硝酸钠
18.(1)
解:根据图示,反应中生成的碳酸钙质量为5g。
设该纯碱样品中碳酸钠的质量为 x。
X=5.3g;
该纯碱样品中碳酸钠的质量分数为:;
答:纯碱样品中碳酸钠的质量分数为88.3%;
(2)溶液由红色变为无色,有白色沉淀生成
19.(1)由图象和质量守恒定律可知,生成二氧化碳的质量为:178.8g﹣170.0g=8.8g;
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
解得:x=21.2g,y=23.4g,
22.8g样品中氯化钠的质量为:22.8g﹣21.2g=1.6g
(3)完全反应后所得氯化钠溶液的溶质质量分数14.7%
故答为:(1)8.8;
(2)22.8g样品中氯化钠的质量为1.6g;
(3)所得溶液中溶质的质量分数为14.7%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列化肥属于氮肥的是
A.KCl
B.CO(NH2)2
C.K2SO4
D.Ca3(PO4)2
2.下列化肥中,从外观即可与其他化肥相区别的是
A.磷矿粉 B.硝酸铵 C.硫酸钾 D.氯化钾
3.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
4.小美发现荔枝园旁边的水稻叶子发黄,并倒下了一片,你认为应该向稻田施用的复合肥是( )
A.CO(NH2)2 B.KCl C.Ca3(PO4)2 D.KNO3
5.下列关于氯化钠的认识,正确的是
A.组成:含有钠和氯两种单质 B.性质:与盐酸类似,能与碳酸盐反应
C.用途:可用于生产金属钠 D.生产:常用钠与氯气通过化合反应获得
6.下表用甲试剂鉴别乙中的两种化肥,难以实现的是
甲 乙 甲 乙
A Ca(OH)2 CO(NH2)2、NH4HCO3 B Ba(NO3)2 KCl、(NH4)2SO4
C AgNO3 NH4Cl、NH4NO3 D NaCl K2SO4、KNO3
A.A
B.B
C.C
D.D
7.根据下面实验过程得出的结论,不正确的是
选项 实验过程 实验结论
A 红热的木炭放入盛有氧气的集气瓶中,剧烈燃烧发出白光 氧气浓度大,木炭燃烧剧烈
B 湿润的蓝色石蕊试纸放入盛有二氧化碳气体的集气瓶中,蓝色石蕊试纸变为红色 二氧化碳能与水反应生成碳酸
C 氢氧化钠固体置于空气中,表面很快变得潮湿并逐渐溶解 氢氧化钠固体有吸水性
D 向未知溶液中滴加氯化钡试液,有白色沉淀生成,再滴加稀硝酸,沉淀不消失 溶液中一定含有
A.A B.B C.C D.D
8.下列四组实验中,不能体现酸的通性的是( )
A. B.
C. D.
9.一定温度下,向a g FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如下图所示。下列叙述错误的是
A.Fe(OH)3沉淀完全时消耗NaOH的质量为ng
B.P点对应的溶液中 NaOH达到饱和状态
C.m=c-a
D.生成Fe(OH)3的质量为(n-b+a)g
二、简答题
10.(1)生活中处处有化学.请按要求将下列各组物质的序号填到横线上;①尿素、磷铵、硫酸钾;②塑料、合成纤维、合成橡胶;③铜、钢材、铝合金;④无机盐、糖类、维生素;⑤天然气、汽油、煤.
常用作燃料的是_____;常见的金属材料是_____;常见的有机合成材料是_____;人类重要的营养素是_____;常用的化学肥料是_____.
(2)锂(Li)电池因质量轻、能量密度高、充电快被广泛应用.锂原子核内有_____个质子,在反应中容易_____(填“得到”或“失去”)1个电子,锂离子符号为_____.
11.用珍珠(主要成分CaCO3)加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假.为了向消费者提供鉴别方法,需找出真假“珍珠粉”理化性质上的差异,工商局提供了真、假“珍珠粉”样品,请你展开探究:(主要写出猜想、方案,不需要说出方案实施的具体结果)
猜想一:_____.
方案一:_____.
猜想二:_____.
方案二:_____.
猜想三:_____.
方案三:_____.
12.根据实验回答:
(1)图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现象为:浑浊→变红→红色消失。根据现象判断氢氧化钙的性质有___________、___________(物理和化学性质,各填一条)。
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是___________,可能有的溶质是___________。
(3)图2装置气密性良好。取0.5g碳酸氢钠于甲中,加入2mL盐酸,___________(填操作),并将导管伸入澄清石灰水中,观察到___________。乙中反应的化学方程式为___________。
(4)图2中甲作为发生装置还可制得的气体是___________(填一种)。
三、推断题
13.推理和判断是学习化学的重要方法。
A、B、C为初中化学常见的三种物质,它们之间的转化关系如图所示(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物的反应条件已略去)请回答下列问题:
(1)若A、B、C均含有同一种元素,B、C组成元素相同,C的固体俗称“干冰”,则B的化学式是______________。
(2)若A、B、C是含相同金属元素的化合物,B、C的水溶液为蓝色,三种物质相互间发生的反应均为复分解反应,则A的化学式可能是____________(合理即可得分)。
(3)若A、B、C均为碱,其中B易溶于水,C难溶于水,写出一个由B转化为C的化学方程式_____________(合理即可得分)。
14.在下图有关物质间转化关系中,涉及物质均为初中化学常见的物质。其中A、B、C 均为氧化物,A为黑色固体,C可用作蔬菜大棚中的气体肥料;D、E、F为不同类型的化合物,F俗称纯碱,E和G按照一定比例混合可制备波尔多液(图中部分反应物、生成物已略)。
(1)固态C的俗称为________。
(2)写出D的一点用途________。
(3)写出A→C的化学方程式________。
(4)写出E与F发生反应的化学方程式_______。
15.已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种化合物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的 ____________ (填化学式)有关。
(2)E物质的化学式是 _______ 。
(3)在①~⑥反应中属于化合反应的是 _______ (填数字序号)。
(4)反应⑤的化学方程式 ___________________________________________________ 。
四、实验题
16.甲、乙两同学想了解碳酸钠溶液的酸碱性。他们做了以下研究:
实 验 操 作 检测结果
甲同学 取pH试纸放在玻璃片上;用玻璃棒蘸取碳酸钠溶液沾在pH试纸上;将试纸显示的颜色与标准比色卡比较。 pH>7
乙同学 将pH试纸直接浸入碳酸钠溶液中,把试纸显示的颜色与标准比色卡比较。 pH>7
(1)碳酸钠的化学式为__________,它属于________(填酸、碱、盐、氧化物)
(2)根据两位同学的实验可得出碳酸钠溶液酸碱性的结论:__________________
(3)根据两位同学的实验操作,你认为_________同学操作不规范。为什么 _____________。
(4)如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用__________试液来进行实验。
17.将硝酸钠和硝酸钡的混合物进行分离,实验方法如下;
1、向混合物溶液里加入过量的碳酸钠溶液,有白色沉淀生成;
2、过滤,滤出沉淀并进行洗涤;
3、向沉淀中加入硝酸,至沉淀完全溶解后,蒸发溶液得到晶体;
4、向滤液中加入硝酸,到不再产生气泡为止;
5、蒸发中所得溶液,得到晶体;
请回答下列问题:
(1)得到的沉淀是________,实验得到的晶体是________,实验得到的晶体是________,
(2)实验为什么要加入过量的溶液________?
(3)实验中为什么要向滤液中加入硝酸________?
(4)写出实验1,3,4中的化学方程式________、________、________.
五、计算题
18.某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取6g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题:
(1)该样品中碳酸钠的质量分数是多少?(写出计算步骤,计算结果精确到0.1%)
(2)如果反应开始前,向烧杯中滴加几滴无色酚酞试液,在整个测定过程中可观察到的现象是: 。
19.某纯碱样品中含有少量氯化钠杂质。称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。试回答:
(1)生成CO2的质量_____。
(2)22.8g样品中氯化钠的质量为_____。
(3)计算所得溶液中溶质的质量分数_________。(写出解题过程,计算结果精确到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.B
4.D
5.C
6.D
7.D
8.C
9.C
10. ⑤ ③ ② ④ ① 3 失去 Li+
11. 真假“珍珠粉”灼烧后可能有不同现象 取样,在酒精灯火焰上灼烧片刻,观察颜色、状态变化 真、假“珍珠粉”的溶解性可能不同 取样,分别将它们的放入足量的水中,分辨溶解性有无差异 真、假“珍珠粉”的是否与盐酸反应冒气泡 取样,分别将它们的放入装有盐酸的试管中,观察气泡有无差异
12. 微溶于水 能和盐酸反应 氯化钙 氯化氢 塞紧橡皮塞 澄清石灰水变浑浊 氧气等
13. CO CuO或Cu(OH)2(合理均可)
14. 干冰 除铁锈(合理即可) (合理即可)
15. CO2 CuSO4 ③
16. 盐 碳酸钠溶液显碱性 乙 使用pH试纸测定溶液酸碱度时,不能把pH试纸直接放入被测液中,这样会污染试剂 紫色石蕊试液
17. 碳酸钡 硝酸钡 硝酸钠 让硝酸钡完全反应变成碳酸钡 把过量的碳酸钠除去,变为硝酸钠
18.(1)
解:根据图示,反应中生成的碳酸钙质量为5g。
设该纯碱样品中碳酸钠的质量为 x。
X=5.3g;
该纯碱样品中碳酸钠的质量分数为:;
答:纯碱样品中碳酸钠的质量分数为88.3%;
(2)溶液由红色变为无色,有白色沉淀生成
19.(1)由图象和质量守恒定律可知,生成二氧化碳的质量为:178.8g﹣170.0g=8.8g;
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
解得:x=21.2g,y=23.4g,
22.8g样品中氯化钠的质量为:22.8g﹣21.2g=1.6g
(3)完全反应后所得氯化钠溶液的溶质质量分数14.7%
故答为:(1)8.8;
(2)22.8g样品中氯化钠的质量为1.6g;
(3)所得溶液中溶质的质量分数为14.7%。
答案第1页,共2页
答案第1页,共2页
