第二节_富集在海水中的元素---氯
文档属性
| 名称 | 第二节_富集在海水中的元素---氯 |

|
|
| 格式 | zip | ||
| 文件大小 | 335.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-01-02 00:00:00 | ||
图片预览











文档简介
课件30张PPT。海洋是巨大的资源宝库海洋中含有大量的盐类,主要为NaCl,此外还有MgCl2、MgSO4等,致使海水既咸又苦,不能直接饮用。资料卡片
如果将海水中的盐类全部提 取出来,铺在地球的陆地
上,可以使陆地平均升高
150mNaCl也大量存在于陆地盐矿中氯元素主要以什么形式存在于哪里?
氯元素主要以NaCl的形式存在于海水
及陆地的盐矿中,所以说海水中富集
了丰富的氯。 第二节 富集在海水中的元素——氯一、氯与其单质1、氯的原子结构和性质性质:化合价:-1,+1,+2,+3,
+4,+5,+6,+7
得电子能力强,非金属性强2、氯气的分子结构Cl2 ;Cl—Cl ;氯气属于双原子分子结构3、氯气的物理性质(色、状、味、水溶性、密度、毒性)(1)、氯气是黄绿色有刺激性气味的有毒气体,易液化(2)、氯气可溶于水,氯水呈浅黄绿色
(常温常压下,1体积水可溶解2体积氯气)(3)、密度比空气大?闻氯气的方法是:
用手轻轻地在瓶口扇动,仅使极少量的氯气飘进鼻孔。
?注意:
这是闻各种气体的气味的方法。
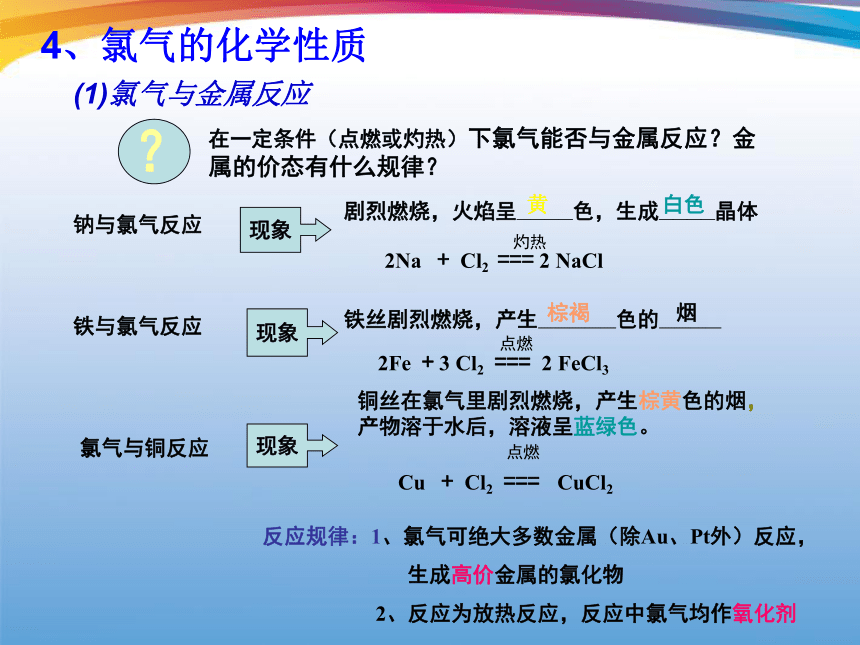
在一定条件(点燃或灼热)下氯气能否与金属反应?金属的价态有什么规律?氯气与铜反应铜丝在氯气里剧烈燃烧,产生棕黄色的烟,产物溶于水后,溶液呈蓝绿色。现象铁与氯气反应现象铁丝剧烈燃烧,产生—————色的————棕褐烟钠与氯气反应现象剧烈燃烧,火焰呈————色,生成————晶体白色反应规律:1、氯气可绝大多数金属(除Au、Pt外)反应,
生成高价金属的氯化物
2、反应为放热反应,反应中氯气均作氧化剂黄(1)氯气与金属反应 ?4、氯气的化学性质例2:怎样制取FeCl2。 Fe+2HCl FeCl2+H2↑例1:下列化合物中,不能由氯气和相应的金属直接反应来制取的是
A. FeCl3 B. CaCl2 C. FeCl2 D. KCl(C)(2)、氯气与某些非金属反应 氯气与金属反应时,是实实在在的得电子,
而在与非金属(如H2)反应时,氯原子和氢原
子都想得电子,最后双方为了达到稳定,形成
共用电子对。 即使这样,形成的共用电子对还
是偏向氯,偏离氢,从而使氯显-1价。
在点燃(或光照)下氯气均能与氢气反应H2 + Cl2 === 2HCl点燃纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰,放出大量的热;生成的气体HCl极易溶于水,其水溶液叫盐酸,我们观察到的白雾就是HCl气体跟空气中的水蒸气结合所形成的盐酸小液滴 。实验证明,在一定条件下,Cl2还能与P、S、C等非金属直接化合。H2作还原剂Cl2作氧化剂实验4-3探究:通过以上实验,你对燃烧条件和本质有什么新的认识?①燃烧不一定有氧气参加,物质并不是只有
在氧气中才可以燃烧。②燃烧的本质是氧化还原反应,所有发光发
热的剧烈的化学反应都称为燃烧。(3)、氯气与水的反应关于次氯酸(HClO)的性质一元弱酸(酸性比碳酸还弱),强氧化性(杀菌、消毒),漂白性,不稳定易分解关于氯水的成分,新制氯水与久置的氯水相比,成分相同吗?干燥的氯气与湿润的氯气在性质上有区别吗?液氯与氯水是否相同?(4)、与碱溶液的反应氯气与水反应生成了盐酸和次氯酸,如果
把氯气通如NaOH溶液中,能否发生反应?
为什么? 思考 Cl2 + 2OH- === Cl- + ClO- + H2O实验室制氯气时,多余的氯气用NaOH溶液吸收关于漂白粉的制取、成分、漂白原理:2Ca(OH)2 + 2Cl2 === CaCl2 + Ca(ClO)2 + 2H2O漂白粉的成分 漂白粉的有效成分 CaCl2 和 Ca(ClO)2的混合物Ca(ClO)2(5)、与盐溶液的反应漂白粉的漂白原理:它的水溶液与空气中的CO2接触反应生成次氯酸的过程。Ca(ClO)2 + CO2 + H2O === CaCO3 + 2HClO与FeCl2 、NaBr、KI等盐溶液反应(表现氯气的强氧化性)2Fe2+ + Cl2 === 2Fe3+ + 2Cl-
Cl2 + 2Br- === 2Cl- + Br2
Cl2 + 2 I- === 2Cl- + I2探究:新制的氯水有什么性质?能与那些物质发生反应?思考与交流1. 从氯气的发现到确认为一种新的元素,时间长达三十多年。你从这一史实中得到什么启示?2.舍勒发现氯气的方法至今还是实验室 制 取氯气的主要方法之一。请写出舍勒发现氯 气的化学反应方程式(1)、反应原理 1.二氧化锰为难溶于水的黑色粉末。
2.要用浓盐酸(有强挥发性)。
3.此反应必须加热。5、氯气的实验室制备固+液(加热)型
有关仪器的名称:铁架台(带铁圈、铁夹)、酒精灯、石棉网、烧瓶、双孔塞、分液漏斗、玻璃导管。
组装时必须由下到上,从左到右。(2)、发生装置a. 向上排空气法b. 排饱和食盐水法(3)、收集装置(4)、尾气吸收 氯气有毒,会污染空气,故用饱和氢氧化钠溶液吸收。饱和NaOH Cl2 + 2NaOH == NaCl + NaClO + H2O 、HCl气体水蒸气饱和食盐水浓硫酸浓 H2SO4 饱和食盐水(5)、净化装置1、下列关于氯水的说法中正确的是:
A、新制氯水中只含有Cl2和H2O分子
B、新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
C、光照氯水有气泡逸出,该气体是Cl2
D、氯水放置数天后酸性增强
2、下列物质能使红墨水褪色的是
A、活性炭 B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液3、当有大量Cl2逸出在周围空间时,可以用含有一定浓度某种物质的水溶液的毛巾捂住鼻子,该物质最好是:
A、NaOH B、NaCl
C、KBr D、Na2CO34、实验室用二氧化锰和浓盐酸制氯气,主要操作有:①将烧瓶固定在铁架台上;②把酒精灯放在铁架台上,根据酒精灯确定铁圈的高度,固定铁圈放好石棉网;③向烧瓶中加入MnO2,再向分液漏斗中加入浓盐酸,并将导管放入集气瓶中;④检查装置的气密性;⑤在烧瓶上装好分液漏斗,连接好导气管。
最好的实验步骤是:
A、②③④①⑤ B、②①③⑤④
C、②①⑤④③ D、②①③④⑤5、下列物质既能由两种单质化合而生成,又能由单质与酸反应而生成的是:
A、FeCl2 B、CuCl2
C、AlCl3 D、FeCl3
6、密闭容器中充有H2、O2、Cl2,充分燃烧后,冷却至室温,容器内无气体剩余,且所得溶液中溶质的质量分数为33.6%,则原气体中的H2、O2、Cl2的体积比为:
A 、9∶4∶2 B、9∶4∶1
C、2∶1∶1 D、2∶1∶1 7、标准状况下,有O2和Cl2组成的混合气体共500mL,通入H2使其恰好完全燃烧,用水吸收生成物得250mL溶液,从中取出25mL,用0.125mol.L-1NaOH溶液20mL恰好中和,则与混合气体反应的H2的体积为
A、280mL B、440mL
C、500mL D、720mL
8、氯气能使湿润的蓝色石蕊试纸
A、褪色 B、变成红色
C、先褪色后变红 D、先变红后褪色 启示1:科学研究需要有正确的理论作指导,错误的理论只能浪费时间和精力。启示2:科学研究需要以大量事实为依据,只有大量事实才能推翻错误 的理论,建立正确的理论或推动科学理论的发展。启示3:科学研究需要有热爱科学的思想和奉献科学的精神。
如果将海水中的盐类全部提 取出来,铺在地球的陆地
上,可以使陆地平均升高
150mNaCl也大量存在于陆地盐矿中氯元素主要以什么形式存在于哪里?
氯元素主要以NaCl的形式存在于海水
及陆地的盐矿中,所以说海水中富集
了丰富的氯。 第二节 富集在海水中的元素——氯一、氯与其单质1、氯的原子结构和性质性质:化合价:-1,+1,+2,+3,
+4,+5,+6,+7
得电子能力强,非金属性强2、氯气的分子结构Cl2 ;Cl—Cl ;氯气属于双原子分子结构3、氯气的物理性质(色、状、味、水溶性、密度、毒性)(1)、氯气是黄绿色有刺激性气味的有毒气体,易液化(2)、氯气可溶于水,氯水呈浅黄绿色
(常温常压下,1体积水可溶解2体积氯气)(3)、密度比空气大?闻氯气的方法是:
用手轻轻地在瓶口扇动,仅使极少量的氯气飘进鼻孔。
?注意:
这是闻各种气体的气味的方法。
在一定条件(点燃或灼热)下氯气能否与金属反应?金属的价态有什么规律?氯气与铜反应铜丝在氯气里剧烈燃烧,产生棕黄色的烟,产物溶于水后,溶液呈蓝绿色。现象铁与氯气反应现象铁丝剧烈燃烧,产生—————色的————棕褐烟钠与氯气反应现象剧烈燃烧,火焰呈————色,生成————晶体白色反应规律:1、氯气可绝大多数金属(除Au、Pt外)反应,
生成高价金属的氯化物
2、反应为放热反应,反应中氯气均作氧化剂黄(1)氯气与金属反应 ?4、氯气的化学性质例2:怎样制取FeCl2。 Fe+2HCl FeCl2+H2↑例1:下列化合物中,不能由氯气和相应的金属直接反应来制取的是
A. FeCl3 B. CaCl2 C. FeCl2 D. KCl(C)(2)、氯气与某些非金属反应 氯气与金属反应时,是实实在在的得电子,
而在与非金属(如H2)反应时,氯原子和氢原
子都想得电子,最后双方为了达到稳定,形成
共用电子对。 即使这样,形成的共用电子对还
是偏向氯,偏离氢,从而使氯显-1价。
在点燃(或光照)下氯气均能与氢气反应H2 + Cl2 === 2HCl点燃纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰,放出大量的热;生成的气体HCl极易溶于水,其水溶液叫盐酸,我们观察到的白雾就是HCl气体跟空气中的水蒸气结合所形成的盐酸小液滴 。实验证明,在一定条件下,Cl2还能与P、S、C等非金属直接化合。H2作还原剂Cl2作氧化剂实验4-3探究:通过以上实验,你对燃烧条件和本质有什么新的认识?①燃烧不一定有氧气参加,物质并不是只有
在氧气中才可以燃烧。②燃烧的本质是氧化还原反应,所有发光发
热的剧烈的化学反应都称为燃烧。(3)、氯气与水的反应关于次氯酸(HClO)的性质一元弱酸(酸性比碳酸还弱),强氧化性(杀菌、消毒),漂白性,不稳定易分解关于氯水的成分,新制氯水与久置的氯水相比,成分相同吗?干燥的氯气与湿润的氯气在性质上有区别吗?液氯与氯水是否相同?(4)、与碱溶液的反应氯气与水反应生成了盐酸和次氯酸,如果
把氯气通如NaOH溶液中,能否发生反应?
为什么? 思考 Cl2 + 2OH- === Cl- + ClO- + H2O实验室制氯气时,多余的氯气用NaOH溶液吸收关于漂白粉的制取、成分、漂白原理:2Ca(OH)2 + 2Cl2 === CaCl2 + Ca(ClO)2 + 2H2O漂白粉的成分 漂白粉的有效成分 CaCl2 和 Ca(ClO)2的混合物Ca(ClO)2(5)、与盐溶液的反应漂白粉的漂白原理:它的水溶液与空气中的CO2接触反应生成次氯酸的过程。Ca(ClO)2 + CO2 + H2O === CaCO3 + 2HClO与FeCl2 、NaBr、KI等盐溶液反应(表现氯气的强氧化性)2Fe2+ + Cl2 === 2Fe3+ + 2Cl-
Cl2 + 2Br- === 2Cl- + Br2
Cl2 + 2 I- === 2Cl- + I2探究:新制的氯水有什么性质?能与那些物质发生反应?思考与交流1. 从氯气的发现到确认为一种新的元素,时间长达三十多年。你从这一史实中得到什么启示?2.舍勒发现氯气的方法至今还是实验室 制 取氯气的主要方法之一。请写出舍勒发现氯 气的化学反应方程式(1)、反应原理 1.二氧化锰为难溶于水的黑色粉末。
2.要用浓盐酸(有强挥发性)。
3.此反应必须加热。5、氯气的实验室制备固+液(加热)型
有关仪器的名称:铁架台(带铁圈、铁夹)、酒精灯、石棉网、烧瓶、双孔塞、分液漏斗、玻璃导管。
组装时必须由下到上,从左到右。(2)、发生装置a. 向上排空气法b. 排饱和食盐水法(3)、收集装置(4)、尾气吸收 氯气有毒,会污染空气,故用饱和氢氧化钠溶液吸收。饱和NaOH Cl2 + 2NaOH == NaCl + NaClO + H2O 、HCl气体水蒸气饱和食盐水浓硫酸浓 H2SO4 饱和食盐水(5)、净化装置1、下列关于氯水的说法中正确的是:
A、新制氯水中只含有Cl2和H2O分子
B、新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
C、光照氯水有气泡逸出,该气体是Cl2
D、氯水放置数天后酸性增强
2、下列物质能使红墨水褪色的是
A、活性炭 B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液3、当有大量Cl2逸出在周围空间时,可以用含有一定浓度某种物质的水溶液的毛巾捂住鼻子,该物质最好是:
A、NaOH B、NaCl
C、KBr D、Na2CO34、实验室用二氧化锰和浓盐酸制氯气,主要操作有:①将烧瓶固定在铁架台上;②把酒精灯放在铁架台上,根据酒精灯确定铁圈的高度,固定铁圈放好石棉网;③向烧瓶中加入MnO2,再向分液漏斗中加入浓盐酸,并将导管放入集气瓶中;④检查装置的气密性;⑤在烧瓶上装好分液漏斗,连接好导气管。
最好的实验步骤是:
A、②③④①⑤ B、②①③⑤④
C、②①⑤④③ D、②①③④⑤5、下列物质既能由两种单质化合而生成,又能由单质与酸反应而生成的是:
A、FeCl2 B、CuCl2
C、AlCl3 D、FeCl3
6、密闭容器中充有H2、O2、Cl2,充分燃烧后,冷却至室温,容器内无气体剩余,且所得溶液中溶质的质量分数为33.6%,则原气体中的H2、O2、Cl2的体积比为:
A 、9∶4∶2 B、9∶4∶1
C、2∶1∶1 D、2∶1∶1 7、标准状况下,有O2和Cl2组成的混合气体共500mL,通入H2使其恰好完全燃烧,用水吸收生成物得250mL溶液,从中取出25mL,用0.125mol.L-1NaOH溶液20mL恰好中和,则与混合气体反应的H2的体积为
A、280mL B、440mL
C、500mL D、720mL
8、氯气能使湿润的蓝色石蕊试纸
A、褪色 B、变成红色
C、先褪色后变红 D、先变红后褪色 启示1:科学研究需要有正确的理论作指导,错误的理论只能浪费时间和精力。启示2:科学研究需要以大量事实为依据,只有大量事实才能推翻错误 的理论,建立正确的理论或推动科学理论的发展。启示3:科学研究需要有热爱科学的思想和奉献科学的精神。
