第四单元盐 化肥单元训练--2021-2022学年九年级化学人教版(五四学制)全一册(word版 含答案)
文档属性
| 名称 | 第四单元盐 化肥单元训练--2021-2022学年九年级化学人教版(五四学制)全一册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 90.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-17 00:00:00 | ||
图片预览



文档简介
第四单元盐 化肥训练2021-2022学年九年级化学人教版(五四学制)全一册
一、单选题
1.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是
A.NH4NO3 B.KNO3
C.Ca3(PO4)2 D.KCl
2.下列化肥从外观即可与其他化肥相区别的是( )
A.硝酸钾 B.氯化铵 C.磷矿粉 D.氯化钾
3.下列化学方程式所表示的化学反应能发生的是 ( )
A.Cu+H2SO4=CuSO4+H2↑ B.Fe+ Zn( NO3)2=Fe(NO3)2+Zn↓
C.CuCl2+2NaOH=Cu(OH)2↓+2NaCl D.Na2CO3+2KNO3=K2CO3+ 2NaNO3
4.下列化肥属于复合肥料的是
A.KCl
B.Ca2(PO4)3
C.KNO3
D.CO(NH2)2
5.下列物质的用途不正确的是( )
A.用金属铜作导线
B.用浓盐酸作干燥剂
C.用金刚石切割玻璃
D.用小苏打治疗胃酸过多
6.草木灰是一种农家肥,其主要成分是K2CO3,它属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
7.下列实验方案不能达到目的的是( )
A.NaOH溶液除去稀盐酸中的FeCl3 B.用带火星的木条鉴别O2和CO2
C.高温下足量Fe2O3除去CO2中的CO D.用水鉴别NH4NO3和NaOH两种固体
8.已知,常温下氯化钠、氯化钡的水溶液呈中性,向含有盐酸和氯化钡的混合溶液中逐滴滴入过量的X,溶液pH与滴入X的量的关系如图所示,则X可能是下列物质中的( )
A.NaOH溶液
B.H2O
C.AgNO3溶液
D.Na2CO3溶液
9.三瓶无标签的无色溶液,只知道它们分别是稀盐酸、BaCl2溶液和KNO3溶液中的各一种。下列四种试液中,能将三种无色溶液一次鉴别开来的是
A.NaC1溶液 B.稀硫酸 C.Na2CO3溶液 D.AgNO3溶液
10.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项 物质 选用试剂 操作方法
A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干
B CO(CO2) NaOH溶液、浓硫酸 洗气、干燥
C CaO(CaCO3) 水 过滤、烘干
D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
11.化学美无处不在,如图是物质间发生化学反应的颜色变化,其中X是
A.稀盐酸
B.稀硫酸
C.硫酸钠溶液
D.氢氧化钠溶液
二、简答题
12.化学老师在课堂上组织同学们开展“使用农药、化肥‘利’与‘弊’”的辩论,请你从化学的角度各说出一个观点。
(1)“利”:_____________________________________。
(2)“弊”:_______________________________________。
13.庄稼一枝花,全靠肥当家。现有失去标签的两种氮肥;碳酸氢铵( NH4HCO3)和尿素(CO(NH2)2)。
(1)这两种氮肥,哪一种含氮量高_____?
(2)设计实验鉴别这两种氮肥,写出实验步骤、现象和结论_____。
14.根据复分解反应发生的条件,并利用书后附录1所提供的信息,判断下列物质间能否发生复分解反应。如能发生反应,写出反应的化学方程式。
(1)碳酸钠溶液和氯化钙溶液
(2)氢氧化钾溶液和盐酸
(3)氢氧化钠溶液和氯化钾溶液
(4)碳酸钾溶液和盐酸
(5)硫酸铜溶液和氯化钡溶液
三、推断题
15.有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是:Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“﹣”表示观察不到明显变化。试回答下面问题:
A B C D E F G
A ﹣ ﹣ ﹣ ﹣ ﹣ ﹣ ↓
B ﹣ ﹣ ﹣ ﹣ ↓ ↓ ↓
C ﹣ ﹣ ﹣ ↓ ﹣ ↓ ↓
D ﹣ ﹣ ↓ ﹣ ↓ ↓ ↓
E ﹣ ↓ ﹣ ↓ ﹣ ↓ ﹣
F ﹣ ↓ ↓ ↓ ↓ ﹣ ↓
G ↓ ↓ ↓ ↓ ﹣ ↓ ﹣
(1)A、G的化学式分别是_______,判断的理由是_______。
(2)写出下列物质间的反应方程式。B和F_______;D和E_______。
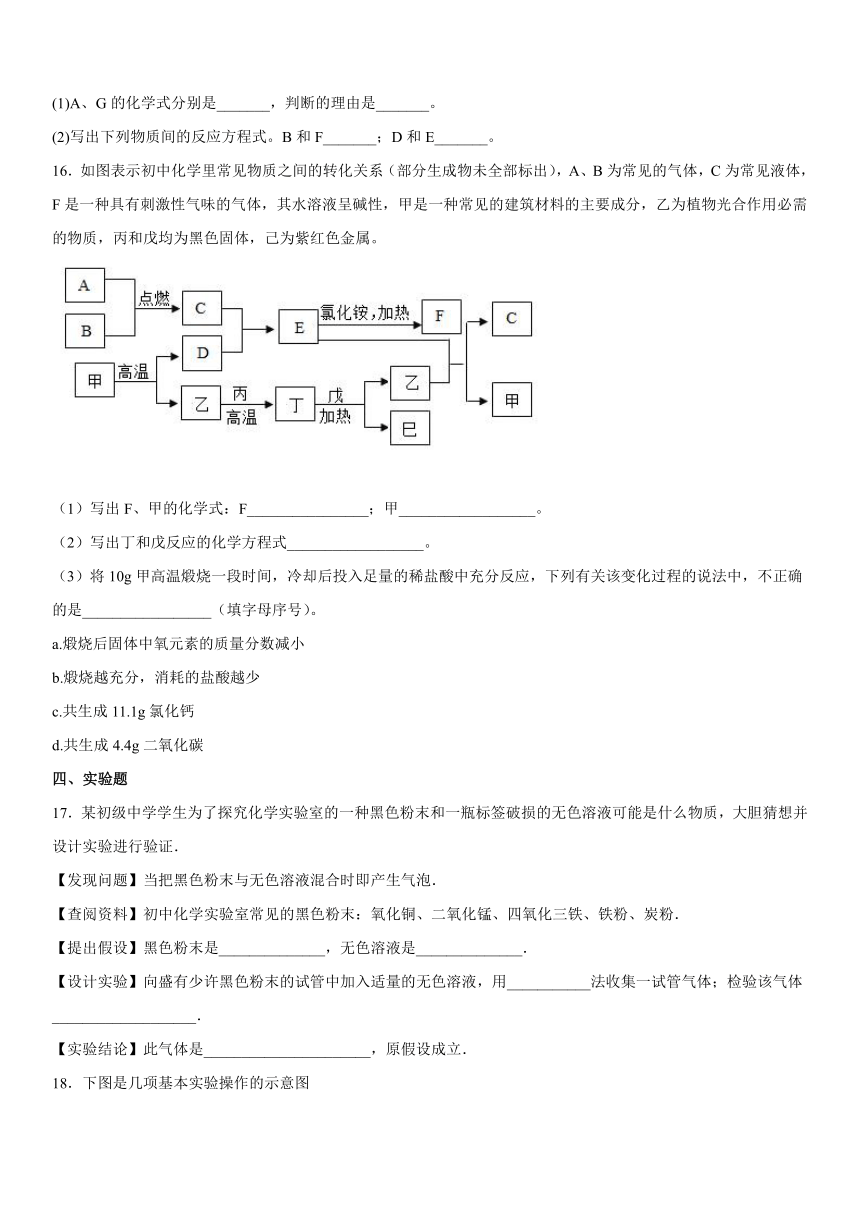
16.如图表示初中化学里常见物质之间的转化关系(部分生成物未全部标出),A、B为常见的气体,C为常见液体,F是一种具有刺激性气味的气体,其水溶液呈碱性,甲是一种常见的建筑材料的主要成分,乙为植物光合作用必需的物质,丙和戊均为黑色固体,己为紫红色金属。
(1)写出F、甲的化学式:F________________;甲__________________。
(2)写出丁和戊反应的化学方程式__________________。
(3)将10g甲高温煅烧一段时间,冷却后投入足量的稀盐酸中充分反应,下列有关该变化过程的说法中,不正确的是_________________(填字母序号)。
a.煅烧后固体中氧元素的质量分数减小
b.煅烧越充分,消耗的盐酸越少
c.共生成11.1g氯化钙
d.共生成4.4g二氧化碳
四、实验题
17.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
18.下图是几项基本实验操作的示意图
(1)仪器X的名称是____________;加热液体时,液体体积不能超过试管容积的_______;
(2)蒸发结晶时,用玻璃棒搅拌,当_______________________,停止加热;
(3)测定溶液pH时,用玻璃棒蘸取待测液滴到pH试纸上,______________,读出pH。
19.一包白色粉末可能含有碳酸钙、碳酸钠、硫酸钠、氯化钠、硝酸钾中的一种或几种,为了确定其组成,进行实验,按要求进行回答:
实验步骤 实验过程 实验现象 结论
① 取样,进行焰色反应,透过蓝色钴玻璃 火焰呈__________ 原粉末中含有硝酸钾
② _____________ 原粉末中肯定不含碳酸钙
③ 有气泡产生 原粉末中肯定有_______
④ 取步骤③试管中的溶液 Ⅰ.先加入__________ Ⅱ.再加入__________ __________________ 原粉末中肯定还有的物质是氯化钠肯定没有硫酸钠
⑤ 反思:在步骤③中加入的稀硝酸是否一定要过量,理由是______________
五、计算题
20.用“侯氏制碱法”制取的纯碱中常含有少量的氯化钠。某化学实验小组同学为测定某厂生产的纯碱中碳酸钠的含量,称取12g样品放入烧杯中并滴加稀盐酸,当盐酸滴加至73g时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6g。
试计算:
(1)产生二氧化碳气体的质量是_______。
(2)该纯碱样品中氯化钠的质量。
(3)此次反应所得溶液中溶质的质量分数。(计算结果精确到0.1%)
21.工业纯碱中含少量氯化钠。兴趣小组采用如图装置测定工业纯碱样品中碳酸钠的质量分数。称取12g样品与足量的稀盐酸充分反应,生成的二氧化碳通入乙装置,实验测得乙装置增加的质量为 4.4g。
(1)计算样品中碳酸钠的质量。
(2)实验分析:该方法测得的碳酸钠的质量分数偏______,原因是______。
试卷第1页,共3页
参考答案:
1.B
2.C
3.C
4.C
5.B
6.A
7.A
8.D
9.C
10.B
11.B
12. 促进物作物增产 污染环境,影响人体健康
13. 尿素[或CO(NH2)2] 取少量的两种氮肥,分别加入一定量的熟石灰,研磨(或加热),有刺激性气味产生的是碳酸氢铵,无刺激性气味产生的是尿素(或取少量的两种氮肥,分别滴加稀盐酸,有气泡产生的是碳酸氢铵,无气泡产生的是尿素)
14.(1)
(2)
(3)不能发生反应
(4)
(5)
15. KCl,AgNO3 物质间混合时只生成一种沉淀的是KCl,生成AgCl为沉淀 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3
16. NH3 CaCO3 b
17. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
18. 试管夹 1/3 较多固体时 显色与标准比色卡比较
19. 紫色 得到澄清溶液 碳酸钠 过量的Ba(NO3)2溶液 适量的AgNO3溶液 加入Ba(NO3)2溶液无现象,加入AgNO3溶液产生白色沉淀 除去Na2CO3,防止对NaCl 、Na2SO4的检验造成干扰
20.(1)4.4;(2)1.4;(3)16.3%
21.(1)解:设样品中碳酸钠的质量为x
答:样品中碳酸钠的质量为10.6g。
(2)大;乙装置中氢氧化钠会吸收来自于甲装置中挥发出的氯化氢气体
答案第1页,共2页
答案第1页,共2页
一、单选题
1.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是
A.NH4NO3 B.KNO3
C.Ca3(PO4)2 D.KCl
2.下列化肥从外观即可与其他化肥相区别的是( )
A.硝酸钾 B.氯化铵 C.磷矿粉 D.氯化钾
3.下列化学方程式所表示的化学反应能发生的是 ( )
A.Cu+H2SO4=CuSO4+H2↑ B.Fe+ Zn( NO3)2=Fe(NO3)2+Zn↓
C.CuCl2+2NaOH=Cu(OH)2↓+2NaCl D.Na2CO3+2KNO3=K2CO3+ 2NaNO3
4.下列化肥属于复合肥料的是
A.KCl
B.Ca2(PO4)3
C.KNO3
D.CO(NH2)2
5.下列物质的用途不正确的是( )
A.用金属铜作导线
B.用浓盐酸作干燥剂
C.用金刚石切割玻璃
D.用小苏打治疗胃酸过多
6.草木灰是一种农家肥,其主要成分是K2CO3,它属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
7.下列实验方案不能达到目的的是( )
A.NaOH溶液除去稀盐酸中的FeCl3 B.用带火星的木条鉴别O2和CO2
C.高温下足量Fe2O3除去CO2中的CO D.用水鉴别NH4NO3和NaOH两种固体
8.已知,常温下氯化钠、氯化钡的水溶液呈中性,向含有盐酸和氯化钡的混合溶液中逐滴滴入过量的X,溶液pH与滴入X的量的关系如图所示,则X可能是下列物质中的( )
A.NaOH溶液
B.H2O
C.AgNO3溶液
D.Na2CO3溶液
9.三瓶无标签的无色溶液,只知道它们分别是稀盐酸、BaCl2溶液和KNO3溶液中的各一种。下列四种试液中,能将三种无色溶液一次鉴别开来的是
A.NaC1溶液 B.稀硫酸 C.Na2CO3溶液 D.AgNO3溶液
10.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项 物质 选用试剂 操作方法
A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干
B CO(CO2) NaOH溶液、浓硫酸 洗气、干燥
C CaO(CaCO3) 水 过滤、烘干
D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
11.化学美无处不在,如图是物质间发生化学反应的颜色变化,其中X是
A.稀盐酸
B.稀硫酸
C.硫酸钠溶液
D.氢氧化钠溶液
二、简答题
12.化学老师在课堂上组织同学们开展“使用农药、化肥‘利’与‘弊’”的辩论,请你从化学的角度各说出一个观点。
(1)“利”:_____________________________________。
(2)“弊”:_______________________________________。
13.庄稼一枝花,全靠肥当家。现有失去标签的两种氮肥;碳酸氢铵( NH4HCO3)和尿素(CO(NH2)2)。
(1)这两种氮肥,哪一种含氮量高_____?
(2)设计实验鉴别这两种氮肥,写出实验步骤、现象和结论_____。
14.根据复分解反应发生的条件,并利用书后附录1所提供的信息,判断下列物质间能否发生复分解反应。如能发生反应,写出反应的化学方程式。
(1)碳酸钠溶液和氯化钙溶液
(2)氢氧化钾溶液和盐酸
(3)氢氧化钠溶液和氯化钾溶液
(4)碳酸钾溶液和盐酸
(5)硫酸铜溶液和氯化钡溶液
三、推断题
15.有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是:Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“﹣”表示观察不到明显变化。试回答下面问题:
A B C D E F G
A ﹣ ﹣ ﹣ ﹣ ﹣ ﹣ ↓
B ﹣ ﹣ ﹣ ﹣ ↓ ↓ ↓
C ﹣ ﹣ ﹣ ↓ ﹣ ↓ ↓
D ﹣ ﹣ ↓ ﹣ ↓ ↓ ↓
E ﹣ ↓ ﹣ ↓ ﹣ ↓ ﹣
F ﹣ ↓ ↓ ↓ ↓ ﹣ ↓
G ↓ ↓ ↓ ↓ ﹣ ↓ ﹣
(1)A、G的化学式分别是_______,判断的理由是_______。
(2)写出下列物质间的反应方程式。B和F_______;D和E_______。
16.如图表示初中化学里常见物质之间的转化关系(部分生成物未全部标出),A、B为常见的气体,C为常见液体,F是一种具有刺激性气味的气体,其水溶液呈碱性,甲是一种常见的建筑材料的主要成分,乙为植物光合作用必需的物质,丙和戊均为黑色固体,己为紫红色金属。
(1)写出F、甲的化学式:F________________;甲__________________。
(2)写出丁和戊反应的化学方程式__________________。
(3)将10g甲高温煅烧一段时间,冷却后投入足量的稀盐酸中充分反应,下列有关该变化过程的说法中,不正确的是_________________(填字母序号)。
a.煅烧后固体中氧元素的质量分数减小
b.煅烧越充分,消耗的盐酸越少
c.共生成11.1g氯化钙
d.共生成4.4g二氧化碳
四、实验题
17.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
18.下图是几项基本实验操作的示意图
(1)仪器X的名称是____________;加热液体时,液体体积不能超过试管容积的_______;
(2)蒸发结晶时,用玻璃棒搅拌,当_______________________,停止加热;
(3)测定溶液pH时,用玻璃棒蘸取待测液滴到pH试纸上,______________,读出pH。
19.一包白色粉末可能含有碳酸钙、碳酸钠、硫酸钠、氯化钠、硝酸钾中的一种或几种,为了确定其组成,进行实验,按要求进行回答:
实验步骤 实验过程 实验现象 结论
① 取样,进行焰色反应,透过蓝色钴玻璃 火焰呈__________ 原粉末中含有硝酸钾
② _____________ 原粉末中肯定不含碳酸钙
③ 有气泡产生 原粉末中肯定有_______
④ 取步骤③试管中的溶液 Ⅰ.先加入__________ Ⅱ.再加入__________ __________________ 原粉末中肯定还有的物质是氯化钠肯定没有硫酸钠
⑤ 反思:在步骤③中加入的稀硝酸是否一定要过量,理由是______________
五、计算题
20.用“侯氏制碱法”制取的纯碱中常含有少量的氯化钠。某化学实验小组同学为测定某厂生产的纯碱中碳酸钠的含量,称取12g样品放入烧杯中并滴加稀盐酸,当盐酸滴加至73g时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6g。
试计算:
(1)产生二氧化碳气体的质量是_______。
(2)该纯碱样品中氯化钠的质量。
(3)此次反应所得溶液中溶质的质量分数。(计算结果精确到0.1%)
21.工业纯碱中含少量氯化钠。兴趣小组采用如图装置测定工业纯碱样品中碳酸钠的质量分数。称取12g样品与足量的稀盐酸充分反应,生成的二氧化碳通入乙装置,实验测得乙装置增加的质量为 4.4g。
(1)计算样品中碳酸钠的质量。
(2)实验分析:该方法测得的碳酸钠的质量分数偏______,原因是______。
试卷第1页,共3页
参考答案:
1.B
2.C
3.C
4.C
5.B
6.A
7.A
8.D
9.C
10.B
11.B
12. 促进物作物增产 污染环境,影响人体健康
13. 尿素[或CO(NH2)2] 取少量的两种氮肥,分别加入一定量的熟石灰,研磨(或加热),有刺激性气味产生的是碳酸氢铵,无刺激性气味产生的是尿素(或取少量的两种氮肥,分别滴加稀盐酸,有气泡产生的是碳酸氢铵,无气泡产生的是尿素)
14.(1)
(2)
(3)不能发生反应
(4)
(5)
15. KCl,AgNO3 物质间混合时只生成一种沉淀的是KCl,生成AgCl为沉淀 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3
16. NH3 CaCO3 b
17. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
18. 试管夹 1/3 较多固体时 显色与标准比色卡比较
19. 紫色 得到澄清溶液 碳酸钠 过量的Ba(NO3)2溶液 适量的AgNO3溶液 加入Ba(NO3)2溶液无现象,加入AgNO3溶液产生白色沉淀 除去Na2CO3,防止对NaCl 、Na2SO4的检验造成干扰
20.(1)4.4;(2)1.4;(3)16.3%
21.(1)解:设样品中碳酸钠的质量为x
答:样品中碳酸钠的质量为10.6g。
(2)大;乙装置中氢氧化钠会吸收来自于甲装置中挥发出的氯化氢气体
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
