硫和氮的氧化物
图片预览





文档简介
课件57张PPT。1第三节
硫和氮的氧化物第二课时
氮及氮的化合物第一课时
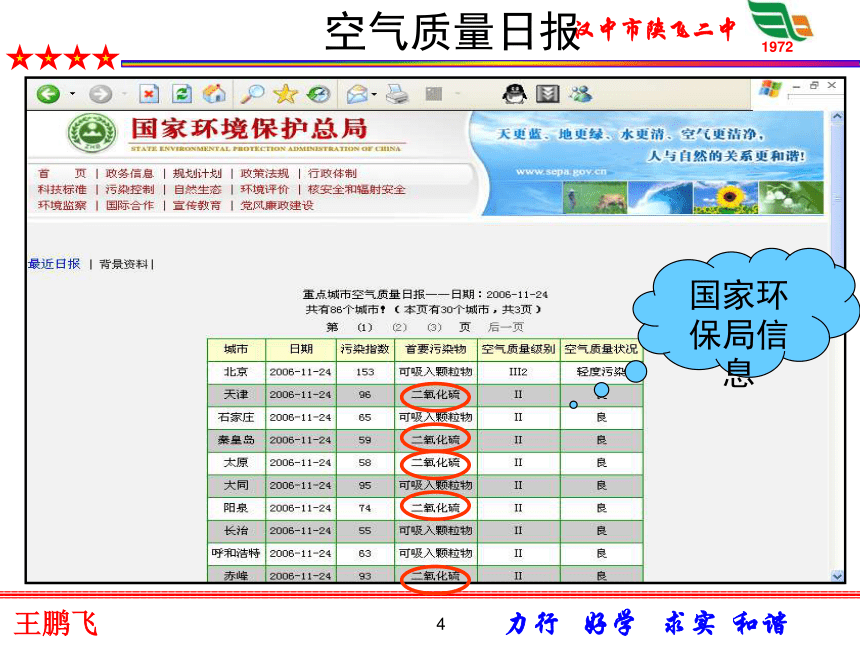
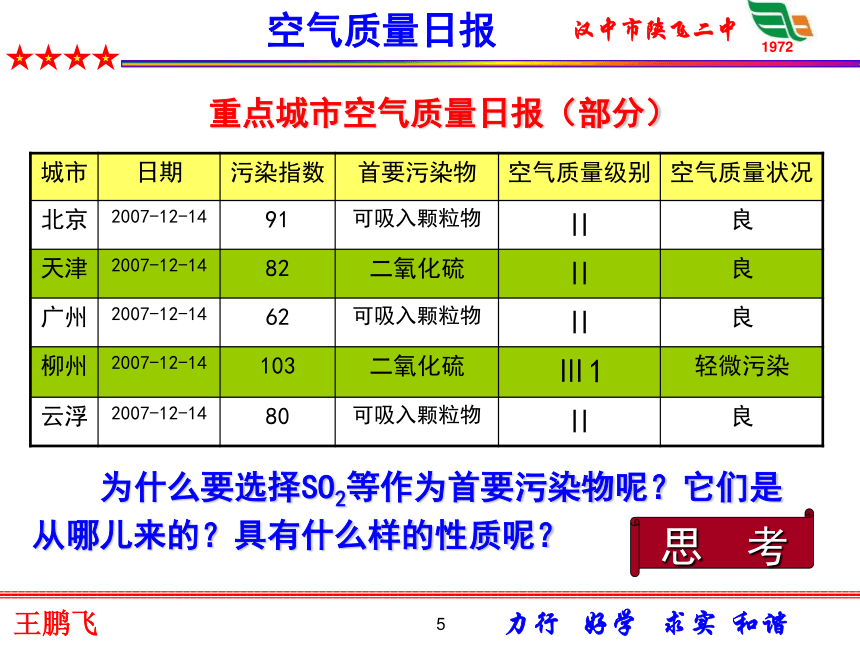
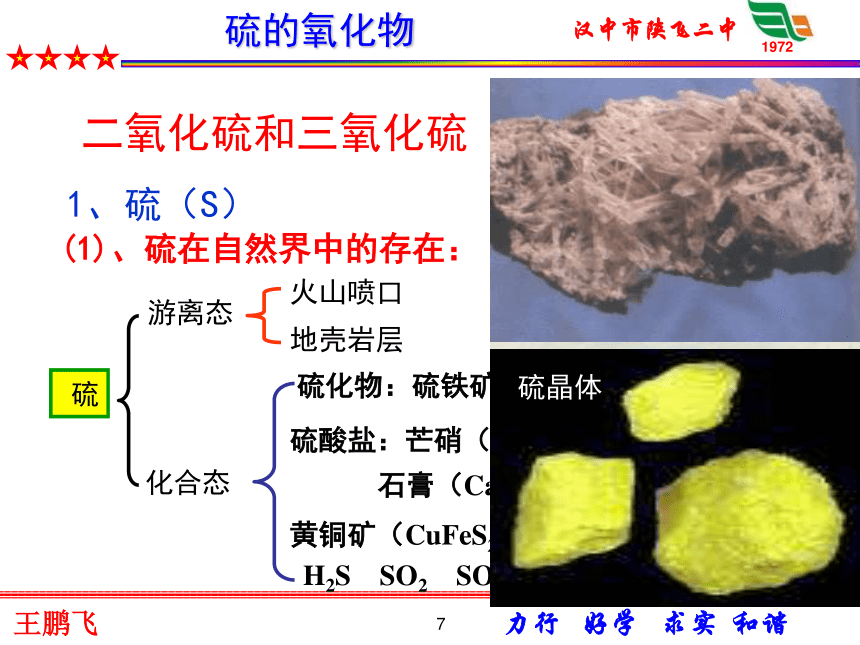
硫及硫的化合物第四章 非金属及其化合物2第四章非金属及其化合物3关于城市空气质量日报比比看谁知道得多??4空气质量日报国家环保局信息5 重点城市空气质量日报(部分) 为什么要选择SO2等作为首要污染物呢?它们是从哪儿来的?具有什么样的性质呢?思 考空气质量日报6 二氧化硫对环境的污染7二1、硫(S)(1)、硫在自然界中的存在:硫游离态化合态火山喷口地壳岩层硫化物:硫铁矿或黄铁矿(FeS2)等硫酸盐:芒硝(Na2SO4·10H2O) 石膏(CaSO4·2H2O)黄铜矿(CuFeS2)H2S SO2 SO3硫粉硫的氧化物 硫晶体 二氧化硫和三氧化硫8 淡黄色晶体 质脆,容易研成粉末。 不溶于水,微溶于酒精,
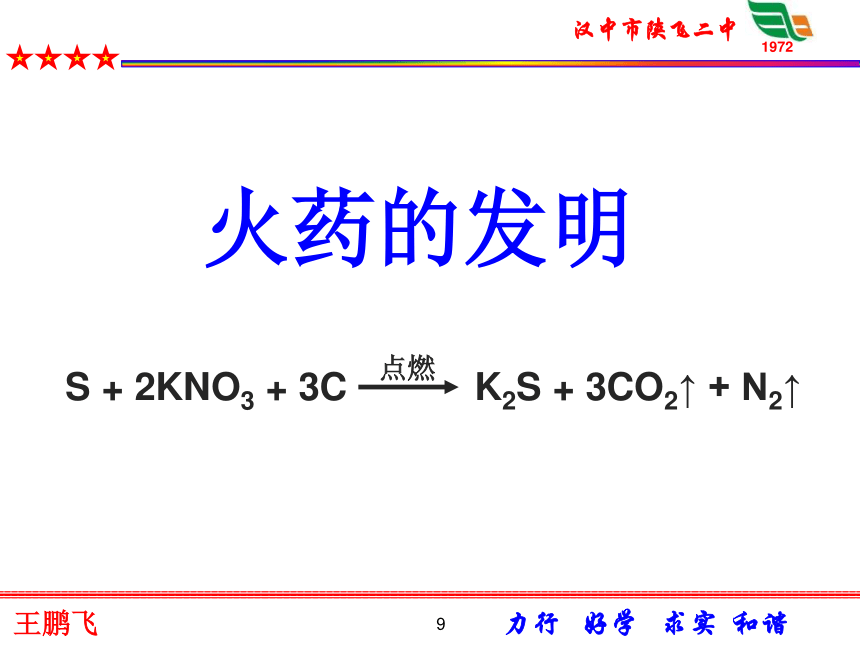
易溶于二硫化碳。 密度比水大(约为2 g/cm3 ) 熔沸点低(112.8℃, 444.6 ℃) 俗称:硫磺(2)硫的物理性质硫的氧化物 9火药的发明10(3)硫的化学性质S + O2 = SO20+4硫作为还原剂,具有还原性。划火柴时常闻到的一股呛鼻的气味,就是火柴头
成份中的硫燃烧后产生的二氧化硫。有刺激性气味的气体生成。
硫在空气中安静地燃烧,发出淡蓝色火焰;
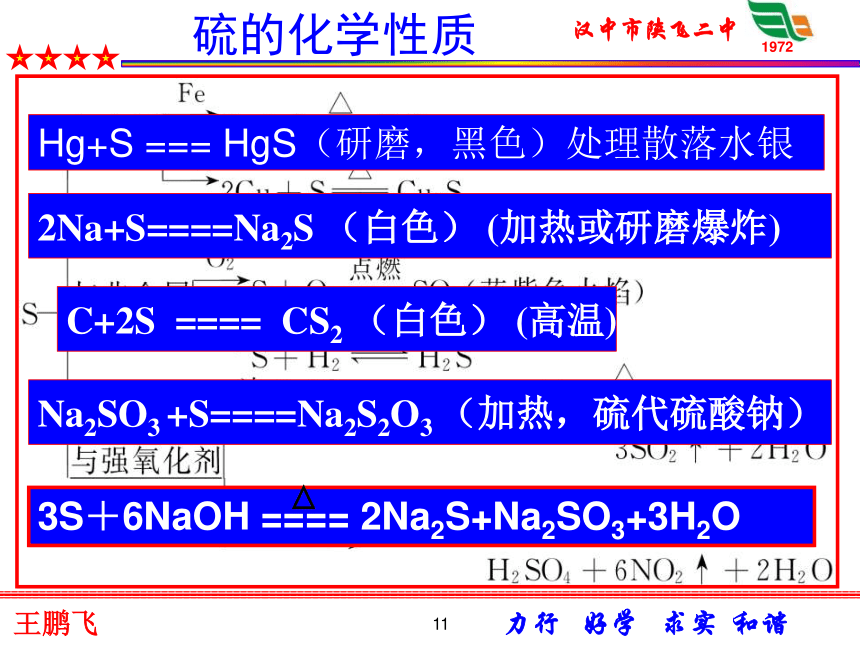
硫在纯氧中燃烧发出蓝紫色火焰点燃硫的氧化物 11硫的化学性质Hg+S === HgS(研磨,黑色)处理散落水银2Na+S====Na2S (白色) (加热或研磨爆炸)C+2S ==== CS2 (白色) (高温)Na2SO3 +S====Na2S2O3 (加热,硫代硫酸钠)12硫的氧化物 二. 二氧化硫(SO2) 1、 SO2的物理性质 现象:试管内水位上升 结论: SO2易溶于水 二氧化硫是污染大气的主要有害物质之一13 1. SO2的物理性质SO2无色气体刺激性气味有毒易溶于水(1:40)密度比空气大易液化二氧化硫是一种无色、有刺激性气味、有毒、比空气重、容易液化、易溶于水的气体。 硫的氧化物 14SO2 + H2O逆反应H2SO3正反应2. SO2的化学性质① SO2能与水反应 可逆反应:在相同条件下,既能向正反应方向进行、又能向逆反应方向进行的反应。 思 考 2H2O 通电 2H2↑ +O2 ↑ 与 2H2+O2 点燃 2H2O
是可逆反应吗? 二氧化硫的化学性质——酸性氧化物的通性(亚硫酸)硫的氧化物 152.SO2的化学性质② SO2的漂白性漂白原理:SO2 能与某些有色物质生成不稳定的无色物质。(暂时性)现象:滴入品红溶液后,颜色褪去;加热时又恢复原来的红色。硫的氧化物 16 ② SO2具有漂白作用:但漂白后的新物质不稳定,易恢复原来的颜色(检验SO2的存在) SO2的化学性质17 SO2的化学性质18 思考:草帽、纸张为什么会泛黄?探讨:你学过的哪些物质具有漂白性?活性炭H2O2Na2O2HClO… ...物理吸附氧化漂白漂白原理是否相同? SO2的化学性质19永久性暂时性氯气中HClO将有色
物质氧化成无色物质氧化还原反应非氧化还原反应可漂白大多数有色物质,能使紫色石蕊试液褪色SO2与有色物质直接结合生成不稳定无色物质 可漂白某些有色物质,不能使紫色石蕊试液褪色二氧化硫与氯气的漂白性比较思考? SO2的化学性质20探 究根据硫原子的结构示意图 ,判断硫元素的最高化合价和最低化合价 。并结合SO2中硫元素的化合价,分析SO2 还可能有什么化学性质? SO2的化学性质21③ SO2既有氧化性,又有还原性(氧化性) (还原性) SO2的化学性质22(工业制硫酸的第二步)SO2+ Cl2+2H2O =H2SO4+2HCl2H2S+SO2=3S↓+2H2OSO2的还原性SO2的氧化性SO2能使溴水褪色,试分析褪色原因? SO2的化学性质23 ④二氧化硫跟碱反应(酸性氧化物) SO2 + Ca(OH)2 = CaSO3 + H2O CaSO3 + SO2 + H2O = Ca(HSO3)2注
意使澄清石灰水先变浑浊后变澄清的气体,除二氧化碳外,还可能是二氧化硫。2SO2 + Ca(OH)2 = Ca(HSO3)2 少量过量 SO2的化学性质24⑤二氧化硫跟碱性氧化物反应
——酸性氧化物的通性——防治大气污染,石灰法脱硫SO2+Na2O=Na2SO3 SO2的化学性质25作漂白剂杀菌、防腐三.SO2的用途SO2的用途制硫酸26无色固体,熔点(16.8℃)
沸点(44.8℃ )都很低工业上常用上面两个反应制取硫酸 3、三氧化硫——酸性氧化物 SO3的化学性质27 SO3 + Ca(OH)2 = CaSO4+ H2O SO3 + CaO = CaSO4三氧化硫跟碱或碱性氧化物反应 SO3的化学性质28硫化氢的性质资料卡片阅读课本P91资料卡片,理解如下内容:1.硫化氢的物理性质:2.硫化氢的化学性质:3.硫化氢的毒性:硫化氢的可燃性.硫化氢与二氧化硫反应写出有关化学方程式,了解硫化氢的还原性29小结——常见硫化物的溶解性①既溶于水,又溶于酸:Na2S、K2S、(NH4)2S
②遇水分解的:BaS、CaS、MgS、Al2S3、Fe2S3
③不溶于水,但溶于酸的:ZnS、FeS
④不溶于水,也不溶于酸的:Ag2S、HgS、PbS、CuS30附:溶解度
N2 1:0.015 难溶于水
O2 1:0.03 难溶于水
CO2 1:1 能溶于水
Cl2 1:2 能溶于水
SO2 1:40 易溶于水
HCl 1:500 极易溶于水
NH3 1:700 极易溶于水31品红 褪色(无色) 红色二氧化硫物理
性质无色、有刺激性气味、有毒、易液化、比空气重、易溶于水化学
性质课堂小结Ⅰ、硫元素在自然界中的存在形式Ⅱ、32 一、硫元素在自然界中的存在形式
二、二氧化硫(SO2)
1、SO2的物理性质
2、SO2的化学性质
①能与水和碱反应(酸性氧化物)
②漂白性(暂时的,有选择性的)
③既有氧化性和也有还原性 硫的氧化物 33 2.下列可以用来鉴别SO2和CO2的方法是[ ]
A、通入紫色石蕊试液 B、闻气味 C、通入澄清石灰水 D、通入品红溶液中 B D1.左图是古时用燃烧硫的方法漂白布料的图片。请分析其原理 学与用硫的氧化物 34 随堂
练习 氯气和二氧化硫皆可做漂白剂,若用两者以1:1的物质的量一起漂白一种有色物质时,漂白效果会( )
A. 增强 B. 不变 C. 减弱 D. 难确定CSO2 + Cl2 +2H2O = 2HCl + H2SO4【学与用】硫的氧化物 35 课后调查 2.什么是酸雨?是怎样形成的? 4.酸雨的治理与防治。 1.SO2有哪些危害? 3.SO2的来源?(用文字、数据、图片、视频等方式体现)硫的氧化物 361、氯的原子结构和性质谢谢37第四章非金属及其化合物 第二课时
氮的氧化物及污染第三节硫和氮的氧化物38本课学习内容氮气的性质
NO和NO2的性质
酸雨的形成、危害及环境保护
39二、二氧化氮和一氧化氮1、氮气(N2) 请计算氮气在标准状况下的密度28 g/mol22.4 L/mol=1.2 5 g/L 无色无味气体 比空气稍轻 1)、氮气的物理性质: 不溶于水 空气密度ρ=1.295 g/L40 已知氮气占空气总体积的78%, 试求空气中氮气的质量分数0.78×281×29×100% = 75%41 N2 + O2 ====== 2NO放电或高温2)、氮气的化学性质:3)、氮气的用途:保护气、填充灯泡、焊接金属、低温制冷等42 2NO + O2 = 2NO2 (红棕色气体)2、一氧化氮(NO): 1)、NO的物理性质: 一种无色、不溶于水的有毒气体,是大气的污染物 2)、NO的化学性质:(工业制硝酸的第二步)433、二氧化氮(NO2)1)、NO2的物理性质
——污染大气的有害物质之一红棕色、有刺激性气味的有毒气体,密度比空气大,易液化(20℃),易溶于水并与水反应443NO2 + H2O = 2HNO3 + NO(工业制硝酸的第三步)+4+52)、NO2的化学性质:科学探究 自行设计实验:尽可能多的使NO2被水溶解 填写课本P92页如下表内容45 NO2 和 O2 混和气体溶于水的反应2NO + O2 = 2NO2 ②3NO2 + H2O = 2HNO3 + NO ① ① ×2 + ② 总反应:4NO2 + O2 + 2H2O = 4HNO346三、SO2、NO2对大气的污染: 1、SO2、NO2污染物的形成—— 课本P93 ①、煤、石油、金属矿物质的燃烧和冶炼产生SO2 ②、汽车尾气、硝酸工业产生的NO2471、SO2、NO2污染物的形成: ③、酸雨的形成48 酸雨的形成NO2、SO2与水反应造成的硝酸酸雨:酸雨——指pH小于5.6的降水。3NO2 + H2O = 2HNO3 + NO 硫酸酸雨:SO3 + H2O=H2SO41.酸雨的pH:2.酸雨的形成:49本章所涉及到的与环保有关的知识点: 1.“Cl2的毒性”——Cl2泄漏事件及历史资料,说明Cl2的毒性对环境造成危害,甚至成为杀人武器。 2.SO2的危害
①SO2——人体健康的“杀手”
②——酸雨的形成、危害,防治污染、保护环境的措施。
③大气污染——空气质量日报:空气污染指数项目
(SO2、NO2和可吸入颗粒物)
④漂白性被不法商人利用 3.氮氧化物
①光化学烟雾:震惊世界的伦敦烟雾
②酸雨502005年京沪高速淮安段,一辆槽罐车与一辆迎面驶来大货车相撞后翻倒在地,槽罐车上约32吨液态氯气快速泄漏。事故发生后,组织周围居民逆风撤离,并尽量将居民安置在附近的某些制高点, 迅速向车头喷水和喷洒已稀释的氢氧化钠溶液。氯气吸入后,作用于气管、支气管、细支气管和肺泡,导致相应的病变。高浓度氯会刺激迷走神经引起反射性的心跳停止。 事件链接51 趁着顺风,德军开启了压缩氯气钢瓶,在长约六公里的战线上,黄绿色的云团飘向法军阵地。毫无准备的英法士兵随着黄绿色的气体涌来,先是咳嗽,继而喘息,拼命挣扎,口吐黄液慢慢躺倒。使1.5万人中毒,5000人死亡.这就是战争史上的第一次化学战,从此,化学战作为最邪恶的战争被写入了人类战争的史册。历史事件52 2、大气污染的危害 ①、危害人体健康②、酸雨破坏农作物、森林,土壤酸化,腐蚀建筑等531.用新型的能源(氢能、太阳能、核能)
2.对含硫燃料进行脱硫处理
3.对释放出SO2废气进行处理回收利用
4.提高全民环保意识,加强国际间合作防治酸雨的措施 阅读:课本p94<防治酸雨de措施>54 【问题探究1】
环保部门检测收集酸雨时,pH值在一段时间内会有什么变化?55 你认为减少酸雨产生的途径可采用的措施是______________。
①少用煤作燃料;
②把工厂烟囱造高;
③燃料脱硫;
④在已酸化的土壤中加石灰;
⑤开发新能源。
【问题探究2】56 1.下列污染现象主要与SO2有关的是:( )
A.臭氧空洞 B.酸雨
C.光化学烟雾 D.温室效应
2.以下气体能用NaOH固体干燥的是:( )
A.NH3 B.SO2
C.CO2 D.HCl
3.如何鉴别SO2和CO2?
BA 硫和氮的氧化物随堂练习571、氯的原子结构和性质谢谢
硫和氮的氧化物第二课时
氮及氮的化合物第一课时
硫及硫的化合物第四章 非金属及其化合物2第四章非金属及其化合物3关于城市空气质量日报比比看谁知道得多??4空气质量日报国家环保局信息5 重点城市空气质量日报(部分) 为什么要选择SO2等作为首要污染物呢?它们是从哪儿来的?具有什么样的性质呢?思 考空气质量日报6 二氧化硫对环境的污染7二1、硫(S)(1)、硫在自然界中的存在:硫游离态化合态火山喷口地壳岩层硫化物:硫铁矿或黄铁矿(FeS2)等硫酸盐:芒硝(Na2SO4·10H2O) 石膏(CaSO4·2H2O)黄铜矿(CuFeS2)H2S SO2 SO3硫粉硫的氧化物 硫晶体 二氧化硫和三氧化硫8 淡黄色晶体 质脆,容易研成粉末。 不溶于水,微溶于酒精,
易溶于二硫化碳。 密度比水大(约为2 g/cm3 ) 熔沸点低(112.8℃, 444.6 ℃) 俗称:硫磺(2)硫的物理性质硫的氧化物 9火药的发明10(3)硫的化学性质S + O2 = SO20+4硫作为还原剂,具有还原性。划火柴时常闻到的一股呛鼻的气味,就是火柴头
成份中的硫燃烧后产生的二氧化硫。有刺激性气味的气体生成。
硫在空气中安静地燃烧,发出淡蓝色火焰;
硫在纯氧中燃烧发出蓝紫色火焰点燃硫的氧化物 11硫的化学性质Hg+S === HgS(研磨,黑色)处理散落水银2Na+S====Na2S (白色) (加热或研磨爆炸)C+2S ==== CS2 (白色) (高温)Na2SO3 +S====Na2S2O3 (加热,硫代硫酸钠)12硫的氧化物 二. 二氧化硫(SO2) 1、 SO2的物理性质 现象:试管内水位上升 结论: SO2易溶于水 二氧化硫是污染大气的主要有害物质之一13 1. SO2的物理性质SO2无色气体刺激性气味有毒易溶于水(1:40)密度比空气大易液化二氧化硫是一种无色、有刺激性气味、有毒、比空气重、容易液化、易溶于水的气体。 硫的氧化物 14SO2 + H2O逆反应H2SO3正反应2. SO2的化学性质① SO2能与水反应 可逆反应:在相同条件下,既能向正反应方向进行、又能向逆反应方向进行的反应。 思 考 2H2O 通电 2H2↑ +O2 ↑ 与 2H2+O2 点燃 2H2O
是可逆反应吗? 二氧化硫的化学性质——酸性氧化物的通性(亚硫酸)硫的氧化物 152.SO2的化学性质② SO2的漂白性漂白原理:SO2 能与某些有色物质生成不稳定的无色物质。(暂时性)现象:滴入品红溶液后,颜色褪去;加热时又恢复原来的红色。硫的氧化物 16 ② SO2具有漂白作用:但漂白后的新物质不稳定,易恢复原来的颜色(检验SO2的存在) SO2的化学性质17 SO2的化学性质18 思考:草帽、纸张为什么会泛黄?探讨:你学过的哪些物质具有漂白性?活性炭H2O2Na2O2HClO… ...物理吸附氧化漂白漂白原理是否相同? SO2的化学性质19永久性暂时性氯气中HClO将有色
物质氧化成无色物质氧化还原反应非氧化还原反应可漂白大多数有色物质,能使紫色石蕊试液褪色SO2与有色物质直接结合生成不稳定无色物质 可漂白某些有色物质,不能使紫色石蕊试液褪色二氧化硫与氯气的漂白性比较思考? SO2的化学性质20探 究根据硫原子的结构示意图 ,判断硫元素的最高化合价和最低化合价 。并结合SO2中硫元素的化合价,分析SO2 还可能有什么化学性质? SO2的化学性质21③ SO2既有氧化性,又有还原性(氧化性) (还原性) SO2的化学性质22(工业制硫酸的第二步)SO2+ Cl2+2H2O =H2SO4+2HCl2H2S+SO2=3S↓+2H2OSO2的还原性SO2的氧化性SO2能使溴水褪色,试分析褪色原因? SO2的化学性质23 ④二氧化硫跟碱反应(酸性氧化物) SO2 + Ca(OH)2 = CaSO3 + H2O CaSO3 + SO2 + H2O = Ca(HSO3)2注
意使澄清石灰水先变浑浊后变澄清的气体,除二氧化碳外,还可能是二氧化硫。2SO2 + Ca(OH)2 = Ca(HSO3)2 少量过量 SO2的化学性质24⑤二氧化硫跟碱性氧化物反应
——酸性氧化物的通性——防治大气污染,石灰法脱硫SO2+Na2O=Na2SO3 SO2的化学性质25作漂白剂杀菌、防腐三.SO2的用途SO2的用途制硫酸26无色固体,熔点(16.8℃)
沸点(44.8℃ )都很低工业上常用上面两个反应制取硫酸 3、三氧化硫——酸性氧化物 SO3的化学性质27 SO3 + Ca(OH)2 = CaSO4+ H2O SO3 + CaO = CaSO4三氧化硫跟碱或碱性氧化物反应 SO3的化学性质28硫化氢的性质资料卡片阅读课本P91资料卡片,理解如下内容:1.硫化氢的物理性质:2.硫化氢的化学性质:3.硫化氢的毒性:硫化氢的可燃性.硫化氢与二氧化硫反应写出有关化学方程式,了解硫化氢的还原性29小结——常见硫化物的溶解性①既溶于水,又溶于酸:Na2S、K2S、(NH4)2S
②遇水分解的:BaS、CaS、MgS、Al2S3、Fe2S3
③不溶于水,但溶于酸的:ZnS、FeS
④不溶于水,也不溶于酸的:Ag2S、HgS、PbS、CuS30附:溶解度
N2 1:0.015 难溶于水
O2 1:0.03 难溶于水
CO2 1:1 能溶于水
Cl2 1:2 能溶于水
SO2 1:40 易溶于水
HCl 1:500 极易溶于水
NH3 1:700 极易溶于水31品红 褪色(无色) 红色二氧化硫物理
性质无色、有刺激性气味、有毒、易液化、比空气重、易溶于水化学
性质课堂小结Ⅰ、硫元素在自然界中的存在形式Ⅱ、32 一、硫元素在自然界中的存在形式
二、二氧化硫(SO2)
1、SO2的物理性质
2、SO2的化学性质
①能与水和碱反应(酸性氧化物)
②漂白性(暂时的,有选择性的)
③既有氧化性和也有还原性 硫的氧化物 33 2.下列可以用来鉴别SO2和CO2的方法是[ ]
A、通入紫色石蕊试液 B、闻气味 C、通入澄清石灰水 D、通入品红溶液中 B D1.左图是古时用燃烧硫的方法漂白布料的图片。请分析其原理 学与用硫的氧化物 34 随堂
练习 氯气和二氧化硫皆可做漂白剂,若用两者以1:1的物质的量一起漂白一种有色物质时,漂白效果会( )
A. 增强 B. 不变 C. 减弱 D. 难确定CSO2 + Cl2 +2H2O = 2HCl + H2SO4【学与用】硫的氧化物 35 课后调查 2.什么是酸雨?是怎样形成的? 4.酸雨的治理与防治。 1.SO2有哪些危害? 3.SO2的来源?(用文字、数据、图片、视频等方式体现)硫的氧化物 361、氯的原子结构和性质谢谢37第四章非金属及其化合物 第二课时
氮的氧化物及污染第三节硫和氮的氧化物38本课学习内容氮气的性质
NO和NO2的性质
酸雨的形成、危害及环境保护
39二、二氧化氮和一氧化氮1、氮气(N2) 请计算氮气在标准状况下的密度28 g/mol22.4 L/mol=1.2 5 g/L 无色无味气体 比空气稍轻 1)、氮气的物理性质: 不溶于水 空气密度ρ=1.295 g/L40 已知氮气占空气总体积的78%, 试求空气中氮气的质量分数0.78×281×29×100% = 75%41 N2 + O2 ====== 2NO放电或高温2)、氮气的化学性质:3)、氮气的用途:保护气、填充灯泡、焊接金属、低温制冷等42 2NO + O2 = 2NO2 (红棕色气体)2、一氧化氮(NO): 1)、NO的物理性质: 一种无色、不溶于水的有毒气体,是大气的污染物 2)、NO的化学性质:(工业制硝酸的第二步)433、二氧化氮(NO2)1)、NO2的物理性质
——污染大气的有害物质之一红棕色、有刺激性气味的有毒气体,密度比空气大,易液化(20℃),易溶于水并与水反应443NO2 + H2O = 2HNO3 + NO(工业制硝酸的第三步)+4+52)、NO2的化学性质:科学探究 自行设计实验:尽可能多的使NO2被水溶解 填写课本P92页如下表内容45 NO2 和 O2 混和气体溶于水的反应2NO + O2 = 2NO2 ②3NO2 + H2O = 2HNO3 + NO ① ① ×2 + ② 总反应:4NO2 + O2 + 2H2O = 4HNO346三、SO2、NO2对大气的污染: 1、SO2、NO2污染物的形成—— 课本P93 ①、煤、石油、金属矿物质的燃烧和冶炼产生SO2 ②、汽车尾气、硝酸工业产生的NO2471、SO2、NO2污染物的形成: ③、酸雨的形成48 酸雨的形成NO2、SO2与水反应造成的硝酸酸雨:酸雨——指pH小于5.6的降水。3NO2 + H2O = 2HNO3 + NO 硫酸酸雨:SO3 + H2O=H2SO41.酸雨的pH:2.酸雨的形成:49本章所涉及到的与环保有关的知识点: 1.“Cl2的毒性”——Cl2泄漏事件及历史资料,说明Cl2的毒性对环境造成危害,甚至成为杀人武器。 2.SO2的危害
①SO2——人体健康的“杀手”
②——酸雨的形成、危害,防治污染、保护环境的措施。
③大气污染——空气质量日报:空气污染指数项目
(SO2、NO2和可吸入颗粒物)
④漂白性被不法商人利用 3.氮氧化物
①光化学烟雾:震惊世界的伦敦烟雾
②酸雨502005年京沪高速淮安段,一辆槽罐车与一辆迎面驶来大货车相撞后翻倒在地,槽罐车上约32吨液态氯气快速泄漏。事故发生后,组织周围居民逆风撤离,并尽量将居民安置在附近的某些制高点, 迅速向车头喷水和喷洒已稀释的氢氧化钠溶液。氯气吸入后,作用于气管、支气管、细支气管和肺泡,导致相应的病变。高浓度氯会刺激迷走神经引起反射性的心跳停止。 事件链接51 趁着顺风,德军开启了压缩氯气钢瓶,在长约六公里的战线上,黄绿色的云团飘向法军阵地。毫无准备的英法士兵随着黄绿色的气体涌来,先是咳嗽,继而喘息,拼命挣扎,口吐黄液慢慢躺倒。使1.5万人中毒,5000人死亡.这就是战争史上的第一次化学战,从此,化学战作为最邪恶的战争被写入了人类战争的史册。历史事件52 2、大气污染的危害 ①、危害人体健康②、酸雨破坏农作物、森林,土壤酸化,腐蚀建筑等531.用新型的能源(氢能、太阳能、核能)
2.对含硫燃料进行脱硫处理
3.对释放出SO2废气进行处理回收利用
4.提高全民环保意识,加强国际间合作防治酸雨的措施 阅读:课本p94<防治酸雨de措施>54 【问题探究1】
环保部门检测收集酸雨时,pH值在一段时间内会有什么变化?55 你认为减少酸雨产生的途径可采用的措施是______________。
①少用煤作燃料;
②把工厂烟囱造高;
③燃料脱硫;
④在已酸化的土壤中加石灰;
⑤开发新能源。
【问题探究2】56 1.下列污染现象主要与SO2有关的是:( )
A.臭氧空洞 B.酸雨
C.光化学烟雾 D.温室效应
2.以下气体能用NaOH固体干燥的是:( )
A.NH3 B.SO2
C.CO2 D.HCl
3.如何鉴别SO2和CO2?
BA 硫和氮的氧化物随堂练习571、氯的原子结构和性质谢谢
