高中化学人教版(2019)选择性必修3第3章第4节第2课时羧酸衍生物(共30张ppt)
文档属性
| 名称 | 高中化学人教版(2019)选择性必修3第3章第4节第2课时羧酸衍生物(共30张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-17 00:00:00 | ||
图片预览









文档简介
(共30张PPT)
第3章 烃的衍生物
第四节 羧酸 羧酸衍生物
第2课时 羧酸衍生物
【思考】什么是羧酸衍生物?
羧酸分子中羧基上的羟基被其他原子或原子团取代后的产物。
例如:
R
X
R
OR’
R
OCR’
O=
R
NH2
酰卤
酯
酸酐
酰胺
R
羧酸分子中羧基去掉羟基后剩余部分为酰基
酰基:
一.【思考】什么是酯?
饱和一元羧酸酯的通式为
酯是羧酸分子中羧基上的—OH被—OR’取代后的产物
或RCOOR'
OR’
R
羧酸酯可表示为:
其中R和R'可以相同,也可以不同。R'只能是烃基
CnH2nO2
官能团:
酯基
OR’
【例1】写出分子式为C4H8O2的酯的同分异构体并命名。
写出分子式为C5H10O2的酯的同分异构体并命名。
碳原子数相同的饱和一元酯与饱和一元羧酸互为同分异构体。
酯的命名:某酸某(醇的烃基名称)酯。
二.酯的物理性质:
具有芳香气味的液体,密度一般比水小;
广泛存在于各种水果和花草中。
低级酯
( C10以下 )
难溶于水,易溶于乙醇、乙醚等有机溶剂;
常作有机溶剂,也用作饮料、糕点的酯类香料;
戊酸戊酯
丁酸乙酯
乙酸异戊酯
三.酯的化学性质:
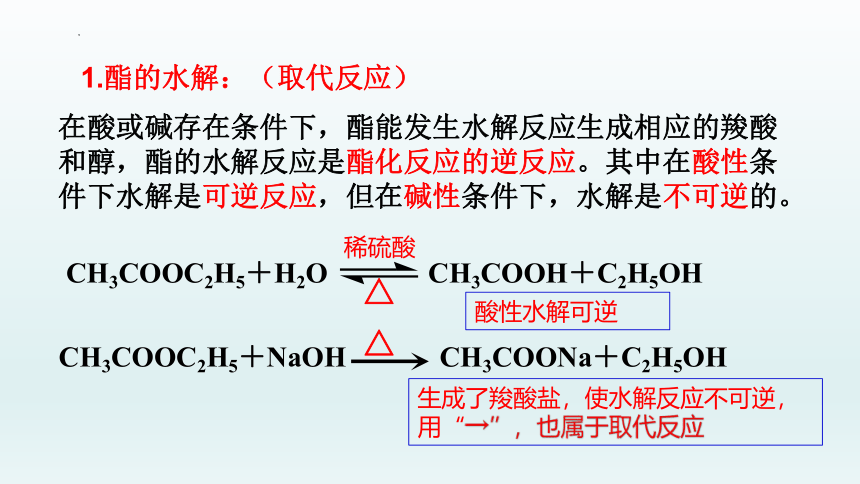
1.酯的水解:(取代反应)
乙酸乙酯+水
70℃
乙酸乙酯+稀硫酸
70℃
乙酸乙酯+NaOH+酚酞
70℃
分层,酯层基本不变,未水解
酯层和香味消失慢
酯层和香味消失很快,红色退去
1.酯的水解:(取代反应)
⑴酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
⑵温度越高,酯水解程度越大。
(水解反应是吸热反应)
酯的水解规律:
问题:①酯的酸性水解能否用盐酸或硝酸?
②酯的酸性水解用稀硫酸,能否用浓硫酸?
③酯的水解用水浴加热,能否直接加热?
在酸或碱存在条件下,酯能发生水解反应生成相应的羧酸和醇,酯的水解反应是酯化反应的逆反应。其中在酸性条件下水解是可逆反应,但在碱性条件下,水解是不可逆的。
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
酸性水解可逆
生成了羧酸盐,使水解反应不可逆,用“→”,也属于取代反应
1.酯的水解:(取代反应)
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
酯水解时怎样断键?
1.酯的水解:(取代反应)
酯水解时断酰氧键!
酸上羟基醇上氢
总结:
酯化反应 水解
反应关系
催化剂
催化剂的其他作用
反应类型
加热类型
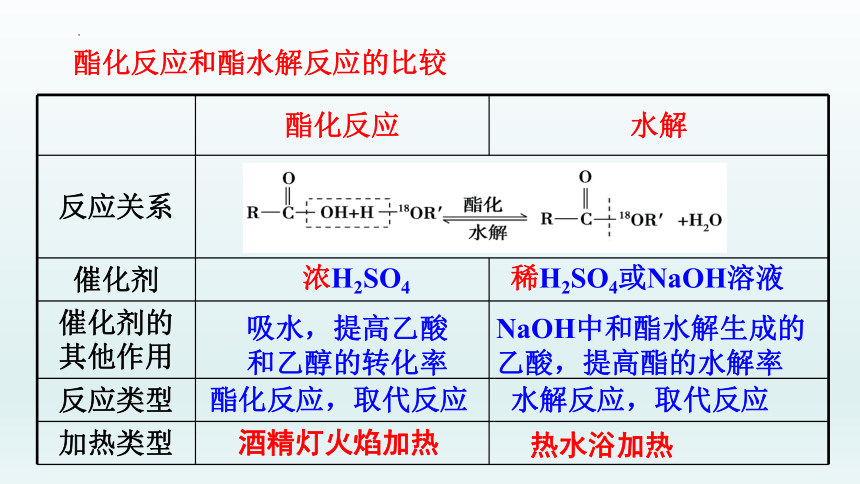
酯化反应和酯水解反应的比较
浓H2SO4
稀H2SO4或NaOH溶液
吸水,提高乙酸和乙醇的转化率
NaOH中和酯水解生成的乙酸,提高酯的水解率
酯化反应,取代反应
水解反应,取代反应
酒精灯火焰加热
热水浴加热
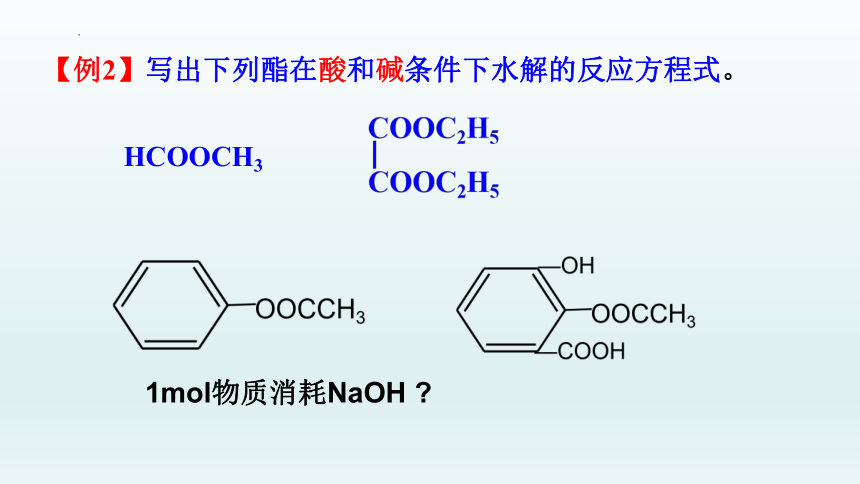
【例2】写出下列酯在酸和碱条件下水解的反应方程式。
HCOOCH3
1mol物质消耗NaOH
2.酯的醇解:(取代反应)
定义:酯(RCOOR')中的OR'被另一个醇的OR”置换。
条件:在酸(HCl、H2SO4)或醇钠催化下加热。
RCOOR' + R”OH
H+或OR”
RCOOR” + R'OH
例如;聚乙烯醇是通过聚乙酸乙烯酯的醇解反应得到的,因为聚乙酸乙烯酯不溶于水,不能进行水解,可以用过量甲醇进行醇解。
反应方程式?
酯交换反应
【例3】一环酯化合物,结构简式如下:
1.在酸性条件下水解的产物?
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应?
二、油脂
1.定义:主要成分是高级脂肪酸与甘油(丙三醇)形成的酯,属于酯类化合物。
油脂
油
脂肪
常温呈液态的油脂
常温呈固态的油脂
如花生油、芝麻油、大豆油等植物油
如牛油、羊油等动物油脂
2.油脂的结构:
其中R1、R2、R3代表高级脂肪酸的烃基,可以相同也可以不同;
当其相同时称为单甘油酯,不相同时称为混甘油酯;
天然油脂大多是混甘油酯,且都是混合物,无固定熔沸点;
酯基
元素组成:
C、H、O
硬脂酸:
软脂酸:
C17H35COOH
C15H31COOH
油酸:
亚油酸:
C17H33COOH
C17H31COOH
饱和脂肪酸
不饱和脂肪酸
油:不饱和的高级脂肪酸甘油酯
脂肪:饱和的高级脂肪酸甘油酯
3.常见高级脂肪酸
脂肪酸的饱和程度对油脂的熔点影响很大,含较多不饱和脂肪酸的甘油酯,熔点较低;含较多饱和高级脂肪酸的甘油酯,熔点较高。
3.油脂的物理性质:
纯净的甘油三脂是无色、无臭、无味的,但普通油脂往往溶解有维生素、色素等,故带有香味或特殊气味,并呈现黄色或红色。
油脂密度比水小,黏度比较大,触摸时有明显的油腻感,难溶于水,易溶于汽油有机溶剂。
天然油脂都是混合物,无固定熔沸点。
4.油脂的化学性质:
⑴油脂的碱性水解(皂化反应)
3C17H35COONa
+
高级脂肪酸盐可以作肥皂,所以油脂在碱性条件下的水解又叫皂化反应,工业常用来制取肥皂。
硬脂酸钠
油脂 + NaOH
高级脂肪酸钠盐 + 甘油
+3NaOH―→
硬脂酸甘油酯
4.油脂的化学性质:
⑵油脂的酸性水解
⑶油脂的氢化
加氢后的人造脂肪又叫硬化油,性质稳定,不易变质,便于储存和运输,可用于制造肥皂和人造奶油等。
——不饱和油脂的催化加氢(油脂的硬化)
油酸甘油酯
硬脂酸甘油酯
液态油通过催化加氢可提高饱和度,转变成半固态脂肪的过程。
+3H2
催化剂
4.油脂在生产、生活中的应用
是产生能量最高的营养物质。
具有保持体温和保护内脏器官的作用。
油脂能促进脂溶性维生素的吸收。
工业上生产高级脂肪酸和甘油,制肥皂等。
油脂
1克油脂在完全氧化时释放的能量大约为39.9kJ,是等质量糖类或蛋白质的2倍。
5.实验:用油脂制造肥皂的过程:
(1)在圆底烧瓶中加入6g动物脂肪和5mL 95%的酒精,然后加10mL40%的NaOH溶液。用玻棒搅拌,使其溶解。
(2)用酒精灯加热,直至反应液变成黄棕色黏稠状。
(3)在另一只烧杯中加入60 mL 热的饱和食盐水,把得到的反应液倒入食盐水中,搅拌,静置后,肥皂便盐析上浮,待肥皂全部析出、凝固后可用玻棒取出,肥皂即制成。
5.实验:用油脂制造肥皂的过程:
①加入乙醇的作用是什么?
②怎样检验皂化反应已经完成?
③饱和食盐水的作用是什么?
④皂化反应完成后,所得混合物为: 。
(填“悬浊液”或“乳浊液”或“溶液”或“胶体”)。
胶体
(1)油脂是高分子化合物( )
(2)植物油可以作为萃取剂,萃取溴水中的溴( )
(3)牛油在碱性条件下可制得肥皂。( )
(4)能发生氢化反应的油脂,也能使酸性KMnO4溶液褪色( )
(5)植物油在空气中久置,会产生“哈喇”味,变质原因是
发生加成反应。 ( )
(6)油脂是人类主要营养物质之一,是热量最高的营养成分。
( )
×
×
√
练习:1.判断
×
√
√
2.若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )
A 1种 B 2种 C 3 种 D 4种
生成物中水的相对分子质量为 。
C
20
3.由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH反应的有( )
①—OH ②—CH3 ③—COOH ④ ⑤—CHO
A.2种 B.3种 C.4种 D.5种
D
取少量液体,加含酚酞的NaOH溶液,加热,若液体不分层,且红色变浅的为植物油,若液体分层,颜色无变化的为矿物油。
4.如何利用化学方法鉴别植物油和矿物油
5.在油、脂肪、酯、汽油中一定能使酸性高锰酸钾溶液或溴水褪色的是哪种
油。从结构中是否含有碳碳双键进行考虑,油一定有碳碳双键,脂肪一般没有,酯可能有,直馏汽油一般没有而裂化汽油有。
油
脂肪
酯
矿物油
不饱和高级脂肪酸的甘油酯
饱和高级脂肪酸的甘油酯
羧酸与醇反应产物
多种烃(石油及其分馏产品)
液态 固态 液态或固态 液态
油与脂肪属于酯,能水解,油含碳碳双键 混合烃,不能水解
再 见
谢谢
第3章 烃的衍生物
第四节 羧酸 羧酸衍生物
第2课时 羧酸衍生物
【思考】什么是羧酸衍生物?
羧酸分子中羧基上的羟基被其他原子或原子团取代后的产物。
例如:
R
X
R
OR’
R
OCR’
O=
R
NH2
酰卤
酯
酸酐
酰胺
R
羧酸分子中羧基去掉羟基后剩余部分为酰基
酰基:
一.【思考】什么是酯?
饱和一元羧酸酯的通式为
酯是羧酸分子中羧基上的—OH被—OR’取代后的产物
或RCOOR'
OR’
R
羧酸酯可表示为:
其中R和R'可以相同,也可以不同。R'只能是烃基
CnH2nO2
官能团:
酯基
OR’
【例1】写出分子式为C4H8O2的酯的同分异构体并命名。
写出分子式为C5H10O2的酯的同分异构体并命名。
碳原子数相同的饱和一元酯与饱和一元羧酸互为同分异构体。
酯的命名:某酸某(醇的烃基名称)酯。
二.酯的物理性质:
具有芳香气味的液体,密度一般比水小;
广泛存在于各种水果和花草中。
低级酯
( C10以下 )
难溶于水,易溶于乙醇、乙醚等有机溶剂;
常作有机溶剂,也用作饮料、糕点的酯类香料;
戊酸戊酯
丁酸乙酯
乙酸异戊酯
三.酯的化学性质:
1.酯的水解:(取代反应)
乙酸乙酯+水
70℃
乙酸乙酯+稀硫酸
70℃
乙酸乙酯+NaOH+酚酞
70℃
分层,酯层基本不变,未水解
酯层和香味消失慢
酯层和香味消失很快,红色退去
1.酯的水解:(取代反应)
⑴酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
⑵温度越高,酯水解程度越大。
(水解反应是吸热反应)
酯的水解规律:
问题:①酯的酸性水解能否用盐酸或硝酸?
②酯的酸性水解用稀硫酸,能否用浓硫酸?
③酯的水解用水浴加热,能否直接加热?
在酸或碱存在条件下,酯能发生水解反应生成相应的羧酸和醇,酯的水解反应是酯化反应的逆反应。其中在酸性条件下水解是可逆反应,但在碱性条件下,水解是不可逆的。
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
酸性水解可逆
生成了羧酸盐,使水解反应不可逆,用“→”,也属于取代反应
1.酯的水解:(取代反应)
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
酯水解时怎样断键?
1.酯的水解:(取代反应)
酯水解时断酰氧键!
酸上羟基醇上氢
总结:
酯化反应 水解
反应关系
催化剂
催化剂的其他作用
反应类型
加热类型
酯化反应和酯水解反应的比较
浓H2SO4
稀H2SO4或NaOH溶液
吸水,提高乙酸和乙醇的转化率
NaOH中和酯水解生成的乙酸,提高酯的水解率
酯化反应,取代反应
水解反应,取代反应
酒精灯火焰加热
热水浴加热
【例2】写出下列酯在酸和碱条件下水解的反应方程式。
HCOOCH3
1mol物质消耗NaOH
2.酯的醇解:(取代反应)
定义:酯(RCOOR')中的OR'被另一个醇的OR”置换。
条件:在酸(HCl、H2SO4)或醇钠催化下加热。
RCOOR' + R”OH
H+或OR”
RCOOR” + R'OH
例如;聚乙烯醇是通过聚乙酸乙烯酯的醇解反应得到的,因为聚乙酸乙烯酯不溶于水,不能进行水解,可以用过量甲醇进行醇解。
反应方程式?
酯交换反应
【例3】一环酯化合物,结构简式如下:
1.在酸性条件下水解的产物?
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应?
二、油脂
1.定义:主要成分是高级脂肪酸与甘油(丙三醇)形成的酯,属于酯类化合物。
油脂
油
脂肪
常温呈液态的油脂
常温呈固态的油脂
如花生油、芝麻油、大豆油等植物油
如牛油、羊油等动物油脂
2.油脂的结构:
其中R1、R2、R3代表高级脂肪酸的烃基,可以相同也可以不同;
当其相同时称为单甘油酯,不相同时称为混甘油酯;
天然油脂大多是混甘油酯,且都是混合物,无固定熔沸点;
酯基
元素组成:
C、H、O
硬脂酸:
软脂酸:
C17H35COOH
C15H31COOH
油酸:
亚油酸:
C17H33COOH
C17H31COOH
饱和脂肪酸
不饱和脂肪酸
油:不饱和的高级脂肪酸甘油酯
脂肪:饱和的高级脂肪酸甘油酯
3.常见高级脂肪酸
脂肪酸的饱和程度对油脂的熔点影响很大,含较多不饱和脂肪酸的甘油酯,熔点较低;含较多饱和高级脂肪酸的甘油酯,熔点较高。
3.油脂的物理性质:
纯净的甘油三脂是无色、无臭、无味的,但普通油脂往往溶解有维生素、色素等,故带有香味或特殊气味,并呈现黄色或红色。
油脂密度比水小,黏度比较大,触摸时有明显的油腻感,难溶于水,易溶于汽油有机溶剂。
天然油脂都是混合物,无固定熔沸点。
4.油脂的化学性质:
⑴油脂的碱性水解(皂化反应)
3C17H35COONa
+
高级脂肪酸盐可以作肥皂,所以油脂在碱性条件下的水解又叫皂化反应,工业常用来制取肥皂。
硬脂酸钠
油脂 + NaOH
高级脂肪酸钠盐 + 甘油
+3NaOH―→
硬脂酸甘油酯
4.油脂的化学性质:
⑵油脂的酸性水解
⑶油脂的氢化
加氢后的人造脂肪又叫硬化油,性质稳定,不易变质,便于储存和运输,可用于制造肥皂和人造奶油等。
——不饱和油脂的催化加氢(油脂的硬化)
油酸甘油酯
硬脂酸甘油酯
液态油通过催化加氢可提高饱和度,转变成半固态脂肪的过程。
+3H2
催化剂
4.油脂在生产、生活中的应用
是产生能量最高的营养物质。
具有保持体温和保护内脏器官的作用。
油脂能促进脂溶性维生素的吸收。
工业上生产高级脂肪酸和甘油,制肥皂等。
油脂
1克油脂在完全氧化时释放的能量大约为39.9kJ,是等质量糖类或蛋白质的2倍。
5.实验:用油脂制造肥皂的过程:
(1)在圆底烧瓶中加入6g动物脂肪和5mL 95%的酒精,然后加10mL40%的NaOH溶液。用玻棒搅拌,使其溶解。
(2)用酒精灯加热,直至反应液变成黄棕色黏稠状。
(3)在另一只烧杯中加入60 mL 热的饱和食盐水,把得到的反应液倒入食盐水中,搅拌,静置后,肥皂便盐析上浮,待肥皂全部析出、凝固后可用玻棒取出,肥皂即制成。
5.实验:用油脂制造肥皂的过程:
①加入乙醇的作用是什么?
②怎样检验皂化反应已经完成?
③饱和食盐水的作用是什么?
④皂化反应完成后,所得混合物为: 。
(填“悬浊液”或“乳浊液”或“溶液”或“胶体”)。
胶体
(1)油脂是高分子化合物( )
(2)植物油可以作为萃取剂,萃取溴水中的溴( )
(3)牛油在碱性条件下可制得肥皂。( )
(4)能发生氢化反应的油脂,也能使酸性KMnO4溶液褪色( )
(5)植物油在空气中久置,会产生“哈喇”味,变质原因是
发生加成反应。 ( )
(6)油脂是人类主要营养物质之一,是热量最高的营养成分。
( )
×
×
√
练习:1.判断
×
√
√
2.若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )
A 1种 B 2种 C 3 种 D 4种
生成物中水的相对分子质量为 。
C
20
3.由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH反应的有( )
①—OH ②—CH3 ③—COOH ④ ⑤—CHO
A.2种 B.3种 C.4种 D.5种
D
取少量液体,加含酚酞的NaOH溶液,加热,若液体不分层,且红色变浅的为植物油,若液体分层,颜色无变化的为矿物油。
4.如何利用化学方法鉴别植物油和矿物油
5.在油、脂肪、酯、汽油中一定能使酸性高锰酸钾溶液或溴水褪色的是哪种
油。从结构中是否含有碳碳双键进行考虑,油一定有碳碳双键,脂肪一般没有,酯可能有,直馏汽油一般没有而裂化汽油有。
油
脂肪
酯
矿物油
不饱和高级脂肪酸的甘油酯
饱和高级脂肪酸的甘油酯
羧酸与醇反应产物
多种烃(石油及其分馏产品)
液态 固态 液态或固态 液态
油与脂肪属于酯,能水解,油含碳碳双键 混合烃,不能水解
再 见
谢谢
