第12章盐复习题---2021-2022学年九年级化学京改版(2013)下册(word版有答案)
文档属性
| 名称 | 第12章盐复习题---2021-2022学年九年级化学京改版(2013)下册(word版有答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 111.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-18 00:00:00 | ||
图片预览



文档简介
第12章盐复习题2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.下列有关碳及碳的化合物的说法正确的是
A.金刚石、石墨和C60的化学性质相似,物理性质有很大差异,是因为它们由不同的原子构成
B.煤炉上放一盆水就能防止一氧化碳中毒
C.碳酸钙在医疗上可用作补钙剂
D.空气中二氧化碳含量过高可形成酸雨
2.Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于
A.氧化物
B.盐
C.有机物
D.混合物
3.下列有关常见酸、碱、盐的说法不正确的是( )
A.浓盐酸具有挥发性,浓硫酸具有吸水性
B.Na2CO3和CaCO3都是白色易溶于水的固体
C.NaCl是白色易溶于水的固体,溶解度受温度影响小
D.NaOH和Ca(OH)2露置在空气中容易变质
4.下列化学反应属于置换反应的是( )
A.H2O+CaO═Ca(OH)2
B.Na2SO4+BaCl2═2NaCl+BaSO4↓
C.H2+CuOCu+H2O
D.3CO+Fe2O32Fe+3CO2
5.下列反应属于复分解反应的是
A.CO2+ H2O=H2CO3 B.2HC1 +Ca(OH)2=CaCl2+ 2H2O
C.2KMnO4K2MnO4+MnO2+O2↑ D.2Na+2H2O=2NaOH + H2↑
6.某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
7.下列物质长期放置在空气中,溶液质量因发生化学变化而减小的是
A.NaCl溶液 B.NaOH溶液 C.浓盐酸 D.石灰水
8.向盐酸和氯化铜混合溶液中加入一定质量分数的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,下列说法不正确的是
A.a点溶液中的pH<7
B.bc段(不含b、c点)反应的化学方程式为
C.c点溶液中含有两种溶质
D.整个变化过程中氯离子的数目没有改变
9.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项 物质 选用试剂 操作方法
A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干
B CO(CO2) NaOH溶液、浓硫酸 洗气、干燥
C CaO(CaCO3) 水 过滤、烘干
D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
10.去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是( )
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用题35图装置加热蒸发,至水分完全蒸干时停止加热
11.下列除去物质中所含少量杂质的方法错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B CaSO4溶液 稀硫酸 过量CaCO3 粉末、过滤
C FeCl2溶液 CuCl2 过量铁粉、过滤
D 二氧化碳 一氧化碳 点燃
A.A B.B C.C D.D
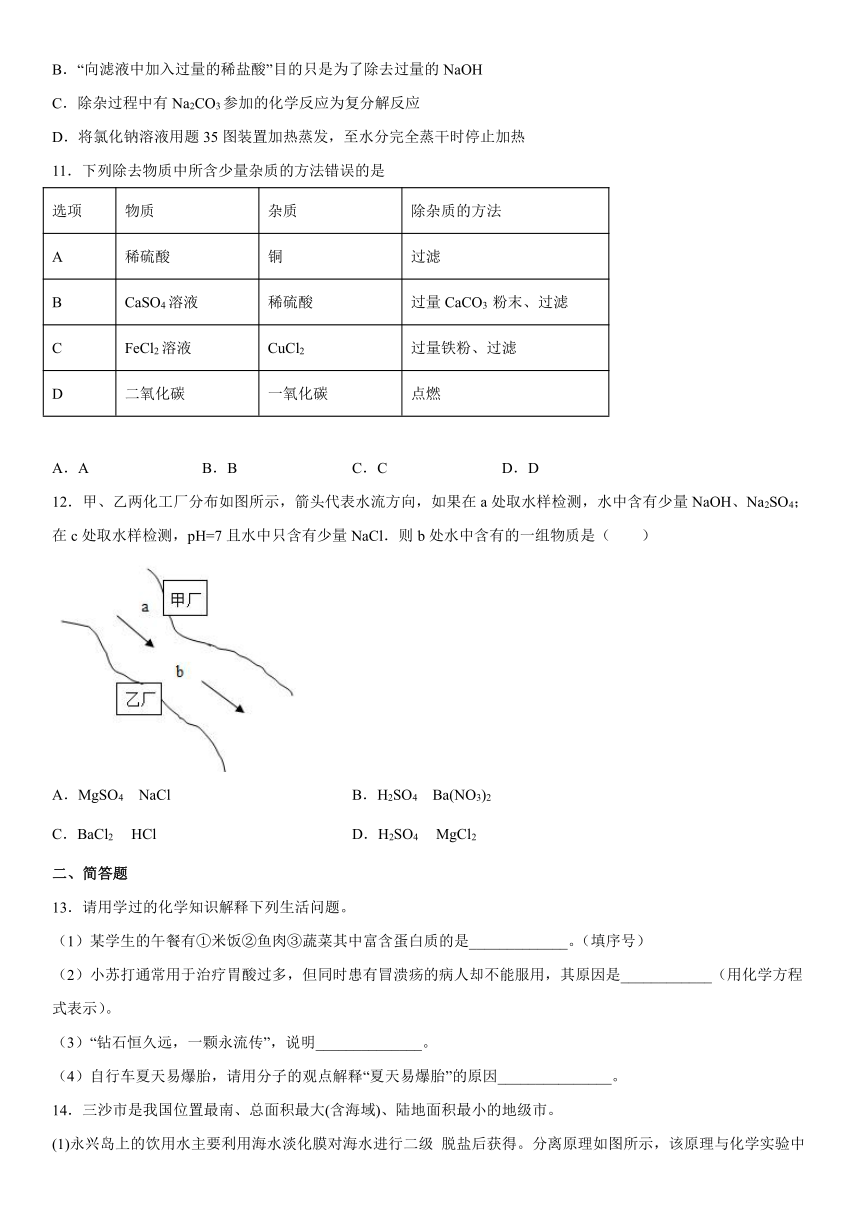
12.甲、乙两化工厂分布如图所示,箭头代表水流方向,如果在a处取水样检测,水中含有少量NaOH、Na2SO4;在c处取水样检测,pH=7且水中只含有少量NaCl.则b处水中含有的一组物质是( )
A.MgSO4 NaCl B.H2SO4 Ba(NO3)2
C.BaCl2 HCl D.H2SO4 MgCl2
二、简答题
13.请用学过的化学知识解释下列生活问题。
(1)某学生的午餐有①米饭②鱼肉③蔬菜其中富含蛋白质的是_____________。(填序号)
(2)小苏打通常用于治疗胃酸过多,但同时患有冒溃疡的病人却不能服用,其原因是____________(用化学方程式表示)。
(3)“钻石恒久远,一颗永流传”,说明______________。
(4)自行车夏天易爆胎,请用分子的观点解释“夏天易爆胎”的原因_______________。
14.三沙市是我国位置最南、总面积最大(含海域)、陆地面积最小的地级市。
(1)永兴岛上的饮用水主要利用海水淡化膜对海水进行二级 脱盐后获得。分离原理如图所示,该原理与化学实验中常见的_____操作相似;
(2)三沙海域的海水盐度高,从海水中获取食盐的方法是_____;
(3)海水提取粗盐后的母液还可以用来提取金属镁,其流程如下:
该流程中,溶液 A 为_____,其中没有发生的基本反应类型为_____。
15.请用所学化学知识解释下列原理。
(1)铝的化学性质活泼,而铝制品具有良好的抗腐蚀性能的原因是什么?_______________________
(2)盐酸除铁锈(Fe2O3)的化学方程式为________________________________。
(3)工业上可用Cl2与NaOH溶液反应制取漂白液:Cl2+2NaOH===NaCl+NaClO+H2O。与此类似,可用Cl2与石灰乳[主要成分Ca(OH)2]反应来制取漂白粉,试写出此反应的化学方程式________________________________。
三、推断题
16.抗击疫情,我们众志成城,万众一心,便能马到成功。小万用化学物质七巧板拼成的小马如图所示,拼图的规则是有一条边相互接触(包括部分接触)的物质之间能发生化学反应(所涉及反应均为初中常见化学反应)。A~G分别是盐酸、碳酸钙、氢氧化钠、二氧化碳、氧化铜、硫酸铜、氢气中的一种,A是单质,G常用于配制农药波尔多液。
请回答下列问题:
(1)F的化学式为_______。
(2)A与B反应的基本反应类型为_______。
(3)C与D反应的化学方程式为_______。
(4)E与G反应的现象是有蓝色沉淀生成,能够代替E的物质是_______。
17.实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种。为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如图实验(此处箭头表示得出实验结论):
根据上述实验回答:
(1)写出三种化肥的名称:A______;B______;C______。
(2)如果实验Ⅱ中B、C两种样品没有另取,对实验结果______(填“有”或“无”)影响。
(3)常温下如要鉴别B、C两种样品,______(填“能”或“不能”)采取闻气味的方法。
(4)写出操作Ⅱ中涉及的化学反应的方程式:______。
四、实验题
18.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
19.现有一包固体粉末,可能含有C粉、KMnO4、NaCl、NH4HCO3、Fe粉中的一种或几种。现做如下实验:
(1)取少量固体加热,无氨味,则原固体中一定不含________。
(2)另取少量固体溶于足量水过滤,得到无色澄清滤液和黑色固体,则原固体中一定不含__________。
(3)取(2)中无色澄清滤液适量,蒸发,出现较多固体,则原固体中一定含有_____。
(4)取(2)中得到的黑色固体,加入足量的稀盐酸,固体全部溶解并有气体放出,由此判断原固体中还含有_________。
五、计算题
20.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
21.厨房中;使用的食用碱(主要成分是碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学对其组成展开探究。他们实验的过程和数据如图所示:
请你据图分析:
(1)反应后滤液中含有的溶质是_____(写化学式)
(2)通过已知数据,能求出的量有_____(写字母序号)
a反应后滤液的总质量
b参加反应的氯化钙的质量
c样品中碳酸钠的质量
d氯化钙溶液中溶质的质量分数
(3)计算食用碱样品碳酸钠的质量分数_____(写出计算过程,结果保留到0.1%)
22.某化学研究小组为了测定一工厂废水中硫酸的溶质质量分数,取100克废水置于烧杯中,加入100克一定质量分数的硝酸钡溶液恰好完全反应(废水中其它成分不与硝酸钡反应)。反应后过滤,将得到的沉淀洗涤、干燥、称重,称得质量为2.33克。(化学反应方程式为:Ba(NO3)2+H2SO4==BaSO4↓+2HNO3)请计算:
(1)完全反应后烧杯内剩余的溶液质量为__________克。
(2)100克废水中硫酸的溶质质量分数是多少?
23.侯德榜成功研制了“侯氏制碱法”,打破了西方发达国家对我国制碱技术的封锁,为世界制碱工业做出了杰出贡献。某工厂为了测定用“侯氏制碱法”制得的纯碱样品中纯碱的质量分数,工厂技术员完成了图所示的测定工作(不考虑其它因素对测定结果的影响),请根据图中数据计算:样品中纯碱的质量分数。(计算结果精确到0.1%)
试卷第1页,共3页
参考答案:
1.C
2.B
3.B
4.C
5.B
6.B
7.D
8.C
9.B
10.C
11.D
12.C
13. ② NaHCO3+ HCl = NaCl + H2O + CO2↑ 常温下,碳的化学性质稳定 温度升高,压强增大
14. 过滤 蒸发结晶或蒸发溶剂 稀盐酸 化合反应和置换反应
15. 铝和氧气反应生成致密的氧化铝保护膜 Fe2O3+6HCl===2FeCl3+3H2O 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
16. CO2 置换反应 氢氧化钙(或氢氧化钾、氢氧化钡)
17. 尿素 碳酸氢铵 氯化铵 无 能 NH4HCO3+HCl═NH4Cl+H2O+CO2↑
18. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
19. NH4HCO3 KMnO4 NaCl Fe
20.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
21. CaCl2和NaCl abc 87.9%
22.(1)197.67;(2)0.98%
23.解:由质量守恒定律可得,反应产生的二氧化碳的质量=378.5g-376.3g=2.2g
设样品中纯碱的质量为x,
样品中纯碱的质量分数=
答:样品中纯碱的质量分数为96.4%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列有关碳及碳的化合物的说法正确的是
A.金刚石、石墨和C60的化学性质相似,物理性质有很大差异,是因为它们由不同的原子构成
B.煤炉上放一盆水就能防止一氧化碳中毒
C.碳酸钙在医疗上可用作补钙剂
D.空气中二氧化碳含量过高可形成酸雨
2.Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于
A.氧化物
B.盐
C.有机物
D.混合物
3.下列有关常见酸、碱、盐的说法不正确的是( )
A.浓盐酸具有挥发性,浓硫酸具有吸水性
B.Na2CO3和CaCO3都是白色易溶于水的固体
C.NaCl是白色易溶于水的固体,溶解度受温度影响小
D.NaOH和Ca(OH)2露置在空气中容易变质
4.下列化学反应属于置换反应的是( )
A.H2O+CaO═Ca(OH)2
B.Na2SO4+BaCl2═2NaCl+BaSO4↓
C.H2+CuOCu+H2O
D.3CO+Fe2O32Fe+3CO2
5.下列反应属于复分解反应的是
A.CO2+ H2O=H2CO3 B.2HC1 +Ca(OH)2=CaCl2+ 2H2O
C.2KMnO4K2MnO4+MnO2+O2↑ D.2Na+2H2O=2NaOH + H2↑
6.某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
7.下列物质长期放置在空气中,溶液质量因发生化学变化而减小的是
A.NaCl溶液 B.NaOH溶液 C.浓盐酸 D.石灰水
8.向盐酸和氯化铜混合溶液中加入一定质量分数的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,下列说法不正确的是
A.a点溶液中的pH<7
B.bc段(不含b、c点)反应的化学方程式为
C.c点溶液中含有两种溶质
D.整个变化过程中氯离子的数目没有改变
9.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项 物质 选用试剂 操作方法
A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干
B CO(CO2) NaOH溶液、浓硫酸 洗气、干燥
C CaO(CaCO3) 水 过滤、烘干
D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
10.去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是( )
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用题35图装置加热蒸发,至水分完全蒸干时停止加热
11.下列除去物质中所含少量杂质的方法错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B CaSO4溶液 稀硫酸 过量CaCO3 粉末、过滤
C FeCl2溶液 CuCl2 过量铁粉、过滤
D 二氧化碳 一氧化碳 点燃
A.A B.B C.C D.D
12.甲、乙两化工厂分布如图所示,箭头代表水流方向,如果在a处取水样检测,水中含有少量NaOH、Na2SO4;在c处取水样检测,pH=7且水中只含有少量NaCl.则b处水中含有的一组物质是( )
A.MgSO4 NaCl B.H2SO4 Ba(NO3)2
C.BaCl2 HCl D.H2SO4 MgCl2
二、简答题
13.请用学过的化学知识解释下列生活问题。
(1)某学生的午餐有①米饭②鱼肉③蔬菜其中富含蛋白质的是_____________。(填序号)
(2)小苏打通常用于治疗胃酸过多,但同时患有冒溃疡的病人却不能服用,其原因是____________(用化学方程式表示)。
(3)“钻石恒久远,一颗永流传”,说明______________。
(4)自行车夏天易爆胎,请用分子的观点解释“夏天易爆胎”的原因_______________。
14.三沙市是我国位置最南、总面积最大(含海域)、陆地面积最小的地级市。
(1)永兴岛上的饮用水主要利用海水淡化膜对海水进行二级 脱盐后获得。分离原理如图所示,该原理与化学实验中常见的_____操作相似;
(2)三沙海域的海水盐度高,从海水中获取食盐的方法是_____;
(3)海水提取粗盐后的母液还可以用来提取金属镁,其流程如下:
该流程中,溶液 A 为_____,其中没有发生的基本反应类型为_____。
15.请用所学化学知识解释下列原理。
(1)铝的化学性质活泼,而铝制品具有良好的抗腐蚀性能的原因是什么?_______________________
(2)盐酸除铁锈(Fe2O3)的化学方程式为________________________________。
(3)工业上可用Cl2与NaOH溶液反应制取漂白液:Cl2+2NaOH===NaCl+NaClO+H2O。与此类似,可用Cl2与石灰乳[主要成分Ca(OH)2]反应来制取漂白粉,试写出此反应的化学方程式________________________________。
三、推断题
16.抗击疫情,我们众志成城,万众一心,便能马到成功。小万用化学物质七巧板拼成的小马如图所示,拼图的规则是有一条边相互接触(包括部分接触)的物质之间能发生化学反应(所涉及反应均为初中常见化学反应)。A~G分别是盐酸、碳酸钙、氢氧化钠、二氧化碳、氧化铜、硫酸铜、氢气中的一种,A是单质,G常用于配制农药波尔多液。
请回答下列问题:
(1)F的化学式为_______。
(2)A与B反应的基本反应类型为_______。
(3)C与D反应的化学方程式为_______。
(4)E与G反应的现象是有蓝色沉淀生成,能够代替E的物质是_______。
17.实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种。为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如图实验(此处箭头表示得出实验结论):
根据上述实验回答:
(1)写出三种化肥的名称:A______;B______;C______。
(2)如果实验Ⅱ中B、C两种样品没有另取,对实验结果______(填“有”或“无”)影响。
(3)常温下如要鉴别B、C两种样品,______(填“能”或“不能”)采取闻气味的方法。
(4)写出操作Ⅱ中涉及的化学反应的方程式:______。
四、实验题
18.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
19.现有一包固体粉末,可能含有C粉、KMnO4、NaCl、NH4HCO3、Fe粉中的一种或几种。现做如下实验:
(1)取少量固体加热,无氨味,则原固体中一定不含________。
(2)另取少量固体溶于足量水过滤,得到无色澄清滤液和黑色固体,则原固体中一定不含__________。
(3)取(2)中无色澄清滤液适量,蒸发,出现较多固体,则原固体中一定含有_____。
(4)取(2)中得到的黑色固体,加入足量的稀盐酸,固体全部溶解并有气体放出,由此判断原固体中还含有_________。
五、计算题
20.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
21.厨房中;使用的食用碱(主要成分是碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学对其组成展开探究。他们实验的过程和数据如图所示:
请你据图分析:
(1)反应后滤液中含有的溶质是_____(写化学式)
(2)通过已知数据,能求出的量有_____(写字母序号)
a反应后滤液的总质量
b参加反应的氯化钙的质量
c样品中碳酸钠的质量
d氯化钙溶液中溶质的质量分数
(3)计算食用碱样品碳酸钠的质量分数_____(写出计算过程,结果保留到0.1%)
22.某化学研究小组为了测定一工厂废水中硫酸的溶质质量分数,取100克废水置于烧杯中,加入100克一定质量分数的硝酸钡溶液恰好完全反应(废水中其它成分不与硝酸钡反应)。反应后过滤,将得到的沉淀洗涤、干燥、称重,称得质量为2.33克。(化学反应方程式为:Ba(NO3)2+H2SO4==BaSO4↓+2HNO3)请计算:
(1)完全反应后烧杯内剩余的溶液质量为__________克。
(2)100克废水中硫酸的溶质质量分数是多少?
23.侯德榜成功研制了“侯氏制碱法”,打破了西方发达国家对我国制碱技术的封锁,为世界制碱工业做出了杰出贡献。某工厂为了测定用“侯氏制碱法”制得的纯碱样品中纯碱的质量分数,工厂技术员完成了图所示的测定工作(不考虑其它因素对测定结果的影响),请根据图中数据计算:样品中纯碱的质量分数。(计算结果精确到0.1%)
试卷第1页,共3页
参考答案:
1.C
2.B
3.B
4.C
5.B
6.B
7.D
8.C
9.B
10.C
11.D
12.C
13. ② NaHCO3+ HCl = NaCl + H2O + CO2↑ 常温下,碳的化学性质稳定 温度升高,压强增大
14. 过滤 蒸发结晶或蒸发溶剂 稀盐酸 化合反应和置换反应
15. 铝和氧气反应生成致密的氧化铝保护膜 Fe2O3+6HCl===2FeCl3+3H2O 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
16. CO2 置换反应 氢氧化钙(或氢氧化钾、氢氧化钡)
17. 尿素 碳酸氢铵 氯化铵 无 能 NH4HCO3+HCl═NH4Cl+H2O+CO2↑
18. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
19. NH4HCO3 KMnO4 NaCl Fe
20.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
21. CaCl2和NaCl abc 87.9%
22.(1)197.67;(2)0.98%
23.解:由质量守恒定律可得,反应产生的二氧化碳的质量=378.5g-376.3g=2.2g
设样品中纯碱的质量为x,
样品中纯碱的质量分数=
答:样品中纯碱的质量分数为96.4%。
答案第1页,共2页
答案第1页,共2页
