11.2化学肥料同步测试——2021-2022学年人教版九年级下册(word版 含答案)
文档属性
| 名称 | 11.2化学肥料同步测试——2021-2022学年人教版九年级下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 144.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-19 00:00:00 | ||
图片预览




文档简介
11.2 化学肥料
一、单选题
1.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
2.下列实验设计,不合理的是
选项 实验内容 实验过程
A 二氧化碳的溶解性 在充满二氧化碳气体的软塑料瓶中倒入1/3的水,拧紧瓶盖,振荡,塑料瓶迅速变瘪
B 浓盐酸的挥发性 打开盛有浓盐酸的细口瓶,瓶口有白雾产生
C 鉴定某溶液是氯化铁溶液 向溶液中滴加氢氧化钠溶液,有白色沉淀产生
D 硫酸铵是一种铵态氮肥 硫酸铵样品与熟石灰混合后研磨,有刺激性气味气体生成
A.A B.B C.C D.D
3.小芳家里种的空心菜叶子发黄、长势不好,是缺氮肥的表现,她应该给空心菜施放的肥料是( )
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2 D.K2SO4
4.今年夏粮又获丰收,再显中国饭碗自信,其中化肥功不可没。下列说法错误的是( )
A.尿素[CO(NH2)2]能使作物枝叶繁茂、叶色浓绿
B.磷酸二氢铵(NH4H2PO4)属于复合肥
C.含氮量为31.5%的硝酸铵(NH4NO3)化肥样品为纯净物
D.化肥虽好不能滥用,过度施肥会造成土壤退化和水体污染
5.下列化肥中,从外观即可与其他化肥相区别的是
A.磷矿粉 B.硝酸铵 C.硫酸钾 D.氯化钾
6.下列关于化肥 NH4H2PO4(磷酸二氢铵)的说法错误的是
A.P元素的化合价是+3价
B.N元素的化合价是-3价
C.NH4H2PO4属于复合肥料
D.NH4H2PO4不能与草木灰混合使用
7.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
8.雷电能自然固氮并最终形成氮肥,下列属于含氮复合肥料的是( )
A.KNO3 B.Ca(NO3)2 C.NH4NO3 D.NaNO3
9.化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
选项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
A.A B.B C.C D.D
10.“实施国家节水行动,建设节水型社会”必须坚持人与自然和谐相处。下列做法符合建设节水型社会的是( )
A.抑制河湖中所有植物的生长
B.整治河流水域周边的禽畜养殖业
C.禁止使用农药和化肥
D.生活污水可以不经处理直接排放
11.利用化学知识能帮你在“3.15打假”中识别伪劣商品,下列“打假”方法中错误的是( )
选项 假商品 替代商品 鉴别方法
A 假化肥 用NH4Cl代替尿素[CO(NH2)2] 与氢氧化钠溶液混合后加热,闻气味
B 假黄金 用铜锌合金代替金首饰 放入稀盐酸中,观察是否有气泡冒出
C 假纯水 用自来水(含有Cl-)代替纯水 加硝酸银溶液,观察是否产生白色沉淀
D 假药 用BaCO3代替BaSO4做钡餐 加水观察两种钡盐是否溶解
A.A B.B C.C D.D
12.下列实验方案设计不合理的是
选项 实验内容 操作或所用试剂
A 鉴别铁粉和木炭粉 观察颜色
B 鉴别氯化铵和氯化钾 加熟石灰,混合研磨
C 除去铜中混有的氧化铜 加过量稀硫酸,过滤
D 除去氧化钙中混有的碳酸钙 高温煅烧
A.A B.B C.C D.D
13.长期挑食、偏食不利于中学生的健康,每天的食物必须注意合理搭配。下列食物中富含维生素的是
A.西红柿 B.鱼 C.米饭 D.鸡蛋
14.化学与我们的生活 相关。以下说法正确的是
①为保护水资源应禁止使用化肥农药
②回收废旧金属有利于节约资源
③天然气泄漏应立即打开排气扇换气
④用聚氯乙烯塑料包装食品
⑤减少燃煤发电,增加太阳能发电,有利于治理雾霾
A.②⑤ B.②③⑤ C.④⑤ D.①③④
15.使用下列试剂能将氯化钠、碳酸钠、氯化钡三种溶液鉴别出来的是
A.稀硫酸 B.氯化钠溶液 C.铁片 D.氢氧化钠溶液
16.甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是
A.C、CO、CO2 B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3 D.Fe2O3、FeCl3、Fe(OH)3
二、综合应用题
17.酸、碱、盐是中学化学学习和研究的重要内容。
(1)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2]可用稀盐酸除掉,写出稀盐酸与CaCO3反应的化学方程式_____。
(2)采用氨碱法生产纯碱,主要流程如图:
①上述Ⅰ、Ⅱ两个步骤总反应的化学方程式是_____。
②从步骤Ⅱ过滤后的滤液中可获得铵态氮肥.检验铵态氮肥的方法是_____。
(3)蒸发海水得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
①加入过量Na2CO3溶液的目的是____,溶液B中含有的溶质有____,步骤④用到玻璃棒的作用是______。
②固体X的成分是CaCO3、BaCO3、BaSO4和 Mg(OH)2,请写出生成Mg(OH)2的化学方程式_______。
(4)在13.25g含氯化钠杂质的纯碱样品中逐步加入质量分数为7.3%的稀盐酸,当加入100g稀盐酸时,所得溶液的pH为7。求样品中纯碱的质量分数是多少?______
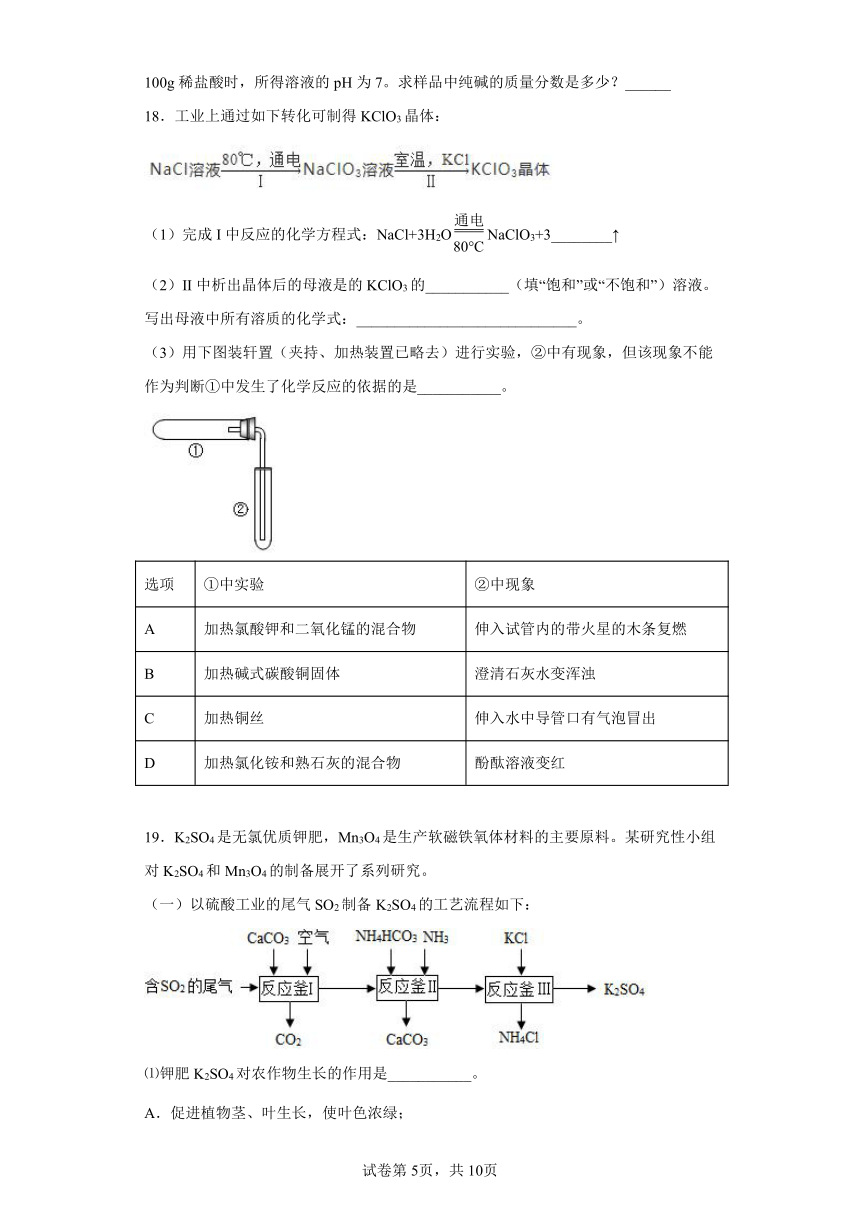
18.工业上通过如下转化可制得KClO3晶体:
(1)完成I中反应的化学方程式:NaCl+3H2ONaClO3+3________↑
(2)II中析出晶体后的母液是的KClO3的___________(填“饱和”或“不饱和”)溶液。写出母液中所有溶质的化学式:_____________________________。
(3)用下图装轩置(夹持、加热装置已略去)进行实验,②中有现象,但该现象不能作为判断①中发生了化学反应的依据的是___________。
选项 ①中实验 ②中现象
A 加热氯酸钾和二氧化锰的混合物 伸入试管内的带火星的木条复燃
B 加热碱式碳酸铜固体 澄清石灰水变浑浊
C 加热铜丝 伸入水中导管口有气泡冒出
D 加热氯化铵和熟石灰的混合物 酚酞溶液变红
19.K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。某研究性小组对K2SO4和Mn3O4的制备展开了系列研究。
(一)以硫酸工业的尾气SO2制备K2SO4的工艺流程如下:
⑴钾肥K2SO4对农作物生长的作用是___________。
A.促进植物茎、叶生长,使叶色浓绿;
B.增强植物的抗寒、抗旱能力
C.增强植物的抗病虫害、抗倒伏能力
⑵反应釜I中发生的反应包括:①碳酸钙高温分解的化学方程式为________;
②CaO + SO2==CaSO3③ 2CaSO3+O2==2CaSO4
⑶反应釜III:向反应II 所得(NH4)2SO4溶液中加入KCl溶液充分反应后,经蒸发浓缩、过滤 、洗涤、干燥等操作即可制得K2SO4产品。为提高K2SO4产品纯度,过滤时应控制反应液的温度范围为____________(填字母序号,如图为几种盐的溶解度曲线)。
A.0℃-10℃ B.20℃-30℃ C.60℃-65℃ D.80℃-90℃
⑷上述工艺流程中循环利用的物质是_______;证明产品K2SO4中不含杂质的实验方法是_______写出方法、现象)。
(二)实验室以SO2气体为原料制备少量高纯Mn3O4的操作步骤如下:
【步骤I】制备MnSO4溶液:在三颈烧瓶中(装置见图) 加入一定量MnO2和水,先通氮气,再通入SO2和N2混合气体,搅拌反应3小时。停止通SO2,继续反应片刻后过滤得MnSO4溶液。
[资料1]亚硫酸(H2SO3)在Mn2+催化作用下被O2氧化为硫酸,硫酸与MnO2在常温下不易发生反应。
⑸烧杯中石灰乳(有效成分为氢氧化钙)的作用为________。
⑹三颈烧瓶中生成MnSO4的反应化学方程式为____________。
⑺步骤I中,先通入氮气的目的是_________。为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有:及时搅拌反应液、_______(任写1条)。
【步骤II】制备MnSO4 H2O晶体:利用硫酸锰的溶解度在100℃以上随温度升高而急剧降低的原理,采用压力釜升温加压结晶法后过滤、洗涤、低温干燥得纯净的MnSO4 H2O晶体。
【步骤III】制备Mn3O4固体:准确称取101.4mg MnSO4 H2O,将MnSO4 H2O晶体在空气中高温煅烧,下图是用热重分析仪测定煅烧时温度与剩余固体质量变化曲线。
[资料2] MnSO4在空气中高温煅烧生成Mn3O4和三氧化硫,当温度超过1000℃时,Mn3O4又被氧气氧化为Mn2O3或MnO2
⑻该曲线中A段所表示物质的化学式为___________。
20.从微观和宏观两方面研究质量守恒定律对化学科学发展具有重大意义。
(1)通过称量下列各组试剂在烧杯内混合前后的总质量,能验证质量守恒定律的是_______(填标号)。
A 蔗糖和水 B 石灰石和稀盐酸
C 铁屑和硫酸铜溶液 D 生石灰和水
(2)在氧气中点燃红磷的实验过程,固体变化如图1所示。
①燃烧条件分析,固体质量在前没有发生变化的原因是________。
②该反应的化学方程式为_______。
③参加反应的氧气质量为_______g。
(3)某反应的微观示意如图2所示:
①反应所属的基本反应类型为________。
②参加反应的甲物质和生成的丙物质分子数目比为______。
(4)用镁条在空气中燃烧的实验验证质量守恒定律。
①称量燃烧产物:质量大于反应物镁条的质量,是否该反应不遵循质量守恒定律。我______(“同意”或“不同意”),我的理由是_______。
②用如图(3)所示装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。对黄色固体进行探究。自学资料:镁能与氮气剧烈反应生成黄色的氮化镁()固体;氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。请设计实验,验证黄色固体是。
实验操作 实验现象 有关的化学方程式及结论
____ ____ ____
③空气中的含量远大于的含量,而镁条在空气中燃烧生成的却远多于,为什么呢?请给出合理的解释:_______。
(5)应用质量守恒定律探究镁条与盐溶液的反应,实验组合及现象如下:
实验序号 实验1 实验2 实验3 实验4
与镁条反应的溶液 溶液 溶液 溶液
实验现象 有大量气泡产生 有较多气泡产生 有少量气泡产生 气泡很少
加热后,实验现象 气泡明显增多,可闻到氨味 气泡增多 气泡增多 气泡增多
①分别收集各组实验产生的气体,均可点燃产生淡蓝色火焰,这种可燃性气体是___。
②实验4的目的是_______;镁条与热水反应的化学方程式是_______。
③实验1中可闻到氨味的原因是(用化学方程式表示)________。
④根据上表中的实验现象,还能获得的两条结论是_______。
21.酸、碱、盐是九年级化学学习的重要知识,并且它们具有广泛的用途。
(1)下列关于酸、碱、盐的生产或应用中的说法合理的是( )
A 将氯化铵与草木灰混合施用
B 烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
C 用小苏打治疗胃酸过多
D 高温煅烧生石灰可以得到熟石灰
(2)随着新能源汽车的发展,动力电池领域对氢氧化锂的需求量越来越大。氢氧化锂(LiOH)与氢氧化钠化学性质相似,其原因是溶液中都有_______(填离子符号)。
(3)盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式_______。
(4)粗盐中含有泥沙、MgCl2、CaCl2、Na2SO4等杂质,为了得到纯净的氯化钠,化学兴趣小组设计如下实验:
Ⅰ.在操作①、操作②、操作③中都会用到同一种玻璃仪器,该仪器在操作③中的作用是什么?____
Ⅱ.写出一个加入Na2CO3溶液时所发生反应的化学方程式_______。
Ⅲ.上述流程中若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含有哪些杂质?_____(BaSO4不溶于水也不溶于酸)。
Ⅳ.如何判断加入盐酸达到适量_____。
(5)10g碳酸钙与100g稀盐酸恰好完全反应,生成4.4g二氧化碳,则反应所得氯化钙溶液的溶质质量分数为______(准确到0.1%)?
22.硫酸铵[(NH4)2SO4]简称硫铵,俗称肥田粉,是我国使用和生产最早的一个氮肥品种.
(1)硫酸铵中铵根(NH4+)的化合价为_____,氮元素的化合价为_____.
(2)硫酸铵中各元素的质量比为m(N):m(H):m(S):m(O)=_____(互质比).
(3)100g硫酸铵中氮元素的质量是_____(精确到0.1).
(4)_____g硫酸铵中的氮元素与100g硝酸铵中氮元素的质量相等.
(5)若某化肥主要含硫酸铵,测得其中氮元素的质量分数为21.0%(杂质不含氮),则该化肥中硫酸铵的质量分数为_____(精确到0.1%).
(6)尿素[CO(NH2)2]和碳酸氢铵(NH4HCO3,简称碳铵)是苏州地区常用的氮肥,某月市场报价为:尿素2200元/吨,碳铵700元/吨,若你用500元前去购买氮肥,为了使所购的化肥得到的氮最多,你选择这两种氮肥中的_____(写名称).
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.B
4.C
5.A
6.A
7.B
8.A
9.C
10.B
11.D
12.A
13.A
14.A
15.A
16.C
17.(1)
(2)
与熟石灰混合研磨,闻气味
(3) 除去氯化钙和过量的氯化钡 氯化钠、氢氧化钠、碳酸钠 搅拌,防止局部温度过高,造成液滴飞溅
(4)解:设样品中纯碱的质量分数是x
x=80%
答:样品中纯碱的质量分数是80%
18. H2 饱和 KClO3、NaCl、NaClO3、KCl C
19. C CaCO3CaO+CO2↑ D CaCO3 取少量样品,加水配成溶液,先滴加足量Ba(NO3)2溶液,取上层清液滴加AgNO3溶液,若无沉淀生成,说明K2SO4中不含杂质。 吸收二氧化硫气体,防止空气污染 MnO2+SO2===MnSO4 排尽装置内的空气,防止SO2气体被氧化为硫酸,导致转化率降低。 微热提高温度 MnSO4
20. C 温度未达到红磷的着火点 8.0 置换反应 不同意 镁燃烧是镁与空气中氧气等发生了反应 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 试管中有气泡产生,湿润的红色石蕊试纸变蓝 、,证明该黄色固体是 比活泼(其他合理答案均可) 对比作用 加热能加快镁条与水的反应速率;水溶液中的盐对镁条与水的反应起催化作用,盐酸盐(氯离子)的催化作用更好
21. C OH- 搅拌,防止因局部温度过高造成液滴飞溅 (或) 氯化钙、氯化钡、氯化镁 当不再有气泡出时停止滴加稀盐酸 解:设反应后生成氯化钙质量为x
x=11.1g
答:滤液中氯化钙的质量分数是10.5%。
22. +1价 ﹣3价 7:2:8:16 21.2g 165.1g 99.1% 碳酸氢铵
答案第1页,共2页
答案第1页,共2页
一、单选题
1.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
2.下列实验设计,不合理的是
选项 实验内容 实验过程
A 二氧化碳的溶解性 在充满二氧化碳气体的软塑料瓶中倒入1/3的水,拧紧瓶盖,振荡,塑料瓶迅速变瘪
B 浓盐酸的挥发性 打开盛有浓盐酸的细口瓶,瓶口有白雾产生
C 鉴定某溶液是氯化铁溶液 向溶液中滴加氢氧化钠溶液,有白色沉淀产生
D 硫酸铵是一种铵态氮肥 硫酸铵样品与熟石灰混合后研磨,有刺激性气味气体生成
A.A B.B C.C D.D
3.小芳家里种的空心菜叶子发黄、长势不好,是缺氮肥的表现,她应该给空心菜施放的肥料是( )
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2 D.K2SO4
4.今年夏粮又获丰收,再显中国饭碗自信,其中化肥功不可没。下列说法错误的是( )
A.尿素[CO(NH2)2]能使作物枝叶繁茂、叶色浓绿
B.磷酸二氢铵(NH4H2PO4)属于复合肥
C.含氮量为31.5%的硝酸铵(NH4NO3)化肥样品为纯净物
D.化肥虽好不能滥用,过度施肥会造成土壤退化和水体污染
5.下列化肥中,从外观即可与其他化肥相区别的是
A.磷矿粉 B.硝酸铵 C.硫酸钾 D.氯化钾
6.下列关于化肥 NH4H2PO4(磷酸二氢铵)的说法错误的是
A.P元素的化合价是+3价
B.N元素的化合价是-3价
C.NH4H2PO4属于复合肥料
D.NH4H2PO4不能与草木灰混合使用
7.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
8.雷电能自然固氮并最终形成氮肥,下列属于含氮复合肥料的是( )
A.KNO3 B.Ca(NO3)2 C.NH4NO3 D.NaNO3
9.化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
选项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
A.A B.B C.C D.D
10.“实施国家节水行动,建设节水型社会”必须坚持人与自然和谐相处。下列做法符合建设节水型社会的是( )
A.抑制河湖中所有植物的生长
B.整治河流水域周边的禽畜养殖业
C.禁止使用农药和化肥
D.生活污水可以不经处理直接排放
11.利用化学知识能帮你在“3.15打假”中识别伪劣商品,下列“打假”方法中错误的是( )
选项 假商品 替代商品 鉴别方法
A 假化肥 用NH4Cl代替尿素[CO(NH2)2] 与氢氧化钠溶液混合后加热,闻气味
B 假黄金 用铜锌合金代替金首饰 放入稀盐酸中,观察是否有气泡冒出
C 假纯水 用自来水(含有Cl-)代替纯水 加硝酸银溶液,观察是否产生白色沉淀
D 假药 用BaCO3代替BaSO4做钡餐 加水观察两种钡盐是否溶解
A.A B.B C.C D.D
12.下列实验方案设计不合理的是
选项 实验内容 操作或所用试剂
A 鉴别铁粉和木炭粉 观察颜色
B 鉴别氯化铵和氯化钾 加熟石灰,混合研磨
C 除去铜中混有的氧化铜 加过量稀硫酸,过滤
D 除去氧化钙中混有的碳酸钙 高温煅烧
A.A B.B C.C D.D
13.长期挑食、偏食不利于中学生的健康,每天的食物必须注意合理搭配。下列食物中富含维生素的是
A.西红柿 B.鱼 C.米饭 D.鸡蛋
14.化学与我们的生活 相关。以下说法正确的是
①为保护水资源应禁止使用化肥农药
②回收废旧金属有利于节约资源
③天然气泄漏应立即打开排气扇换气
④用聚氯乙烯塑料包装食品
⑤减少燃煤发电,增加太阳能发电,有利于治理雾霾
A.②⑤ B.②③⑤ C.④⑤ D.①③④
15.使用下列试剂能将氯化钠、碳酸钠、氯化钡三种溶液鉴别出来的是
A.稀硫酸 B.氯化钠溶液 C.铁片 D.氢氧化钠溶液
16.甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是
A.C、CO、CO2 B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3 D.Fe2O3、FeCl3、Fe(OH)3
二、综合应用题
17.酸、碱、盐是中学化学学习和研究的重要内容。
(1)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2]可用稀盐酸除掉,写出稀盐酸与CaCO3反应的化学方程式_____。
(2)采用氨碱法生产纯碱,主要流程如图:
①上述Ⅰ、Ⅱ两个步骤总反应的化学方程式是_____。
②从步骤Ⅱ过滤后的滤液中可获得铵态氮肥.检验铵态氮肥的方法是_____。
(3)蒸发海水得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
①加入过量Na2CO3溶液的目的是____,溶液B中含有的溶质有____,步骤④用到玻璃棒的作用是______。
②固体X的成分是CaCO3、BaCO3、BaSO4和 Mg(OH)2,请写出生成Mg(OH)2的化学方程式_______。
(4)在13.25g含氯化钠杂质的纯碱样品中逐步加入质量分数为7.3%的稀盐酸,当加入100g稀盐酸时,所得溶液的pH为7。求样品中纯碱的质量分数是多少?______
18.工业上通过如下转化可制得KClO3晶体:
(1)完成I中反应的化学方程式:NaCl+3H2ONaClO3+3________↑
(2)II中析出晶体后的母液是的KClO3的___________(填“饱和”或“不饱和”)溶液。写出母液中所有溶质的化学式:_____________________________。
(3)用下图装轩置(夹持、加热装置已略去)进行实验,②中有现象,但该现象不能作为判断①中发生了化学反应的依据的是___________。
选项 ①中实验 ②中现象
A 加热氯酸钾和二氧化锰的混合物 伸入试管内的带火星的木条复燃
B 加热碱式碳酸铜固体 澄清石灰水变浑浊
C 加热铜丝 伸入水中导管口有气泡冒出
D 加热氯化铵和熟石灰的混合物 酚酞溶液变红
19.K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。某研究性小组对K2SO4和Mn3O4的制备展开了系列研究。
(一)以硫酸工业的尾气SO2制备K2SO4的工艺流程如下:
⑴钾肥K2SO4对农作物生长的作用是___________。
A.促进植物茎、叶生长,使叶色浓绿;
B.增强植物的抗寒、抗旱能力
C.增强植物的抗病虫害、抗倒伏能力
⑵反应釜I中发生的反应包括:①碳酸钙高温分解的化学方程式为________;
②CaO + SO2==CaSO3③ 2CaSO3+O2==2CaSO4
⑶反应釜III:向反应II 所得(NH4)2SO4溶液中加入KCl溶液充分反应后,经蒸发浓缩、过滤 、洗涤、干燥等操作即可制得K2SO4产品。为提高K2SO4产品纯度,过滤时应控制反应液的温度范围为____________(填字母序号,如图为几种盐的溶解度曲线)。
A.0℃-10℃ B.20℃-30℃ C.60℃-65℃ D.80℃-90℃
⑷上述工艺流程中循环利用的物质是_______;证明产品K2SO4中不含杂质的实验方法是_______写出方法、现象)。
(二)实验室以SO2气体为原料制备少量高纯Mn3O4的操作步骤如下:
【步骤I】制备MnSO4溶液:在三颈烧瓶中(装置见图) 加入一定量MnO2和水,先通氮气,再通入SO2和N2混合气体,搅拌反应3小时。停止通SO2,继续反应片刻后过滤得MnSO4溶液。
[资料1]亚硫酸(H2SO3)在Mn2+催化作用下被O2氧化为硫酸,硫酸与MnO2在常温下不易发生反应。
⑸烧杯中石灰乳(有效成分为氢氧化钙)的作用为________。
⑹三颈烧瓶中生成MnSO4的反应化学方程式为____________。
⑺步骤I中,先通入氮气的目的是_________。为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有:及时搅拌反应液、_______(任写1条)。
【步骤II】制备MnSO4 H2O晶体:利用硫酸锰的溶解度在100℃以上随温度升高而急剧降低的原理,采用压力釜升温加压结晶法后过滤、洗涤、低温干燥得纯净的MnSO4 H2O晶体。
【步骤III】制备Mn3O4固体:准确称取101.4mg MnSO4 H2O,将MnSO4 H2O晶体在空气中高温煅烧,下图是用热重分析仪测定煅烧时温度与剩余固体质量变化曲线。
[资料2] MnSO4在空气中高温煅烧生成Mn3O4和三氧化硫,当温度超过1000℃时,Mn3O4又被氧气氧化为Mn2O3或MnO2
⑻该曲线中A段所表示物质的化学式为___________。
20.从微观和宏观两方面研究质量守恒定律对化学科学发展具有重大意义。
(1)通过称量下列各组试剂在烧杯内混合前后的总质量,能验证质量守恒定律的是_______(填标号)。
A 蔗糖和水 B 石灰石和稀盐酸
C 铁屑和硫酸铜溶液 D 生石灰和水
(2)在氧气中点燃红磷的实验过程,固体变化如图1所示。
①燃烧条件分析,固体质量在前没有发生变化的原因是________。
②该反应的化学方程式为_______。
③参加反应的氧气质量为_______g。
(3)某反应的微观示意如图2所示:
①反应所属的基本反应类型为________。
②参加反应的甲物质和生成的丙物质分子数目比为______。
(4)用镁条在空气中燃烧的实验验证质量守恒定律。
①称量燃烧产物:质量大于反应物镁条的质量,是否该反应不遵循质量守恒定律。我______(“同意”或“不同意”),我的理由是_______。
②用如图(3)所示装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。对黄色固体进行探究。自学资料:镁能与氮气剧烈反应生成黄色的氮化镁()固体;氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。请设计实验,验证黄色固体是。
实验操作 实验现象 有关的化学方程式及结论
____ ____ ____
③空气中的含量远大于的含量,而镁条在空气中燃烧生成的却远多于,为什么呢?请给出合理的解释:_______。
(5)应用质量守恒定律探究镁条与盐溶液的反应,实验组合及现象如下:
实验序号 实验1 实验2 实验3 实验4
与镁条反应的溶液 溶液 溶液 溶液
实验现象 有大量气泡产生 有较多气泡产生 有少量气泡产生 气泡很少
加热后,实验现象 气泡明显增多,可闻到氨味 气泡增多 气泡增多 气泡增多
①分别收集各组实验产生的气体,均可点燃产生淡蓝色火焰,这种可燃性气体是___。
②实验4的目的是_______;镁条与热水反应的化学方程式是_______。
③实验1中可闻到氨味的原因是(用化学方程式表示)________。
④根据上表中的实验现象,还能获得的两条结论是_______。
21.酸、碱、盐是九年级化学学习的重要知识,并且它们具有广泛的用途。
(1)下列关于酸、碱、盐的生产或应用中的说法合理的是( )
A 将氯化铵与草木灰混合施用
B 烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
C 用小苏打治疗胃酸过多
D 高温煅烧生石灰可以得到熟石灰
(2)随着新能源汽车的发展,动力电池领域对氢氧化锂的需求量越来越大。氢氧化锂(LiOH)与氢氧化钠化学性质相似,其原因是溶液中都有_______(填离子符号)。
(3)盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式_______。
(4)粗盐中含有泥沙、MgCl2、CaCl2、Na2SO4等杂质,为了得到纯净的氯化钠,化学兴趣小组设计如下实验:
Ⅰ.在操作①、操作②、操作③中都会用到同一种玻璃仪器,该仪器在操作③中的作用是什么?____
Ⅱ.写出一个加入Na2CO3溶液时所发生反应的化学方程式_______。
Ⅲ.上述流程中若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含有哪些杂质?_____(BaSO4不溶于水也不溶于酸)。
Ⅳ.如何判断加入盐酸达到适量_____。
(5)10g碳酸钙与100g稀盐酸恰好完全反应,生成4.4g二氧化碳,则反应所得氯化钙溶液的溶质质量分数为______(准确到0.1%)?
22.硫酸铵[(NH4)2SO4]简称硫铵,俗称肥田粉,是我国使用和生产最早的一个氮肥品种.
(1)硫酸铵中铵根(NH4+)的化合价为_____,氮元素的化合价为_____.
(2)硫酸铵中各元素的质量比为m(N):m(H):m(S):m(O)=_____(互质比).
(3)100g硫酸铵中氮元素的质量是_____(精确到0.1).
(4)_____g硫酸铵中的氮元素与100g硝酸铵中氮元素的质量相等.
(5)若某化肥主要含硫酸铵,测得其中氮元素的质量分数为21.0%(杂质不含氮),则该化肥中硫酸铵的质量分数为_____(精确到0.1%).
(6)尿素[CO(NH2)2]和碳酸氢铵(NH4HCO3,简称碳铵)是苏州地区常用的氮肥,某月市场报价为:尿素2200元/吨,碳铵700元/吨,若你用500元前去购买氮肥,为了使所购的化肥得到的氮最多,你选择这两种氮肥中的_____(写名称).
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.B
4.C
5.A
6.A
7.B
8.A
9.C
10.B
11.D
12.A
13.A
14.A
15.A
16.C
17.(1)
(2)
与熟石灰混合研磨,闻气味
(3) 除去氯化钙和过量的氯化钡 氯化钠、氢氧化钠、碳酸钠 搅拌,防止局部温度过高,造成液滴飞溅
(4)解:设样品中纯碱的质量分数是x
x=80%
答:样品中纯碱的质量分数是80%
18. H2 饱和 KClO3、NaCl、NaClO3、KCl C
19. C CaCO3CaO+CO2↑ D CaCO3 取少量样品,加水配成溶液,先滴加足量Ba(NO3)2溶液,取上层清液滴加AgNO3溶液,若无沉淀生成,说明K2SO4中不含杂质。 吸收二氧化硫气体,防止空气污染 MnO2+SO2===MnSO4 排尽装置内的空气,防止SO2气体被氧化为硫酸,导致转化率降低。 微热提高温度 MnSO4
20. C 温度未达到红磷的着火点 8.0 置换反应 不同意 镁燃烧是镁与空气中氧气等发生了反应 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 试管中有气泡产生,湿润的红色石蕊试纸变蓝 、,证明该黄色固体是 比活泼(其他合理答案均可) 对比作用 加热能加快镁条与水的反应速率;水溶液中的盐对镁条与水的反应起催化作用,盐酸盐(氯离子)的催化作用更好
21. C OH- 搅拌,防止因局部温度过高造成液滴飞溅 (或) 氯化钙、氯化钡、氯化镁 当不再有气泡出时停止滴加稀盐酸 解:设反应后生成氯化钙质量为x
x=11.1g
答:滤液中氯化钙的质量分数是10.5%。
22. +1价 ﹣3价 7:2:8:16 21.2g 165.1g 99.1% 碳酸氢铵
答案第1页,共2页
答案第1页,共2页
同课章节目录
