7.3溶液浓稀的表示 同步练习(word版有答案)
文档属性
| 名称 | 7.3溶液浓稀的表示 同步练习(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 132.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-19 00:00:00 | ||
图片预览



文档简介
7.3 溶液浓稀的表示
一、单选题
1.稀释质量分数为98%(密度为1.84g/ mL)的浓硫酸配制500 mL质量分数为20%的稀硫酸(密度为1.14g/ mL),稀释时需用的水的体积约为
A.436.8 mL B.453.7mL C.456.0 mL D.458.3mL
2.家用食醋是含醋酸质量分数为10%的水溶液,其中的“10%”的含义是( )
A.100 g醋酸中含醋为10 g B.100 g醋酸的水溶液中含醋酸10g
C.100 g水中含醋酸为10g D.100 g醋酸的水溶液中含水10g
3.KNO3 的溶解度曲线如下图所示。下列说法错误的是( )
A.0~60℃,KNO3 的溶解度随温度升高而增大
B.60℃时的 KNO3 饱和溶液降温至 20℃,有晶体析出
C.20℃,100g 水中最多能溶解 31.6g KNO3
D.60℃时,可配制溶质质量分数为 60%的 KNO3 溶液
4.将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )
A.甲的溶解度随温度升高而增大
B.t1℃时,甲、乙的溶解度均为20g
C.温度由t2℃降低到t1℃时,甲溶液析出5g固体
D.a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b
5.现有100mL 20%的硫酸,其密度为1.14g/cm3,下列说法正确的是( )
A.该溶液含溶质20 g
B.该溶液中,溶质质量:溶液质量=1:6
C.该溶液中,溶质质量:溶剂质量=1:5
D.该溶液中,溶液质量:溶剂质量=5:4
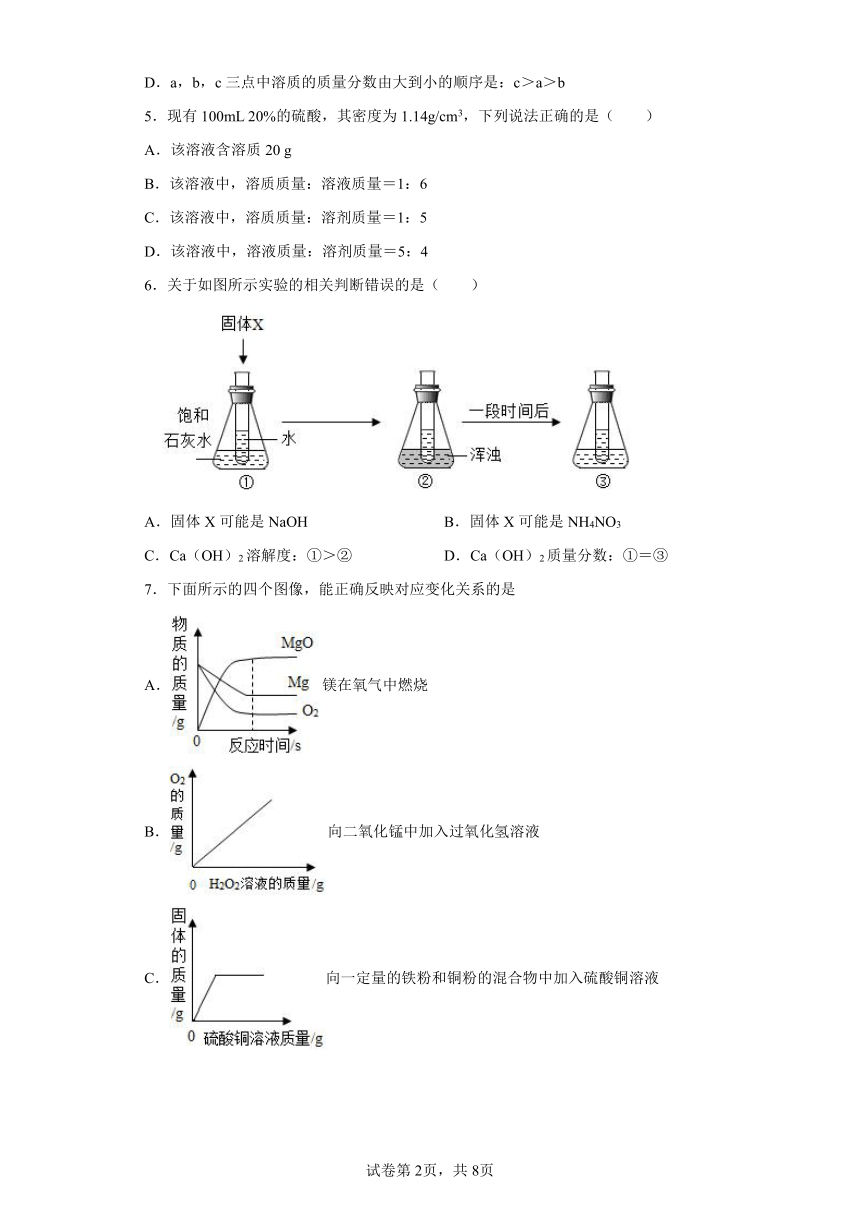
6.关于如图所示实验的相关判断错误的是( )
A.固体X可能是NaOH B.固体X可能是NH4NO3
C.Ca(OH)2溶解度:①>② D.Ca(OH)2质量分数:①=③
7.下面所示的四个图像,能正确反映对应变化关系的是
A.镁在氧气中燃烧
B.向二氧化锰中加入过氧化氢溶液
C.向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液
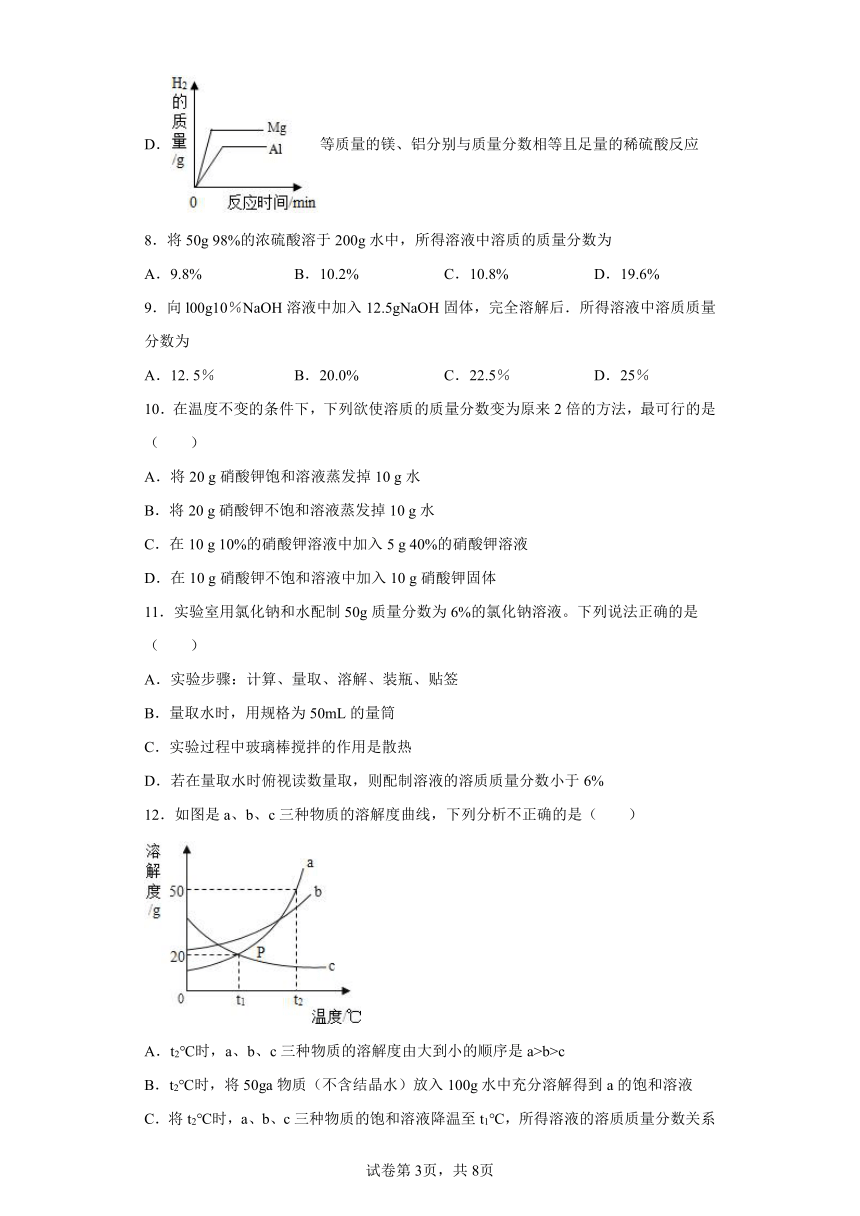
D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
8.将50g 98%的浓硫酸溶于200g水中,所得溶液中溶质的质量分数为
A.9.8% B.10.2% C.10.8% D.19.6%
9.向l00g10%NaOH溶液中加入12.5gNaOH固体,完全溶解后.所得溶液中溶质质量分数为
A.12. 5% B.20.0% C.22.5% D.25%
10.在温度不变的条件下,下列欲使溶质的质量分数变为原来2倍的方法,最可行的是( )
A.将20 g硝酸钾饱和溶液蒸发掉10 g水
B.将20 g硝酸钾不饱和溶液蒸发掉10 g水
C.在10 g 10%的硝酸钾溶液中加入5 g 40%的硝酸钾溶液
D.在10 g硝酸钾不饱和溶液中加入10 g硝酸钾固体
11.实验室用氯化钠和水配制50g质量分数为6%的氯化钠溶液。下列说法正确的是( )
A.实验步骤:计算、量取、溶解、装瓶、贴签
B.量取水时,用规格为50mL的量筒
C.实验过程中玻璃棒搅拌的作用是散热
D.若在量取水时俯视读数量取,则配制溶液的溶质质量分数小于6%
12.如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
A.t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.t2℃时,将50ga物质(不含结晶水)放入100g水中充分溶解得到a的饱和溶液
C.将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D.将c的饱和溶液变为不饱和溶液,可采用降温的方法
13.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是
A.甲和丙的溶解度相等
B.在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质量为78g
C.t2℃时,等质量的甲、乙、丙三种固体配制成饱和溶液所需溶剂质量的大小关系是甲<乙<丙
D.将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是甲>乙>丙
14.保持温度不变,小心蒸发NaCl不饱和溶液(蒸发皿中始终有溶液),则溶液中溶质的质量分数(m%)与时间(t)的关系合理的是
A. B. C. D.
15.如图是采用膜分离技术的海水淡化装置,对海水加压后,只有水分子可以通过淡化膜,离子等其他粒子不能通过淡化膜.加压后,装置右侧海水中增加的是( )
A.溶质质量分数 B.溶剂质量
C.溶液质量 D.溶质质量
16.下列关于溶液的说法正确的是
A.溶液一定是无色透明的
B.溶液一定是均一的、稳定的混合物
C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
D.将40g溶质质量分数为20%的氯化钠溶液倒出20g,剩余溶液溶质质量分数为10%
二、综合应用题
17.水是宝贵的自然资料,让我们一起走进“水”的世界。
①下图电解水实验中,反应的化学方程式是___。水电解过程发生改变的微粒名称是______。
②医疗上常用0.9%NaCl溶液作生理盐水,配制1000g生理盐水需要氯化钠固体的质量为_______还可以制取碳酸饮料,该过程中发生反应的化学方程式为_____________。
③某化学兴趣小组欲进行粗盐的初步提纯。粗盐的提纯实验步骤包括:a计算产率,b过滤,c溶解,d蒸发,e称量。实验步骤的正确顺序是:e、_________、a(填序号)。若NaCl的产率偏低,则可能的原因是_________(填字母)。
A.过滤时滤纸有破损B.蒸发后所得精盐未完全蒸干,含有水
C.溶解含泥沙的粗食盐时,加入的水量不足
提示:产率=×100%
④已知KCl的溶解度20℃时为34g/100g水,40℃时为40g/100g水。某实验小组做了如下实验。
A中所得溶液中溶质与溶剂的质量比为__________;溶质的质量分数相等的是___________。
I. B和CII. B和EⅢ. C和DIV. D和E
18.某化学兴趣小组为测定一定量生铁样品(样品中的其他成分不参加反应,也不溶于水)中铁的质量,并得到纯净的一定浓度的硫酸亚铁溶液。进行了如下实验
注:反应①结束后,所加稀硫酸刚好反应一半,反应②恰好完全反应。
请回答下列问题:
(1) 写出发生反应的化学方程式____________________________________。
(2) 根据已知条件列出求解①中参加反应的铁的质量(X)的比例式_________。
(3)该生铁样品中铁的质量为___________;
(4) 若最终得到的滤液为不饱和溶液,则所得滤液中溶质的质量分数为_______。
(5)若用98%的浓硫酸配制上述实验所用的稀硫酸,需加水的质量为_________。
19.在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如下图所示,甲、丙还有剩余固体,乙固体全部溶解。升温到80 ℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化。
(1)室温时,________(选填“甲”、“乙”或“丙”)溶液可能是不饱和溶液。
(2)上图中能表示乙物质的溶解度曲线的是____________(填“a”、“b”或“c”,下同),
(3)t2 ℃时,甲、乙、丙三种物质的等质量的饱和溶液降到t1 ℃时,所得溶液中水的质量由大到小的顺序是_______________________
(4)小强同学要在实验室配制15%的氯化钠溶液50 g。需要量筒规格为__________ml(填“20或50或100”),该同学按下图所示步骤依次操作:
按B量取所需的水配得的溶液溶质质量分数____________(填“偏大或偏小或无影响”);E中玻璃棒的作用是__________________。若上图A中砝码的质量为5 g,游码为2.5 g,则称得氯化钠的质量____________克
20.溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①时,A、B、C三种物质的溶解度由大到小的顺序是 _____ 。
②A、B、C三种物质中,溶解度随温度升高而减小的是 _____ 。
③时,完全溶解ag A物质最少需要水的质量是 _____ g。
④时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量 _____ B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、 _____ 和滤纸。
(3)在实验室中,配制溶质质量分数为的氯化钠溶液45g,需要氯化钠固体的质量是 _____ g。将的氯化钠溶液配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是 _____ g。
21.如表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃),回答下列问题:
溶液中溶质的质量分数/% 4 12 16 24 28
硫酸溶液的密度/g·mL-1 1.02 1.08 1.11 1.17 1.20
氨水的密度/g·mL-1 0.98 0.95 0.94 0.91 0.90
(1)20℃时,随着溶液中溶质质量分数逐渐增大,氨水的密度逐渐_____(填“增大”、“减小”或“不变”)。
(2)取12%的硫酸溶液100mL,可配制成6%的硫酸溶液_____g。
(3)向100g24%的氨水中加入100g水,摇匀,所得溶液体积是_____mL(结果精确到0.1)。
(4)配制溶质质量分数4%的硫酸溶液50mL,需要溶质质量分数24%的硫酸溶液多少毫升?(写出计算过程,结果精确到0.1)
22.在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如下图所示。请计算:
(1)完全反应时,生成氧气的质量为________克。
(2)完全反应后,剩余固体物质是_________(填化学式)。
(3)完全反应后,把剩余固体倒入100g蒸馏水中,充分溶解,求所得溶液中溶质的质量分数为_____________(最后结果保留0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.D
5.D
6.B
7.B
8.D
9.B
10.C
11.B
12.C
13.C
14.A
15.A
16.B
17. 2H2O2H2↑+O2↑ 水分子 9 CO2+H2O=H2CO3 c、b、d、e C 25:100(1:4) II、Ⅲ
18. Fe+ H2SO4= Fe SO4+ H2↑ 56/2==X/0.8g 22.4g 25% 320g
19. 乙 C c>b>a 50、 偏小、 搅拌,加快氯化钠溶解速率 , 2.5
20. CBA .C 100 小于 漏斗 4.5 500
21.(1)减小
(2)216
(3)210.5
(4)设需要溶质质量分数24%的硫酸溶液的质量为。
需要溶质质量分数24%的硫酸溶液的体积为:
答:需要溶质质量分数24%的硫酸溶液7.3mL。
22.(1)9.6g (2)KCl和MnO2(3)13.0%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.稀释质量分数为98%(密度为1.84g/ mL)的浓硫酸配制500 mL质量分数为20%的稀硫酸(密度为1.14g/ mL),稀释时需用的水的体积约为
A.436.8 mL B.453.7mL C.456.0 mL D.458.3mL
2.家用食醋是含醋酸质量分数为10%的水溶液,其中的“10%”的含义是( )
A.100 g醋酸中含醋为10 g B.100 g醋酸的水溶液中含醋酸10g
C.100 g水中含醋酸为10g D.100 g醋酸的水溶液中含水10g
3.KNO3 的溶解度曲线如下图所示。下列说法错误的是( )
A.0~60℃,KNO3 的溶解度随温度升高而增大
B.60℃时的 KNO3 饱和溶液降温至 20℃,有晶体析出
C.20℃,100g 水中最多能溶解 31.6g KNO3
D.60℃时,可配制溶质质量分数为 60%的 KNO3 溶液
4.将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )
A.甲的溶解度随温度升高而增大
B.t1℃时,甲、乙的溶解度均为20g
C.温度由t2℃降低到t1℃时,甲溶液析出5g固体
D.a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b
5.现有100mL 20%的硫酸,其密度为1.14g/cm3,下列说法正确的是( )
A.该溶液含溶质20 g
B.该溶液中,溶质质量:溶液质量=1:6
C.该溶液中,溶质质量:溶剂质量=1:5
D.该溶液中,溶液质量:溶剂质量=5:4
6.关于如图所示实验的相关判断错误的是( )
A.固体X可能是NaOH B.固体X可能是NH4NO3
C.Ca(OH)2溶解度:①>② D.Ca(OH)2质量分数:①=③
7.下面所示的四个图像,能正确反映对应变化关系的是
A.镁在氧气中燃烧
B.向二氧化锰中加入过氧化氢溶液
C.向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液
D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
8.将50g 98%的浓硫酸溶于200g水中,所得溶液中溶质的质量分数为
A.9.8% B.10.2% C.10.8% D.19.6%
9.向l00g10%NaOH溶液中加入12.5gNaOH固体,完全溶解后.所得溶液中溶质质量分数为
A.12. 5% B.20.0% C.22.5% D.25%
10.在温度不变的条件下,下列欲使溶质的质量分数变为原来2倍的方法,最可行的是( )
A.将20 g硝酸钾饱和溶液蒸发掉10 g水
B.将20 g硝酸钾不饱和溶液蒸发掉10 g水
C.在10 g 10%的硝酸钾溶液中加入5 g 40%的硝酸钾溶液
D.在10 g硝酸钾不饱和溶液中加入10 g硝酸钾固体
11.实验室用氯化钠和水配制50g质量分数为6%的氯化钠溶液。下列说法正确的是( )
A.实验步骤:计算、量取、溶解、装瓶、贴签
B.量取水时,用规格为50mL的量筒
C.实验过程中玻璃棒搅拌的作用是散热
D.若在量取水时俯视读数量取,则配制溶液的溶质质量分数小于6%
12.如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
A.t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.t2℃时,将50ga物质(不含结晶水)放入100g水中充分溶解得到a的饱和溶液
C.将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D.将c的饱和溶液变为不饱和溶液,可采用降温的方法
13.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是
A.甲和丙的溶解度相等
B.在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质量为78g
C.t2℃时,等质量的甲、乙、丙三种固体配制成饱和溶液所需溶剂质量的大小关系是甲<乙<丙
D.将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是甲>乙>丙
14.保持温度不变,小心蒸发NaCl不饱和溶液(蒸发皿中始终有溶液),则溶液中溶质的质量分数(m%)与时间(t)的关系合理的是
A. B. C. D.
15.如图是采用膜分离技术的海水淡化装置,对海水加压后,只有水分子可以通过淡化膜,离子等其他粒子不能通过淡化膜.加压后,装置右侧海水中增加的是( )
A.溶质质量分数 B.溶剂质量
C.溶液质量 D.溶质质量
16.下列关于溶液的说法正确的是
A.溶液一定是无色透明的
B.溶液一定是均一的、稳定的混合物
C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
D.将40g溶质质量分数为20%的氯化钠溶液倒出20g,剩余溶液溶质质量分数为10%
二、综合应用题
17.水是宝贵的自然资料,让我们一起走进“水”的世界。
①下图电解水实验中,反应的化学方程式是___。水电解过程发生改变的微粒名称是______。
②医疗上常用0.9%NaCl溶液作生理盐水,配制1000g生理盐水需要氯化钠固体的质量为_______还可以制取碳酸饮料,该过程中发生反应的化学方程式为_____________。
③某化学兴趣小组欲进行粗盐的初步提纯。粗盐的提纯实验步骤包括:a计算产率,b过滤,c溶解,d蒸发,e称量。实验步骤的正确顺序是:e、_________、a(填序号)。若NaCl的产率偏低,则可能的原因是_________(填字母)。
A.过滤时滤纸有破损B.蒸发后所得精盐未完全蒸干,含有水
C.溶解含泥沙的粗食盐时,加入的水量不足
提示:产率=×100%
④已知KCl的溶解度20℃时为34g/100g水,40℃时为40g/100g水。某实验小组做了如下实验。
A中所得溶液中溶质与溶剂的质量比为__________;溶质的质量分数相等的是___________。
I. B和CII. B和EⅢ. C和DIV. D和E
18.某化学兴趣小组为测定一定量生铁样品(样品中的其他成分不参加反应,也不溶于水)中铁的质量,并得到纯净的一定浓度的硫酸亚铁溶液。进行了如下实验
注:反应①结束后,所加稀硫酸刚好反应一半,反应②恰好完全反应。
请回答下列问题:
(1) 写出发生反应的化学方程式____________________________________。
(2) 根据已知条件列出求解①中参加反应的铁的质量(X)的比例式_________。
(3)该生铁样品中铁的质量为___________;
(4) 若最终得到的滤液为不饱和溶液,则所得滤液中溶质的质量分数为_______。
(5)若用98%的浓硫酸配制上述实验所用的稀硫酸,需加水的质量为_________。
19.在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如下图所示,甲、丙还有剩余固体,乙固体全部溶解。升温到80 ℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化。
(1)室温时,________(选填“甲”、“乙”或“丙”)溶液可能是不饱和溶液。
(2)上图中能表示乙物质的溶解度曲线的是____________(填“a”、“b”或“c”,下同),
(3)t2 ℃时,甲、乙、丙三种物质的等质量的饱和溶液降到t1 ℃时,所得溶液中水的质量由大到小的顺序是_______________________
(4)小强同学要在实验室配制15%的氯化钠溶液50 g。需要量筒规格为__________ml(填“20或50或100”),该同学按下图所示步骤依次操作:
按B量取所需的水配得的溶液溶质质量分数____________(填“偏大或偏小或无影响”);E中玻璃棒的作用是__________________。若上图A中砝码的质量为5 g,游码为2.5 g,则称得氯化钠的质量____________克
20.溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①时,A、B、C三种物质的溶解度由大到小的顺序是 _____ 。
②A、B、C三种物质中,溶解度随温度升高而减小的是 _____ 。
③时,完全溶解ag A物质最少需要水的质量是 _____ g。
④时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量 _____ B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、 _____ 和滤纸。
(3)在实验室中,配制溶质质量分数为的氯化钠溶液45g,需要氯化钠固体的质量是 _____ g。将的氯化钠溶液配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是 _____ g。
21.如表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃),回答下列问题:
溶液中溶质的质量分数/% 4 12 16 24 28
硫酸溶液的密度/g·mL-1 1.02 1.08 1.11 1.17 1.20
氨水的密度/g·mL-1 0.98 0.95 0.94 0.91 0.90
(1)20℃时,随着溶液中溶质质量分数逐渐增大,氨水的密度逐渐_____(填“增大”、“减小”或“不变”)。
(2)取12%的硫酸溶液100mL,可配制成6%的硫酸溶液_____g。
(3)向100g24%的氨水中加入100g水,摇匀,所得溶液体积是_____mL(结果精确到0.1)。
(4)配制溶质质量分数4%的硫酸溶液50mL,需要溶质质量分数24%的硫酸溶液多少毫升?(写出计算过程,结果精确到0.1)
22.在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如下图所示。请计算:
(1)完全反应时,生成氧气的质量为________克。
(2)完全反应后,剩余固体物质是_________(填化学式)。
(3)完全反应后,把剩余固体倒入100g蒸馏水中,充分溶解,求所得溶液中溶质的质量分数为_____________(最后结果保留0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.D
5.D
6.B
7.B
8.D
9.B
10.C
11.B
12.C
13.C
14.A
15.A
16.B
17. 2H2O2H2↑+O2↑ 水分子 9 CO2+H2O=H2CO3 c、b、d、e C 25:100(1:4) II、Ⅲ
18. Fe+ H2SO4= Fe SO4+ H2↑ 56/2==X/0.8g 22.4g 25% 320g
19. 乙 C c>b>a 50、 偏小、 搅拌,加快氯化钠溶解速率 , 2.5
20. CBA .C 100 小于 漏斗 4.5 500
21.(1)减小
(2)216
(3)210.5
(4)设需要溶质质量分数24%的硫酸溶液的质量为。
需要溶质质量分数24%的硫酸溶液的体积为:
答:需要溶质质量分数24%的硫酸溶液7.3mL。
22.(1)9.6g (2)KCl和MnO2(3)13.0%
答案第1页,共2页
答案第1页,共2页
