7.4结晶现象 同步测试——2021-2022学年粤教版九年级下册(Word版 含答案)
文档属性
| 名称 | 7.4结晶现象 同步测试——2021-2022学年粤教版九年级下册(Word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 115.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-20 00:00:00 | ||
图片预览



文档简介
7.4 结晶现象
一、单选题
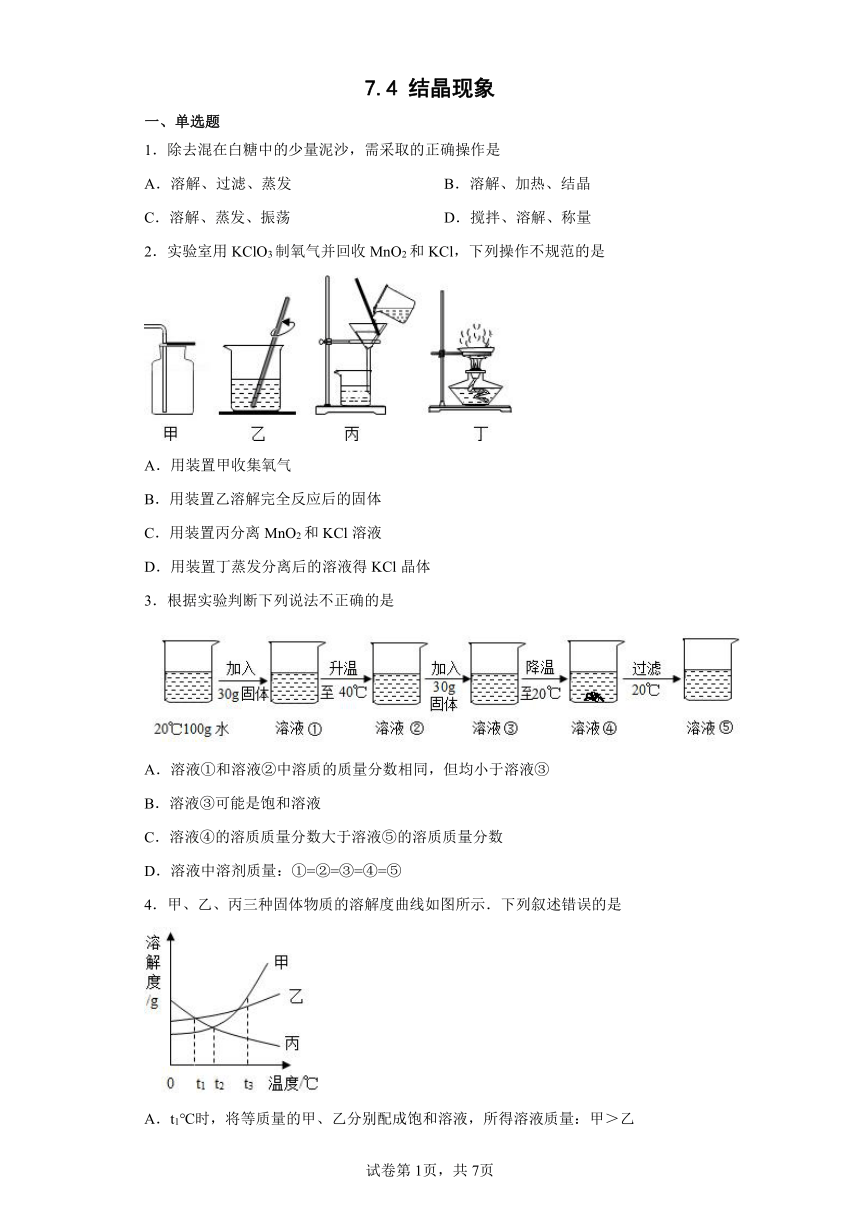
1.除去混在白糖中的少量泥沙,需采取的正确操作是
A.溶解、过滤、蒸发 B.溶解、加热、结晶
C.溶解、蒸发、振荡 D.搅拌、溶解、称量
2.实验室用KClO3制氧气并回收MnO2和KCl,下列操作不规范的是
A.用装置甲收集氧气
B.用装置乙溶解完全反应后的固体
C.用装置丙分离MnO2和KCl溶液
D.用装置丁蒸发分离后的溶液得KCl晶体
3.根据实验判断下列说法不正确的是
A.溶液①和溶液②中溶质的质量分数相同,但均小于溶液③
B.溶液③可能是饱和溶液
C.溶液④的溶质质量分数大于溶液⑤的溶质质量分数
D.溶液中溶剂质量:①=②=③=④=⑤
4.甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是
A.t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙
B.将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等
C.将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法
D.将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙
5.下列哪种方法不可能用于分离饱和溶液中的溶质和溶剂
A.过滤 B.蒸发
C.蒸馏 D.结晶
6.下列有关溶液的说法正确的是
A.饱和溶液一定是浓溶液
B.溶液是均一、稳定的混合物
C.溶液蒸发溶剂,一定会析出晶体
D.不饱和溶液一定是稀溶液
7.如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
A.甲的溶解度等于乙的溶解度
B.升高温度可将甲的不饱和溶液变为饱和溶液
C.20℃时,100g乙的饱和溶液中溶质质量是30g
D.40℃时,分别用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
8.如图是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.升高温度可使接近饱和的甲溶液变成饱和溶液
C.10℃时,甲、乙两种溶液的溶质质量分数一定相等
D.甲中含有少量乙,可以用冷却热饱和溶液的方法提纯甲
9.下列是某同学进行过滤操作时的一些做法,其中错误的是( )
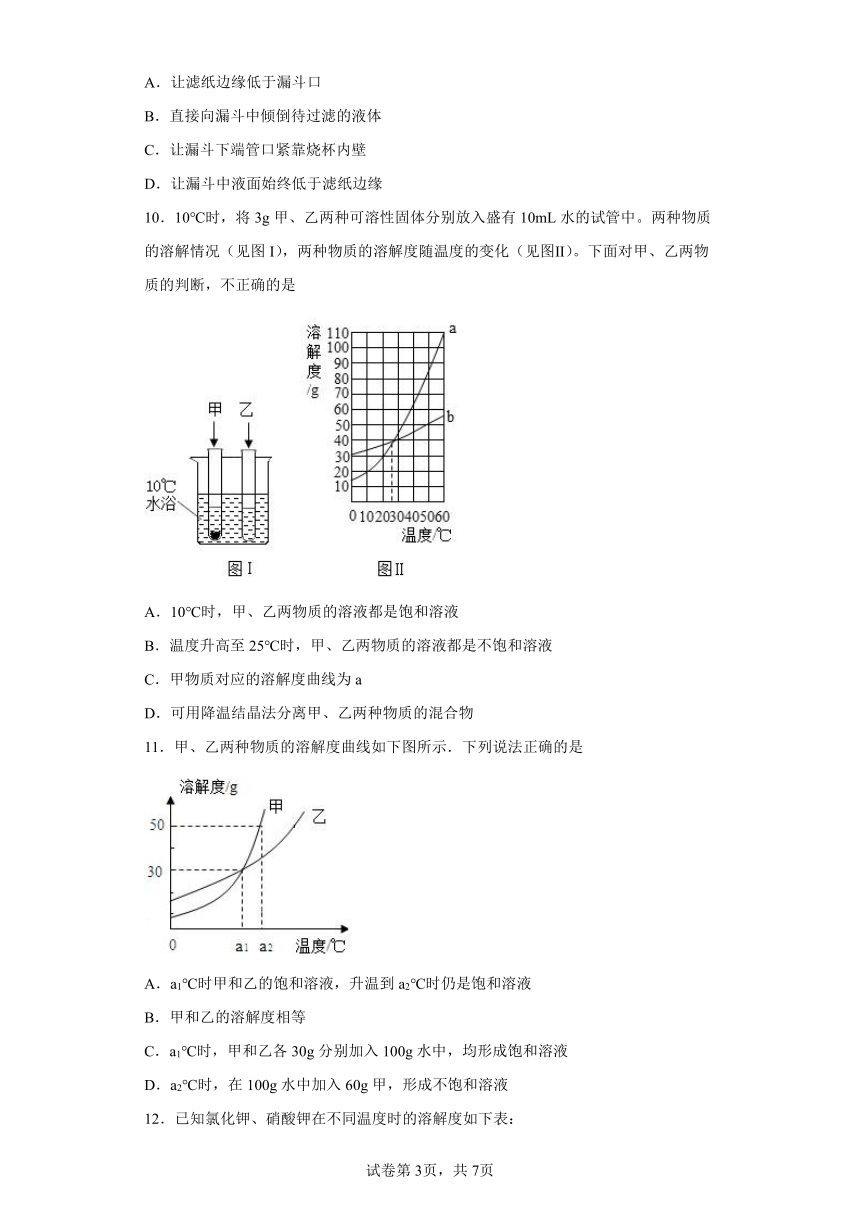
A.让滤纸边缘低于漏斗口
B.直接向漏斗中倾倒待过滤的液体
C.让漏斗下端管口紧靠烧杯内壁
D.让漏斗中液面始终低于滤纸边缘
10.10℃时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况(见图I),两种物质的溶解度随温度的变化(见图Ⅱ)。下面对甲、乙两物质的判断,不正确的是
A.10℃时,甲、乙两物质的溶液都是饱和溶液
B.温度升高至25℃时,甲、乙两物质的溶液都是不饱和溶液
C.甲物质对应的溶解度曲线为a
D.可用降温结晶法分离甲、乙两种物质的混合物
11.甲、乙两种物质的溶解度曲线如下图所示.下列说法正确的是
A.a1℃时甲和乙的饱和溶液,升温到a2℃时仍是饱和溶液
B.甲和乙的溶解度相等
C.a1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液
D.a2℃时,在100g水中加入60g甲,形成不饱和溶液
12.已知氯化钾、硝酸钾在不同温度时的溶解度如下表:
温度/℃ 0 20 40 60
溶解度/g 氯化钾 27.6 34.0 40.0 45.5
硝酸钾 13.3 31.6 63.9 110.0
依据上表数据和溶解度曲线判断,下列说法错误的是A.能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙
B.t1℃时,氯化钾和硝酸钾的溶解度相等,在 34.0 g 至 35.0 g 之间
C.t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液
D.氯化钾中混有少量的硝酸钾,可采用降温结晶的方法提纯
二、填空题
13.下图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
(1)M点表示的含义是_______ 。
(2)50℃时,将40g甲物质加入50g水中,充分溶解后,所形成的溶液中溶质与溶剂的质量比为_______ 。
(3)20℃时,处于a点状态的甲溶液,升温至50℃时,所得溶液中溶质质量分数_______(填“变大”、“变小”或“不变”)
(4)除去甲中混有的少量乙,步骤是:加水溶解、加热浓缩、_______、过滤、洗涤、干燥。
(5)分别将50℃甲、乙、丙三种物质的饱和溶液100g降温到20℃时,下列关于所得溶液的说法正确的有
A.溶液质量:丙>乙>甲
B.溶剂质量:乙>甲=丙
C.溶质质量分数:乙>甲>丙
14.某兴趣小组欲在实验室对一瓶浑浊的河水进行净化,其流程如下:
(1)操作①中物质A可以是________。
(2)操作②所需的玻璃仪器除烧杯外,还有________。
(3)消毒剂ClO2读作________。
(4)操作①~④中,单一净化程度最高的是________(填操作名称)。
15.从物质的溶解度曲线中,可以获得很多信息。甲、乙两种固体物质的溶解度曲线如图所示。
(1)t1℃时,甲、乙两种物质的溶解度_______(填“相等”或“不相等”)。
(2)两种物质中,_______的溶解度受温度的影响较大。
(3)要使接近饱和的乙溶液变成饱和溶液,可采用的方法有_______(写一种即可)。
三、综合应用题
16.某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费。初三(2)班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理。
(1)复习常见金属活动顺序表,在下表空格中分别填入对应的元素符号。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg _____ Pt Au
金属活动性由强到弱
(2)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:
①废水在加入金属X前需进行过滤,目的是将其中_________性杂质除去。进行过滤的操作所需的仪器有:_____________(请从下图中选择合适仪器,并用仪器序号填写)。
②金属X是_______,其加入废水后发生反应的化学方程式为_______________________;
溶液Y是_______,利用其除去铜中杂质,有关反应的化学方程式为________
17.小小同学从太阳山水库中取出浑浊水祥进行实验。
(1)将水样静置,用如图所示装置进行过滤,其操作规范的是___________(填字母)。
A.用玻璃棒引流
B.滤纸边缘高出漏斗口
C.漏斗下端管口颈尖靠紧烧杯内壁
D.将滤纸湿润,使其紧贴漏斗内壁,中间不要留有气泡
E.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(2)向过滤后所得水样中加入一定量活性炭利用活性炭的___________性除去杂质和臭味。
(3)在处理后的水样中加入一定量肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该水样属于___________(填“硬水”或“软水”)
(4)生活中常用___________(填“煮沸”“静置沉淀”或“过滤”)的方法降低水的硬度,并起到消毒杀菌的作用。
(5)为了人类的生存和发展,人类必须节约水资源,爱惜水资源。下列做法有利于节约保护水资源的是___________(填序号)
A.生活污水直接排放 B.工业上冷却水重复利用
C.园林浇灌用滴灌、喷灌 D.提倡使用节水器具
18.(1)在过滤操作中,图中还缺少的一种仪器是__________,其作用是______________;
(2)过滤时漏斗下端管口应________,漏斗中液面应______滤纸边缘。若过滤后滤液仍然浑浊,应该___________________。出现浑浊的可能原因是__________________________。
(3)蒸发过程中,等到蒸发皿中出现____________时,停止加热,利用蒸发皿的余热使滤液蒸干。
(4)现有A、B、C、D四种物质,A是无色无味的气体;B在A中燃烧发出明亮的蓝紫色火焰,同时生成一种无色有刺激性气味的气体C;D是一种无色的气体,把D通入澄清的石灰水中,石灰水变浑浊。试判断A、B、C、D是什么物质,请将答案填在空格内。
A_________________ B_________________ C _______________ D_______________
(5)写出下列反应的文字(或符号)表达式,并指出是分解反应还是化合反应。
①过氧化氢在二氧化锰的催化下制氧气 :_____________( )
②燃烧硫磺: _____________( )
③燃烧红磷: _____________________ ( )
④铁丝在氧气中燃烧 :_______________( )
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.C
4.B
5.A
6.B
7.D
8.D
9.B
10.A
11.C
12.D
13.(1)50℃时,甲、乙溶解度相同都为40g
(2)2:5
(3)不变
(4)降温结晶
(5)AC
14.(1)明矾
(2)漏斗、玻璃棒
(3)二氧化氯
(4)蒸馏
15. 相等 甲
增加溶质或恒温蒸发溶剂
16. Ag 不溶 ADE Fe##铁 Fe+CuSO4=FeSO4+Cu 稀硫酸 Fe+H2SO4=FeSO4+H2↑
17.(1)ACD
(2)吸附性
(3)硬水
(4)煮沸
(5)BCD
18. 玻璃棒 引流 紧贴烧杯内壁 低于 再过滤一次 滤纸损坏或液面高于滤纸边缘或仪器不干净 大量固体 氧气(O2) 硫(S) 二氧化硫(SO2) 二氧化碳(CO2) H2O2 H2O + O2 (分解反应) S+O2SO2 (化合反应) P+O2 P2O5 (化合反应) Fe+O2Fe3O4 (化合反应)
答案第1页,共2页
答案第1页,共2页
一、单选题
1.除去混在白糖中的少量泥沙,需采取的正确操作是
A.溶解、过滤、蒸发 B.溶解、加热、结晶
C.溶解、蒸发、振荡 D.搅拌、溶解、称量
2.实验室用KClO3制氧气并回收MnO2和KCl,下列操作不规范的是
A.用装置甲收集氧气
B.用装置乙溶解完全反应后的固体
C.用装置丙分离MnO2和KCl溶液
D.用装置丁蒸发分离后的溶液得KCl晶体
3.根据实验判断下列说法不正确的是
A.溶液①和溶液②中溶质的质量分数相同,但均小于溶液③
B.溶液③可能是饱和溶液
C.溶液④的溶质质量分数大于溶液⑤的溶质质量分数
D.溶液中溶剂质量:①=②=③=④=⑤
4.甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是
A.t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙
B.将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等
C.将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法
D.将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙
5.下列哪种方法不可能用于分离饱和溶液中的溶质和溶剂
A.过滤 B.蒸发
C.蒸馏 D.结晶
6.下列有关溶液的说法正确的是
A.饱和溶液一定是浓溶液
B.溶液是均一、稳定的混合物
C.溶液蒸发溶剂,一定会析出晶体
D.不饱和溶液一定是稀溶液
7.如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
A.甲的溶解度等于乙的溶解度
B.升高温度可将甲的不饱和溶液变为饱和溶液
C.20℃时,100g乙的饱和溶液中溶质质量是30g
D.40℃时,分别用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
8.如图是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.升高温度可使接近饱和的甲溶液变成饱和溶液
C.10℃时,甲、乙两种溶液的溶质质量分数一定相等
D.甲中含有少量乙,可以用冷却热饱和溶液的方法提纯甲
9.下列是某同学进行过滤操作时的一些做法,其中错误的是( )
A.让滤纸边缘低于漏斗口
B.直接向漏斗中倾倒待过滤的液体
C.让漏斗下端管口紧靠烧杯内壁
D.让漏斗中液面始终低于滤纸边缘
10.10℃时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况(见图I),两种物质的溶解度随温度的变化(见图Ⅱ)。下面对甲、乙两物质的判断,不正确的是
A.10℃时,甲、乙两物质的溶液都是饱和溶液
B.温度升高至25℃时,甲、乙两物质的溶液都是不饱和溶液
C.甲物质对应的溶解度曲线为a
D.可用降温结晶法分离甲、乙两种物质的混合物
11.甲、乙两种物质的溶解度曲线如下图所示.下列说法正确的是
A.a1℃时甲和乙的饱和溶液,升温到a2℃时仍是饱和溶液
B.甲和乙的溶解度相等
C.a1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液
D.a2℃时,在100g水中加入60g甲,形成不饱和溶液
12.已知氯化钾、硝酸钾在不同温度时的溶解度如下表:
温度/℃ 0 20 40 60
溶解度/g 氯化钾 27.6 34.0 40.0 45.5
硝酸钾 13.3 31.6 63.9 110.0
依据上表数据和溶解度曲线判断,下列说法错误的是A.能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙
B.t1℃时,氯化钾和硝酸钾的溶解度相等,在 34.0 g 至 35.0 g 之间
C.t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液
D.氯化钾中混有少量的硝酸钾,可采用降温结晶的方法提纯
二、填空题
13.下图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
(1)M点表示的含义是_______ 。
(2)50℃时,将40g甲物质加入50g水中,充分溶解后,所形成的溶液中溶质与溶剂的质量比为_______ 。
(3)20℃时,处于a点状态的甲溶液,升温至50℃时,所得溶液中溶质质量分数_______(填“变大”、“变小”或“不变”)
(4)除去甲中混有的少量乙,步骤是:加水溶解、加热浓缩、_______、过滤、洗涤、干燥。
(5)分别将50℃甲、乙、丙三种物质的饱和溶液100g降温到20℃时,下列关于所得溶液的说法正确的有
A.溶液质量:丙>乙>甲
B.溶剂质量:乙>甲=丙
C.溶质质量分数:乙>甲>丙
14.某兴趣小组欲在实验室对一瓶浑浊的河水进行净化,其流程如下:
(1)操作①中物质A可以是________。
(2)操作②所需的玻璃仪器除烧杯外,还有________。
(3)消毒剂ClO2读作________。
(4)操作①~④中,单一净化程度最高的是________(填操作名称)。
15.从物质的溶解度曲线中,可以获得很多信息。甲、乙两种固体物质的溶解度曲线如图所示。
(1)t1℃时,甲、乙两种物质的溶解度_______(填“相等”或“不相等”)。
(2)两种物质中,_______的溶解度受温度的影响较大。
(3)要使接近饱和的乙溶液变成饱和溶液,可采用的方法有_______(写一种即可)。
三、综合应用题
16.某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费。初三(2)班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理。
(1)复习常见金属活动顺序表,在下表空格中分别填入对应的元素符号。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg _____ Pt Au
金属活动性由强到弱
(2)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:
①废水在加入金属X前需进行过滤,目的是将其中_________性杂质除去。进行过滤的操作所需的仪器有:_____________(请从下图中选择合适仪器,并用仪器序号填写)。
②金属X是_______,其加入废水后发生反应的化学方程式为_______________________;
溶液Y是_______,利用其除去铜中杂质,有关反应的化学方程式为________
17.小小同学从太阳山水库中取出浑浊水祥进行实验。
(1)将水样静置,用如图所示装置进行过滤,其操作规范的是___________(填字母)。
A.用玻璃棒引流
B.滤纸边缘高出漏斗口
C.漏斗下端管口颈尖靠紧烧杯内壁
D.将滤纸湿润,使其紧贴漏斗内壁,中间不要留有气泡
E.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(2)向过滤后所得水样中加入一定量活性炭利用活性炭的___________性除去杂质和臭味。
(3)在处理后的水样中加入一定量肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该水样属于___________(填“硬水”或“软水”)
(4)生活中常用___________(填“煮沸”“静置沉淀”或“过滤”)的方法降低水的硬度,并起到消毒杀菌的作用。
(5)为了人类的生存和发展,人类必须节约水资源,爱惜水资源。下列做法有利于节约保护水资源的是___________(填序号)
A.生活污水直接排放 B.工业上冷却水重复利用
C.园林浇灌用滴灌、喷灌 D.提倡使用节水器具
18.(1)在过滤操作中,图中还缺少的一种仪器是__________,其作用是______________;
(2)过滤时漏斗下端管口应________,漏斗中液面应______滤纸边缘。若过滤后滤液仍然浑浊,应该___________________。出现浑浊的可能原因是__________________________。
(3)蒸发过程中,等到蒸发皿中出现____________时,停止加热,利用蒸发皿的余热使滤液蒸干。
(4)现有A、B、C、D四种物质,A是无色无味的气体;B在A中燃烧发出明亮的蓝紫色火焰,同时生成一种无色有刺激性气味的气体C;D是一种无色的气体,把D通入澄清的石灰水中,石灰水变浑浊。试判断A、B、C、D是什么物质,请将答案填在空格内。
A_________________ B_________________ C _______________ D_______________
(5)写出下列反应的文字(或符号)表达式,并指出是分解反应还是化合反应。
①过氧化氢在二氧化锰的催化下制氧气 :_____________( )
②燃烧硫磺: _____________( )
③燃烧红磷: _____________________ ( )
④铁丝在氧气中燃烧 :_______________( )
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.C
4.B
5.A
6.B
7.D
8.D
9.B
10.A
11.C
12.D
13.(1)50℃时,甲、乙溶解度相同都为40g
(2)2:5
(3)不变
(4)降温结晶
(5)AC
14.(1)明矾
(2)漏斗、玻璃棒
(3)二氧化氯
(4)蒸馏
15. 相等 甲
增加溶质或恒温蒸发溶剂
16. Ag 不溶 ADE Fe##铁 Fe+CuSO4=FeSO4+Cu 稀硫酸 Fe+H2SO4=FeSO4+H2↑
17.(1)ACD
(2)吸附性
(3)硬水
(4)煮沸
(5)BCD
18. 玻璃棒 引流 紧贴烧杯内壁 低于 再过滤一次 滤纸损坏或液面高于滤纸边缘或仪器不干净 大量固体 氧气(O2) 硫(S) 二氧化硫(SO2) 二氧化碳(CO2) H2O2 H2O + O2 (分解反应) S+O2SO2 (化合反应) P+O2 P2O5 (化合反应) Fe+O2Fe3O4 (化合反应)
答案第1页,共2页
答案第1页,共2页
