第八单元海水中的化学测试题 -2021-2022学年九年级化学鲁教版下册(word版有答案)
文档属性
| 名称 | 第八单元海水中的化学测试题 -2021-2022学年九年级化学鲁教版下册(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 189.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-20 00:00:00 | ||
图片预览


文档简介
第八单元《海水中的化学》测试题
一、单选题
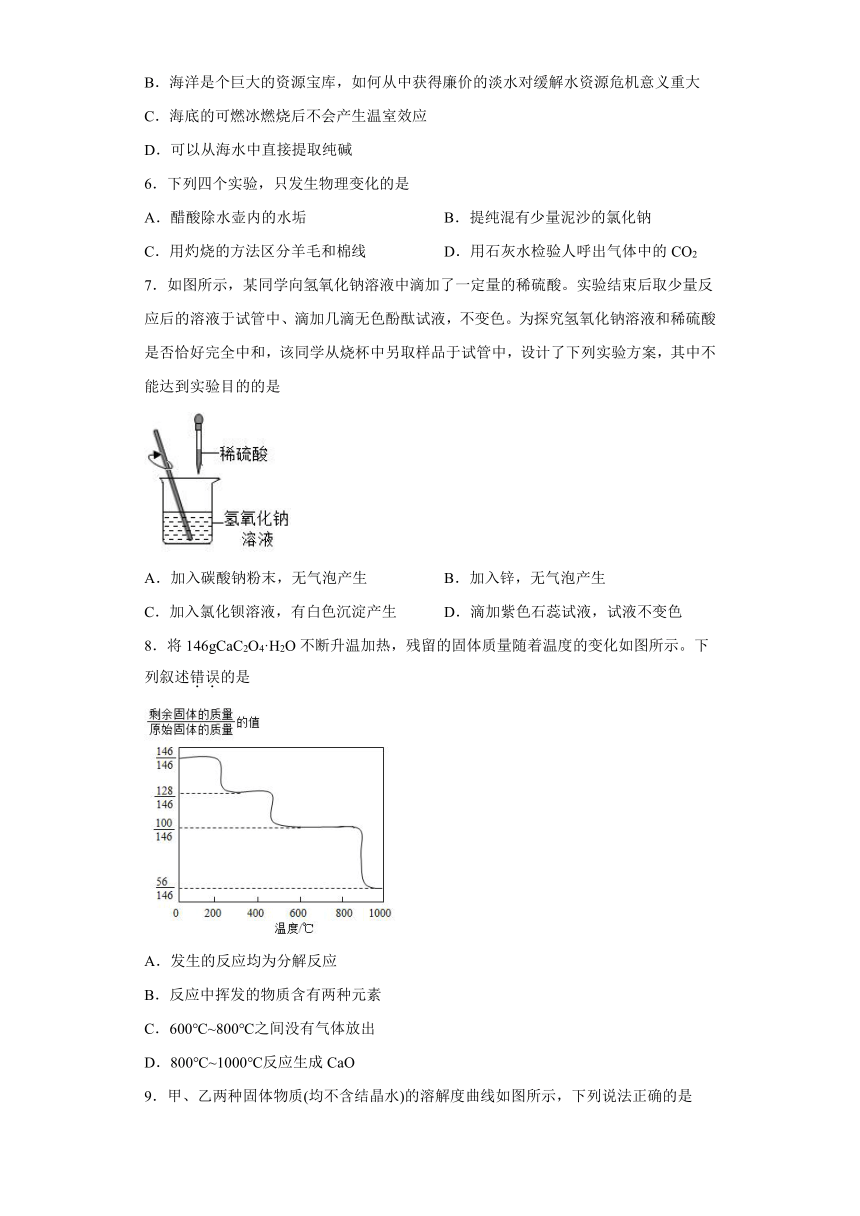
1.如图为两种物质的溶解度曲线,下列说法正确的是
A.两种物质的溶解度都随温度升高而增大
B.20℃时,Na2Cr2O7饱和溶液的溶质质量分数为80%
C.60℃时,Na2SO4的溶解度大于 Na2Cr2O7的溶解度
D.可以配制溶质质量分数相同的 Na2Cr2O7、Na2SO4溶液
2.下列物质属于混合物的是
A.消石灰 B.石灰石 C.苛性钠 D.苏打
3.下列物质的俗称、化学式和分类完全正确的是
A.苏打、NaHCO3,盐 B.烧碱、NaOH、碱
C.生石灰、Ca(OH)2、氧化物 D.水银、、单质
4.甲、乙两物质的溶解度曲线如图所示。下列说法正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.20℃时,甲、乙两物质的饱和溶液中溶质的质量相等
C.甲物质的溶解度受温度的影响比乙大
D.将t℃时的甲、乙两种物质的饱和溶液降温至20℃时,都会析出晶体
5.下列对于海洋开发利用的说法,正确的是
A.海水 “晒盐”得到的是纯净食盐
B.海洋是个巨大的资源宝库,如何从中获得廉价的淡水对缓解水资源危机意义重大
C.海底的可燃冰燃烧后不会产生温室效应
D.可以从海水中直接提取纯碱
6.下列四个实验,只发生物理变化的是
A.醋酸除水壶内的水垢 B.提纯混有少量泥沙的氯化钠
C.用灼烧的方法区分羊毛和棉线 D.用石灰水检验人呼出气体中的CO2
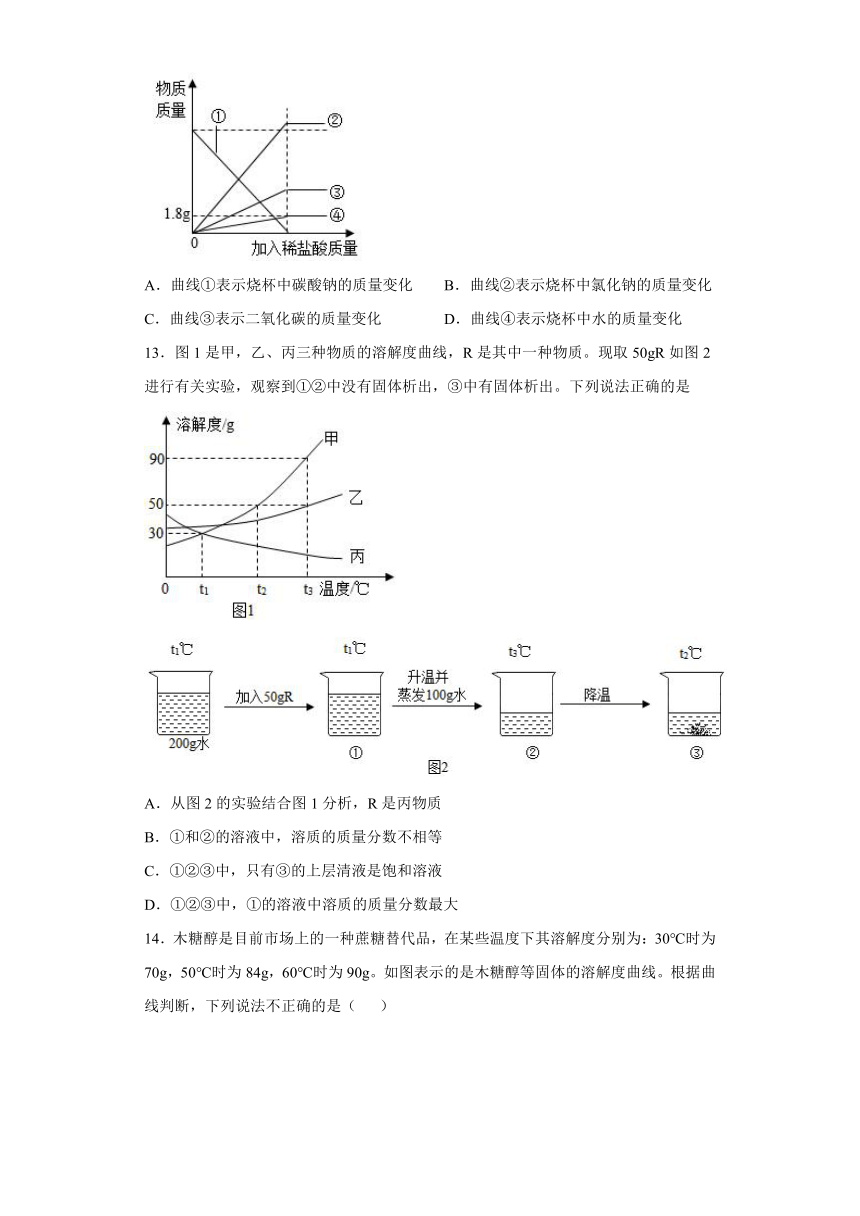
7.如图所示,某同学向氢氧化钠溶液中滴加了一定量的稀硫酸。实验结束后取少量反应后的溶液于试管中、滴加几滴无色酚酞试液,不变色。为探究氢氧化钠溶液和稀硫酸是否恰好完全中和,该同学从烧杯中另取样品于试管中,设计了下列实验方案,其中不能达到实验目的的是
A.加入碳酸钠粉末,无气泡产生 B.加入锌,无气泡产生
C.加入氯化钡溶液,有白色沉淀产生 D.滴加紫色石蕊试液,试液不变色
8.将146gCaC2O4·H2O不断升温加热,残留的固体质量随着温度的变化如图所示。下列叙述错误的是
A.发生的反应均为分解反应
B.反应中挥发的物质含有两种元素
C.600℃~800℃之间没有气体放出
D.800℃~1000℃反应生成CaO
9.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是
A.甲、乙物质都适用降温结晶法使溶质从溶液中析出
B.60℃时将40g甲物质加入50g水中能得到90g饱和溶液
C.通过升温能使A点甲的不饱和溶液变为饱和溶液
D.40℃时,甲、乙两物质的饱和溶液中,溶质质量分数相等
10.下列实验方案不能达到实验目的的是
选项 实验目的 实验方案
A 验证浓硫酸具有脱水性 用玻璃棒蘸取少量浓硫酸滴在纸片上
B 区分和N2两种气体 分别向盛有气体的集气瓶中伸入燃着木条
C 鉴别和溶液 分别滴入溶液
D 除去固体中的少量 加入足量的稀HCl,充分反应后蒸发
A.A B.B C.C D.D
11.氢氧化钠在生产和生活中的用途很广,能与多种物质发生反应。下列物质能与氢氧化钠溶液反应且观察到白色沉淀的是
A.B.C. D.
12.一烧杯中盛有10.6g碳酸钠粉末,向其中逐滴加入稀盐酸,该反应中有关物质质量与加入稀盐酸质量之间的关系如图所示,下列说法错误的是
A.曲线①表示烧杯中碳酸钠的质量变化 B.曲线②表示烧杯中氯化钠的质量变化
C.曲线③表示二氧化碳的质量变化 D.曲线④表示烧杯中水的质量变化
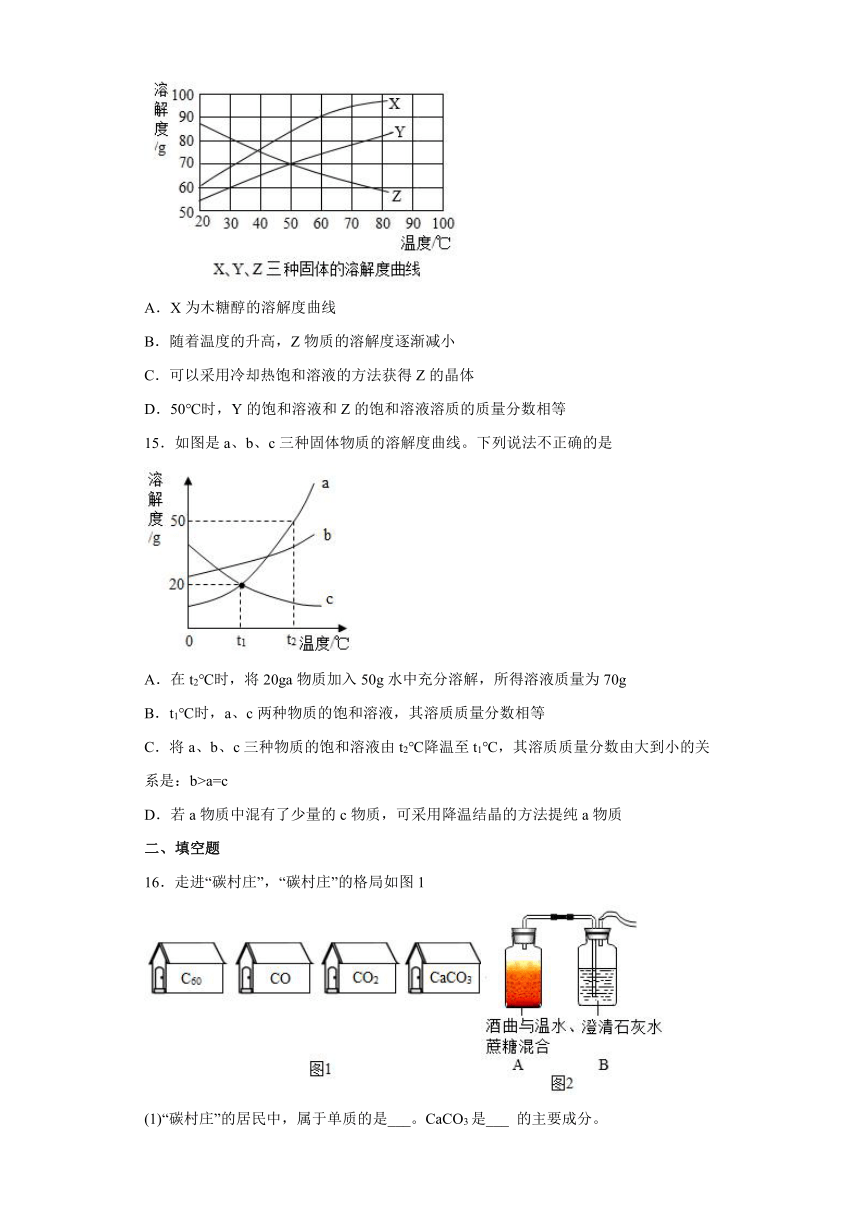
13.图1是甲,乙、丙三种物质的溶解度曲线,R是其中一种物质。现取50gR如图2进行有关实验,观察到①②中没有固体析出,③中有固体析出。下列说法正确的是
A.从图2的实验结合图1分析,R是丙物质
B.①和②的溶液中,溶质的质量分数不相等
C.①②③中,只有③的上层清液是饱和溶液
D.①②③中,①的溶液中溶质的质量分数最大
14.木糖醇是目前市场上的一种蔗糖替代品,在某些温度下其溶解度分别为:30℃时为70g,50℃时为84g,60℃时为90g。如图表示的是木糖醇等固体的溶解度曲线。根据曲线判断,下列说法不正确的是( )
A.X为木糖醇的溶解度曲线
B.随着温度的升高,Z物质的溶解度逐渐减小
C.可以采用冷却热饱和溶液的方法获得Z的晶体
D.50℃时,Y的饱和溶液和Z的饱和溶液溶质的质量分数相等
15.如图是a、b、c三种固体物质的溶解度曲线。下列说法不正确的是
A.在t2℃时,将20ga物质加入50g水中充分溶解,所得溶液质量为70g
B.t1℃时,a、c两种物质的饱和溶液,其溶质质量分数相等
C.将a、b、c三种物质的饱和溶液由t2℃降温至t1℃,其溶质质量分数由大到小的关系是:b>a=c
D.若a物质中混有了少量的c物质,可采用降温结晶的方法提纯a物质
二、填空题
16.走进“碳村庄”,“碳村庄”的格局如图1
(1)“碳村庄”的居民中,属于单质的是___。CaCO3是___ 的主要成分。
(2)“碳村庄”中的部分居民可以相互转化,写出通过化合反应将CO转化为CO2和CO2转化为CO的化学方程式________。
(3)“碳村庄”又来了一位新成员——蔗糖(C12H22O11),它在酒曲的催化下,经过发酵过程可以转变成酒精和二氧化碳。如图2所示。可以说明该反应已经发生的现象是______,B中相应反应的化学方程式为___。
17.化学源于生活,生活中蕴含着许多化学知识。
(1)生活用水有硬水和软水之分,化学课上用______来区分。
(2)我们的生活用水多是硬水,生活中常用______的方法降低水的硬度。
(3)打开的薯片放一个晚上就变得不脆了,说明空气中含有______。
(4)防毒面具是利用了活性炭具有______的性质。
(5)打开汽水瓶盖时,汽水瓶内会产生一个个小气泡,该气泡是______气体。
(6)打火机的主要部件是打火石和贮气箱,按下开关时,打火石发出电火花,引燃贮气箱释放的燃气,根据燃烧的条件分析,打火石的作用是______。
18.化学就在我们身边,它能改善我们的生活。请回答下列问题:
(1)打开汽水瓶盖能听到“嘶嘶”声,这说明气体的溶解能力和______有关。
(2)锌是人体不可缺少的一种元素。锌相对原子质量的国际新标准由张青莲教授主持测定。根据图示可知锌元素的相对原子质量为______,锌原子在化学反应中容易______(选填“得到”或“失去”)电子。
19.如图是五种化合物常温在溶液中两两之间发生的某些转化关系图,图中的“→”表示由某种物质可通过一步反应直接转化为另一种物质(部分反应物、生成物略去)。回答问题。
(1)①NaCl→NaNO3:____________。
②NaOH→NaCl:____________。
③Na2SO4→NaCl:____________。
④以上三个反应的转化是:酸、碱、盐在水溶液中发生的都是_________(填基本反应类型);这类反应实质上是_______的过程。
(2)在图中物质间转化关系中有的可以逆向转化它们分别是①_______→_______②_______→_______。
20.下列物质与人类生活密切相关,请选择相应的编号填空。
A.CH4 B.NaHCO3 C.Na2CO3 D.NaCI
(1)常用作调味品的是______。
(2)用于生产发酵粉的是______。
(3)用于生产洗涤剂的是______。
(4)“可燃冰”的主要成分是______。
三、推断题
21.甲、乙、丙、丁、戊是初中化学常见的物质,其中甲是一种常见气体,丁是大理石的主要成分,乙的固体俗称干冰,它们之间部分转化关系如图所示。(“→“表示某种物质经一步反应可转化成另一种物质,“一”表示两种物质能发生化学反应)
(1)戊的化学式为_____________。
(2)丙和戊发生的反应是__________(填“放热”或“吸热”)反应。
22.如图是初中化学中常见物质间的转化关系,其中A是氧化物,B是碱,C是单质,无色溶液中只含一种溶质,各物质间恰好完全反应(部分产物已略去)。请根据信息回答下列有关问题。
(1)无色溶液中含有的离子符号是___________。
(2)A物质的化学式为___________。
(3)黄色溶液和浅绿色溶液颜色不同的微观原因是___________。
(4)物质X在农业上还可用于改良酸性土壤,该物质的俗名为___________。
(5)上述溶液中,单独使用可鉴别稀硫酸和氢氧化钠溶液的有___________(填序号)。
A.无色溶液 B.红色溶液 C.黄色溶液 D.蓝色溶液
四、实验题
23.根据实验回答下列问题:
(1)下图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现象为浑浊→变红→红色消失。
根据实验现象判断氢氧化钙的性质有_____________、_____________(物理和化学性质各填一条)。
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是__________(填化学式),可能有的溶质是__________。(填化学式)
(3)上图2装置气密性良好。取0.2g碳酸钠于甲中,加入2mL稀硫酸,_____________(填实验操作),并将导管伸入澄清石灰水中,观察到出现浑浊。乙中反应的化学方程式为________________。
(4)上图中甲作为气体发生装置还可制得的气体是___________。(填名称)
24.根据下列实验回答问题。
实验一:炎热的夏天,在家中可以自制汽水来消暑解热。
【制备材料】1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500mL饮料瓶
【制备流程】
【问题讨论】
(1)步骤②中用凉开水制汽水的原因___________。
(2)制汽水时,利用了小苏打能与柠檬酸反应产生气体的性质,为证明柠檬酸溶液中有H+,可以选择下列物质中的 进行验证(填字母)·
A.镁带 B.铜片 C.食盐 D.鸡蛋壳(主要成分碳酸钙)
实验二:据《四川盐法治》记载,“敞锅熬盐”的主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,用木棒不断搅拌,析出粗盐;③用“花水”冲洗粗盐得精品盐。
(3)步骤②中,析出粗盐的过程,当________停止加热,木棒的作用是__________。
(4)步骤③中用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl。则“花水”应当是 (填字母)。
A.蒸馏水 B.饱和NaCl溶液 C.饱和NaOH溶液 D.饱和BaCl2溶液
五、计算题
25.请回答下列问题。
(1)积极应对气候变化,展现大国担当,中国向世界宣布了 2030 年前实现“碳达峰”、2060 年前实现“碳中和”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳 420 亿吨,在这些二氧化碳中含碳元素的质量为多少亿吨?(写出计算过程,计算结果精确至 0.1 亿吨)
(2)20℃时,向 3 个盛有 100 克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据,回答:
实验编号 A B C
加入氯化钠的质量(克) 20 36 50
溶液质量(克) 120 136 136
①实验所得 3 杯溶液中,属于不饱和溶液的是_______(填实验编号)。
②求溶液 C 的溶质质量分数_______。(写出计算过程,计算结果精确至 0.1%)。
26.鸡蛋壳的主要成分是CaCO3,现在取15g干燥的鸡蛋壳放入20g的烧杯中,向其中加入40g稀盐酸恰好完全反应(杂质不溶于水,且不与稀盐酸反应),反应后烧杯和物质的总质量为70.6g,计算鸡量中的CaCO3的质量分数是多少?(结果保留到0.1%)
参考答案:
1.D 2.B 3.B 4.C 5.B 6.B 7.C 8.B 9.D 10.B 11.C 12.D 13.B 14.C 15.C
16.(1) C60 大理石(或石灰石)
(2) ;
(3) 澄清石灰水变浑浊
17.(1)肥皂水
(2)煮沸
(3)水蒸气
(4)吸附性
(5)二氧化碳
(6)使温度达到燃气的着火点
18.(1)压强
(2) 65.38 失去
19.(1)
复分解反应 离子重新组合
(2) Na2SO4 NaOH Na2CO3 NaOH
20.(1)D
(2)B
(3)C
(4)A
21.(1)CaO
(2)放热
22.(1)H+、SO42-
(2)Fe2O3
(3)黄色溶液中含有Fe3+,浅绿色溶液中含有的是Fe2+
(4)熟石灰、消石灰
(5)BCD
23.(1) 微溶于水 能与稀盐酸反应(或能使酚酞试液变红)
(2) CaCl2 HCl
(3) 立即塞紧橡皮塞
(4)氧气(或氢气)
24.(1)CO2的溶解度随温度的降低而增大,凉开水温度低,溶解的CO2较多
(2)AD
(3) 敞口锅中出现较多量晶体 搅拌,防止液体因局部温度过高,造成液滴飞溅
(4)B
25.(1)解:二氧化碳中含碳元素的质量为:
答:二氧化碳中碳元素的质量为114.5亿吨。
(2) A 解:溶液 C 的溶质质量分数为:
答:溶液 C 的溶质质量分数为26.5%。
26.解:由质量守恒定律可知,生成二氧化碳的质量=15g+20g+40g 70.6g=4.4g
设鸡量中的CaCO3的质量为x
=
x=10g
鸡量中的CaCO3的质量分数=×100%≈66.7%
答:鸡量中的CaCO3的质量分数为66.7%。
一、单选题
1.如图为两种物质的溶解度曲线,下列说法正确的是
A.两种物质的溶解度都随温度升高而增大
B.20℃时,Na2Cr2O7饱和溶液的溶质质量分数为80%
C.60℃时,Na2SO4的溶解度大于 Na2Cr2O7的溶解度
D.可以配制溶质质量分数相同的 Na2Cr2O7、Na2SO4溶液
2.下列物质属于混合物的是
A.消石灰 B.石灰石 C.苛性钠 D.苏打
3.下列物质的俗称、化学式和分类完全正确的是
A.苏打、NaHCO3,盐 B.烧碱、NaOH、碱
C.生石灰、Ca(OH)2、氧化物 D.水银、、单质
4.甲、乙两物质的溶解度曲线如图所示。下列说法正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.20℃时,甲、乙两物质的饱和溶液中溶质的质量相等
C.甲物质的溶解度受温度的影响比乙大
D.将t℃时的甲、乙两种物质的饱和溶液降温至20℃时,都会析出晶体
5.下列对于海洋开发利用的说法,正确的是
A.海水 “晒盐”得到的是纯净食盐
B.海洋是个巨大的资源宝库,如何从中获得廉价的淡水对缓解水资源危机意义重大
C.海底的可燃冰燃烧后不会产生温室效应
D.可以从海水中直接提取纯碱
6.下列四个实验,只发生物理变化的是
A.醋酸除水壶内的水垢 B.提纯混有少量泥沙的氯化钠
C.用灼烧的方法区分羊毛和棉线 D.用石灰水检验人呼出气体中的CO2
7.如图所示,某同学向氢氧化钠溶液中滴加了一定量的稀硫酸。实验结束后取少量反应后的溶液于试管中、滴加几滴无色酚酞试液,不变色。为探究氢氧化钠溶液和稀硫酸是否恰好完全中和,该同学从烧杯中另取样品于试管中,设计了下列实验方案,其中不能达到实验目的的是
A.加入碳酸钠粉末,无气泡产生 B.加入锌,无气泡产生
C.加入氯化钡溶液,有白色沉淀产生 D.滴加紫色石蕊试液,试液不变色
8.将146gCaC2O4·H2O不断升温加热,残留的固体质量随着温度的变化如图所示。下列叙述错误的是
A.发生的反应均为分解反应
B.反应中挥发的物质含有两种元素
C.600℃~800℃之间没有气体放出
D.800℃~1000℃反应生成CaO
9.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是
A.甲、乙物质都适用降温结晶法使溶质从溶液中析出
B.60℃时将40g甲物质加入50g水中能得到90g饱和溶液
C.通过升温能使A点甲的不饱和溶液变为饱和溶液
D.40℃时,甲、乙两物质的饱和溶液中,溶质质量分数相等
10.下列实验方案不能达到实验目的的是
选项 实验目的 实验方案
A 验证浓硫酸具有脱水性 用玻璃棒蘸取少量浓硫酸滴在纸片上
B 区分和N2两种气体 分别向盛有气体的集气瓶中伸入燃着木条
C 鉴别和溶液 分别滴入溶液
D 除去固体中的少量 加入足量的稀HCl,充分反应后蒸发
A.A B.B C.C D.D
11.氢氧化钠在生产和生活中的用途很广,能与多种物质发生反应。下列物质能与氢氧化钠溶液反应且观察到白色沉淀的是
A.B.C. D.
12.一烧杯中盛有10.6g碳酸钠粉末,向其中逐滴加入稀盐酸,该反应中有关物质质量与加入稀盐酸质量之间的关系如图所示,下列说法错误的是
A.曲线①表示烧杯中碳酸钠的质量变化 B.曲线②表示烧杯中氯化钠的质量变化
C.曲线③表示二氧化碳的质量变化 D.曲线④表示烧杯中水的质量变化
13.图1是甲,乙、丙三种物质的溶解度曲线,R是其中一种物质。现取50gR如图2进行有关实验,观察到①②中没有固体析出,③中有固体析出。下列说法正确的是
A.从图2的实验结合图1分析,R是丙物质
B.①和②的溶液中,溶质的质量分数不相等
C.①②③中,只有③的上层清液是饱和溶液
D.①②③中,①的溶液中溶质的质量分数最大
14.木糖醇是目前市场上的一种蔗糖替代品,在某些温度下其溶解度分别为:30℃时为70g,50℃时为84g,60℃时为90g。如图表示的是木糖醇等固体的溶解度曲线。根据曲线判断,下列说法不正确的是( )
A.X为木糖醇的溶解度曲线
B.随着温度的升高,Z物质的溶解度逐渐减小
C.可以采用冷却热饱和溶液的方法获得Z的晶体
D.50℃时,Y的饱和溶液和Z的饱和溶液溶质的质量分数相等
15.如图是a、b、c三种固体物质的溶解度曲线。下列说法不正确的是
A.在t2℃时,将20ga物质加入50g水中充分溶解,所得溶液质量为70g
B.t1℃时,a、c两种物质的饱和溶液,其溶质质量分数相等
C.将a、b、c三种物质的饱和溶液由t2℃降温至t1℃,其溶质质量分数由大到小的关系是:b>a=c
D.若a物质中混有了少量的c物质,可采用降温结晶的方法提纯a物质
二、填空题
16.走进“碳村庄”,“碳村庄”的格局如图1
(1)“碳村庄”的居民中,属于单质的是___。CaCO3是___ 的主要成分。
(2)“碳村庄”中的部分居民可以相互转化,写出通过化合反应将CO转化为CO2和CO2转化为CO的化学方程式________。
(3)“碳村庄”又来了一位新成员——蔗糖(C12H22O11),它在酒曲的催化下,经过发酵过程可以转变成酒精和二氧化碳。如图2所示。可以说明该反应已经发生的现象是______,B中相应反应的化学方程式为___。
17.化学源于生活,生活中蕴含着许多化学知识。
(1)生活用水有硬水和软水之分,化学课上用______来区分。
(2)我们的生活用水多是硬水,生活中常用______的方法降低水的硬度。
(3)打开的薯片放一个晚上就变得不脆了,说明空气中含有______。
(4)防毒面具是利用了活性炭具有______的性质。
(5)打开汽水瓶盖时,汽水瓶内会产生一个个小气泡,该气泡是______气体。
(6)打火机的主要部件是打火石和贮气箱,按下开关时,打火石发出电火花,引燃贮气箱释放的燃气,根据燃烧的条件分析,打火石的作用是______。
18.化学就在我们身边,它能改善我们的生活。请回答下列问题:
(1)打开汽水瓶盖能听到“嘶嘶”声,这说明气体的溶解能力和______有关。
(2)锌是人体不可缺少的一种元素。锌相对原子质量的国际新标准由张青莲教授主持测定。根据图示可知锌元素的相对原子质量为______,锌原子在化学反应中容易______(选填“得到”或“失去”)电子。
19.如图是五种化合物常温在溶液中两两之间发生的某些转化关系图,图中的“→”表示由某种物质可通过一步反应直接转化为另一种物质(部分反应物、生成物略去)。回答问题。
(1)①NaCl→NaNO3:____________。
②NaOH→NaCl:____________。
③Na2SO4→NaCl:____________。
④以上三个反应的转化是:酸、碱、盐在水溶液中发生的都是_________(填基本反应类型);这类反应实质上是_______的过程。
(2)在图中物质间转化关系中有的可以逆向转化它们分别是①_______→_______②_______→_______。
20.下列物质与人类生活密切相关,请选择相应的编号填空。
A.CH4 B.NaHCO3 C.Na2CO3 D.NaCI
(1)常用作调味品的是______。
(2)用于生产发酵粉的是______。
(3)用于生产洗涤剂的是______。
(4)“可燃冰”的主要成分是______。
三、推断题
21.甲、乙、丙、丁、戊是初中化学常见的物质,其中甲是一种常见气体,丁是大理石的主要成分,乙的固体俗称干冰,它们之间部分转化关系如图所示。(“→“表示某种物质经一步反应可转化成另一种物质,“一”表示两种物质能发生化学反应)
(1)戊的化学式为_____________。
(2)丙和戊发生的反应是__________(填“放热”或“吸热”)反应。
22.如图是初中化学中常见物质间的转化关系,其中A是氧化物,B是碱,C是单质,无色溶液中只含一种溶质,各物质间恰好完全反应(部分产物已略去)。请根据信息回答下列有关问题。
(1)无色溶液中含有的离子符号是___________。
(2)A物质的化学式为___________。
(3)黄色溶液和浅绿色溶液颜色不同的微观原因是___________。
(4)物质X在农业上还可用于改良酸性土壤,该物质的俗名为___________。
(5)上述溶液中,单独使用可鉴别稀硫酸和氢氧化钠溶液的有___________(填序号)。
A.无色溶液 B.红色溶液 C.黄色溶液 D.蓝色溶液
四、实验题
23.根据实验回答下列问题:
(1)下图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现象为浑浊→变红→红色消失。
根据实验现象判断氢氧化钙的性质有_____________、_____________(物理和化学性质各填一条)。
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是__________(填化学式),可能有的溶质是__________。(填化学式)
(3)上图2装置气密性良好。取0.2g碳酸钠于甲中,加入2mL稀硫酸,_____________(填实验操作),并将导管伸入澄清石灰水中,观察到出现浑浊。乙中反应的化学方程式为________________。
(4)上图中甲作为气体发生装置还可制得的气体是___________。(填名称)
24.根据下列实验回答问题。
实验一:炎热的夏天,在家中可以自制汽水来消暑解热。
【制备材料】1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500mL饮料瓶
【制备流程】
【问题讨论】
(1)步骤②中用凉开水制汽水的原因___________。
(2)制汽水时,利用了小苏打能与柠檬酸反应产生气体的性质,为证明柠檬酸溶液中有H+,可以选择下列物质中的 进行验证(填字母)·
A.镁带 B.铜片 C.食盐 D.鸡蛋壳(主要成分碳酸钙)
实验二:据《四川盐法治》记载,“敞锅熬盐”的主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,用木棒不断搅拌,析出粗盐;③用“花水”冲洗粗盐得精品盐。
(3)步骤②中,析出粗盐的过程,当________停止加热,木棒的作用是__________。
(4)步骤③中用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl。则“花水”应当是 (填字母)。
A.蒸馏水 B.饱和NaCl溶液 C.饱和NaOH溶液 D.饱和BaCl2溶液
五、计算题
25.请回答下列问题。
(1)积极应对气候变化,展现大国担当,中国向世界宣布了 2030 年前实现“碳达峰”、2060 年前实现“碳中和”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳 420 亿吨,在这些二氧化碳中含碳元素的质量为多少亿吨?(写出计算过程,计算结果精确至 0.1 亿吨)
(2)20℃时,向 3 个盛有 100 克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据,回答:
实验编号 A B C
加入氯化钠的质量(克) 20 36 50
溶液质量(克) 120 136 136
①实验所得 3 杯溶液中,属于不饱和溶液的是_______(填实验编号)。
②求溶液 C 的溶质质量分数_______。(写出计算过程,计算结果精确至 0.1%)。
26.鸡蛋壳的主要成分是CaCO3,现在取15g干燥的鸡蛋壳放入20g的烧杯中,向其中加入40g稀盐酸恰好完全反应(杂质不溶于水,且不与稀盐酸反应),反应后烧杯和物质的总质量为70.6g,计算鸡量中的CaCO3的质量分数是多少?(结果保留到0.1%)
参考答案:
1.D 2.B 3.B 4.C 5.B 6.B 7.C 8.B 9.D 10.B 11.C 12.D 13.B 14.C 15.C
16.(1) C60 大理石(或石灰石)
(2) ;
(3) 澄清石灰水变浑浊
17.(1)肥皂水
(2)煮沸
(3)水蒸气
(4)吸附性
(5)二氧化碳
(6)使温度达到燃气的着火点
18.(1)压强
(2) 65.38 失去
19.(1)
复分解反应 离子重新组合
(2) Na2SO4 NaOH Na2CO3 NaOH
20.(1)D
(2)B
(3)C
(4)A
21.(1)CaO
(2)放热
22.(1)H+、SO42-
(2)Fe2O3
(3)黄色溶液中含有Fe3+,浅绿色溶液中含有的是Fe2+
(4)熟石灰、消石灰
(5)BCD
23.(1) 微溶于水 能与稀盐酸反应(或能使酚酞试液变红)
(2) CaCl2 HCl
(3) 立即塞紧橡皮塞
(4)氧气(或氢气)
24.(1)CO2的溶解度随温度的降低而增大,凉开水温度低,溶解的CO2较多
(2)AD
(3) 敞口锅中出现较多量晶体 搅拌,防止液体因局部温度过高,造成液滴飞溅
(4)B
25.(1)解:二氧化碳中含碳元素的质量为:
答:二氧化碳中碳元素的质量为114.5亿吨。
(2) A 解:溶液 C 的溶质质量分数为:
答:溶液 C 的溶质质量分数为26.5%。
26.解:由质量守恒定律可知,生成二氧化碳的质量=15g+20g+40g 70.6g=4.4g
设鸡量中的CaCO3的质量为x
=
x=10g
鸡量中的CaCO3的质量分数=×100%≈66.7%
答:鸡量中的CaCO3的质量分数为66.7%。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
