第七单元常见的酸和碱测试题-2021-2022学年九年级化学鲁教版下册(word版 含答案)
文档属性
| 名称 | 第七单元常见的酸和碱测试题-2021-2022学年九年级化学鲁教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 159.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-20 00:00:00 | ||
图片预览



文档简介
第七单元《常见的酸和碱》测试题
一、单选题
1.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
2.pH是水质监测的重要指标之一,下列水样酸性最强的是
A.pH=1.3的工业废水 B.pH=4.5的雨水
C.pH=7.0的蒸馏水 D.pH=7.3的矿泉水
3.下列人体体液中,酸性最强的是
A.唾液(pH约6.6~7.1) B.胃液(pH约0.8~1.5)
C.胆汁(pH约6.8~7.4) D.血液(pH约7.35~7.45)
4.向石蕊试液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是( )
A.红色——紫色——红色 B.紫色——红色——紫色
C.红色——紫色——蓝色 D.红色——无色——红色
5.下列关于氢氧化钠的说法中错误的是
A.俗名苛性钠、火碱或烧碱
B.易溶于水,溶于水时吸收大量的热
C.氢氧化钠固体露置在空气中容易变质
D.是重要的化工原料广泛用于肥皂、纺织、印刷等工业
6.以下实验操作正确的是
A.振荡试管 B.两人合作滴加液体
C.过滤 D.稀释浓硫酸
7.下列药品需要密封保存的原因,解释错误的是( )
A.浓盐酸—— 防止挥发 B.氢氧化钠溶液 ——防止与二氧化碳反应
C.浓硫酸 ——防止吸水 D.生石灰 —— 防止与氧气反应
8.下列有关氢氧化钠的说法,错误的是( )
A.氢氧化钠俗称烧碱
B.氢氧化钠有强烈的腐蚀性
C.氢氧化钠固体可用于干燥二氧化碳气体
D.氢氧化钠可用于制肥皂、洗涤剂、造纸、纺织工业等
9.根据下列实验现象可以判断某溶液一定呈碱性的是( )
A.溶液中滴入石蕊仍为紫色 B.溶液中滴入酚酞显红色
C.溶液中滴入石蕊显红色 D.溶液中滴入酚酞不显色
10.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
11.盐酸先生闯迷宫(见图),请你帮他选择行进路线(不发生化学反应)。( )
A.A B.B C.C D.D
12.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
13.实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示,下列说法不正确的是
A.反应过程中有热量放出
B.30 s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液
D.从20 s到40 s,溶液的温度升高,pH增大
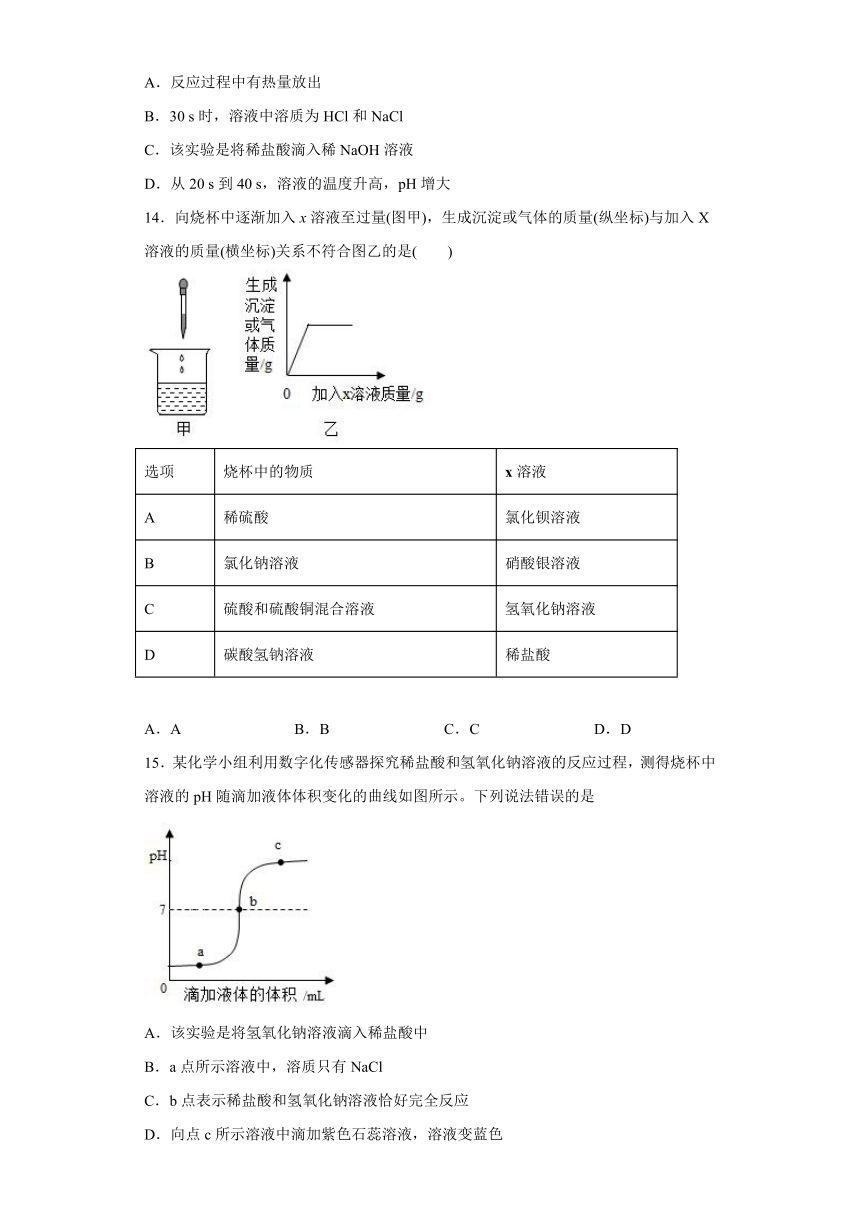
14.向烧杯中逐渐加入x溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
选项 烧杯中的物质 x溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
A.A B.B C.C D.D
15.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是
A.该实验是将氢氧化钠溶液滴入稀盐酸中
B.a点所示溶液中,溶质只有NaCl
C.b点表示稀盐酸和氢氧化钠溶液恰好完全反应
D.向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
二、填空题
16.某同学将一朵紫色牵牛花泡在石灰水里,牵牛花很快就变成了蓝色,又将牵牛花泡在稀盐酸中,牵牛花又变成了红色,请你根据以上实验现象回答:
(1)该同学将紫色牵牛花泡在肥皂水里,牵牛花很快就变成了蓝色,据此可推断肥皂水显_____(填“酸性”或“碱性”)。
(2)该牵牛花的汁液_____(填“能”或“不能”)用作指示剂。
17.醋酸(CH3COOH)是一种常见的酸,具有酸的通性。例如:醋酸与氢氧化钠溶液反应生成醋酸钠和水,化学方程式为CH3COOH+NaOH=CH3COONa+H2O。
(1)氢氧化钾与氢氧化钠是同一类物质,具有通性。请写出醋酸与氢氧化钾溶液发生反应生成的盐的化学式______。
(2)醋酸与盐酸一样,能与活泼金属反应生成氢气。请写出醋酸与金属锌反应的化学方程式:___________________________________________________。
18.盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中化学中许多实验都用到了盐酸。
(1)打开浓盐酸的试剂瓶,观察到瓶口有 ___________ 产生。下列实验中一定不会用到盐酸的是 ____________ (填序号)。
A.除去熟石灰中的石灰石 B.鉴别氯化钠和碳酸钠
C.实验室制取二氧化碳 D.除去铁钉上的锈迹
(2)用盐酸按照下图的方式进行中和反应实验,其化学反应方程式是 ___________________________ ,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是 _________________________ 。以下证明盐酸过量的操作及实验现象的叙述正确的是 _________ (填序号)。
A.滴加石蕊溶液,搅拌后溶液变蓝
B.另滴加氢氧化钠溶液,搅拌后溶液颜色不变
C.加入蒸馏水,搅拌后溶液颜色不变
D.加入金属Cu片,产生气泡
19.许多植物的果实和花瓣中含有色素。现提取几种植物的果实或花瓣的汁液,用稀酸、稀碱和水逐一检验,现象记录如下表。
植物的汁液 在酸性溶液中 在水中 在碱性溶液中
牵牛花 红色 紫色 蓝色
万寿菊 黄色 黄色 黄色
胡萝卜 橙色 橙色 橙色
玫瑰 浅红色 浅红色 绿色
(1)上述植物的汁液不能用来区别稀硫酸和氢氧化钠溶液的是 、 。(填植物的名称)
(2)手工制作一朵纸玫瑰花,用pH=12的某种溶液浸泡后晾干,用所提取的玫瑰的汁液均匀的涂在纸玫瑰花上,纸花会变成 色。
(3)与实验中常用的指示剂石蕊的变色原理相似的是 。(填植物的名称)
三、推断题
20.如图,A、B、C、D、E、F 分别表示六种物质,A 是目前世界年产量最高的金属且具有银白色金属光泽,B 物质由三种元素组成, 溶于水后其溶液为蓝色,C 是地壳中含量最高的金属元素组成的单质,E 会造成温室效应,E 和 D 两种物质中不含相同种类的元素,“─”或“表示两种物质之间能发生反应,“”表示一种物质可以转化为另一 种物质,部分反应物和生成物已略去,请回答下列问题:
(1)请写出 D、F 的化学式:D_______F_______;
(2)写出图中两物质反应生成气体单质的化学方程式:_______;
(3)写出 D 与过量 A 反应的现象:_______。
21.推断题:如下图所示,A~H是初中化学常见的物质,已知A中含有两种元素,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂。Y为单质。
请根据图示回答下列问题:
(1)H的化学式为______。
(2)反应②的基本类型为______。
(3)A和B反应的化学方程式为_________。
(4)写出物质B的一种用途_________。
四、实验题
22.制取气体是重要的化学实验活动,请根据给出的装置,回答下列问题。
(1)请写出图A中仪器a的名称:_________。
(2)用高锰酸钾制取并收集较纯的氧气,选择的装置组合是_________(填字母序号)。
(3)在实验室中选用B装置制取氧气,用这种方法制得的氧气常含有少量水蒸气。若用下图所示装置除去水蒸气,气体应从_________(选填“b”或“c”)端进入。
(4)实验室制取二氧化碳时,可将__________放到集气瓶口来判断是否已集满二氧化碳气体,实验室不适宜用排水法收集二氧化碳的理由是_________。
23.某雪饼包装袋中的干燥剂主要成分是氧化钙。
(1)该干燥剂的干燥原理是_____(用化学方程式表示),该反应的基本类型是_____。
(2)该干燥剂在空气中放置一段时间后,主要成分可能有:氧化钙、氢氧化钙和碳酸钙。为探究其成分,取放置后的干燥剂样品进行如下实验:(杂质不参与反应)
实验操作 实验现象(依据) 实验结论
I. 取少量样品于试管中,加少量水,再滴入酚酞。 无色酚酞变红 该样品中_____(填“可能”或“一 定”)有氧化钙
II. 取少量样品于试管中,滴加足量盐酸。 _____ 该样品中一定没有碳酸钙。
III. 称取该样品 5.6 克,放入足量 水中,得到悬浊液,蒸干得到白色固体 m 克。 m 的数值范围为_____ 该样品的成分是氧化钙和氢氧化钙。
五、计算题
24.赤铁矿石的主要成分为氧化铁。将10g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,再加入92g稀硫酸,恰好完全反应,过滤,得到滤液和2g滤渣。请计算:
(1)赤铁矿石样品中氧化铁的质量分数。
(2)反应后所得溶液中溶质质量分数。
25.现有一瓶敞口放置在空气中的NaOH固体,欲知其组成成分,取样品9.3克向其中逐渐加入一定质量分数的稀盐酸,产生气体的质量与加入稀盐酸质量关系如图所示,试回答:
(1)产生二氧化碳气体的质量为_______克。
(2)所用稀盐酸溶质质量分数为___________。
(3)求样品中氢氧化钠的质量分数为___________。(精确到0.1%)
试卷第1页,共3页
参考答案:
1.C 2.A 3.B 4.B 5.B 6.C 7.D 8.C 9.B 10.B 11.B 12.D 13.C 14.C 15.B
16. 碱性 能
17. CH3COOK 2CH3COOH+Zn=(CH3COO)2Zn+H2↑
18. 白雾 A 溶液红色褪去 B
19.(1)万寿菊 胡萝卜
(2)绿色
(3)牵牛花
20. HCl CaCO3 、 银白色固体逐渐减少,表面有气泡产生,溶液逐渐变为浅绿色
21. 化合反应 改良酸性士壤(合理即可)
22. 试管 AC b 燃着的木条 二氧化碳能溶于水且能与水反应
23. CaO+H2O=Ca(OH)2 化合反应 可能 固体逐渐溶解,无气泡产生
5.6g<m<7.4g
24.(1)80%;
(2)解:设生成硫酸铁的质量为x
x=20g
滤液中溶质的质量分数为100%=20%。
答:反应后所得溶液中溶质质量分数20%。
25.(1)2.2(2)7.3% (3)43.0%
答案第1页,共2页
一、单选题
1.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
2.pH是水质监测的重要指标之一,下列水样酸性最强的是
A.pH=1.3的工业废水 B.pH=4.5的雨水
C.pH=7.0的蒸馏水 D.pH=7.3的矿泉水
3.下列人体体液中,酸性最强的是
A.唾液(pH约6.6~7.1) B.胃液(pH约0.8~1.5)
C.胆汁(pH约6.8~7.4) D.血液(pH约7.35~7.45)
4.向石蕊试液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是( )
A.红色——紫色——红色 B.紫色——红色——紫色
C.红色——紫色——蓝色 D.红色——无色——红色
5.下列关于氢氧化钠的说法中错误的是
A.俗名苛性钠、火碱或烧碱
B.易溶于水,溶于水时吸收大量的热
C.氢氧化钠固体露置在空气中容易变质
D.是重要的化工原料广泛用于肥皂、纺织、印刷等工业
6.以下实验操作正确的是
A.振荡试管 B.两人合作滴加液体
C.过滤 D.稀释浓硫酸
7.下列药品需要密封保存的原因,解释错误的是( )
A.浓盐酸—— 防止挥发 B.氢氧化钠溶液 ——防止与二氧化碳反应
C.浓硫酸 ——防止吸水 D.生石灰 —— 防止与氧气反应
8.下列有关氢氧化钠的说法,错误的是( )
A.氢氧化钠俗称烧碱
B.氢氧化钠有强烈的腐蚀性
C.氢氧化钠固体可用于干燥二氧化碳气体
D.氢氧化钠可用于制肥皂、洗涤剂、造纸、纺织工业等
9.根据下列实验现象可以判断某溶液一定呈碱性的是( )
A.溶液中滴入石蕊仍为紫色 B.溶液中滴入酚酞显红色
C.溶液中滴入石蕊显红色 D.溶液中滴入酚酞不显色
10.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
11.盐酸先生闯迷宫(见图),请你帮他选择行进路线(不发生化学反应)。( )
A.A B.B C.C D.D
12.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
13.实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示,下列说法不正确的是
A.反应过程中有热量放出
B.30 s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液
D.从20 s到40 s,溶液的温度升高,pH增大
14.向烧杯中逐渐加入x溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
选项 烧杯中的物质 x溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
A.A B.B C.C D.D
15.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是
A.该实验是将氢氧化钠溶液滴入稀盐酸中
B.a点所示溶液中,溶质只有NaCl
C.b点表示稀盐酸和氢氧化钠溶液恰好完全反应
D.向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
二、填空题
16.某同学将一朵紫色牵牛花泡在石灰水里,牵牛花很快就变成了蓝色,又将牵牛花泡在稀盐酸中,牵牛花又变成了红色,请你根据以上实验现象回答:
(1)该同学将紫色牵牛花泡在肥皂水里,牵牛花很快就变成了蓝色,据此可推断肥皂水显_____(填“酸性”或“碱性”)。
(2)该牵牛花的汁液_____(填“能”或“不能”)用作指示剂。
17.醋酸(CH3COOH)是一种常见的酸,具有酸的通性。例如:醋酸与氢氧化钠溶液反应生成醋酸钠和水,化学方程式为CH3COOH+NaOH=CH3COONa+H2O。
(1)氢氧化钾与氢氧化钠是同一类物质,具有通性。请写出醋酸与氢氧化钾溶液发生反应生成的盐的化学式______。
(2)醋酸与盐酸一样,能与活泼金属反应生成氢气。请写出醋酸与金属锌反应的化学方程式:___________________________________________________。
18.盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中化学中许多实验都用到了盐酸。
(1)打开浓盐酸的试剂瓶,观察到瓶口有 ___________ 产生。下列实验中一定不会用到盐酸的是 ____________ (填序号)。
A.除去熟石灰中的石灰石 B.鉴别氯化钠和碳酸钠
C.实验室制取二氧化碳 D.除去铁钉上的锈迹
(2)用盐酸按照下图的方式进行中和反应实验,其化学反应方程式是 ___________________________ ,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是 _________________________ 。以下证明盐酸过量的操作及实验现象的叙述正确的是 _________ (填序号)。
A.滴加石蕊溶液,搅拌后溶液变蓝
B.另滴加氢氧化钠溶液,搅拌后溶液颜色不变
C.加入蒸馏水,搅拌后溶液颜色不变
D.加入金属Cu片,产生气泡
19.许多植物的果实和花瓣中含有色素。现提取几种植物的果实或花瓣的汁液,用稀酸、稀碱和水逐一检验,现象记录如下表。
植物的汁液 在酸性溶液中 在水中 在碱性溶液中
牵牛花 红色 紫色 蓝色
万寿菊 黄色 黄色 黄色
胡萝卜 橙色 橙色 橙色
玫瑰 浅红色 浅红色 绿色
(1)上述植物的汁液不能用来区别稀硫酸和氢氧化钠溶液的是 、 。(填植物的名称)
(2)手工制作一朵纸玫瑰花,用pH=12的某种溶液浸泡后晾干,用所提取的玫瑰的汁液均匀的涂在纸玫瑰花上,纸花会变成 色。
(3)与实验中常用的指示剂石蕊的变色原理相似的是 。(填植物的名称)
三、推断题
20.如图,A、B、C、D、E、F 分别表示六种物质,A 是目前世界年产量最高的金属且具有银白色金属光泽,B 物质由三种元素组成, 溶于水后其溶液为蓝色,C 是地壳中含量最高的金属元素组成的单质,E 会造成温室效应,E 和 D 两种物质中不含相同种类的元素,“─”或“表示两种物质之间能发生反应,“”表示一种物质可以转化为另一 种物质,部分反应物和生成物已略去,请回答下列问题:
(1)请写出 D、F 的化学式:D_______F_______;
(2)写出图中两物质反应生成气体单质的化学方程式:_______;
(3)写出 D 与过量 A 反应的现象:_______。
21.推断题:如下图所示,A~H是初中化学常见的物质,已知A中含有两种元素,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂。Y为单质。
请根据图示回答下列问题:
(1)H的化学式为______。
(2)反应②的基本类型为______。
(3)A和B反应的化学方程式为_________。
(4)写出物质B的一种用途_________。
四、实验题
22.制取气体是重要的化学实验活动,请根据给出的装置,回答下列问题。
(1)请写出图A中仪器a的名称:_________。
(2)用高锰酸钾制取并收集较纯的氧气,选择的装置组合是_________(填字母序号)。
(3)在实验室中选用B装置制取氧气,用这种方法制得的氧气常含有少量水蒸气。若用下图所示装置除去水蒸气,气体应从_________(选填“b”或“c”)端进入。
(4)实验室制取二氧化碳时,可将__________放到集气瓶口来判断是否已集满二氧化碳气体,实验室不适宜用排水法收集二氧化碳的理由是_________。
23.某雪饼包装袋中的干燥剂主要成分是氧化钙。
(1)该干燥剂的干燥原理是_____(用化学方程式表示),该反应的基本类型是_____。
(2)该干燥剂在空气中放置一段时间后,主要成分可能有:氧化钙、氢氧化钙和碳酸钙。为探究其成分,取放置后的干燥剂样品进行如下实验:(杂质不参与反应)
实验操作 实验现象(依据) 实验结论
I. 取少量样品于试管中,加少量水,再滴入酚酞。 无色酚酞变红 该样品中_____(填“可能”或“一 定”)有氧化钙
II. 取少量样品于试管中,滴加足量盐酸。 _____ 该样品中一定没有碳酸钙。
III. 称取该样品 5.6 克,放入足量 水中,得到悬浊液,蒸干得到白色固体 m 克。 m 的数值范围为_____ 该样品的成分是氧化钙和氢氧化钙。
五、计算题
24.赤铁矿石的主要成分为氧化铁。将10g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,再加入92g稀硫酸,恰好完全反应,过滤,得到滤液和2g滤渣。请计算:
(1)赤铁矿石样品中氧化铁的质量分数。
(2)反应后所得溶液中溶质质量分数。
25.现有一瓶敞口放置在空气中的NaOH固体,欲知其组成成分,取样品9.3克向其中逐渐加入一定质量分数的稀盐酸,产生气体的质量与加入稀盐酸质量关系如图所示,试回答:
(1)产生二氧化碳气体的质量为_______克。
(2)所用稀盐酸溶质质量分数为___________。
(3)求样品中氢氧化钠的质量分数为___________。(精确到0.1%)
试卷第1页,共3页
参考答案:
1.C 2.A 3.B 4.B 5.B 6.C 7.D 8.C 9.B 10.B 11.B 12.D 13.C 14.C 15.B
16. 碱性 能
17. CH3COOK 2CH3COOH+Zn=(CH3COO)2Zn+H2↑
18. 白雾 A 溶液红色褪去 B
19.(1)万寿菊 胡萝卜
(2)绿色
(3)牵牛花
20. HCl CaCO3 、 银白色固体逐渐减少,表面有气泡产生,溶液逐渐变为浅绿色
21. 化合反应 改良酸性士壤(合理即可)
22. 试管 AC b 燃着的木条 二氧化碳能溶于水且能与水反应
23. CaO+H2O=Ca(OH)2 化合反应 可能 固体逐渐溶解,无气泡产生
5.6g<m<7.4g
24.(1)80%;
(2)解:设生成硫酸铁的质量为x
x=20g
滤液中溶质的质量分数为100%=20%。
答:反应后所得溶液中溶质质量分数20%。
25.(1)2.2(2)7.3% (3)43.0%
答案第1页,共2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
