人教版(五四学制)化学八年级全册第六单元 课题3 二氧化碳和一氧化碳教案(表格式)
文档属性
| 名称 | 人教版(五四学制)化学八年级全册第六单元 课题3 二氧化碳和一氧化碳教案(表格式) |

|
|
| 格式 | docx | ||
| 文件大小 | 30.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-21 00:00:00 | ||
图片预览


文档简介
课题3 二氧化碳性质
教 学 目 标 知识传授目标 (1)了解二氧化碳性质。 (2)了解二氧化碳的用途。 (3)了解并关注温室效应。
能力培养目标 (1)会对实验现象进行观察分析、归纳。 (2)会运用已学知识解决实际问题。
思想教育目标 强化保护环境、解决环境问题的意识。
教学分析 教学难点 1.CO2与水的反应。2.CO2与澄清石灰水的反应。
教学重点 二氧化碳的性质。
教学方法 实验
教学工具 实验仪器、多媒体
教学课时 1课时
教 学 内 容 及 过 程 二 备 过 程
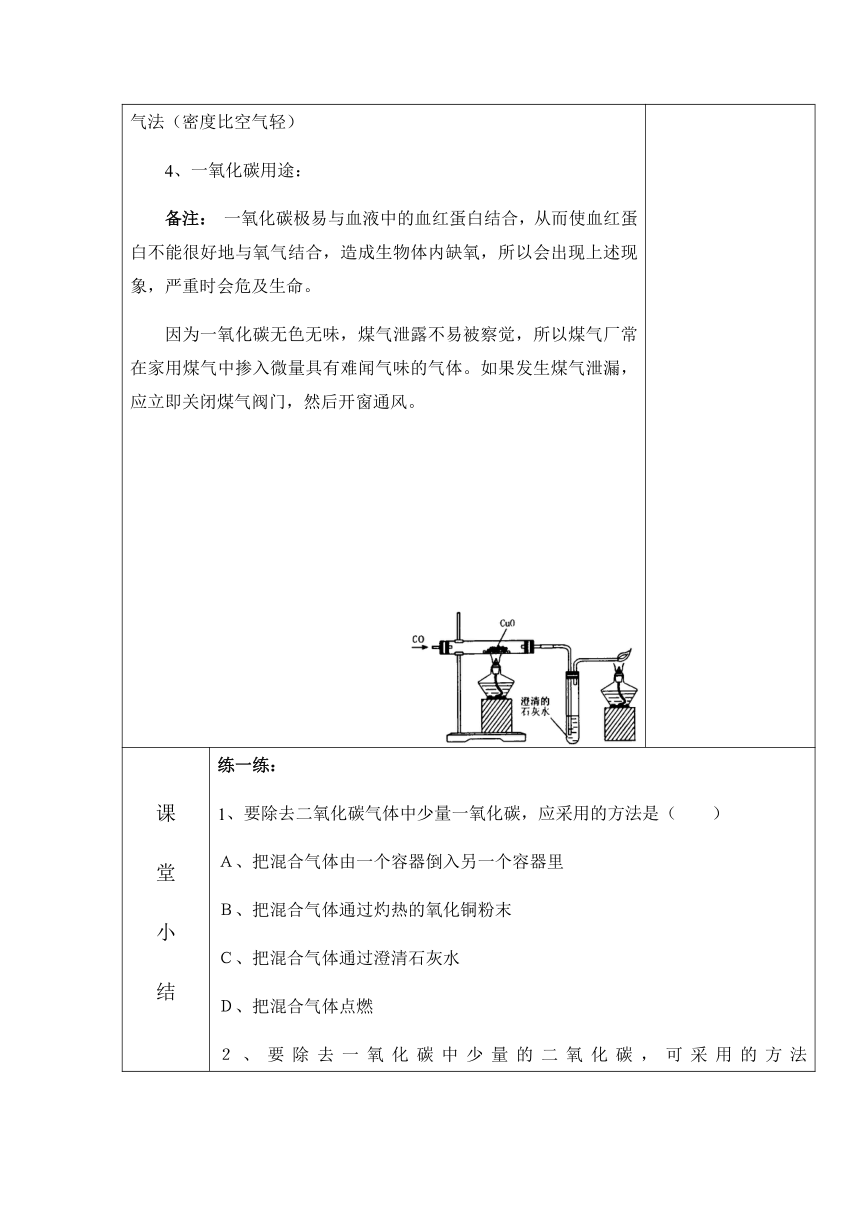
复习引入:二氧化碳的收集方法和检验方法 板书:一、二氧化碳 1、二氧化碳的物理性质 无色无味气体,密度比空气大,易溶于水,无毒性。固体二氧化碳叫“干冰”。 2、二氧化碳的化学性质 1)二氧化碳不能燃烧,也不支持燃烧 2)二氧化碳能与水反应生成碳酸 CO2+H2O==H2CO3 3)二氧化碳能与澄清石灰水反应 CO2+Ca(OH)2==CaCO3↓+H2O 3、二氧化碳用途:促进植物的光和作用 制冷剂 人工降雨 温室肥料 二、一氧化碳 1、一氧化碳物理性质: 无色无味气体,密度比空气小,极难溶于水,剧有毒性。一氧化碳跟氧气燃烧时火焰呈蓝色。 2、一氧化碳化学性质: 1)可燃性:2CO+O22CO2 2)还原性: CO+CuOCu+CO2 3、一氧化碳的收集方法:a.排水法(极难溶于水) b.向下排空气法(密度比空气轻) 4、一氧化碳用途: 备注: 一氧化碳极易与血液中的血红蛋白结合,从而使血红蛋白不能很好地与氧气结合,造成生物体内缺氧,所以会出现上述现象,严重时会危及生命。 因为一氧化碳无色无味,煤气泄露不易被察觉,所以煤气厂常在家用煤气中掺入微量具有难闻气味的气体。如果发生煤气泄漏,应立即关闭煤气阀门,然后开窗通风。
课 堂 小 结 练一练: 1、要除去二氧化碳气体中少量一氧化碳,应采用的方法是( ) A、把混合气体由一个容器倒入另一个容器里 B、把混合气体通过灼热的氧化铜粉末 C、把混合气体通过澄清石灰水 D、把混合气体点燃 2、要除去一氧化碳中少量的二氧化碳,可采用的方法有 。 3、抹墙壁的石灰浆主要成分是氢氧化钙,请用化学方程式解释墙壁逐渐变硬的原因 。 考题回顾 1. 5月31日是“世界无烟日”。吸烟时产生的烟气中含有一种能与人体内血红蛋白相结合的有毒物质,该物质是( ) A.CO2 B.CO C.SO2 D.N2 2. 如图所示,将集气瓶中二氧化碳气体沿烧杯壁倒入烧杯中,看到下层的蜡烛先熄灭。由此实验可以证明二氧化碳的性质( ) ①二氧化碳的密度比空气大 ②二氧化碳能溶于水 ③二 氧化碳能使澄清的石灰水变浑浊 ④二氧化碳能与水反应生成碳酸 ⑤二氧化碳不能燃烧也不能支持燃烧 A. ①⑤ B.③④ C. ④⑤ D.②③④ 3.要区分二氧化碳、氧气两瓶无色气体,下列方法中不可行的是…( ) A. 加入适量紫色石蕊试液 B.加入适量澄清石灰水 C.加入适量氢氧化钠溶液 D.将燃着的木条伸入瓶口内 4.盛放石灰水的试剂放置时间长了,在瓶口会形成一些白色粉末,写出生成白色粉末的化学方程式。
板书设计 课题3 二氧化碳和一氧化碳 二氧化碳 二、一氧化碳 课后作业 习题:1、2、(必做) 5、6、(选做)
教 学 反 思 1、对于二氧化碳的物理性质的学习,建议以探究式学习为主,让学生根据实验现象,得出二氧化碳的性质,而不是教师先讲二氧化碳的性质,然后做实验验证给学生看。 2、对二氧化碳的化学性质,在强调不可燃性和与水反应生成碳酸的同时,单独列出二氧化碳的不可燃性和一般情况下不支持燃烧的性质,有利于学生理解灭火这一二氧化碳的重要用途。 3、二氧化碳使学生比较熟悉的物质,他的化学性质并不难掌握,学生对一氧化碳的了解并不多,另外两者性质的巨大差异也增加了学生学习和应用知识的难度,建议在二氧化碳的教学中采用以学生自主学习、学生之间合作学习为主,但一氧化碳的学习则通过教师边实验边与二氧化碳的性质进行对比,同时启发学生对实验结果进行分析的方法来掌握。 总之,本节内容实验的分量较大,教师不应把全部实验总为掩饰实验来做,应挑一两个既富有探究性有比较好把握的小实验让学生亲手去做,这样既能训练学生动手操作的基本能力,又能提高学生对实验的初步设计能力,还能进一步及其学生对化学这门学科的兴趣。
教 学 目 标 知识传授目标 (1)了解二氧化碳性质。 (2)了解二氧化碳的用途。 (3)了解并关注温室效应。
能力培养目标 (1)会对实验现象进行观察分析、归纳。 (2)会运用已学知识解决实际问题。
思想教育目标 强化保护环境、解决环境问题的意识。
教学分析 教学难点 1.CO2与水的反应。2.CO2与澄清石灰水的反应。
教学重点 二氧化碳的性质。
教学方法 实验
教学工具 实验仪器、多媒体
教学课时 1课时
教 学 内 容 及 过 程 二 备 过 程
复习引入:二氧化碳的收集方法和检验方法 板书:一、二氧化碳 1、二氧化碳的物理性质 无色无味气体,密度比空气大,易溶于水,无毒性。固体二氧化碳叫“干冰”。 2、二氧化碳的化学性质 1)二氧化碳不能燃烧,也不支持燃烧 2)二氧化碳能与水反应生成碳酸 CO2+H2O==H2CO3 3)二氧化碳能与澄清石灰水反应 CO2+Ca(OH)2==CaCO3↓+H2O 3、二氧化碳用途:促进植物的光和作用 制冷剂 人工降雨 温室肥料 二、一氧化碳 1、一氧化碳物理性质: 无色无味气体,密度比空气小,极难溶于水,剧有毒性。一氧化碳跟氧气燃烧时火焰呈蓝色。 2、一氧化碳化学性质: 1)可燃性:2CO+O22CO2 2)还原性: CO+CuOCu+CO2 3、一氧化碳的收集方法:a.排水法(极难溶于水) b.向下排空气法(密度比空气轻) 4、一氧化碳用途: 备注: 一氧化碳极易与血液中的血红蛋白结合,从而使血红蛋白不能很好地与氧气结合,造成生物体内缺氧,所以会出现上述现象,严重时会危及生命。 因为一氧化碳无色无味,煤气泄露不易被察觉,所以煤气厂常在家用煤气中掺入微量具有难闻气味的气体。如果发生煤气泄漏,应立即关闭煤气阀门,然后开窗通风。
课 堂 小 结 练一练: 1、要除去二氧化碳气体中少量一氧化碳,应采用的方法是( ) A、把混合气体由一个容器倒入另一个容器里 B、把混合气体通过灼热的氧化铜粉末 C、把混合气体通过澄清石灰水 D、把混合气体点燃 2、要除去一氧化碳中少量的二氧化碳,可采用的方法有 。 3、抹墙壁的石灰浆主要成分是氢氧化钙,请用化学方程式解释墙壁逐渐变硬的原因 。 考题回顾 1. 5月31日是“世界无烟日”。吸烟时产生的烟气中含有一种能与人体内血红蛋白相结合的有毒物质,该物质是( ) A.CO2 B.CO C.SO2 D.N2 2. 如图所示,将集气瓶中二氧化碳气体沿烧杯壁倒入烧杯中,看到下层的蜡烛先熄灭。由此实验可以证明二氧化碳的性质( ) ①二氧化碳的密度比空气大 ②二氧化碳能溶于水 ③二 氧化碳能使澄清的石灰水变浑浊 ④二氧化碳能与水反应生成碳酸 ⑤二氧化碳不能燃烧也不能支持燃烧 A. ①⑤ B.③④ C. ④⑤ D.②③④ 3.要区分二氧化碳、氧气两瓶无色气体,下列方法中不可行的是…( ) A. 加入适量紫色石蕊试液 B.加入适量澄清石灰水 C.加入适量氢氧化钠溶液 D.将燃着的木条伸入瓶口内 4.盛放石灰水的试剂放置时间长了,在瓶口会形成一些白色粉末,写出生成白色粉末的化学方程式。
板书设计 课题3 二氧化碳和一氧化碳 二氧化碳 二、一氧化碳 课后作业 习题:1、2、(必做) 5、6、(选做)
教 学 反 思 1、对于二氧化碳的物理性质的学习,建议以探究式学习为主,让学生根据实验现象,得出二氧化碳的性质,而不是教师先讲二氧化碳的性质,然后做实验验证给学生看。 2、对二氧化碳的化学性质,在强调不可燃性和与水反应生成碳酸的同时,单独列出二氧化碳的不可燃性和一般情况下不支持燃烧的性质,有利于学生理解灭火这一二氧化碳的重要用途。 3、二氧化碳使学生比较熟悉的物质,他的化学性质并不难掌握,学生对一氧化碳的了解并不多,另外两者性质的巨大差异也增加了学生学习和应用知识的难度,建议在二氧化碳的教学中采用以学生自主学习、学生之间合作学习为主,但一氧化碳的学习则通过教师边实验边与二氧化碳的性质进行对比,同时启发学生对实验结果进行分析的方法来掌握。 总之,本节内容实验的分量较大,教师不应把全部实验总为掩饰实验来做,应挑一两个既富有探究性有比较好把握的小实验让学生亲手去做,这样既能训练学生动手操作的基本能力,又能提高学生对实验的初步设计能力,还能进一步及其学生对化学这门学科的兴趣。
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
