第5章初识酸和碱检测题-2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案)
文档属性
| 名称 | 第5章初识酸和碱检测题-2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 230.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-22 00:00:00 | ||
图片预览


文档简介
第5章《初识酸和碱》检测题
一、单选题
1.2021年“世界水日”的主题为“珍惜水、爱护水”。下列关于水的说法正确的是
A.过滤能将硬水转化为软水 B.用明矾对自来水进行杀菌消毒
C.用肥皂水区别硬水与软水 D.有水生成的反应一定是中和反应
2.某无色混合气体可能由CH4、H2、CO、CO2和HCl中的若干种气体组成,将此混合气体通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使白色CuSO4粉末变蓝色。则原混合气体中一定含有
A.HCl和CO B.HC1、H2和CO2 C.CH4和H2 D.CO和CO2
3.酸溶液中都含有H+,因此不同酸表现出一些共同性质。下列关于盐酸性质的描述中,不属于酸的共同性质的是
A.能使紫色石蕊试液变为红色 B.能与氢氧化钠溶液反应生成盐和水
C.能与硝酸银溶液反应生成白色沉淀 D.能与锌反应生成氢气
4.下列变化属于化学变化的是
A.分离液态空气制氧气 B.食品久置发生霉变
C.活性炭吸附除异味 D.浓盐酸敞口产生大量白雾
5.下列有关实验的描述错误的是
A.用肥皂水可区分硬水和蒸馏水
B.稀释浓硫酸时,应将水倒入浓硫酸中
C.用氢氧化钠溶液可以除去一氧化碳中混有的二氧化碳
D.蒸发结晶时,当蒸发皿中出现较多固体可停止加热
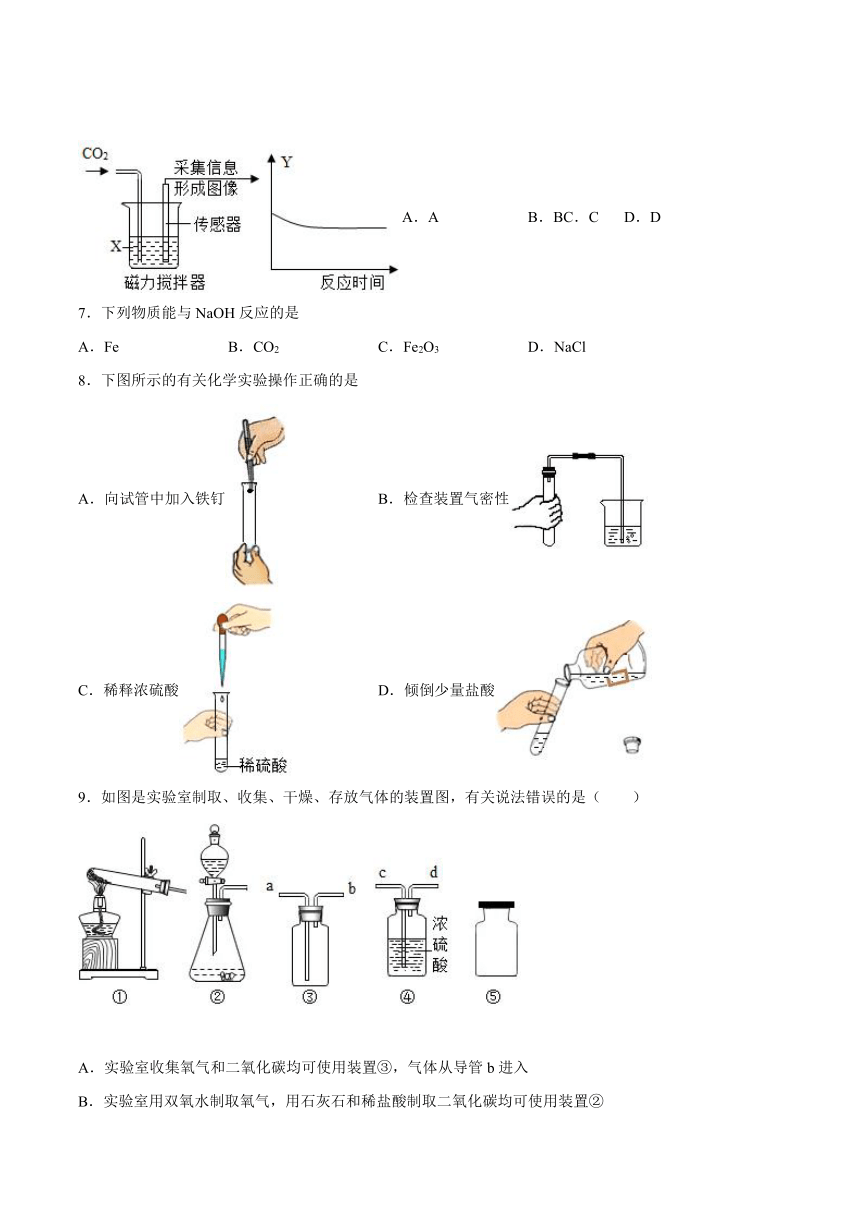
6.图为采用"数字化"实验,由传感器采集实验相关信息描绘出曲线,其中物质X表示能与二氧化碳反应的某液体,纵坐标Y表示烧杯中的某个量,下列对物质X与纵坐标Y的分析正确是
选项 物质X 纵坐标Y
A 水 溶液的质量
B 水 溶液的pH值
C 氢氧化钠溶液 溶质的质量
D 氢氧化钙溶液 溶液中钙元素的质量
A.A B.B C.C D.D
7.下列物质能与NaOH反应的是
A.Fe B.CO2 C.Fe2O3 D.NaCl
8.下图所示的有关化学实验操作正确的是
A.向试管中加入铁钉 B.检查装置气密性
C.稀释浓硫酸 D.倾倒少量盐酸
9.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
10.下列关于盐酸用途的叙述中错误的是
A.用于金属表面除锈
B.在实验室用作干燥剂
C.人体胃液中含有盐酸,可帮助消化
D.实验室用稀盐酸与石灰石反应来制取二氧化碳
11.衣服上沾了铁锈(主要成分是Fe2O3),直接用水很难洗净,要除去白色衬衣上的铁锈,你认为比较适宜的液体是
A.白醋 B.酱油 C.酒精 D.洗洁精
12.下列关于物质用途的叙述错误的是
A.稀硫酸可用于除铁锈
B.氢氧化钙用于改良酸性土壤
C.氧气可用作燃料
D.明矾用于处理水中微小悬浮物
二、简答题
13.自然界中的物质在不断地发生着变化,有些变化使人类的生存环境发生了恶化,例如,随着大量化石燃料(如含硫的煤)的使用,导致酸雨频发,致使大理石建筑物遭受严重侵蚀,请根据如图,解释大理石雕像受到侵蚀的主要原因._________.
14.铁锈的主要成分是________,将一枚生锈的铁钉放入足量的稀盐酸中,你首先观察到的现象是________,过一会儿,你还可以观察到的现象是________请写出有关反应的化学方程式________。
三、推断题
15.A、B、C、D四种化合物,均含有同一种金属元素,它们的转化关系如图所示(部分物质已略去)。
己知A是大理石的主要成分。请回答下列问题:
(1)B的一种用途是_________;
(2)C的化学式为_________;
(3)B转化为D的化学方程式为__________________。
16.A~G 为初中化学常见的七种物质,其中 A、B、C、D、E 属于五种不同类别的物质(单质、氧化物、酸、碱、盐),C、G 的水溶液均呈碱性,且C 广泛应用于制取肥皂和做炉具清洁剂。D、E 中不含相同的元素。它们之间发生反应或转化的关系如图所示(“—”表示两种物质之间能发生化学反应,“→”表示两种物质之间能通过一步反应转化,部分反应物、生成物以及反应条件已略去)。请回答:
(1)C 的化学式_____________;
(2)E 和 F 反应的化学方程式______________。
四、实验题
17.某兴趣小组利用下列装置进行实验室制取并收集气体的实验,请回答:
(1)双氧水和二氧化锰制取并收集较纯净的氧气,应选用的装置组合是______(从A→E中选择字母序号),其反应的化学方程式是______。如果把60g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液来制取氧气,则需加水的质量为______g。
(2)下图是在收集氧气的过程中,会依次观察到的现象是______(用字母序号排序)。
氧气收集完毕取出集气瓶的具体操作是______。
(3)实验室用加热氯化铵固体和熟石灰混合物制取氨气,现要制取并收集干燥的氨气,装置正确连接顺序是:A→______(填字母序号)→E,请说明氨气的物理性质______(写一点)。
五、计算题
18.为了测定某铁矿石中氧化铁(Fe2O3)的质量分数,取矿石样品20g,加入稀盐酸,恰好完全反应时,共消耗稀盐酸219g,经过处理后得到滤渣4g(注:矿石中的杂质既不溶于水,也不与盐酸反应),请计算:
(1)该铁矿石中氧化铁的质量分数 。
(2)所用稀盐酸的溶质质量分数。
19.取含有MgCl2和HC1的混合溶液165.8g于烧杯中,向其中缓慢加入200g溶质质量分数为8%的NaOH溶液,恰好完全反应后过滤得到沉淀和滤液,其中滤液的质量为360g。请计算:
(1)生成沉淀的质量是多少克。
(2)原混合溶液中,MgCl2的质量是多少?(请写出具体的计算过程,下同)
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?(结果保留至0.1%)
20.取NaOH和NaCl的混合物3.63g放入烧杯中,加水溶解配制成70g溶液。向该溶液滴加溶质质量分数为7.3%的稀盐酸,测得溶液pH与滴入稀盐酸的质量关系,如图所示。
(1)当滴入稀盐酸的质量为11.2g时,此时溶液中的溶质是 。(填化学式)
(2)求原混合物中氯化钠的质量。(写出计算过程,提示:根据pH=7时消耗盐酸的质量)
参考答案:
1.C 2.A 3.C 4.B 5.B 6.B 7.B 8.B 9.A 10.B 11.A 12.C
13.大理石的主要成分是碳酸钙,碳酸钙能和酸雨中的酸性物质反应,侵蚀大理石
14. 氧化铁 溶液由无色变成黄色 产生气泡 Fe2O3+6HCl=2FeCl3+3H2O,Fe+2HCl=FeCl2+H2↑
15. 用作干燥剂 Ca(OH)2 CaO+2HCl=CaCl2+H2O
16. NaOH 2HCl+Ca(OH)2=CaCl2+2H2O
17. BC 180 bac 在水面以下盖上玻璃片、取出集气瓶,最后正放在实验台上 G 氨气的密度比空气小
18.(1)80%;(2)10%
19.(1)5.8g;(2)9.5g;(3)6.5%
20.(1)NaCl、HCl
(2)解:设氢氧化钠质量为x
3.63g-0.8g=2.83g
答:原混合物中氯化钠的质量为2.83g。
一、单选题
1.2021年“世界水日”的主题为“珍惜水、爱护水”。下列关于水的说法正确的是
A.过滤能将硬水转化为软水 B.用明矾对自来水进行杀菌消毒
C.用肥皂水区别硬水与软水 D.有水生成的反应一定是中和反应
2.某无色混合气体可能由CH4、H2、CO、CO2和HCl中的若干种气体组成,将此混合气体通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使白色CuSO4粉末变蓝色。则原混合气体中一定含有
A.HCl和CO B.HC1、H2和CO2 C.CH4和H2 D.CO和CO2
3.酸溶液中都含有H+,因此不同酸表现出一些共同性质。下列关于盐酸性质的描述中,不属于酸的共同性质的是
A.能使紫色石蕊试液变为红色 B.能与氢氧化钠溶液反应生成盐和水
C.能与硝酸银溶液反应生成白色沉淀 D.能与锌反应生成氢气
4.下列变化属于化学变化的是
A.分离液态空气制氧气 B.食品久置发生霉变
C.活性炭吸附除异味 D.浓盐酸敞口产生大量白雾
5.下列有关实验的描述错误的是
A.用肥皂水可区分硬水和蒸馏水
B.稀释浓硫酸时,应将水倒入浓硫酸中
C.用氢氧化钠溶液可以除去一氧化碳中混有的二氧化碳
D.蒸发结晶时,当蒸发皿中出现较多固体可停止加热
6.图为采用"数字化"实验,由传感器采集实验相关信息描绘出曲线,其中物质X表示能与二氧化碳反应的某液体,纵坐标Y表示烧杯中的某个量,下列对物质X与纵坐标Y的分析正确是
选项 物质X 纵坐标Y
A 水 溶液的质量
B 水 溶液的pH值
C 氢氧化钠溶液 溶质的质量
D 氢氧化钙溶液 溶液中钙元素的质量
A.A B.B C.C D.D
7.下列物质能与NaOH反应的是
A.Fe B.CO2 C.Fe2O3 D.NaCl
8.下图所示的有关化学实验操作正确的是
A.向试管中加入铁钉 B.检查装置气密性
C.稀释浓硫酸 D.倾倒少量盐酸
9.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
10.下列关于盐酸用途的叙述中错误的是
A.用于金属表面除锈
B.在实验室用作干燥剂
C.人体胃液中含有盐酸,可帮助消化
D.实验室用稀盐酸与石灰石反应来制取二氧化碳
11.衣服上沾了铁锈(主要成分是Fe2O3),直接用水很难洗净,要除去白色衬衣上的铁锈,你认为比较适宜的液体是
A.白醋 B.酱油 C.酒精 D.洗洁精
12.下列关于物质用途的叙述错误的是
A.稀硫酸可用于除铁锈
B.氢氧化钙用于改良酸性土壤
C.氧气可用作燃料
D.明矾用于处理水中微小悬浮物
二、简答题
13.自然界中的物质在不断地发生着变化,有些变化使人类的生存环境发生了恶化,例如,随着大量化石燃料(如含硫的煤)的使用,导致酸雨频发,致使大理石建筑物遭受严重侵蚀,请根据如图,解释大理石雕像受到侵蚀的主要原因._________.
14.铁锈的主要成分是________,将一枚生锈的铁钉放入足量的稀盐酸中,你首先观察到的现象是________,过一会儿,你还可以观察到的现象是________请写出有关反应的化学方程式________。
三、推断题
15.A、B、C、D四种化合物,均含有同一种金属元素,它们的转化关系如图所示(部分物质已略去)。
己知A是大理石的主要成分。请回答下列问题:
(1)B的一种用途是_________;
(2)C的化学式为_________;
(3)B转化为D的化学方程式为__________________。
16.A~G 为初中化学常见的七种物质,其中 A、B、C、D、E 属于五种不同类别的物质(单质、氧化物、酸、碱、盐),C、G 的水溶液均呈碱性,且C 广泛应用于制取肥皂和做炉具清洁剂。D、E 中不含相同的元素。它们之间发生反应或转化的关系如图所示(“—”表示两种物质之间能发生化学反应,“→”表示两种物质之间能通过一步反应转化,部分反应物、生成物以及反应条件已略去)。请回答:
(1)C 的化学式_____________;
(2)E 和 F 反应的化学方程式______________。
四、实验题
17.某兴趣小组利用下列装置进行实验室制取并收集气体的实验,请回答:
(1)双氧水和二氧化锰制取并收集较纯净的氧气,应选用的装置组合是______(从A→E中选择字母序号),其反应的化学方程式是______。如果把60g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液来制取氧气,则需加水的质量为______g。
(2)下图是在收集氧气的过程中,会依次观察到的现象是______(用字母序号排序)。
氧气收集完毕取出集气瓶的具体操作是______。
(3)实验室用加热氯化铵固体和熟石灰混合物制取氨气,现要制取并收集干燥的氨气,装置正确连接顺序是:A→______(填字母序号)→E,请说明氨气的物理性质______(写一点)。
五、计算题
18.为了测定某铁矿石中氧化铁(Fe2O3)的质量分数,取矿石样品20g,加入稀盐酸,恰好完全反应时,共消耗稀盐酸219g,经过处理后得到滤渣4g(注:矿石中的杂质既不溶于水,也不与盐酸反应),请计算:
(1)该铁矿石中氧化铁的质量分数 。
(2)所用稀盐酸的溶质质量分数。
19.取含有MgCl2和HC1的混合溶液165.8g于烧杯中,向其中缓慢加入200g溶质质量分数为8%的NaOH溶液,恰好完全反应后过滤得到沉淀和滤液,其中滤液的质量为360g。请计算:
(1)生成沉淀的质量是多少克。
(2)原混合溶液中,MgCl2的质量是多少?(请写出具体的计算过程,下同)
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?(结果保留至0.1%)
20.取NaOH和NaCl的混合物3.63g放入烧杯中,加水溶解配制成70g溶液。向该溶液滴加溶质质量分数为7.3%的稀盐酸,测得溶液pH与滴入稀盐酸的质量关系,如图所示。
(1)当滴入稀盐酸的质量为11.2g时,此时溶液中的溶质是 。(填化学式)
(2)求原混合物中氯化钠的质量。(写出计算过程,提示:根据pH=7时消耗盐酸的质量)
参考答案:
1.C 2.A 3.C 4.B 5.B 6.B 7.B 8.B 9.A 10.B 11.A 12.C
13.大理石的主要成分是碳酸钙,碳酸钙能和酸雨中的酸性物质反应,侵蚀大理石
14. 氧化铁 溶液由无色变成黄色 产生气泡 Fe2O3+6HCl=2FeCl3+3H2O,Fe+2HCl=FeCl2+H2↑
15. 用作干燥剂 Ca(OH)2 CaO+2HCl=CaCl2+H2O
16. NaOH 2HCl+Ca(OH)2=CaCl2+2H2O
17. BC 180 bac 在水面以下盖上玻璃片、取出集气瓶,最后正放在实验台上 G 氨气的密度比空气小
18.(1)80%;(2)10%
19.(1)5.8g;(2)9.5g;(3)6.5%
20.(1)NaCl、HCl
(2)解:设氢氧化钠质量为x
3.63g-0.8g=2.83g
答:原混合物中氯化钠的质量为2.83g。
