第9章溶液检测题-2021-2022学年九年级化学京改版(2013)下册(word版 含答案)
文档属性
| 名称 | 第9章溶液检测题-2021-2022学年九年级化学京改版(2013)下册(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 67.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-22 00:00:00 | ||
图片预览


文档简介
第9章《溶液》检测题
一、单选题
1.下列物质不属于溶液的是( )
A.生理盐水 B.白醋 C.医用酒精 D.冰水混合物
2.下列关于溶液的说法正确的是
A.溶液一定是混合物
B.饱和溶液的浓度比不饱和溶液的浓度一定大
C.医用碘酒是碘的水溶液
D.添加溶质是不饱和溶液变成饱和溶液的唯一方法
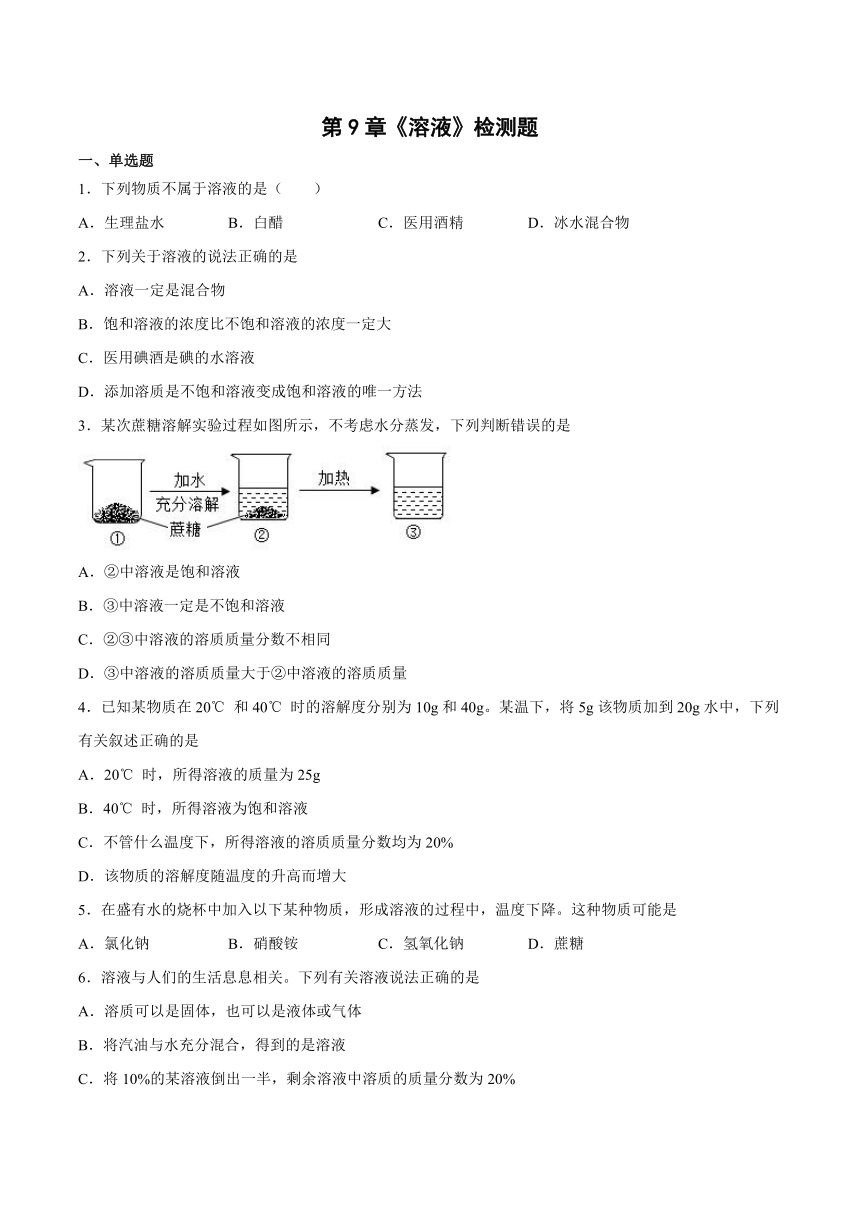
3.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
4.已知某物质在20℃ 和40℃ 时的溶解度分别为10g和40g。某温下,将5g该物质加到20g水中,下列有关叙述正确的是
A.20℃ 时,所得溶液的质量为25g
B.40℃ 时,所得溶液为饱和溶液
C.不管什么温度下,所得溶液的溶质质量分数均为20%
D.该物质的溶解度随温度的升高而增大
5.在盛有水的烧杯中加入以下某种物质,形成溶液的过程中,温度下降。这种物质可能是
A.氯化钠 B.硝酸铵 C.氢氧化钠 D.蔗糖
6.溶液与人们的生活息息相关。下列有关溶液说法正确的是
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液是t°C时的不饱和溶液
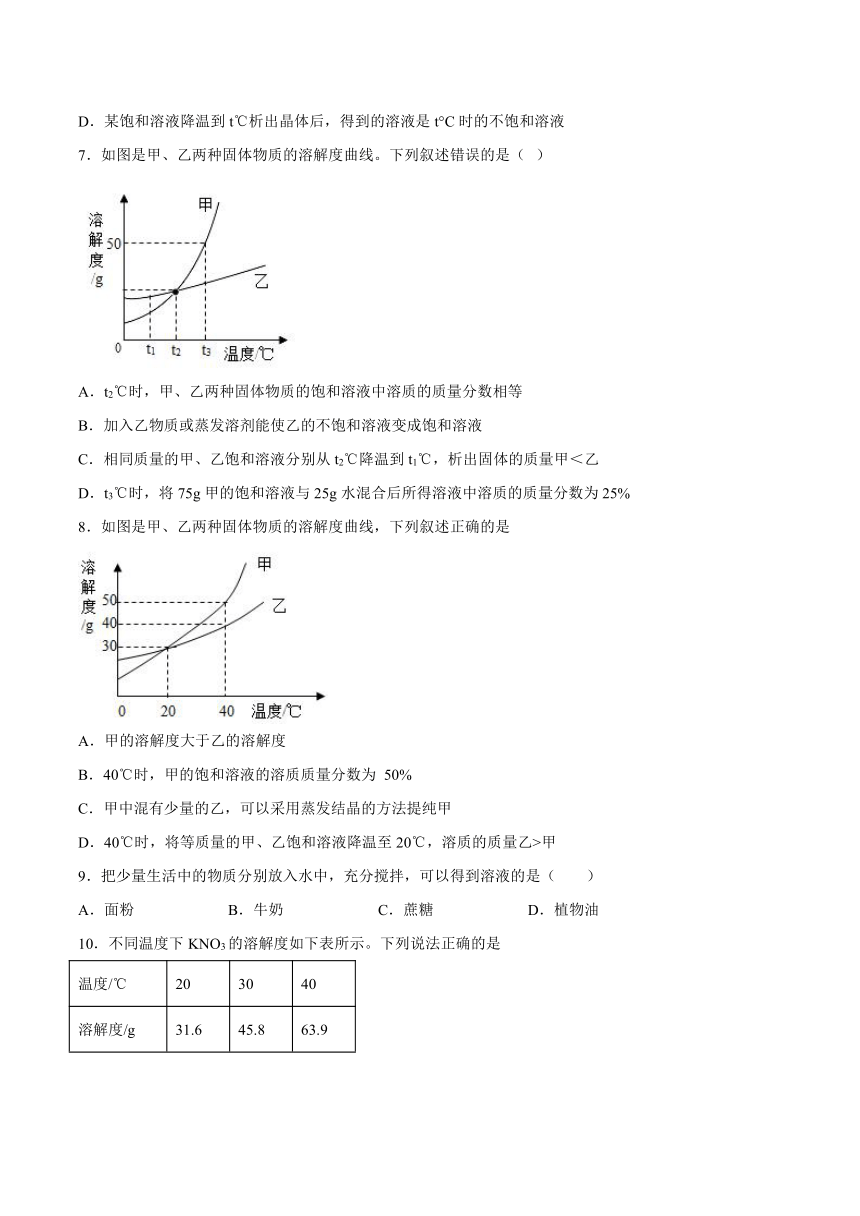
7.如图是甲、乙两种固体物质的溶解度曲线。下列叙述错误的是( )
A.t2℃时,甲、乙两种固体物质的饱和溶液中溶质的质量分数相等
B.加入乙物质或蒸发溶剂能使乙的不饱和溶液变成饱和溶液
C.相同质量的甲、乙饱和溶液分别从t2℃降温到t1℃,析出固体的质量甲<乙
D.t3℃时,将75g甲的饱和溶液与25g水混合后所得溶液中溶质的质量分数为25%
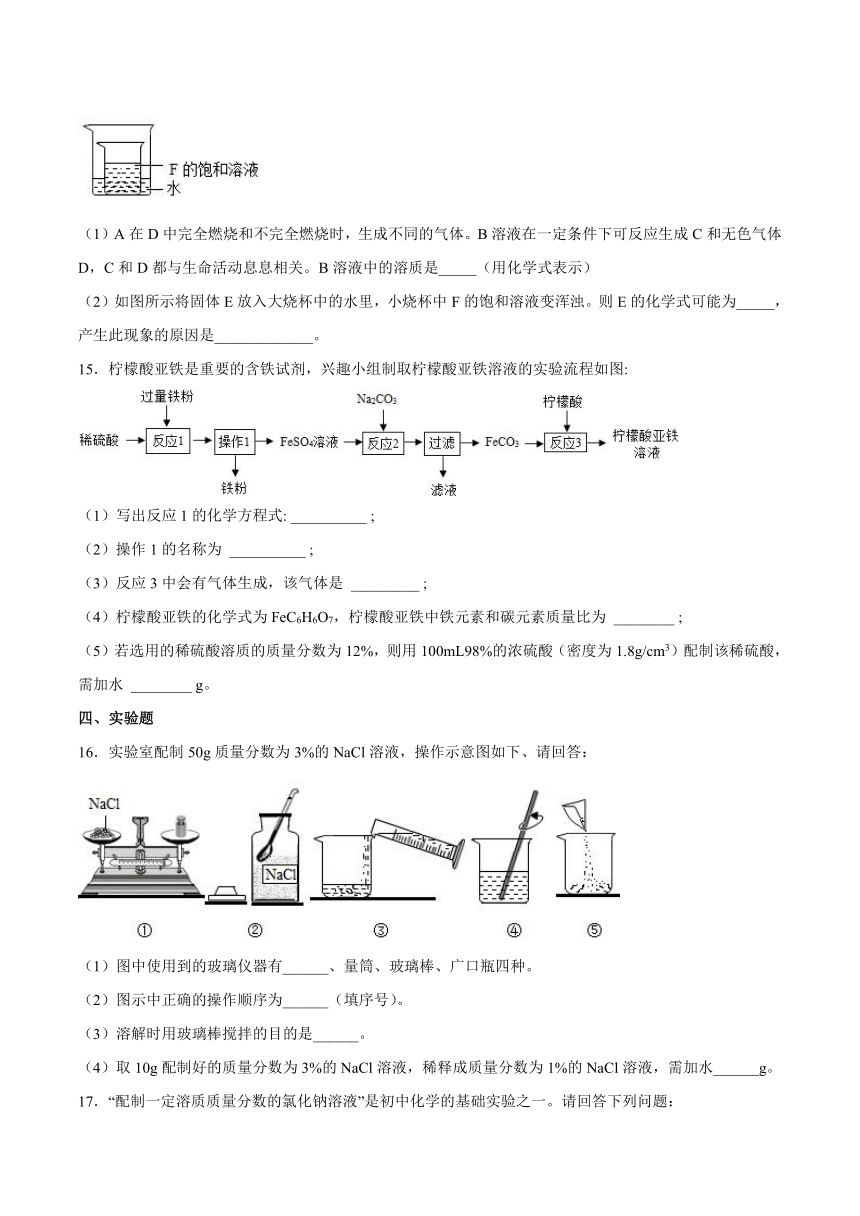
8.如图是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.40℃时,甲的饱和溶液的溶质质量分数为 50%
C.甲中混有少量的乙,可以采用蒸发结晶的方法提纯甲
D.40℃时,将等质量的甲、乙饱和溶液降温至20℃,溶质的质量乙>甲
9.把少量生活中的物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.面粉 B.牛奶 C.蔗糖 D.植物油
10.不同温度下KNO3的溶解度如下表所示。下列说法正确的是
温度/℃ 20 30 40
溶解度/g 31.6 45.8 63.9
A.20℃时,100gKNO3饱和溶液中溶质质量为31.6g
B.30℃时,100gKNO3饱和溶液的溶质质量分数为45.8%
C.30℃时,将50gKNO3放入100g水中得到150g溶液
D.40℃时,100g水最多溶解63.9gKNO3
11.20℃时,硝酸钾的溶解度为31.6g。对这句话理解错误的是
A.20℃时,100g水中最多能溶解硝酸钾31.6g
B.20℃时,100g硝酸钾饱和溶液中含硝酸钾31.6g
C.20℃时,氯化钠饱和溶液中水与硝酸钾的质量比为100∶31.6
D.20℃时,将31.6g硝酸钾溶解于100g水中,所得溶液为该温度下硝酸钾的饱和溶液
12.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是
①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①② B.①③ C.②④ D.③④
二、简答题
13.如图为KNO3和NaCl两种物质的溶解度曲线.
(1)t1℃时,两种物质溶解度的大小关系:NaCl _____ KNO3(填“>”或“=”或“<”)
(2)t2℃时,将25g氯化钠固体投入50g水中,充分溶解后可得到NaCl _____ 溶液(填“不饱和”或“饱和”或“不能确定”).
(3)将饱和KNO3溶液变为不饱和KNO3溶液,可行的方法之一是添加溶剂(水),还可以是 _____ .
(4)你从图中可获得什么信息(写出一条即可): _____ .
三、推断题
14.A、B、C、D、E、F均是初中化学中的常见物质,其中A、D为单质,其余均为化合物,B、C由两种相同元素组成。
(1)A在D中完全燃烧和不完全燃烧时,生成不同的气体。B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是_____(用化学式表示)
(2)如图所示将固体E放入大烧杯中的水里,小烧杯中F的饱和溶液变浑浊。则E的化学式可能为_____,产生此现象的原因是_____________。
15.柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:
(1)写出反应1的化学方程式: __________ ;
(2)操作1的名称为 __________ ;
(3)反应3中会有气体生成,该气体是 _________ ;
(4)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为 ________ ;
(5)若选用的稀硫酸溶质的质量分数为12%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水 ________ g。
四、实验题
16.实验室配制50g质量分数为3%的NaCl溶液,操作示意图如下、请回答:
(1)图中使用到的玻璃仪器有______、量筒、玻璃棒、广口瓶四种。
(2)图示中正确的操作顺序为______(填序号)。
(3)溶解时用玻璃棒搅拌的目的是______。
(4)取10g配制好的质量分数为3%的NaCl溶液,稀释成质量分数为1%的NaCl溶液,需加水______g。
17.“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体____g。下列实验操作与目的分析均正确的一组是____(填序号)。
项目 实验操作 目的分析
A 称量时,将取出的过量氯化钠放回原瓶 节约药品
B 溶解氯化钠时用玻璃棒搅拌 增大氯化钠的溶解度
C 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 整洁美观
D 量取所需水时,视线与量筒内液体凹液面的最低处保持水平 准确读数
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有:烧杯、玻璃棒、量筒和____。
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示。与丙烧杯中溶液溶质质量分数一定相同的是____(填序号)烧杯中的溶液。
五、计算题
18.汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2克/厘米3。若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630克。求:
(1)630克稀硫酸的体积是多少毫升_____?
(2)需要浓硫酸多少克________?
19.“84消毒液”广泛应用于物体表面的消毒,其有效成分是次氯酸钠。
(1)配制50 g溶质质量分数为12%的次氯酸钠溶液中,需要固体次氯酸钠 g;水
mL(g mL-1)。
(2)上述配制的溶液可以稀释成溶质质量分数为0.2%的次氯酸钠溶液 g。
20.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份进行实验,结果如下:
实 验 一 二 三 四
加入样品的质量/g 5 10 15 20
生成CO2的质量/g 1.76 3.52 4.4 m
(1)上表中m的数值是_____;
(2)反应中矿石有剩余是第_____次实验;
(3)这种石灰石矿中碳酸钙的质量分数是_____;
(4)稀盐酸中溶质的质量分数是多少?_____。
参考答案:
1.D 2.A 3.B 4.D 5.B 6.A 7.C 8.D 9.C 10.D 11.B
12.A
13. > 饱和 升高温度 硝酸钾的溶解度随温度升高而增大
14. H2O2 NaOH或CaO E溶于水放热
15. Fe + H2SO4 = Fe SO4 + H2↑ 过滤 CO2 7 : 9 1290
16. 烧杯 ②①⑤③④ 加速溶解 20
17. 4.5 D 胶头滴管 丁
18.(1)525毫升;(2)180克
19.(1)6;44(2)3000
20.(1)4.4(2)三、四(3)80%(4)14.6%
一、单选题
1.下列物质不属于溶液的是( )
A.生理盐水 B.白醋 C.医用酒精 D.冰水混合物
2.下列关于溶液的说法正确的是
A.溶液一定是混合物
B.饱和溶液的浓度比不饱和溶液的浓度一定大
C.医用碘酒是碘的水溶液
D.添加溶质是不饱和溶液变成饱和溶液的唯一方法
3.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
4.已知某物质在20℃ 和40℃ 时的溶解度分别为10g和40g。某温下,将5g该物质加到20g水中,下列有关叙述正确的是
A.20℃ 时,所得溶液的质量为25g
B.40℃ 时,所得溶液为饱和溶液
C.不管什么温度下,所得溶液的溶质质量分数均为20%
D.该物质的溶解度随温度的升高而增大
5.在盛有水的烧杯中加入以下某种物质,形成溶液的过程中,温度下降。这种物质可能是
A.氯化钠 B.硝酸铵 C.氢氧化钠 D.蔗糖
6.溶液与人们的生活息息相关。下列有关溶液说法正确的是
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液是t°C时的不饱和溶液
7.如图是甲、乙两种固体物质的溶解度曲线。下列叙述错误的是( )
A.t2℃时,甲、乙两种固体物质的饱和溶液中溶质的质量分数相等
B.加入乙物质或蒸发溶剂能使乙的不饱和溶液变成饱和溶液
C.相同质量的甲、乙饱和溶液分别从t2℃降温到t1℃,析出固体的质量甲<乙
D.t3℃时,将75g甲的饱和溶液与25g水混合后所得溶液中溶质的质量分数为25%
8.如图是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.40℃时,甲的饱和溶液的溶质质量分数为 50%
C.甲中混有少量的乙,可以采用蒸发结晶的方法提纯甲
D.40℃时,将等质量的甲、乙饱和溶液降温至20℃,溶质的质量乙>甲
9.把少量生活中的物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.面粉 B.牛奶 C.蔗糖 D.植物油
10.不同温度下KNO3的溶解度如下表所示。下列说法正确的是
温度/℃ 20 30 40
溶解度/g 31.6 45.8 63.9
A.20℃时,100gKNO3饱和溶液中溶质质量为31.6g
B.30℃时,100gKNO3饱和溶液的溶质质量分数为45.8%
C.30℃时,将50gKNO3放入100g水中得到150g溶液
D.40℃时,100g水最多溶解63.9gKNO3
11.20℃时,硝酸钾的溶解度为31.6g。对这句话理解错误的是
A.20℃时,100g水中最多能溶解硝酸钾31.6g
B.20℃时,100g硝酸钾饱和溶液中含硝酸钾31.6g
C.20℃时,氯化钠饱和溶液中水与硝酸钾的质量比为100∶31.6
D.20℃时,将31.6g硝酸钾溶解于100g水中,所得溶液为该温度下硝酸钾的饱和溶液
12.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是
①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①② B.①③ C.②④ D.③④
二、简答题
13.如图为KNO3和NaCl两种物质的溶解度曲线.
(1)t1℃时,两种物质溶解度的大小关系:NaCl _____ KNO3(填“>”或“=”或“<”)
(2)t2℃时,将25g氯化钠固体投入50g水中,充分溶解后可得到NaCl _____ 溶液(填“不饱和”或“饱和”或“不能确定”).
(3)将饱和KNO3溶液变为不饱和KNO3溶液,可行的方法之一是添加溶剂(水),还可以是 _____ .
(4)你从图中可获得什么信息(写出一条即可): _____ .
三、推断题
14.A、B、C、D、E、F均是初中化学中的常见物质,其中A、D为单质,其余均为化合物,B、C由两种相同元素组成。
(1)A在D中完全燃烧和不完全燃烧时,生成不同的气体。B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是_____(用化学式表示)
(2)如图所示将固体E放入大烧杯中的水里,小烧杯中F的饱和溶液变浑浊。则E的化学式可能为_____,产生此现象的原因是_____________。
15.柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:
(1)写出反应1的化学方程式: __________ ;
(2)操作1的名称为 __________ ;
(3)反应3中会有气体生成,该气体是 _________ ;
(4)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为 ________ ;
(5)若选用的稀硫酸溶质的质量分数为12%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水 ________ g。
四、实验题
16.实验室配制50g质量分数为3%的NaCl溶液,操作示意图如下、请回答:
(1)图中使用到的玻璃仪器有______、量筒、玻璃棒、广口瓶四种。
(2)图示中正确的操作顺序为______(填序号)。
(3)溶解时用玻璃棒搅拌的目的是______。
(4)取10g配制好的质量分数为3%的NaCl溶液,稀释成质量分数为1%的NaCl溶液,需加水______g。
17.“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体____g。下列实验操作与目的分析均正确的一组是____(填序号)。
项目 实验操作 目的分析
A 称量时,将取出的过量氯化钠放回原瓶 节约药品
B 溶解氯化钠时用玻璃棒搅拌 增大氯化钠的溶解度
C 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 整洁美观
D 量取所需水时,视线与量筒内液体凹液面的最低处保持水平 准确读数
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有:烧杯、玻璃棒、量筒和____。
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示。与丙烧杯中溶液溶质质量分数一定相同的是____(填序号)烧杯中的溶液。
五、计算题
18.汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2克/厘米3。若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630克。求:
(1)630克稀硫酸的体积是多少毫升_____?
(2)需要浓硫酸多少克________?
19.“84消毒液”广泛应用于物体表面的消毒,其有效成分是次氯酸钠。
(1)配制50 g溶质质量分数为12%的次氯酸钠溶液中,需要固体次氯酸钠 g;水
mL(g mL-1)。
(2)上述配制的溶液可以稀释成溶质质量分数为0.2%的次氯酸钠溶液 g。
20.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份进行实验,结果如下:
实 验 一 二 三 四
加入样品的质量/g 5 10 15 20
生成CO2的质量/g 1.76 3.52 4.4 m
(1)上表中m的数值是_____;
(2)反应中矿石有剩余是第_____次实验;
(3)这种石灰石矿中碳酸钙的质量分数是_____;
(4)稀盐酸中溶质的质量分数是多少?_____。
参考答案:
1.D 2.A 3.B 4.D 5.B 6.A 7.C 8.D 9.C 10.D 11.B
12.A
13. > 饱和 升高温度 硝酸钾的溶解度随温度升高而增大
14. H2O2 NaOH或CaO E溶于水放热
15. Fe + H2SO4 = Fe SO4 + H2↑ 过滤 CO2 7 : 9 1290
16. 烧杯 ②①⑤③④ 加速溶解 20
17. 4.5 D 胶头滴管 丁
18.(1)525毫升;(2)180克
19.(1)6;44(2)3000
20.(1)4.4(2)三、四(3)80%(4)14.6%
