【新教材】高中物理选择性必修三--3.2热力学第一定律 同步精选课件(18页ppt)
文档属性
| 名称 | 【新教材】高中物理选择性必修三--3.2热力学第一定律 同步精选课件(18页ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 262.1KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2022-03-23 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
第
节
2
热力学第一定律
高中物理 选择性必修第三册
第三章
能以系统为研究对象,用综合分析的方法推导出热力学第一定律。
能运用热力学第一定律解释和计算能量的转换、转移问题。
学习目标
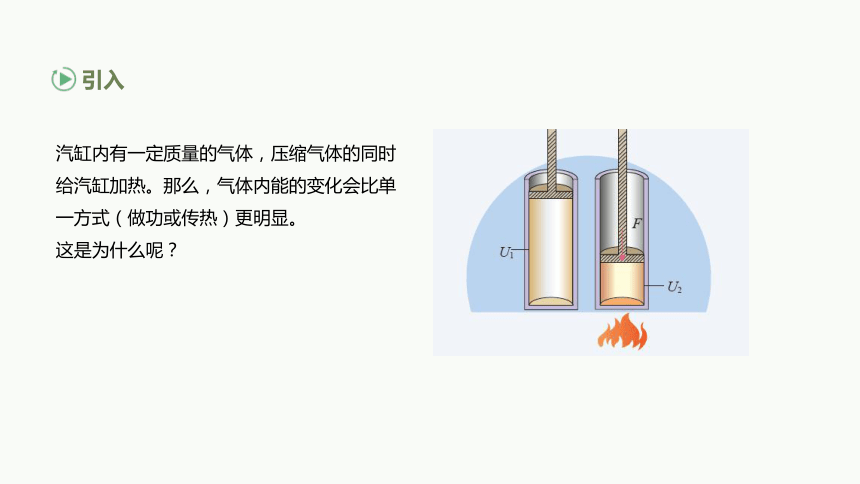
引入
汽缸内有一定质量的气体,压缩气体的同时给汽缸加热。那么,气体内能的变化会比单一方式(做功或传热)更明显。
这是为什么呢?
改变内能的两种方式
做功
热传递
对内
对外
吸热
放热
内能增加
内能增加
内能减少
内能减少
(外界对物体做功)
(物体对外界做功)
(物体从外界吸热)
(物体对外界放热)
绝热过程
仅传热过程
如果物体在跟外界同时发生做功和热传递的过程中,
内能的变化ΔU与热量Q及做的功W之间又有什么关系呢?
一、热力学第一定律
1、表述:一个热力学系统的内能增量等于外界向它传递的热量与外界对它所做的功的和.
2、意义:热力学第一定律反映了功、热量跟系统内能改变之间的定量关系.
3、数学表达式: ΔU= Q +W
思考讨论:一定质量的气体,膨胀过程中是外界对气体做功还是气体对外界做功?如果膨胀时气体对外做功是135J,同时向外放热85J,气体内能的变化量是多少?内能是增加了还是减少了?请你通过这个例子总结功和热量取正、负值的物理意义。
对外界做功
减少了220J
定律中各量的正、负号及含义
物理量 符号 意义 符号 意义
W + 外界对物体做功 - 物体对外界做功
Q + 物体吸收热量 - 物体放出热量
ΔU + 内能增加 - 内能减少
ΔU = W + Q
二、热力学第一定律的应用
例:如图,一台四冲程内燃机,活塞在压缩冲程某段时间内移动的距离为0.1 m,这段过程活塞对气体的压力逐渐增大,其做的功相当于2x 103 N的恒力使活塞移动相同距离所做的功(图3.2-2甲)。内燃机工作时汽缸温度高于环境温度,该过程中压缩气体传递给汽缸的热量为25 J。
(1)求上述压缩过程中气体内能的变化量。
(2)燃烧后的高压气体对活塞做功,气体推动活塞移动0.1 m,其做的功相当于9x103N的恒力使活塞移动相同距离所做的功(图3.2-2乙),该做功过程气体传递给汽缸的热量为30J,求此做功过程气体内能的变化量。
分析: 根据热力学第一定律,在第(1)问中,活塞压缩气体的过程是外界对系统做功,活塞对气体所做的功W1 为正值;在第(2)问中,气体膨胀推动活塞的过程是系统对外界做功,气体对外界所做的功W2 为负值。在两种情况下,气体都把热量传递给了汽缸,都属于放热,因此Q1、Q2 均为负值。
解:(1)压缩过程活塞对气体做的功W1= F1l1= 2x103x0.1 J= 200 J
气体内能的变化量ΔU1=W1+Q1=200J-25J=175J
(2)气体膨胀过程中气体对外界所做的功W2=F2l2=-9x103 x0.1J=-900J
气体内能的变化量ΔU2= W2+ Q2=- 900J- 30J=- 930J
汽缸内气体在压缩过程中内能增加了175 J,在膨胀做功过程中气体内能减少了930 J。
总结:应用热力学第一定律的解题步骤
(1)根据符号法则写出各已知量(W、Q、ΔU)的正、负.
(3)再根据未知量结果的正、负来确定吸热、放热情况或做功情况.
(2)根据方程ΔU=W+Q 求出未知量.
本课小结
1、热力学第一定律:
ΔU = W + Q
ΔU =0,则 W =- Q
W=0,则ΔU = Q
Q =0,则ΔU = W
3、方法总结:应用热力学第一定律解题的一般步骤
(1)首先应明确研究对象是哪个物体或者是哪个热力学系统。
(2)分别列出物体或系统吸收或放出的热量;外界对物体或系统所做的功或物体或系统对外所做的功。
(3)根据热力学第一定律ΔU=Q+W 列出方程进行求解。
(4)特别应注意的就是物理量的正负号及其物理意义。
2、应用
当堂检测
1.[多选]以下过程可能发生的是 ( )
A.对物体做功,物体的内能增加
B.对物体做功,同时物体吸热,物体的内能不变
C.物体对外做功,同时放热,物体的内能不变
D.物体对外做功,同时吸热,物体的内能不变
【解析】 根据热力学第一定律ΔU=Q+W判断
A对:对物体做功,物体的内能会增加。
B错:对物体做功,同时物体吸热,物体的内能增加。
C错:物体对外做功,同时放热,物体的内能减少。
D对:物体对外做功,同时吸热,且做功与吸热的数值相等,物体的内能不变。
AD
2.一定质量的理想气体在某一过程中,外界对气体做功7.0×104 J,气体内能减少1.3×105 J,则此过程( )
A.气体从外界吸收热量2.0×105 J
B.气体向外界放出热量2.0×105 J
C.气体从外界吸收热量6.0×104 J
D.气体向外界放出热量6.0×104 J
解析:根据热力学第一定律可知,Q="U-W=(-1.3×105 J)-7.0×104 J=-2.0×105 J,即气体向外界放出热量2.0×105 J。
B
3. 如图所示,绝热容器中间用隔板隔开,左侧装有气体,右侧为真空。现将隔板抽掉,让左侧气体自由膨胀到右侧直至平衡,在此过程中( )
A.气体对外界做功,温度降低,内能减少
B.气体对外界做功,温度不变,内能不变
C.气体不做功,温度不变,内能不变
D.气体不做功,温度不变,内能减少
解析:右侧为真空,气体自由膨胀没有做功“对象”,故不做功,根据热力学第一定律有:,做功W=0,因为是绝热容器,所以没有热交换,即Q=0,因此内能不变,理想气体,内能由温度决定,所以温度不变,故C正确。
C
4.如图所示,一定质量的理想气体经历A→B、B→C、C→A三个变化过程,
则:
(1)符合查理定律的变化过程是 ;C→A过程中气体 (选填“吸收”或“放出”)热量, (选填“外界对气体”或“气体对外界”)做功,气体的内能 (选填“增加”“减少”或“不变”)。
(2)已知理想气体在状态A时的温度是27 ℃,求气体在状态C时的温度是 。
【解析】(1)B→C过程中,体积不变,为等容变化过程,符合查理定律;C→A过程为等压变化,随着温度升高,气体内能增加,气体膨胀对外界做功,根据热力学第一定律可知,气体吸收热量。
(2)C→A过程中气体压强不变,由盖—吕萨克定律可知:=
解得TC=150 K。
150 K
B→C
吸收
气体对外界
增加
5.如图是用导热性能良好的材料制成的气体实验装置,开始时封闭的空气柱长度为20 cm,用竖直向下的力F压活塞,使空气柱长度变为原来的一半,人对活塞做功10 J,大气压强为p0=1×105 Pa,不计活塞的重力,求:
(1)若用足够长的时间缓慢压缩,压缩后气体的压强;
(2)若以适当的速度压缩气体,此过程气体向外散失的热量为2 J,则气体的内能增加多少?(活塞的横截面积S=1 cm2)
解:(1)设压缩后气体的压强为p,缓慢压缩,气体温度不变,由玻意耳定律:p0V0=pV
解得p=2×105 Pa。
(2)大气压力对活塞做功W1=p0SΔh=1 J,人对活塞做功W2=10 J,由热力学第一定律:ΔU=W1+W2+Q
将数据代入,解得ΔU=9 J。
谢 谢!
第
节
2
热力学第一定律
高中物理 选择性必修第三册
第三章
能以系统为研究对象,用综合分析的方法推导出热力学第一定律。
能运用热力学第一定律解释和计算能量的转换、转移问题。
学习目标
引入
汽缸内有一定质量的气体,压缩气体的同时给汽缸加热。那么,气体内能的变化会比单一方式(做功或传热)更明显。
这是为什么呢?
改变内能的两种方式
做功
热传递
对内
对外
吸热
放热
内能增加
内能增加
内能减少
内能减少
(外界对物体做功)
(物体对外界做功)
(物体从外界吸热)
(物体对外界放热)
绝热过程
仅传热过程
如果物体在跟外界同时发生做功和热传递的过程中,
内能的变化ΔU与热量Q及做的功W之间又有什么关系呢?
一、热力学第一定律
1、表述:一个热力学系统的内能增量等于外界向它传递的热量与外界对它所做的功的和.
2、意义:热力学第一定律反映了功、热量跟系统内能改变之间的定量关系.
3、数学表达式: ΔU= Q +W
思考讨论:一定质量的气体,膨胀过程中是外界对气体做功还是气体对外界做功?如果膨胀时气体对外做功是135J,同时向外放热85J,气体内能的变化量是多少?内能是增加了还是减少了?请你通过这个例子总结功和热量取正、负值的物理意义。
对外界做功
减少了220J
定律中各量的正、负号及含义
物理量 符号 意义 符号 意义
W + 外界对物体做功 - 物体对外界做功
Q + 物体吸收热量 - 物体放出热量
ΔU + 内能增加 - 内能减少
ΔU = W + Q
二、热力学第一定律的应用
例:如图,一台四冲程内燃机,活塞在压缩冲程某段时间内移动的距离为0.1 m,这段过程活塞对气体的压力逐渐增大,其做的功相当于2x 103 N的恒力使活塞移动相同距离所做的功(图3.2-2甲)。内燃机工作时汽缸温度高于环境温度,该过程中压缩气体传递给汽缸的热量为25 J。
(1)求上述压缩过程中气体内能的变化量。
(2)燃烧后的高压气体对活塞做功,气体推动活塞移动0.1 m,其做的功相当于9x103N的恒力使活塞移动相同距离所做的功(图3.2-2乙),该做功过程气体传递给汽缸的热量为30J,求此做功过程气体内能的变化量。
分析: 根据热力学第一定律,在第(1)问中,活塞压缩气体的过程是外界对系统做功,活塞对气体所做的功W1 为正值;在第(2)问中,气体膨胀推动活塞的过程是系统对外界做功,气体对外界所做的功W2 为负值。在两种情况下,气体都把热量传递给了汽缸,都属于放热,因此Q1、Q2 均为负值。
解:(1)压缩过程活塞对气体做的功W1= F1l1= 2x103x0.1 J= 200 J
气体内能的变化量ΔU1=W1+Q1=200J-25J=175J
(2)气体膨胀过程中气体对外界所做的功W2=F2l2=-9x103 x0.1J=-900J
气体内能的变化量ΔU2= W2+ Q2=- 900J- 30J=- 930J
汽缸内气体在压缩过程中内能增加了175 J,在膨胀做功过程中气体内能减少了930 J。
总结:应用热力学第一定律的解题步骤
(1)根据符号法则写出各已知量(W、Q、ΔU)的正、负.
(3)再根据未知量结果的正、负来确定吸热、放热情况或做功情况.
(2)根据方程ΔU=W+Q 求出未知量.
本课小结
1、热力学第一定律:
ΔU = W + Q
ΔU =0,则 W =- Q
W=0,则ΔU = Q
Q =0,则ΔU = W
3、方法总结:应用热力学第一定律解题的一般步骤
(1)首先应明确研究对象是哪个物体或者是哪个热力学系统。
(2)分别列出物体或系统吸收或放出的热量;外界对物体或系统所做的功或物体或系统对外所做的功。
(3)根据热力学第一定律ΔU=Q+W 列出方程进行求解。
(4)特别应注意的就是物理量的正负号及其物理意义。
2、应用
当堂检测
1.[多选]以下过程可能发生的是 ( )
A.对物体做功,物体的内能增加
B.对物体做功,同时物体吸热,物体的内能不变
C.物体对外做功,同时放热,物体的内能不变
D.物体对外做功,同时吸热,物体的内能不变
【解析】 根据热力学第一定律ΔU=Q+W判断
A对:对物体做功,物体的内能会增加。
B错:对物体做功,同时物体吸热,物体的内能增加。
C错:物体对外做功,同时放热,物体的内能减少。
D对:物体对外做功,同时吸热,且做功与吸热的数值相等,物体的内能不变。
AD
2.一定质量的理想气体在某一过程中,外界对气体做功7.0×104 J,气体内能减少1.3×105 J,则此过程( )
A.气体从外界吸收热量2.0×105 J
B.气体向外界放出热量2.0×105 J
C.气体从外界吸收热量6.0×104 J
D.气体向外界放出热量6.0×104 J
解析:根据热力学第一定律可知,Q="U-W=(-1.3×105 J)-7.0×104 J=-2.0×105 J,即气体向外界放出热量2.0×105 J。
B
3. 如图所示,绝热容器中间用隔板隔开,左侧装有气体,右侧为真空。现将隔板抽掉,让左侧气体自由膨胀到右侧直至平衡,在此过程中( )
A.气体对外界做功,温度降低,内能减少
B.气体对外界做功,温度不变,内能不变
C.气体不做功,温度不变,内能不变
D.气体不做功,温度不变,内能减少
解析:右侧为真空,气体自由膨胀没有做功“对象”,故不做功,根据热力学第一定律有:,做功W=0,因为是绝热容器,所以没有热交换,即Q=0,因此内能不变,理想气体,内能由温度决定,所以温度不变,故C正确。
C
4.如图所示,一定质量的理想气体经历A→B、B→C、C→A三个变化过程,
则:
(1)符合查理定律的变化过程是 ;C→A过程中气体 (选填“吸收”或“放出”)热量, (选填“外界对气体”或“气体对外界”)做功,气体的内能 (选填“增加”“减少”或“不变”)。
(2)已知理想气体在状态A时的温度是27 ℃,求气体在状态C时的温度是 。
【解析】(1)B→C过程中,体积不变,为等容变化过程,符合查理定律;C→A过程为等压变化,随着温度升高,气体内能增加,气体膨胀对外界做功,根据热力学第一定律可知,气体吸收热量。
(2)C→A过程中气体压强不变,由盖—吕萨克定律可知:=
解得TC=150 K。
150 K
B→C
吸收
气体对外界
增加
5.如图是用导热性能良好的材料制成的气体实验装置,开始时封闭的空气柱长度为20 cm,用竖直向下的力F压活塞,使空气柱长度变为原来的一半,人对活塞做功10 J,大气压强为p0=1×105 Pa,不计活塞的重力,求:
(1)若用足够长的时间缓慢压缩,压缩后气体的压强;
(2)若以适当的速度压缩气体,此过程气体向外散失的热量为2 J,则气体的内能增加多少?(活塞的横截面积S=1 cm2)
解:(1)设压缩后气体的压强为p,缓慢压缩,气体温度不变,由玻意耳定律:p0V0=pV
解得p=2×105 Pa。
(2)大气压力对活塞做功W1=p0SΔh=1 J,人对活塞做功W2=10 J,由热力学第一定律:ΔU=W1+W2+Q
将数据代入,解得ΔU=9 J。
谢 谢!
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
