4.3.2 羧酸的性质和应用课件
图片预览




文档简介
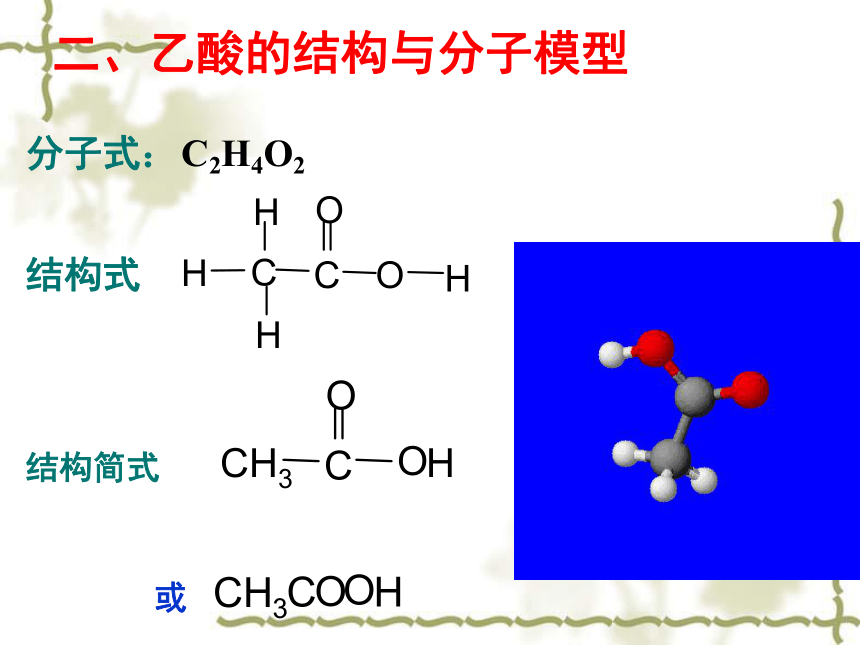
课件27张PPT。 羧酸的性质和应用醋 保 健乙 酸一、乙酸的物理性质:颜色、状态:无色液体气味:有强烈刺激性气味沸点:117.9℃ (易挥发)熔点:16.6℃(无水乙酸又称为:冰醋酸)溶解性:易溶于水、乙醇等溶剂二、乙酸的结构与分子模型分子式:结构式结构简式或C2H4O2想一想? 结 构
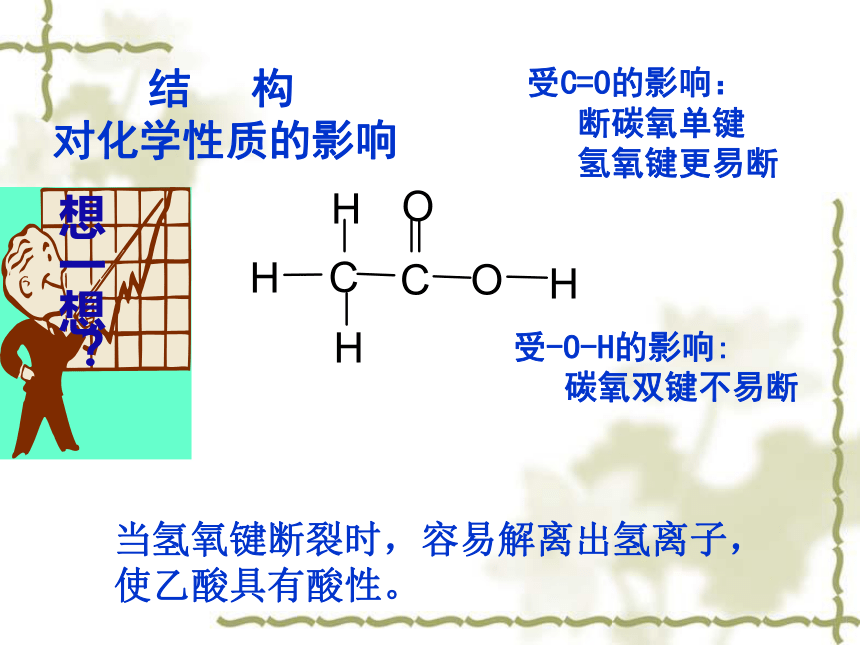
对化学性质的影响受C=O的影响:
断碳氧单键
氢氧键更易断受-O-H的影响:
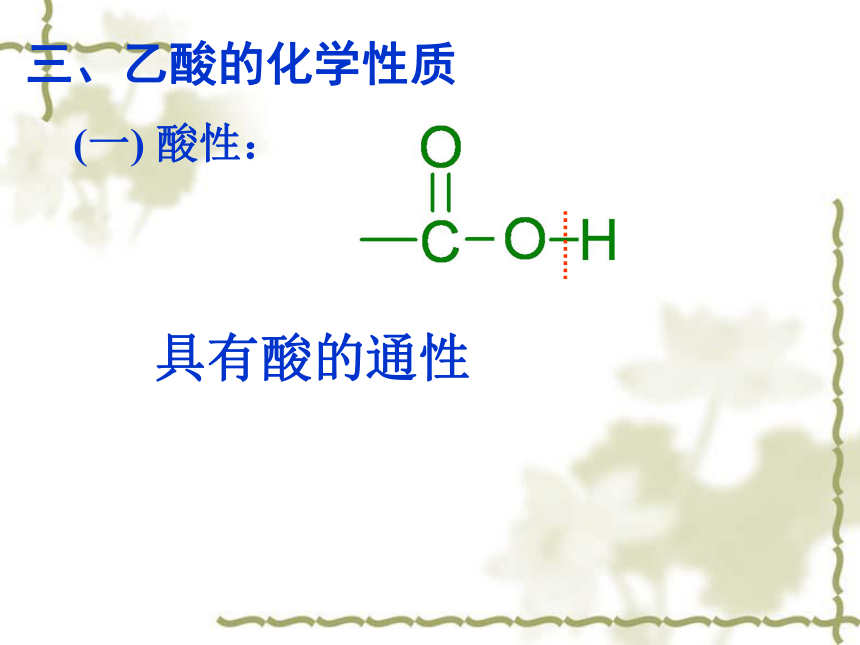
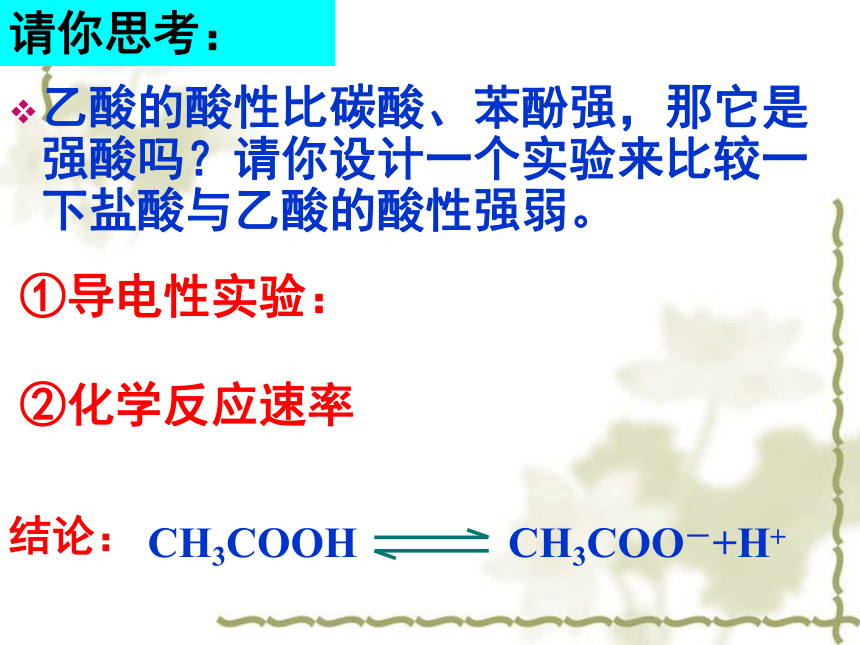
碳氧双键不易断当氢氧键断裂时,容易解离出氢离子,使乙酸具有酸性。三、乙酸的化学性质(一) 酸性:具有酸的通性乙酸的酸性比碳酸、苯酚强,那它是强酸吗?请你设计一个实验来比较一下盐酸与乙酸的酸性强弱。请你思考:①导电性实验: ②化学反应速率结论:探究:
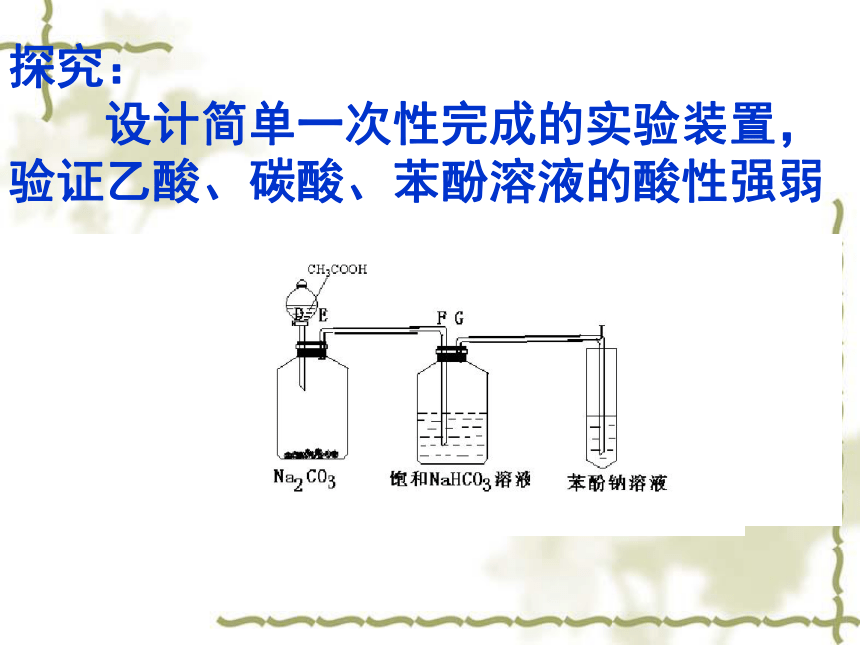
设计简单一次性完成的实验装置,
验证乙酸、碳酸、苯酚溶液的酸性强弱CH3CH2OHC6H5OHCH3COOH增强中性比碳酸弱比碳酸强能能能能能不能不能能能,不产
生CO2醇、酚、羧酸中羟基的比较【知识归纳】乙酸乙酯的实验室制备及其注意事项1.装药品的顺序如何?
2.浓硫酸的作用是什么?
3.如何提高乙酸乙酯的产率?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?能否用氢氧化钠溶液代替饱和碳酸钠溶液?
6.为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?(二)酯化反应(取代反应)催化剂,吸水剂。防止受热不匀发生倒吸乙酸乙酯制取注意事项
2. 浓硫酸的作用: 6. 导管位置高于液面的目的:① 中和乙酸,消除乙酸气味对酯气味的影响,以便
闻到乙酸乙酯的气味.
② 溶解乙醇,吸收乙醇。
③ 降低酯在水中的溶解度,以便使酯分层析出。5. 饱和碳酸钠溶液的作用: 4.杂质有:乙酸;乙醇四、乙酸乙酯的酯化过程 ——酯化反应的脱水方式同位素示踪法实验验证练习:请你完成下列方程式2、( 形成环)思考酯化反应是一个可逆反应,如果要增大乙酸乙酯的产率,你有哪些方法? (1)增大反应物的浓度例:加入过量的酸或醇(2)除去反应生成的水例:采用浓硫酸(3)及时除去反应生成的乙酸乙酯例:蒸馏出乙酸乙酯缩聚反应概念:
由有机化合物分子间脱去小分子获得高分子化合物的反应
举例:
P84推测羧基醛基推测可能发生的化学反应方程式银镜反应
与新制Cu(OH)2
与碱反应
酯化反应羧酸概念:
分子里烃基跟羧基直接相连的有机物。
饱和一元羧酸的通式:
CnH2nO2
羧酸的分类:
食物中存在的酸 CH2-COOH | HO-C-COOH | CH2-COOH柠檬酸 COOH | CH-OH | CH2
|
COOH
苹果酸 COOH | CH-OH | CH -OH
|
COOH
酒石酸 COOH | CH-OH | CH3乳酸C17H35COOH硬脂酸水杨酸分类羧基数烃基结构酯 1.酯类结构特征 (R-COOR’)(R和R’可相同可不同)
2.通式
CnH2nO2 3.酯的同分异构体:
酯类和饱和一元酸互为同分异构体
4、酯类的命名:某酸某(醇)酯(醇字省略) CH3CH2COOCH3 丙酸甲酯 5.酯类的物理性质 无色油状具有芳香味的液体,密度小于水,难溶于水,易溶于有机溶剂。
6、酯的化学性质 酯在稀硫酸或稀碱液做催化剂,加热条件下可与H2O发生水解反应说明:
(1)酯类在碱性溶液中水解生成羧酸盐 CH3COOCH2CH3+NaOH CH3COONa+C2H5OH
RCOOR'+NaOH RCOONa+R'OH
(2)甲酸某酯中,含有醛基,表现还原性,能和银氨溶液,新制氢氧化铜反应。 练习书写下列物质分别在酸性和碱性条件下的水解反应方程式
COOCH2
| |
COOCH2
CH3CH2COOCH3
练习酸牛奶中含有乳酸,结构简式为:
(1)乳酸与碳酸氢钠反应的方程式
;
(2)乳酸与钠反应的方程式________________
(3)乳酸在浓硫酸存在下二分子反应,生成物为环状时,反应方程式为_________________;
(4)乳酸发生消去反应,生成物为 ,该物质与甲醇反应,生成的有机物结构简式为 ,这一产物又可以发生加聚反应,反应方程式为 。CH3─CH─COOH
│
OH
对化学性质的影响受C=O的影响:
断碳氧单键
氢氧键更易断受-O-H的影响:
碳氧双键不易断当氢氧键断裂时,容易解离出氢离子,使乙酸具有酸性。三、乙酸的化学性质(一) 酸性:具有酸的通性乙酸的酸性比碳酸、苯酚强,那它是强酸吗?请你设计一个实验来比较一下盐酸与乙酸的酸性强弱。请你思考:①导电性实验: ②化学反应速率结论:探究:
设计简单一次性完成的实验装置,
验证乙酸、碳酸、苯酚溶液的酸性强弱CH3CH2OHC6H5OHCH3COOH增强中性比碳酸弱比碳酸强能能能能能不能不能能能,不产
生CO2醇、酚、羧酸中羟基的比较【知识归纳】乙酸乙酯的实验室制备及其注意事项1.装药品的顺序如何?
2.浓硫酸的作用是什么?
3.如何提高乙酸乙酯的产率?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?能否用氢氧化钠溶液代替饱和碳酸钠溶液?
6.为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?(二)酯化反应(取代反应)催化剂,吸水剂。防止受热不匀发生倒吸乙酸乙酯制取注意事项
2. 浓硫酸的作用: 6. 导管位置高于液面的目的:① 中和乙酸,消除乙酸气味对酯气味的影响,以便
闻到乙酸乙酯的气味.
② 溶解乙醇,吸收乙醇。
③ 降低酯在水中的溶解度,以便使酯分层析出。5. 饱和碳酸钠溶液的作用: 4.杂质有:乙酸;乙醇四、乙酸乙酯的酯化过程 ——酯化反应的脱水方式同位素示踪法实验验证练习:请你完成下列方程式2、( 形成环)思考酯化反应是一个可逆反应,如果要增大乙酸乙酯的产率,你有哪些方法? (1)增大反应物的浓度例:加入过量的酸或醇(2)除去反应生成的水例:采用浓硫酸(3)及时除去反应生成的乙酸乙酯例:蒸馏出乙酸乙酯缩聚反应概念:
由有机化合物分子间脱去小分子获得高分子化合物的反应
举例:
P84推测羧基醛基推测可能发生的化学反应方程式银镜反应
与新制Cu(OH)2
与碱反应
酯化反应羧酸概念:
分子里烃基跟羧基直接相连的有机物。
饱和一元羧酸的通式:
CnH2nO2
羧酸的分类:
食物中存在的酸 CH2-COOH | HO-C-COOH | CH2-COOH柠檬酸 COOH | CH-OH | CH2
|
COOH
苹果酸 COOH | CH-OH | CH -OH
|
COOH
酒石酸 COOH | CH-OH | CH3乳酸C17H35COOH硬脂酸水杨酸分类羧基数烃基结构酯 1.酯类结构特征 (R-COOR’)(R和R’可相同可不同)
2.通式
CnH2nO2 3.酯的同分异构体:
酯类和饱和一元酸互为同分异构体
4、酯类的命名:某酸某(醇)酯(醇字省略) CH3CH2COOCH3 丙酸甲酯 5.酯类的物理性质 无色油状具有芳香味的液体,密度小于水,难溶于水,易溶于有机溶剂。
6、酯的化学性质 酯在稀硫酸或稀碱液做催化剂,加热条件下可与H2O发生水解反应说明:
(1)酯类在碱性溶液中水解生成羧酸盐 CH3COOCH2CH3+NaOH CH3COONa+C2H5OH
RCOOR'+NaOH RCOONa+R'OH
(2)甲酸某酯中,含有醛基,表现还原性,能和银氨溶液,新制氢氧化铜反应。 练习书写下列物质分别在酸性和碱性条件下的水解反应方程式
COOCH2
| |
COOCH2
CH3CH2COOCH3
练习酸牛奶中含有乳酸,结构简式为:
(1)乳酸与碳酸氢钠反应的方程式
;
(2)乳酸与钠反应的方程式________________
(3)乳酸在浓硫酸存在下二分子反应,生成物为环状时,反应方程式为_________________;
(4)乳酸发生消去反应,生成物为 ,该物质与甲醇反应,生成的有机物结构简式为 ,这一产物又可以发生加聚反应,反应方程式为 。CH3─CH─COOH
│
OH
