第六单元 常用的金属和盐随堂练习题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第六单元 常用的金属和盐随堂练习题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 135.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-23 00:00:00 | ||
图片预览


文档简介
第6章常用的金属和盐随堂练习题2021-2022学年九年级化学沪教版(上海)第二学期
一、单选题
1.下列物质与对应的用途错误的是
A.甲醛—一用于浸泡海产品保鲜
B.氮气——用于生产氮肥
C.小苏打—一用作发酵粉焙制糕点
D.石墨——用于作电极
2.下列物质中,属于合金的是
A.不锈钢 B.氧化铁 C.铜 D.石墨
3.关于复分解反应说法一定正确的是( )
A.反应物为酸和碱 B.伴随有明显现象
C.生成物为盐和水 D.元素化合价不变
4.类推是化学学习中常用的思考方法,以下四个类推结果正确的是( )
A.有氧气参加的反应一定是氧化反应,氧化反应一定有氧气参加
B.化学变化生成了新物质,所以初中阶段有新物质生成的变化都是化学变化
C.分子是保持物质化学性质的一种微粒,保持物质化学性质的唯一微粒是分子
D.分解反应生成了多种物质,因此只要生成了两种或两种以上物质的化学反应就应该是分解反应
5.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
6.生活中的许多日常用品应用了物质的属性,以下说法不正确的是
A.冰箱的门吸应用了磁铁的磁性
B.不锈钢制作餐具利用了它的抗腐蚀性
C.铜制作导线利用了它的导热性
D.活性炭用于净化水利用了它的吸附性
7.工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理如下:
①4FeS2+11O22Fe2O3+8SO2 ②2SO2+O22SO3
③SO3+H2O=H2SO4 ④ Fe2O3+3CO2Fe+3CO2
下列说法不正确的是
A.反应①②④均是在高温条件下进行的
B.只有①②发生的是氧化反应
C.反应②③属于化合反应
D.反应①④不属于四种基本反应类型中的任何一种
8.两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是
A.该图反映出镁比锌的金属活动性强
B.a点时,两个烧杯中的酸都恰好完全反应
C.b点时,两个烧杯中产生氢气的质量相等
D.c点时,两个烧杯中都有金属剩余
9.下列化学方程式书写正确的是( )
A.2H2+O2=2H2O
B.2NaOH+H2SO4=Na2SO4+H2O
C.2Fe+6HCl=2FeCl3+3H2↑
D.2KMnO4K2MnO4+MnO2+O2↑
10.为了发展低碳经济,科学家们提出“绿色自由”构想技术流程如下图所示:把CO2含量高的气体吹入饱和K2CO3溶液中,生成KHCO3,然后利用KHCO3受热易分解的性质,再把CO2提取出来,经化学反应使之变为甲醇(CH3OH)和水(部分条件及物质未标出)。下列说法正确的是( )
A.可循环利用的物质是K2CO3,其中碳元素的化合价为-4
B.碳酸钾溶液所起的作用是富集空气中的CO2,为合成甲醇提供CO2
C.通入高温水蒸气的作用是加快CO2的逸出,以便及时为合成塔提供CO2
D.合成塔中反应的化学方程式为:CO2+3H2═CH3OH+H2O
二、简答题
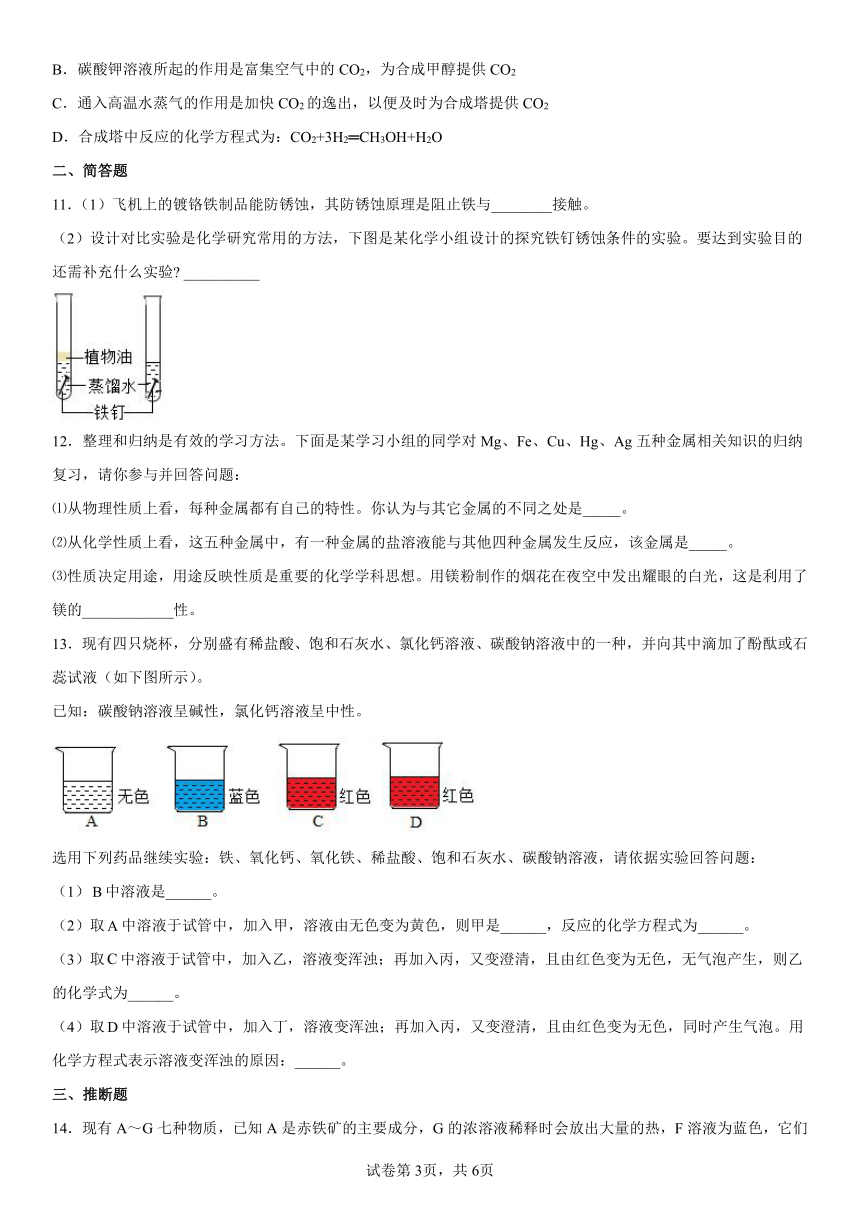
11.(1)飞机上的镀铬铁制品能防锈蚀,其防锈蚀原理是阻止铁与________接触。
(2)设计对比实验是化学研究常用的方法,下图是某化学小组设计的探究铁钉锈蚀条件的实验。要达到实验目的还需补充什么实验 __________
12.整理和归纳是有效的学习方法。下面是某学习小组的同学对Mg、Fe、Cu、Hg、Ag五种金属相关知识的归纳复习,请你参与并回答问题:
⑴从物理性质上看,每种金属都有自己的特性。你认为与其它金属的不同之处是_____。
⑵从化学性质上看,这五种金属中,有一种金属的盐溶液能与其他四种金属发生反应,该金属是_____。
⑶性质决定用途,用途反映性质是重要的化学学科思想。用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的____________性。
13.现有四只烧杯,分别盛有稀盐酸、饱和石灰水、氯化钙溶液、碳酸钠溶液中的一种,并向其中滴加了酚酞或石蕊试液(如下图所示)。
已知:碳酸钠溶液呈碱性,氯化钙溶液呈中性。
选用下列药品继续实验:铁、氧化钙、氧化铁、稀盐酸、饱和石灰水、碳酸钠溶液,请依据实验回答问题:
(1)中溶液是______。
(2)取中溶液于试管中,加入甲,溶液由无色变为黄色,则甲是______,反应的化学方程式为______。
(3)取中溶液于试管中,加入乙,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,无气泡产生,则乙的化学式为______。
(4)取中溶液于试管中,加入丁,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,同时产生气泡。用化学方程式表示溶液变浑浊的原因:______。
三、推断题
14.现有A~G七种物质,已知A是赤铁矿的主要成分,G的浓溶液稀释时会放出大量的热,F溶液为蓝色,它们之间存在如图所示的转化关系:
(1)写出下列物质的化学式:A_______;
(2)在反应①②③中,属于置换反应的是_______(填序号);
(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式_______;
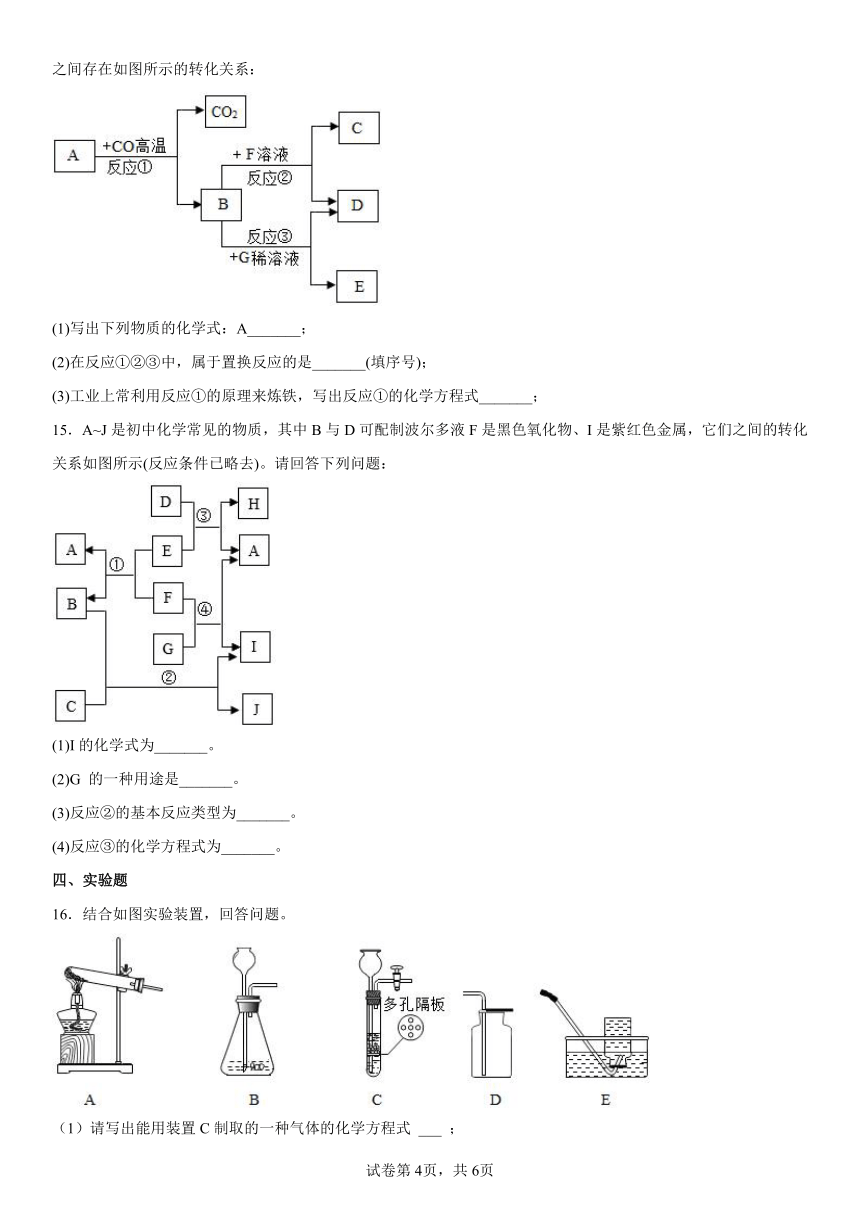
15.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
四、实验题
16.结合如图实验装置,回答问题。
(1)请写出能用装置C制取的一种气体的化学方程式 ___ ;
(2)某气体只能用E装置收集,写出该气体一定具有的性质 ___ 。
17.用如图装置进行实验。实验时,先将浓氢氧化钠溶液挤入盛有CO2的试管中,振荡;然后将止水夹K打开。
(1)A中发生反应的化学方程式为 _____ 。
(2)打开止水夹K后,观察到的现象是 _____ 。
18.根据如图实验装置图,回答相关问题。
(1)甲是测定空气中氧气含量的两个实验,实验时发现实验B测量更准确,原因是___。
(2)乙中铁钉最易生锈的部位是___(填“a”或“b”)。
(3)丙中①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球,缓慢通入CO2后,最先变红的是___。(填编号,下同)不变红的是___。
(4)丁是探究Cu和Ag的金属活动性顺序,无色溶液可能是___(填编号)。
①稀H2SO4
②FeSO4溶液
③Cu(NO3)2溶液
④AgNO3溶液
写出相应反应的化学方程式___。
五、计算题
19.黄铜的主要成分是铜锌合金,将10g黄铜与足量稀硫酸反应,生成0.1g氢气,求该黄铜中铜的质量分数。
20.尿素是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。试计算尿素中氮元素的质量分数。
21.将2.8g铁粉加入160g一定溶质质量分数的硫酸铜溶液中,恰好完全反应后过滤,得到滤液159.6g。求:
(1)生成铜的质量是 ______g。
(2)原硫酸铜溶液的溶质质量分数。
22.某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案,取100g上述废液,向其中加入2.8g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%,求:
⑴回收得到铜的质量为多少_______?(写出计算过程)
⑵回收得到硫酸亚铁的质量是_____g(计算结果保留两位小数)。
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.A
3.D
4.B
5.A
6.C
7.B
8.D
9.D
10.B
11. 氧气和水 补充铁钉在干燥的空气中不发生锈蚀的实验
12. 常温下,Hg是液体而其余均为固体 Ag(或银) 可燃
13. 饱和石灰水或碳酸钠溶液 氧化铁
14. Fe2O3 ②③ 3CO+Fe2O32Fe+3CO2
15. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
16. CaCO3+2HCl=CaCl2+H2O+CO2↑ 或Zn+H2SO4=ZnSO4+H2↑ 一定具有不溶于水,不与水反应的性质
17. CO2+2NaOH=Na2CO3+H2O B中澄清石灰水流到A中,A中液体变浑浊
18. 装置始终密封,气密性更好 b ④ ②③ ④ Cu+2AgNO3═Cu(NO3)2+2Ag
19.解:锌的质量为x
答:黄铜中铜的质量分数为67.5%。
20.尿素中氮元素的质量分数为:。
21.(1)3.2
(2)解:设硫酸铜的质量为x
x=8g
原硫酸铜溶液的溶质质量分数为:
答:原硫酸铜溶液的溶质质量分数5%。
22.(1)3.2g,(2)14.94g
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质与对应的用途错误的是
A.甲醛—一用于浸泡海产品保鲜
B.氮气——用于生产氮肥
C.小苏打—一用作发酵粉焙制糕点
D.石墨——用于作电极
2.下列物质中,属于合金的是
A.不锈钢 B.氧化铁 C.铜 D.石墨
3.关于复分解反应说法一定正确的是( )
A.反应物为酸和碱 B.伴随有明显现象
C.生成物为盐和水 D.元素化合价不变
4.类推是化学学习中常用的思考方法,以下四个类推结果正确的是( )
A.有氧气参加的反应一定是氧化反应,氧化反应一定有氧气参加
B.化学变化生成了新物质,所以初中阶段有新物质生成的变化都是化学变化
C.分子是保持物质化学性质的一种微粒,保持物质化学性质的唯一微粒是分子
D.分解反应生成了多种物质,因此只要生成了两种或两种以上物质的化学反应就应该是分解反应
5.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
6.生活中的许多日常用品应用了物质的属性,以下说法不正确的是
A.冰箱的门吸应用了磁铁的磁性
B.不锈钢制作餐具利用了它的抗腐蚀性
C.铜制作导线利用了它的导热性
D.活性炭用于净化水利用了它的吸附性
7.工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理如下:
①4FeS2+11O22Fe2O3+8SO2 ②2SO2+O22SO3
③SO3+H2O=H2SO4 ④ Fe2O3+3CO2Fe+3CO2
下列说法不正确的是
A.反应①②④均是在高温条件下进行的
B.只有①②发生的是氧化反应
C.反应②③属于化合反应
D.反应①④不属于四种基本反应类型中的任何一种
8.两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是
A.该图反映出镁比锌的金属活动性强
B.a点时,两个烧杯中的酸都恰好完全反应
C.b点时,两个烧杯中产生氢气的质量相等
D.c点时,两个烧杯中都有金属剩余
9.下列化学方程式书写正确的是( )
A.2H2+O2=2H2O
B.2NaOH+H2SO4=Na2SO4+H2O
C.2Fe+6HCl=2FeCl3+3H2↑
D.2KMnO4K2MnO4+MnO2+O2↑
10.为了发展低碳经济,科学家们提出“绿色自由”构想技术流程如下图所示:把CO2含量高的气体吹入饱和K2CO3溶液中,生成KHCO3,然后利用KHCO3受热易分解的性质,再把CO2提取出来,经化学反应使之变为甲醇(CH3OH)和水(部分条件及物质未标出)。下列说法正确的是( )
A.可循环利用的物质是K2CO3,其中碳元素的化合价为-4
B.碳酸钾溶液所起的作用是富集空气中的CO2,为合成甲醇提供CO2
C.通入高温水蒸气的作用是加快CO2的逸出,以便及时为合成塔提供CO2
D.合成塔中反应的化学方程式为:CO2+3H2═CH3OH+H2O
二、简答题
11.(1)飞机上的镀铬铁制品能防锈蚀,其防锈蚀原理是阻止铁与________接触。
(2)设计对比实验是化学研究常用的方法,下图是某化学小组设计的探究铁钉锈蚀条件的实验。要达到实验目的还需补充什么实验 __________
12.整理和归纳是有效的学习方法。下面是某学习小组的同学对Mg、Fe、Cu、Hg、Ag五种金属相关知识的归纳复习,请你参与并回答问题:
⑴从物理性质上看,每种金属都有自己的特性。你认为与其它金属的不同之处是_____。
⑵从化学性质上看,这五种金属中,有一种金属的盐溶液能与其他四种金属发生反应,该金属是_____。
⑶性质决定用途,用途反映性质是重要的化学学科思想。用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的____________性。
13.现有四只烧杯,分别盛有稀盐酸、饱和石灰水、氯化钙溶液、碳酸钠溶液中的一种,并向其中滴加了酚酞或石蕊试液(如下图所示)。
已知:碳酸钠溶液呈碱性,氯化钙溶液呈中性。
选用下列药品继续实验:铁、氧化钙、氧化铁、稀盐酸、饱和石灰水、碳酸钠溶液,请依据实验回答问题:
(1)中溶液是______。
(2)取中溶液于试管中,加入甲,溶液由无色变为黄色,则甲是______,反应的化学方程式为______。
(3)取中溶液于试管中,加入乙,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,无气泡产生,则乙的化学式为______。
(4)取中溶液于试管中,加入丁,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,同时产生气泡。用化学方程式表示溶液变浑浊的原因:______。
三、推断题
14.现有A~G七种物质,已知A是赤铁矿的主要成分,G的浓溶液稀释时会放出大量的热,F溶液为蓝色,它们之间存在如图所示的转化关系:
(1)写出下列物质的化学式:A_______;
(2)在反应①②③中,属于置换反应的是_______(填序号);
(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式_______;
15.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
四、实验题
16.结合如图实验装置,回答问题。
(1)请写出能用装置C制取的一种气体的化学方程式 ___ ;
(2)某气体只能用E装置收集,写出该气体一定具有的性质 ___ 。
17.用如图装置进行实验。实验时,先将浓氢氧化钠溶液挤入盛有CO2的试管中,振荡;然后将止水夹K打开。
(1)A中发生反应的化学方程式为 _____ 。
(2)打开止水夹K后,观察到的现象是 _____ 。
18.根据如图实验装置图,回答相关问题。
(1)甲是测定空气中氧气含量的两个实验,实验时发现实验B测量更准确,原因是___。
(2)乙中铁钉最易生锈的部位是___(填“a”或“b”)。
(3)丙中①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球,缓慢通入CO2后,最先变红的是___。(填编号,下同)不变红的是___。
(4)丁是探究Cu和Ag的金属活动性顺序,无色溶液可能是___(填编号)。
①稀H2SO4
②FeSO4溶液
③Cu(NO3)2溶液
④AgNO3溶液
写出相应反应的化学方程式___。
五、计算题
19.黄铜的主要成分是铜锌合金,将10g黄铜与足量稀硫酸反应,生成0.1g氢气,求该黄铜中铜的质量分数。
20.尿素是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。试计算尿素中氮元素的质量分数。
21.将2.8g铁粉加入160g一定溶质质量分数的硫酸铜溶液中,恰好完全反应后过滤,得到滤液159.6g。求:
(1)生成铜的质量是 ______g。
(2)原硫酸铜溶液的溶质质量分数。
22.某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案,取100g上述废液,向其中加入2.8g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%,求:
⑴回收得到铜的质量为多少_______?(写出计算过程)
⑵回收得到硫酸亚铁的质量是_____g(计算结果保留两位小数)。
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.A
3.D
4.B
5.A
6.C
7.B
8.D
9.D
10.B
11. 氧气和水 补充铁钉在干燥的空气中不发生锈蚀的实验
12. 常温下,Hg是液体而其余均为固体 Ag(或银) 可燃
13. 饱和石灰水或碳酸钠溶液 氧化铁
14. Fe2O3 ②③ 3CO+Fe2O32Fe+3CO2
15. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
16. CaCO3+2HCl=CaCl2+H2O+CO2↑ 或Zn+H2SO4=ZnSO4+H2↑ 一定具有不溶于水,不与水反应的性质
17. CO2+2NaOH=Na2CO3+H2O B中澄清石灰水流到A中,A中液体变浑浊
18. 装置始终密封,气密性更好 b ④ ②③ ④ Cu+2AgNO3═Cu(NO3)2+2Ag
19.解:锌的质量为x
答:黄铜中铜的质量分数为67.5%。
20.尿素中氮元素的质量分数为:。
21.(1)3.2
(2)解:设硫酸铜的质量为x
x=8g
原硫酸铜溶液的溶质质量分数为:
答:原硫酸铜溶液的溶质质量分数5%。
22.(1)3.2g,(2)14.94g
答案第1页,共2页
答案第1页,共2页
