第六单元 常用的金属和盐单元训练-2021-2022学年九年级化学沪教版(上海)下册(word版有答案)
文档属性
| 名称 | 第六单元 常用的金属和盐单元训练-2021-2022学年九年级化学沪教版(上海)下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 236.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-23 00:00:00 | ||
图片预览

文档简介
第6章常用的金属和盐基础练习题2021-2022学年九年级化学沪教版(上海)第二学期
一、单选题
1.东汉时期的“马踏飞燕”堪称我国古代青铜器艺术中无与伦比的珍品。其制作材料属于
A.合成材料
B.天然材料
C.金属材料
D.复合材料
2.我国首架试飞成功的大型客机C919机壳采用了先进的铝锂合金材料,下列不属于锂铝合金在飞机制造中使用的优点的是
A.硬度大 B.密度小 C.易导电 D.耐腐蚀
3.醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
4.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
5.十一世纪,中国就用“卓筒井”凿井技术获取食盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
6.为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是
A.MgCl2溶液、Cu、Sn
B.Mg、Cu、SnCl2溶液
C.Mg、Sn、Cu、盐酸
D.MgCl2溶液、Sn、CuCl2溶液
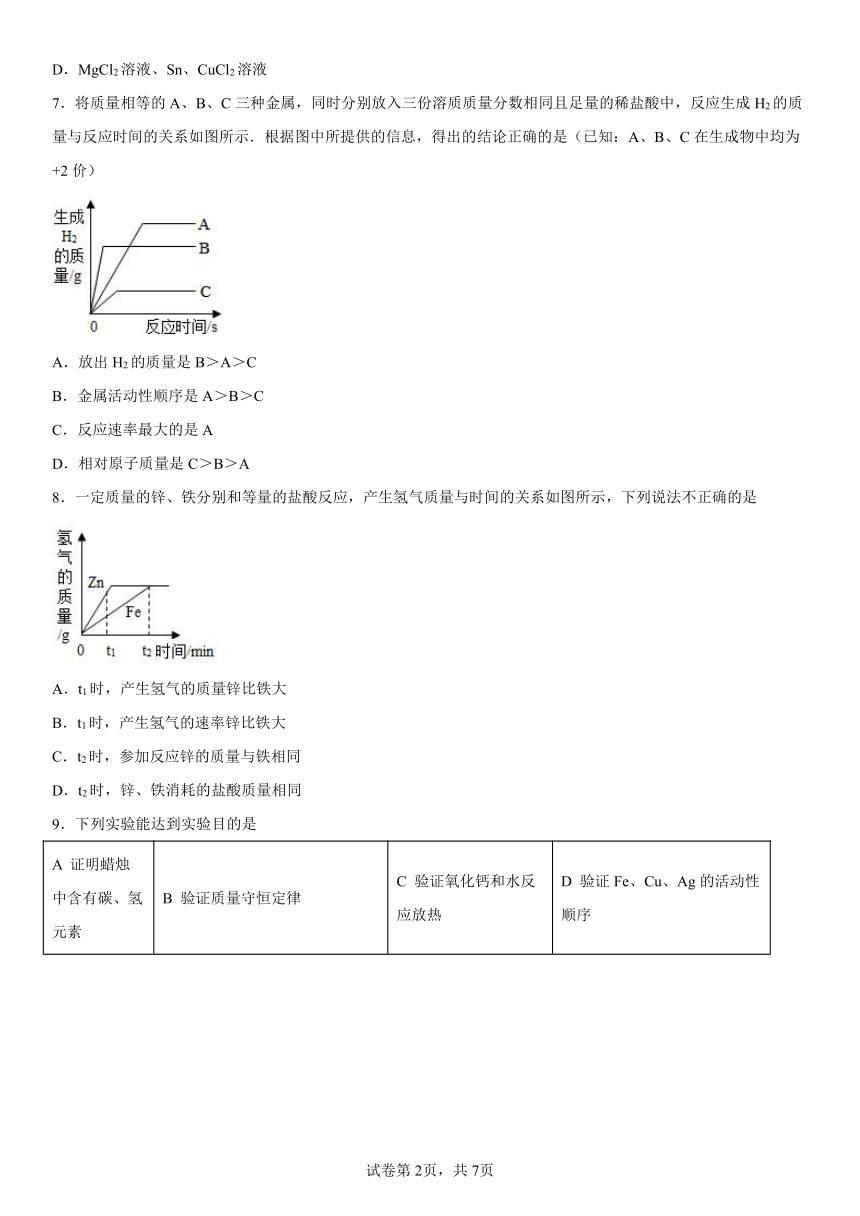
7.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
8.一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
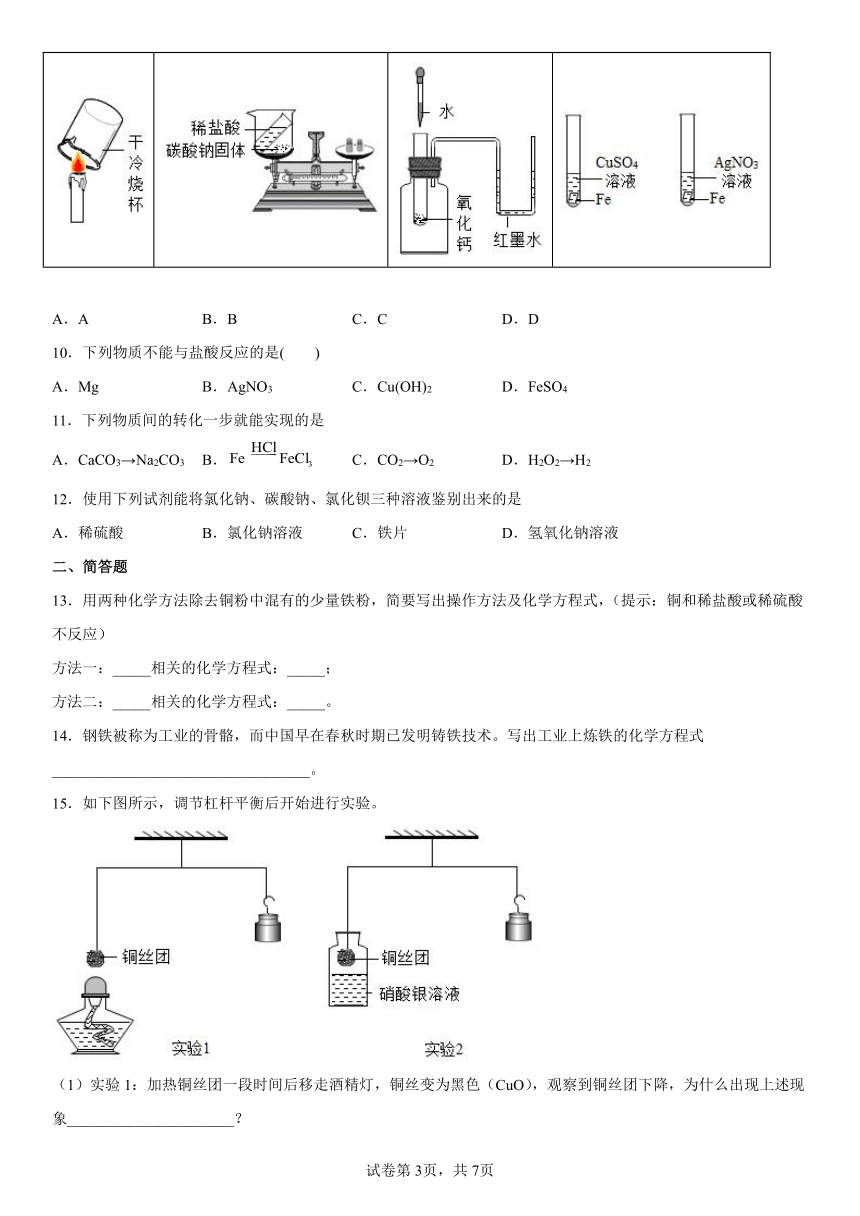
9.下列实验能达到实验目的是
A 证明蜡烛中含有碳、氢元素 B 验证质量守恒定律 C 验证氧化钙和水反应放热 D 验证Fe、Cu、Ag的活动性顺序
A.A B.B C.C D.D
10.下列物质不能与盐酸反应的是( )
A.Mg B.AgNO3 C.Cu(OH)2 D.FeSO4
11.下列物质间的转化一步就能实现的是
A.CaCO3→Na2CO3 B. C.CO2→O2 D.H2O2→H2
12.使用下列试剂能将氯化钠、碳酸钠、氯化钡三种溶液鉴别出来的是
A.稀硫酸 B.氯化钠溶液 C.铁片 D.氢氧化钠溶液
二、简答题
13.用两种化学方法除去铜粉中混有的少量铁粉,简要写出操作方法及化学方程式,(提示:铜和稀盐酸或稀硫酸不反应)
方法一:_____相关的化学方程式:_____;
方法二:_____相关的化学方程式:_____。
14.钢铁被称为工业的骨骼,而中国早在春秋时期已发明铸铁技术。写出工业上炼铁的化学方程式__________________________________。
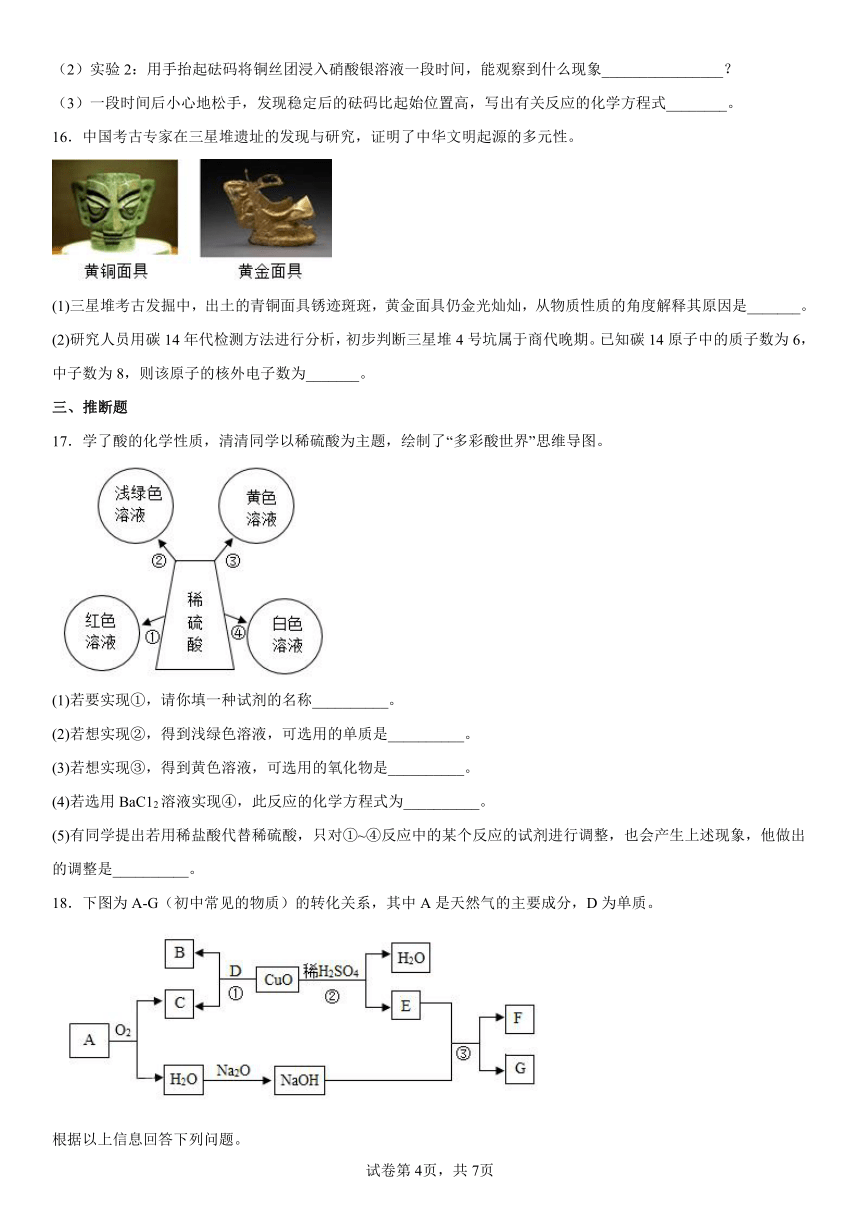
15.如下图所示,调节杠杆平衡后开始进行实验。
(1)实验1:加热铜丝团一段时间后移走酒精灯,铜丝变为黑色(CuO),观察到铜丝团下降,为什么出现上述现象______________________?
(2)实验2:用手抬起砝码将铜丝团浸入硝酸银溶液一段时间,能观察到什么现象________________?
(3)一段时间后小心地松手,发现稳定后的砝码比起始位置高,写出有关反应的化学方程式________。
16.中国考古专家在三星堆遗址的发现与研究,证明了中华文明起源的多元性。
(1)三星堆考古发掘中,出土的青铜面具锈迹斑斑,黄金面具仍金光灿灿,从物质性质的角度解释其原因是_______。
(2)研究人员用碳14年代检测方法进行分析,初步判断三星堆4号坑属于商代晚期。已知碳14原子中的质子数为6,中子数为8,则该原子的核外电子数为_______。
三、推断题
17.学了酸的化学性质,清清同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若要实现①,请你填一种试剂的名称__________。
(2)若想实现②,得到浅绿色溶液,可选用的单质是__________。
(3)若想实现③,得到黄色溶液,可选用的氧化物是__________。
(4)若选用BaC12溶液实现④,此反应的化学方程式为__________。
(5)有同学提出若用稀盐酸代替稀硫酸,只对①~④反应中的某个反应的试剂进行调整,也会产生上述现象,他做出的调整是__________。
18.下图为A-G(初中常见的物质)的转化关系,其中A是天然气的主要成分,D为单质。
根据以上信息回答下列问题。
(1)写出A 的化学式_____,其常见用途为_____(任写一条)。
(2)写出反应①化学方程式_____,该反应属于_____反应(填基本反应类型)。
(3)反应的②现象为_____。
(4)写出反应③的化学方程式_____。
19.如图A、B、C三种物质都含有同一种元素,B是单质,A、C都是氧化物,且A是红色固体。请回答:
(1)写出A的化学式____________;
(2)写出反应①的化学方程式并注明反应类型_____________;_____________。
(3)写出物质C与一种燃烧产物只有水的清洁燃料反应的化学方程式:____________。
四、实验题
20.钢铁是重要的金属材料,人类每年要从自然界获取大量的铁矿资源.
(1)目前世界上已有以上的废钢铁得到回收利用,其目的是________.
A 节约金属资源 B 合理开采矿物 C 防止钢铁生锈
(2)工业上高炉炼铁得到的主要产品是________;(填序号)
A 纯铁 B 生铁 C 钢
(3)一位同学准备在实验室用下图所示装置模拟工业炼铁.请你据此回答下列问题:
①实验中硬质玻璃管里的现象是:_____;硬质玻璃管里发生反应的方程式为_____.
②装置图中澄清石灰水的作用是_____.
③某同学实验完成后,发现过量的澄清石灰水增重0.44g,则该同学通入装置的CO气体质量_____(填“大于”、“小于”或“等于”)0.28g,原因是_____.
(4)某钢铁厂每天消耗5000t含氧化铁84%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是_____?
21.某兴趣小组做了如下实验:
①在止水夹K1、K2处于关闭状态时,将针筒A中溶液挤入试管B中,接着打开止水夹K1,发现D中的部分溶液被吸入试管B中,充分反应后,试管B留下的溶液也显红色;
②打开止水夹K2,风哨振动鸣叫,C中的部分溶液被吸入B和D中,反应后B、D中溶液都变为无色。
回答:
(1)步骤①中,充分反应后,试管B里的CO2最终转化为___________(填化学式)和水。
(2)解释步骤②中“风哨振动鸣叫”的原因___________。
(3)实验开始时C、D中两种溶液中溶质质量分数大小关系为:a%___________b%(选填“>”“=”“<”)。
22.下图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:
(1)描述A中的实验现象________。
(2)写出C中反应的化学方程式__________。
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是___________(填序号)。
(4)开始反应后D中溶液逐渐变为黄色,原因是__________。
五、计算题
23.工业用焦炭还原100kg含Fe2O380%的赤铁矿,理论上可炼得铁的质量为多少?(请写出解题步骤)
24.将20g含有杂质的锌粒放入烧杯中,然后向其中逐渐滴加稀硫酸50g至反应停止,(杂质不参加反应),此时称量烧杯内物质的总质量为69.6g.试计算:
(1)生成氢气的质量为______g.
(2)该锌粒中锌的质量分数.
25.白铜(Cu-Ni)是工业上常用的一种合金,金属镍(Ni)的金属活泼性与铁相似,且化合价显+2价。为测定20g某白铜样品中镍的质量,设计了如下实验:
试问:(1)将白铜研碎的目的是 。
(2)白铜样品中镍的质量 g。
(3)所用稀硫酸中溶质的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.B
5.C
6.A
7.D
8.C
9.C
10.D
11.C
12.A
13. 加入过量的稀硫酸后过滤 Fe+H2SO4═FeSO4+H2↑ 加入过量的硫酸铜溶液后过滤 Fe+CuSO4═FeSO4+Cu
14.2
15. Cu与氧气反应,在表面生成质量更大的CuO 溶液由无色变蓝色 2AgNO3+Cu=Cu(NO3)2+2Ag
16. 黄金金属活动性弱,不容易发生化学反应,青铜中金属活动性强,容易发生化学反应 6
17.(1)紫色石蕊试液
(2)Fe##铁
(3)Fe2O3##氧化铁
(4)
(5)将第④试剂调换为硝酸银(AgNO3)
18. CH4 作燃料 C+2CuO2Cu+CO2↑ 置换 黑色粉末逐渐减少,溶液逐渐变成了蓝色 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
19.(1)Fe2O3
(2) 或 置换反应
(3)
20. A B 红色粉末变成黑色 Fe2O3+3CO2Fe+3CO2 检验有二氧化碳生成 大于 实验开始或结束都要通入一氧化碳,故该实验中实验用量大于量论用量 该厂理论上可日产含铁98%的生铁的质量是3000t
21. Na2CO3 B中二氧化碳和氢氧化钠反应,气体减少,压强减小,在外界大气压的作用下,空气进入C中 >
22. 铜丝表面附着一层银白色固体,溶液变为蓝色 A、B 铁钉未打磨有铁锈或溶液中有Fe2(SO4)3生成
23.解:设理论上可炼得铁的质量为x
答:理论上可炼得铁的质量为56kg。
24.(1)0.4
(2)解:设该锌粒中锌的质量分数为x
x=65%
答:该锌粒中锌的质量分数为65%。
25.(1)增大白铜与稀硫酸的接触面积,使反应更快、更充分(2)2.95(3)9.8%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.东汉时期的“马踏飞燕”堪称我国古代青铜器艺术中无与伦比的珍品。其制作材料属于
A.合成材料
B.天然材料
C.金属材料
D.复合材料
2.我国首架试飞成功的大型客机C919机壳采用了先进的铝锂合金材料,下列不属于锂铝合金在飞机制造中使用的优点的是
A.硬度大 B.密度小 C.易导电 D.耐腐蚀
3.醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
4.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
5.十一世纪,中国就用“卓筒井”凿井技术获取食盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
6.为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是
A.MgCl2溶液、Cu、Sn
B.Mg、Cu、SnCl2溶液
C.Mg、Sn、Cu、盐酸
D.MgCl2溶液、Sn、CuCl2溶液
7.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
8.一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
9.下列实验能达到实验目的是
A 证明蜡烛中含有碳、氢元素 B 验证质量守恒定律 C 验证氧化钙和水反应放热 D 验证Fe、Cu、Ag的活动性顺序
A.A B.B C.C D.D
10.下列物质不能与盐酸反应的是( )
A.Mg B.AgNO3 C.Cu(OH)2 D.FeSO4
11.下列物质间的转化一步就能实现的是
A.CaCO3→Na2CO3 B. C.CO2→O2 D.H2O2→H2
12.使用下列试剂能将氯化钠、碳酸钠、氯化钡三种溶液鉴别出来的是
A.稀硫酸 B.氯化钠溶液 C.铁片 D.氢氧化钠溶液
二、简答题
13.用两种化学方法除去铜粉中混有的少量铁粉,简要写出操作方法及化学方程式,(提示:铜和稀盐酸或稀硫酸不反应)
方法一:_____相关的化学方程式:_____;
方法二:_____相关的化学方程式:_____。
14.钢铁被称为工业的骨骼,而中国早在春秋时期已发明铸铁技术。写出工业上炼铁的化学方程式__________________________________。
15.如下图所示,调节杠杆平衡后开始进行实验。
(1)实验1:加热铜丝团一段时间后移走酒精灯,铜丝变为黑色(CuO),观察到铜丝团下降,为什么出现上述现象______________________?
(2)实验2:用手抬起砝码将铜丝团浸入硝酸银溶液一段时间,能观察到什么现象________________?
(3)一段时间后小心地松手,发现稳定后的砝码比起始位置高,写出有关反应的化学方程式________。
16.中国考古专家在三星堆遗址的发现与研究,证明了中华文明起源的多元性。
(1)三星堆考古发掘中,出土的青铜面具锈迹斑斑,黄金面具仍金光灿灿,从物质性质的角度解释其原因是_______。
(2)研究人员用碳14年代检测方法进行分析,初步判断三星堆4号坑属于商代晚期。已知碳14原子中的质子数为6,中子数为8,则该原子的核外电子数为_______。
三、推断题
17.学了酸的化学性质,清清同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若要实现①,请你填一种试剂的名称__________。
(2)若想实现②,得到浅绿色溶液,可选用的单质是__________。
(3)若想实现③,得到黄色溶液,可选用的氧化物是__________。
(4)若选用BaC12溶液实现④,此反应的化学方程式为__________。
(5)有同学提出若用稀盐酸代替稀硫酸,只对①~④反应中的某个反应的试剂进行调整,也会产生上述现象,他做出的调整是__________。
18.下图为A-G(初中常见的物质)的转化关系,其中A是天然气的主要成分,D为单质。
根据以上信息回答下列问题。
(1)写出A 的化学式_____,其常见用途为_____(任写一条)。
(2)写出反应①化学方程式_____,该反应属于_____反应(填基本反应类型)。
(3)反应的②现象为_____。
(4)写出反应③的化学方程式_____。
19.如图A、B、C三种物质都含有同一种元素,B是单质,A、C都是氧化物,且A是红色固体。请回答:
(1)写出A的化学式____________;
(2)写出反应①的化学方程式并注明反应类型_____________;_____________。
(3)写出物质C与一种燃烧产物只有水的清洁燃料反应的化学方程式:____________。
四、实验题
20.钢铁是重要的金属材料,人类每年要从自然界获取大量的铁矿资源.
(1)目前世界上已有以上的废钢铁得到回收利用,其目的是________.
A 节约金属资源 B 合理开采矿物 C 防止钢铁生锈
(2)工业上高炉炼铁得到的主要产品是________;(填序号)
A 纯铁 B 生铁 C 钢
(3)一位同学准备在实验室用下图所示装置模拟工业炼铁.请你据此回答下列问题:
①实验中硬质玻璃管里的现象是:_____;硬质玻璃管里发生反应的方程式为_____.
②装置图中澄清石灰水的作用是_____.
③某同学实验完成后,发现过量的澄清石灰水增重0.44g,则该同学通入装置的CO气体质量_____(填“大于”、“小于”或“等于”)0.28g,原因是_____.
(4)某钢铁厂每天消耗5000t含氧化铁84%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是_____?
21.某兴趣小组做了如下实验:
①在止水夹K1、K2处于关闭状态时,将针筒A中溶液挤入试管B中,接着打开止水夹K1,发现D中的部分溶液被吸入试管B中,充分反应后,试管B留下的溶液也显红色;
②打开止水夹K2,风哨振动鸣叫,C中的部分溶液被吸入B和D中,反应后B、D中溶液都变为无色。
回答:
(1)步骤①中,充分反应后,试管B里的CO2最终转化为___________(填化学式)和水。
(2)解释步骤②中“风哨振动鸣叫”的原因___________。
(3)实验开始时C、D中两种溶液中溶质质量分数大小关系为:a%___________b%(选填“>”“=”“<”)。
22.下图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:
(1)描述A中的实验现象________。
(2)写出C中反应的化学方程式__________。
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是___________(填序号)。
(4)开始反应后D中溶液逐渐变为黄色,原因是__________。
五、计算题
23.工业用焦炭还原100kg含Fe2O380%的赤铁矿,理论上可炼得铁的质量为多少?(请写出解题步骤)
24.将20g含有杂质的锌粒放入烧杯中,然后向其中逐渐滴加稀硫酸50g至反应停止,(杂质不参加反应),此时称量烧杯内物质的总质量为69.6g.试计算:
(1)生成氢气的质量为______g.
(2)该锌粒中锌的质量分数.
25.白铜(Cu-Ni)是工业上常用的一种合金,金属镍(Ni)的金属活泼性与铁相似,且化合价显+2价。为测定20g某白铜样品中镍的质量,设计了如下实验:
试问:(1)将白铜研碎的目的是 。
(2)白铜样品中镍的质量 g。
(3)所用稀硫酸中溶质的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.B
5.C
6.A
7.D
8.C
9.C
10.D
11.C
12.A
13. 加入过量的稀硫酸后过滤 Fe+H2SO4═FeSO4+H2↑ 加入过量的硫酸铜溶液后过滤 Fe+CuSO4═FeSO4+Cu
14.2
15. Cu与氧气反应,在表面生成质量更大的CuO 溶液由无色变蓝色 2AgNO3+Cu=Cu(NO3)2+2Ag
16. 黄金金属活动性弱,不容易发生化学反应,青铜中金属活动性强,容易发生化学反应 6
17.(1)紫色石蕊试液
(2)Fe##铁
(3)Fe2O3##氧化铁
(4)
(5)将第④试剂调换为硝酸银(AgNO3)
18. CH4 作燃料 C+2CuO2Cu+CO2↑ 置换 黑色粉末逐渐减少,溶液逐渐变成了蓝色 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
19.(1)Fe2O3
(2) 或 置换反应
(3)
20. A B 红色粉末变成黑色 Fe2O3+3CO2Fe+3CO2 检验有二氧化碳生成 大于 实验开始或结束都要通入一氧化碳,故该实验中实验用量大于量论用量 该厂理论上可日产含铁98%的生铁的质量是3000t
21. Na2CO3 B中二氧化碳和氢氧化钠反应,气体减少,压强减小,在外界大气压的作用下,空气进入C中 >
22. 铜丝表面附着一层银白色固体,溶液变为蓝色 A、B 铁钉未打磨有铁锈或溶液中有Fe2(SO4)3生成
23.解:设理论上可炼得铁的质量为x
答:理论上可炼得铁的质量为56kg。
24.(1)0.4
(2)解:设该锌粒中锌的质量分数为x
x=65%
答:该锌粒中锌的质量分数为65%。
25.(1)增大白铜与稀硫酸的接触面积,使反应更快、更充分(2)2.95(3)9.8%
答案第1页,共2页
答案第1页,共2页
