第10章金属检测题-2021-2022学年九年级化学京改版(2013)下册(word版有答案)
文档属性
| 名称 | 第10章金属检测题-2021-2022学年九年级化学京改版(2013)下册(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 112.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-23 00:00:00 | ||
图片预览



文档简介
第10章《金属》检测题
一、单选题
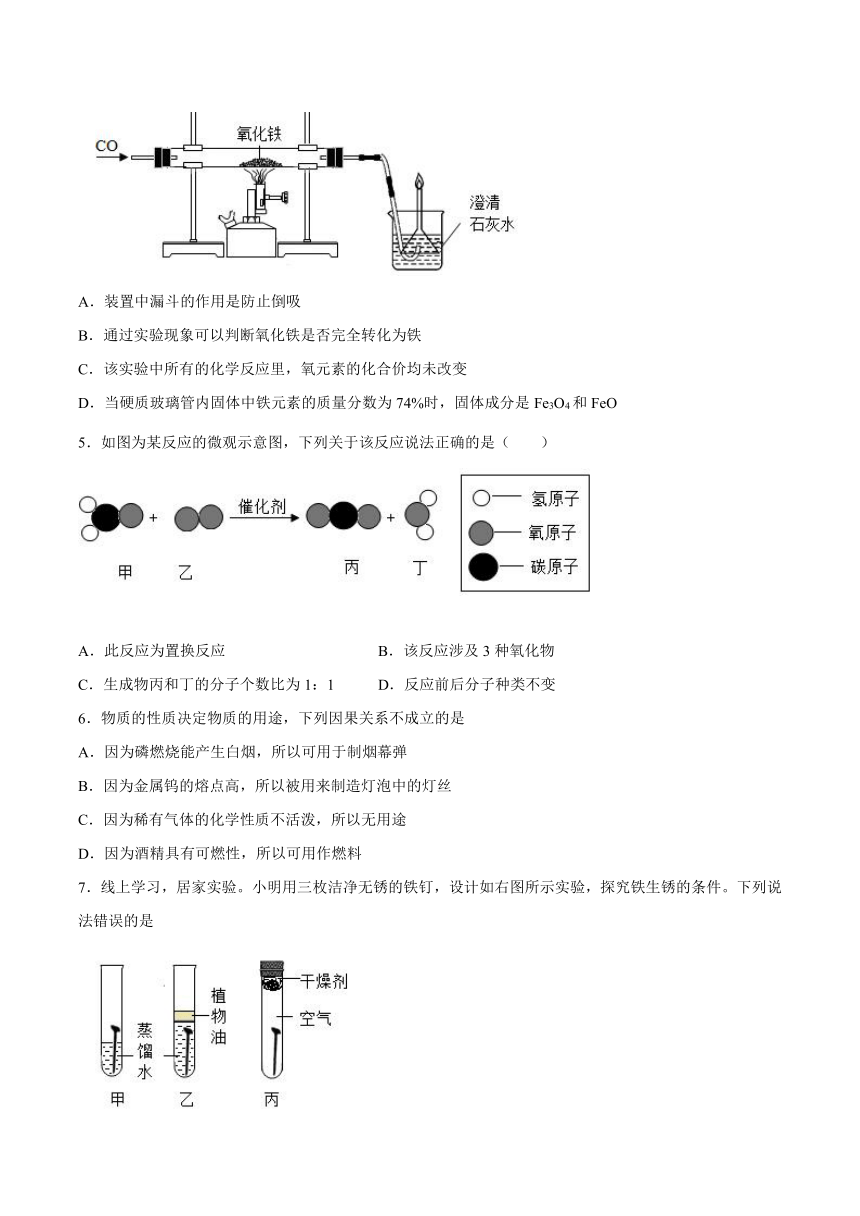
1.如图是探究铁器锈蚀条件的装置。调节L端与R端的液面高度使之相同,塞紧橡皮塞,一周后观察。下列说法错误的是
A.a管中在靠近水面上方且近水面处铁钉上有明显的锈迹
B.L端液面低于R端
C.a管中铁钉明显生锈,b管中铁钉几乎不生锈
D.若将a管中的水改为海水则铁钉生锈更严重
2.某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
3.验证镁、铜的金属活动性顺序,下列试剂不能选用的是( )
A.MgSO4溶液 B.KCl溶液
C.稀盐酸 D.CuCl2溶液
4.用一氧化碳还原氧化铁的实验中,Fe2O3转化为铁的具体过程是: 。已知铁的氧化物除Fe2O3外,其余均为黑色。下列说法正确的是
A.装置中漏斗的作用是防止倒吸
B.通过实验现象可以判断氧化铁是否完全转化为铁
C.该实验中所有的化学反应里,氧元素的化合价均未改变
D.当硬质玻璃管内固体中铁元素的质量分数为74%时,固体成分是Fe3O4和FeO
5.如图为某反应的微观示意图,下列关于该反应说法正确的是( )
A.此反应为置换反应 B.该反应涉及3种氧化物
C.生成物丙和丁的分子个数比为1:1 D.反应前后分子种类不变
6.物质的性质决定物质的用途,下列因果关系不成立的是
A.因为磷燃烧能产生白烟,所以可用于制烟幕弹
B.因为金属钨的熔点高,所以被用来制造灯泡中的灯丝
C.因为稀有气体的化学性质不活泼,所以无用途
D.因为酒精具有可燃性,所以可用作燃料
7.线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如右图所示实验,探究铁生锈的条件。下列说法错误的是
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
8.关于"家庭小实验"的下列说法正确的是
A.用自制简易净水器制纯水
B.向洗净的碎鸡蛋壳中加入食醋可产生一氧化碳
C.用白糖、果汁、小苏打、柠檬酸、水自制汽水
D.把钢针烧红放入水中冷却后取出,钢针变得更容易弯曲
9.有Ⅹ、Y、Z三种金属,Ⅹ的盐溶液能用Y制容器盛放;将X、Y、Z分别投入稀盐酸中,X、Y溶解并产生气泡,Z无变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强到弱的顺序正确的是( )
A.Y Z X B.X Z Y C.X Y Z D.Z Y X
10.将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
11.铁制品通常比铝制品更容易锈蚀,下列说法正确的是
A.铁的金属活动性比铝强
B.铝在自然界中以单质形式存在
C.锈蚀的铁制品无回收价值
D.自行车链条涂油有防锈作用
12.铝是一种应用越来越广泛的金属。下列有关铝的描述正确的是
A.铝是地壳中含量最高的元素
B.单质铝的化合价常表现为+3价
C.铁比铝容易生锈,故铁的化学性质比铝活泼
D.镁和铝的金属活动性可通过等浓度的稀盐酸来判断
13.有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
二、简答题
14.为测定某赤铁矿石中氧化铁的质量分数,小雨同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,氢氧化钠溶液总质量与反应时间的变化关系如图。
请回答:
(1)上述反应产生二氧化碳的质量为________g;
(2)该赤铁矿石中氧化铁的质量分数是_______________?
15.根据所学化学知识回答问题:
(1)请用“>”或“<”或“=”,填空。
①质子数:氯离子_____氯原子;
②沸点:N2_____O2;
③金属与稀盐酸反应的剧烈程度:镁_____铁;
④20℃,1.0g硫粉在2.0g氧气中完全燃烧后生成的二氧化硫的质量_____3.0g;
⑤若用KClO3和MnO2(催化剂)混合制取氧气,则MnO2在反应前后固体混合物中的质量分数:反应前_____反应后。
(2)如图所示,调节杠杆平衡后完成下列实验。
一段时间后,混有炭粉的铁粉包_____ (填“上升”、“下降”“不动”),原因是_____。
三、推断题
16.已知铜在潮湿的环境中也会生绣,铜锈的主要成分俗称“铜绿”化学式[Cu2(OH)2CO3],加热时铜绿分解生成A、B、C三种常见的氧化物,下面是有关物质之间的转化关系图示。
(1)试通过分析推断,确定下列物质并写出化学式:
B_________,D_________,E________,G_______。
(2)写出下列变化的化学方程式:
C→H:________________。
C→F:_________________。
17.将一定量的锌粉加入到A1(NO3)3、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。滤液呈浅绿色,则滤渣中可能含有的物质是______(写出化学式,下同),滤液中一定含有的溶质是______。
18.A、B、C、D都是初中化学中常见的物质,A、C为组成元素相同的两种氧化物,D为紫红色金属单质。它们之间的相互转化关系如图(图中反应条件已略去)。请回答:
(1)写出C转化为A的化学方程式___________。
(2)写出A与B反应的化学方程式___________
(3)碳可以和B在高温条件下发生反应,其化学反应类型属于___________反应。
四、实验题
19.化学是一门以实验为基础的科学,对比法是一种常见的实验方法,回答下列问题:
(1)实验一说明可燃物燃烧需要温度达到着火点的现象是______;
(2)实验二喷水后的石蕊纸花放入二氧化碳中,纸花由紫色变为______色;
(3)实验三说明铁生锈是铁与氧气、______共同作用的结果。
五、计算题
20.为了测定某黄铜样品中铜的质量分数(黄铜样品是由铜、锌组成),某化学小组进行了如下实验:
(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是 ;
(2)黄铜样品是铜的质量分数是 ;
(3)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是多少?(写出计算过程)
21.生铁是由铁和碳组成的合金。某化学兴趣小组的同学为了测定某稀盐酸中溶质的质量分数,取一定量的该生铁样品,分四次加入稀盐酸200g,充分反应后,实验数据如下:
次数 1 2 3 4
稀盐酸质量/g 50 50 50 50
氢气质量/g 0.2 m 0.2 0.1
请根据有关信息完成下列问题:
(1)m=_____。
(2)该稀盐酸中溶质的质量分数。(请写出计算过程,计算结果精确到0.1%)
参考答案:
1.B 2.B 3.B 4.D 5.C 6.C 7.C 8.C 9.C 10.B 11.D 12.D 13.A
14. 6.6 80%
15. = < > < < 下降 混有炭粉的铁粉包和水、氧气反应会发生锈蚀,质量增大
16. CuO O2 H2 Cu CO2 +Ca(OH)2 ==CaCO3↓+ H2O C + CO2 2CO
17. Fe Zn(NO3)2、Fe(NO3)2 、Al(NO3)3
18.(1)
(2)
(3)置换
19. 铜片上的白磷燃烧,铜片上的红磷不燃烧 红 水
20.(1)40g
(2)87%
(3)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数为×100%=13.6%;
答:最终所得溶液中溶质的质量分数是13.6%。
21.(1)0.2
(2)设:稀盐酸溶质质量分数为x。
答:稀盐酸溶质质量分数14.6%。
一、单选题
1.如图是探究铁器锈蚀条件的装置。调节L端与R端的液面高度使之相同,塞紧橡皮塞,一周后观察。下列说法错误的是
A.a管中在靠近水面上方且近水面处铁钉上有明显的锈迹
B.L端液面低于R端
C.a管中铁钉明显生锈,b管中铁钉几乎不生锈
D.若将a管中的水改为海水则铁钉生锈更严重
2.某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
3.验证镁、铜的金属活动性顺序,下列试剂不能选用的是( )
A.MgSO4溶液 B.KCl溶液
C.稀盐酸 D.CuCl2溶液
4.用一氧化碳还原氧化铁的实验中,Fe2O3转化为铁的具体过程是: 。已知铁的氧化物除Fe2O3外,其余均为黑色。下列说法正确的是
A.装置中漏斗的作用是防止倒吸
B.通过实验现象可以判断氧化铁是否完全转化为铁
C.该实验中所有的化学反应里,氧元素的化合价均未改变
D.当硬质玻璃管内固体中铁元素的质量分数为74%时,固体成分是Fe3O4和FeO
5.如图为某反应的微观示意图,下列关于该反应说法正确的是( )
A.此反应为置换反应 B.该反应涉及3种氧化物
C.生成物丙和丁的分子个数比为1:1 D.反应前后分子种类不变
6.物质的性质决定物质的用途,下列因果关系不成立的是
A.因为磷燃烧能产生白烟,所以可用于制烟幕弹
B.因为金属钨的熔点高,所以被用来制造灯泡中的灯丝
C.因为稀有气体的化学性质不活泼,所以无用途
D.因为酒精具有可燃性,所以可用作燃料
7.线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如右图所示实验,探究铁生锈的条件。下列说法错误的是
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
8.关于"家庭小实验"的下列说法正确的是
A.用自制简易净水器制纯水
B.向洗净的碎鸡蛋壳中加入食醋可产生一氧化碳
C.用白糖、果汁、小苏打、柠檬酸、水自制汽水
D.把钢针烧红放入水中冷却后取出,钢针变得更容易弯曲
9.有Ⅹ、Y、Z三种金属,Ⅹ的盐溶液能用Y制容器盛放;将X、Y、Z分别投入稀盐酸中,X、Y溶解并产生气泡,Z无变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强到弱的顺序正确的是( )
A.Y Z X B.X Z Y C.X Y Z D.Z Y X
10.将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
11.铁制品通常比铝制品更容易锈蚀,下列说法正确的是
A.铁的金属活动性比铝强
B.铝在自然界中以单质形式存在
C.锈蚀的铁制品无回收价值
D.自行车链条涂油有防锈作用
12.铝是一种应用越来越广泛的金属。下列有关铝的描述正确的是
A.铝是地壳中含量最高的元素
B.单质铝的化合价常表现为+3价
C.铁比铝容易生锈,故铁的化学性质比铝活泼
D.镁和铝的金属活动性可通过等浓度的稀盐酸来判断
13.有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
二、简答题
14.为测定某赤铁矿石中氧化铁的质量分数,小雨同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,氢氧化钠溶液总质量与反应时间的变化关系如图。
请回答:
(1)上述反应产生二氧化碳的质量为________g;
(2)该赤铁矿石中氧化铁的质量分数是_______________?
15.根据所学化学知识回答问题:
(1)请用“>”或“<”或“=”,填空。
①质子数:氯离子_____氯原子;
②沸点:N2_____O2;
③金属与稀盐酸反应的剧烈程度:镁_____铁;
④20℃,1.0g硫粉在2.0g氧气中完全燃烧后生成的二氧化硫的质量_____3.0g;
⑤若用KClO3和MnO2(催化剂)混合制取氧气,则MnO2在反应前后固体混合物中的质量分数:反应前_____反应后。
(2)如图所示,调节杠杆平衡后完成下列实验。
一段时间后,混有炭粉的铁粉包_____ (填“上升”、“下降”“不动”),原因是_____。
三、推断题
16.已知铜在潮湿的环境中也会生绣,铜锈的主要成分俗称“铜绿”化学式[Cu2(OH)2CO3],加热时铜绿分解生成A、B、C三种常见的氧化物,下面是有关物质之间的转化关系图示。
(1)试通过分析推断,确定下列物质并写出化学式:
B_________,D_________,E________,G_______。
(2)写出下列变化的化学方程式:
C→H:________________。
C→F:_________________。
17.将一定量的锌粉加入到A1(NO3)3、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。滤液呈浅绿色,则滤渣中可能含有的物质是______(写出化学式,下同),滤液中一定含有的溶质是______。
18.A、B、C、D都是初中化学中常见的物质,A、C为组成元素相同的两种氧化物,D为紫红色金属单质。它们之间的相互转化关系如图(图中反应条件已略去)。请回答:
(1)写出C转化为A的化学方程式___________。
(2)写出A与B反应的化学方程式___________
(3)碳可以和B在高温条件下发生反应,其化学反应类型属于___________反应。
四、实验题
19.化学是一门以实验为基础的科学,对比法是一种常见的实验方法,回答下列问题:
(1)实验一说明可燃物燃烧需要温度达到着火点的现象是______;
(2)实验二喷水后的石蕊纸花放入二氧化碳中,纸花由紫色变为______色;
(3)实验三说明铁生锈是铁与氧气、______共同作用的结果。
五、计算题
20.为了测定某黄铜样品中铜的质量分数(黄铜样品是由铜、锌组成),某化学小组进行了如下实验:
(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是 ;
(2)黄铜样品是铜的质量分数是 ;
(3)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是多少?(写出计算过程)
21.生铁是由铁和碳组成的合金。某化学兴趣小组的同学为了测定某稀盐酸中溶质的质量分数,取一定量的该生铁样品,分四次加入稀盐酸200g,充分反应后,实验数据如下:
次数 1 2 3 4
稀盐酸质量/g 50 50 50 50
氢气质量/g 0.2 m 0.2 0.1
请根据有关信息完成下列问题:
(1)m=_____。
(2)该稀盐酸中溶质的质量分数。(请写出计算过程,计算结果精确到0.1%)
参考答案:
1.B 2.B 3.B 4.D 5.C 6.C 7.C 8.C 9.C 10.B 11.D 12.D 13.A
14. 6.6 80%
15. = < > < < 下降 混有炭粉的铁粉包和水、氧气反应会发生锈蚀,质量增大
16. CuO O2 H2 Cu CO2 +Ca(OH)2 ==CaCO3↓+ H2O C + CO2 2CO
17. Fe Zn(NO3)2、Fe(NO3)2 、Al(NO3)3
18.(1)
(2)
(3)置换
19. 铜片上的白磷燃烧,铜片上的红磷不燃烧 红 水
20.(1)40g
(2)87%
(3)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数为×100%=13.6%;
答:最终所得溶液中溶质的质量分数是13.6%。
21.(1)0.2
(2)设:稀盐酸溶质质量分数为x。
答:稀盐酸溶质质量分数14.6%。
