第五章 燃料 检测卷(word版有答案)
文档属性
| 名称 | 第五章 燃料 检测卷(word版有答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 476.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-24 00:00:00 | ||
图片预览


文档简介
第五章达标检测卷
可能用到的相对原子质量:C—12 O—16 Cl—35.5 Ca—40
一、选择题(每题2分,共24分)
1.保护环境,共建美丽地球家园。以下践行“低碳”生活理念的做法不合理的是( )
A.加强新能源汽车的研发和推广应用
B.提高煤的开采水平,推广利用煤进行火力发电
C.废旧书籍、报纸分类回收再利用
D.减少使用化石燃料,开发利用太阳能、风能等
2.二氧化碳和二氧化硫都是由AB2型分子构成的物质,但分子中A原子和B原子的空间位置不同,其模型如图所示。根据此模型,下列叙述错误的是( )
A.两种物质都由两种元素组成
B.两种物质中碳元素和硫元素的化合价相同
C.两种物质的化学性质相同
D.分子中原子空间位置不同是因为A原子种类不同
3.下列物质的用途错误的是( )
A.用石油炼制汽油 B.C60用于超导领域
C.二氧化碳作化工产品的原料 D.炭黑用来制铅笔芯
4.自然界碳循环如图所示。下列说法正确的是( )
A.向空气中排放CO2会形成酸雨
B.无机物和有机物不可相互转化
C.植树造林有利于吸收CO2
D.煤、石油和天然气是可再生能源
5.石墨烯是由碳原子构成的单层片状结构的新材料(如图所示),即极薄的石墨。下列说法正确的是( )
A.石墨烯属于化合物
B.单层和双层石墨烯均有导电性
C.石墨烯叠加过程中有新物质产生
D.石墨烯中碳元素的化合价为+4价
6.下列实验现象描述正确的是( )
A.氢气在空气中燃烧:放热,产生黄色的火焰
B.一氧化碳还原氧化铜:黑色固体逐渐变为银白色
C.二氧化碳通入紫色石蕊溶液中:溶液由紫色变为红色
D.镁带在氧气中燃烧:火星四射,放出大量的热,生成黑色固体
7.熙蕾在学完二氧化碳和一氧化碳后,对有关知识进行了归纳和整理,其中不合理的是( )
A.CO2和CO都是由碳元素和氧元素组成的,在一定条件下可以相互转化
B.CO2通入紫色石蕊溶液中,溶液变为红色,说明二氧化碳具有酸性
C.CO有毒,CO2无毒
D.CO2和CO化学性质不同的原因是分子的构成不同
8.下列有关碳和碳的氧化物的说法正确的是( )
A.金刚石和石墨物理性质不同,是因为构成它们的原子的大小不同
B.C60表示1个C60分子由60个碳原子构成
C.碳在氧气中燃烧生成二氧化碳,在空气中燃烧生成一氧化碳
D.二氧化碳能和碳反应生成一氧化碳且放出热量
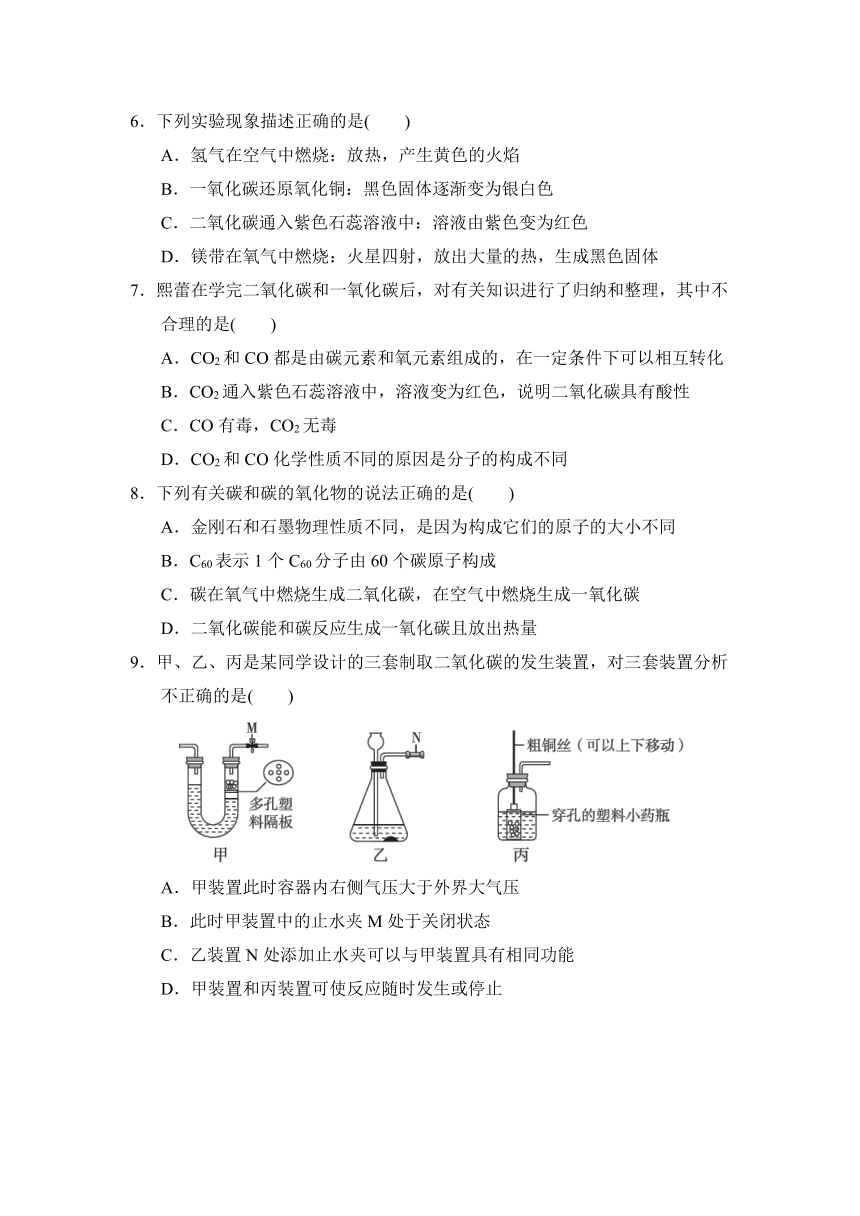
9.甲、乙、丙是某同学设计的三套制取二氧化碳的发生装置,对三套装置分析不正确的是( )
A.甲装置此时容器内右侧气压大于外界大气压
B.此时甲装置中的止水夹M处于关闭状态
C.乙装置N处添加止水夹可以与甲装置具有相同功能
D.甲装置和丙装置可使反应随时发生或停止
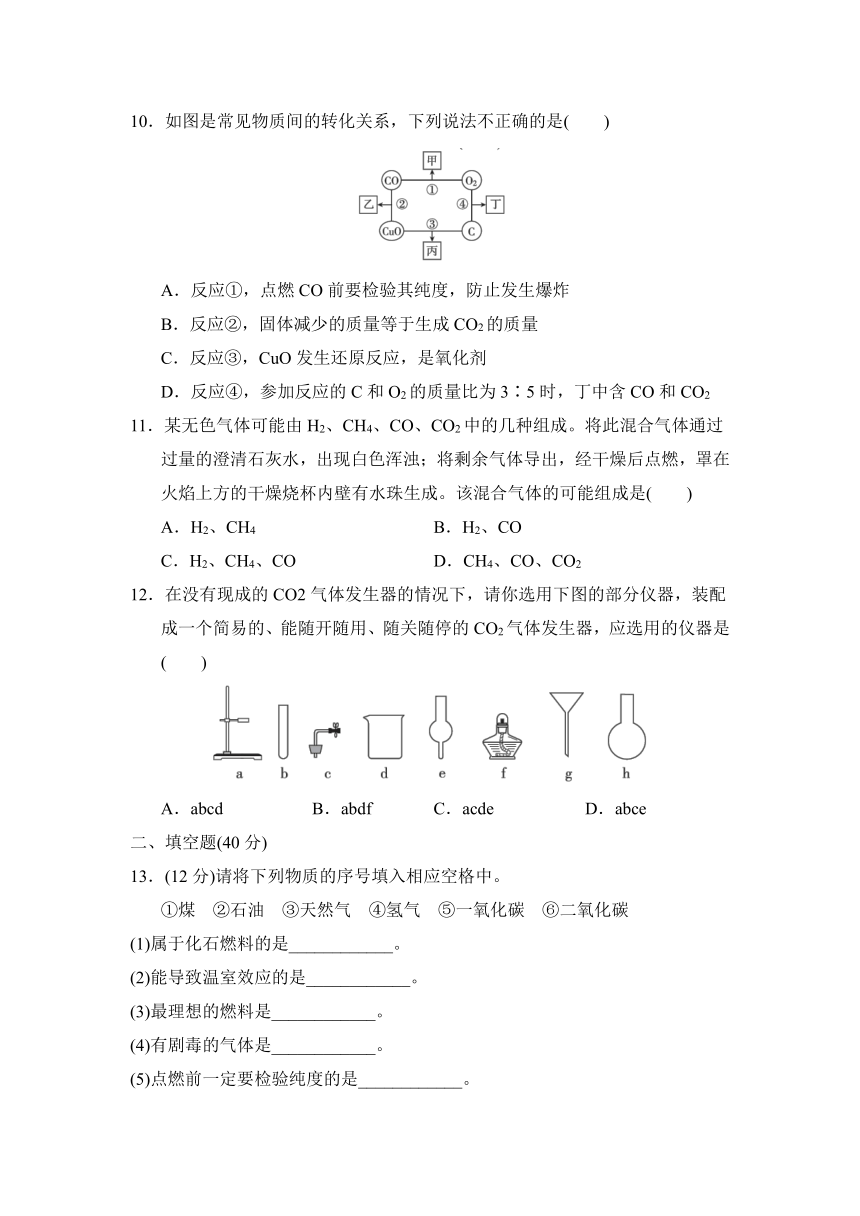
10.如图是常见物质间的转化关系,下列说法不正确的是( )
A.反应①,点燃CO前要检验其纯度,防止发生爆炸
B.反应②,固体减少的质量等于生成CO2的质量
C.反应③,CuO发生还原反应,是氧化剂
D.反应④,参加反应的C和O2的质量比为3∶5时,丁中含CO和CO2
11.某无色气体可能由H2、CH4、CO、CO2中的几种组成。将此混合气体通过过量的澄清石灰水,出现白色浑浊;将剩余气体导出,经干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成。该混合气体的可能组成是( )
A.H2、CH4 B.H2、CO
C.H2、CH4、CO D.CH4、CO、CO2
12.在没有现成的CO2气体发生器的情况下,请你选用下图的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生器,应选用的仪器是( )
A.abcd B.abdf C.acde D.abce
二、填空题(40分)
13.(12分)请将下列物质的序号填入相应空格中。
①煤 ②石油 ③天然气 ④氢气 ⑤一氧化碳 ⑥二氧化碳
(1)属于化石燃料的是____________。
(2)能导致温室效应的是____________。
(3)最理想的燃料是____________。
(4)有剧毒的气体是____________。
(5)点燃前一定要检验纯度的是____________。
(6)既能用排水法又能用向下排空气法收集的单质气体是____________。
14.(6分)木炭燃烧时能生成一氧化碳和二氧化碳。
(1)用墨书写、绘制的字画年深日久仍不掉色的原因是______________________。
(2)木炭和一氧化碳虽然是两种不同的物质,但它们的化学性质有许多相似之处,例如:它们都能与________反应,请写出木炭与其反应的化学方程式:________________________________________________________________。
(3)由于一氧化碳和二氧化碳的分子构成不同,所以其化学性质不同。请写出区分它们的化学方程式____________________________________________(写出一个即可)。
(4)一氧化碳和氢气都既有可燃性,又有还原性,鉴别它们的方法是:分别点燃两种气体,在火焰的上方各罩一个冷而干燥的烧杯,烧杯内壁出现________,则原气体为氢气。
15.(10分)煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源,煤气化和液化流程示意图如下:
(1)第①步操作发生的是________(填“物理”或“化学”)变化。
(2)第②步是精炼煤与水蒸气的反应,化学方程式为________________________。
(3)第③步反应的基本反应类型属于________________反应。
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:含硫化合物氧化得到SO2,SO2进一步氧化得到X,X与水反应得到H2SO4,则X的化学式为________。
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是_________________________________________________________________。
16.(12分)碳和碳的化合物间的部分转化关系如图所示。
(1)物质X的化学式为________。
(2)在物质的分类中,X属于________(填字母)。
A.单质 B.氧化物 C.化合物
(3)写出该图转化关系中①的化学方程式________________________。
(4)转化②在实验中常见的用途是________________________。
(5)转化③是________(填“吸热”或“放热”)反应。
(6)C和CO都能与CuO在一定条件下反应,反应中具有氧化性的物质是_______。
三、实验探究题(22分)
17.如图一中A~G是实验室常用的仪器,请据图回答问题:
(1)认识仪器:仪器A的名称是________。
(2)制取气体:实验室制取二氧化碳的化学方程式为________________________。利用上述仪器组装实验室制取二氧化碳的发生装置和收集装置时,若要实现随时控制反应的发生和停止,则必须选择的仪器是________________(填字母组合),还缺少的一种仪器的名称是__________。
(3)探究性质:实验一中,蜡烛由低到高依次熄灭,由此可知二氧化碳的物理性质是______________________________;实验二中,溶液颜色的变化是______________________;实验三中,澄清的石灰水变浑浊,反应的化学方程式是______________________________。
(4)拓展应用:将图甲所示装置倾斜使两种药品混合,即可制得气体。利用该装置制取氧气发生反应的化学方程式为______________________________,制得的氧气能用排水法收集,原因是______________________________,用排水法收集氧气时,判断氧气收集满的方法是____________________________。利用图甲装置还可制取氢气,制得的氢气点燃前需验纯,用化学方程式说明需验纯的原因____________________________________________________。
四、计算题(14分)
18.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8 g这种石灰石样品,把40 g稀盐酸分四次加入,测量过程所得数据见下表(提示:石灰石样品中含有的杂质不溶于水,不与盐酸反应),请计算:
序号 加入稀盐酸的质量/g 剩余固体质量/g
第一次 10 5.5
第二次 10 3.0
第三次 10 1.2
第四次 10 n
(1)样品中碳酸钙的质量分数为________。
(2)上表中n的数值为________。
(3)求反应生成的氯化钙的总质量。
答案
一、1.B 2.C 3.D 4.C 5.B
6.C 点拨:氢气在空气中燃烧产生淡蓝色火焰,A错误;一氧化碳具有还原性,与氧化铜反应生成紫红色的铜,黑色固体变红色,B错误;二氧化碳与水反应生成碳酸,碳酸可使石蕊变红,C正确;镁带在氧气中燃烧,发出耀眼的白光,放出大量的热,生成白色固体,D错误。
7.B 点拨:二氧化碳与水化合生成碳酸,碳酸使石蕊溶液变红色,二氧化碳不具有酸性,B不正确。
8.B 点拨:金刚石和石墨的物理性质有很大差异是因为碳原子的排列方式不同,A错误;C60可表示1个C60分子由60个碳原子构成,B正确;碳单质燃烧,氧气充足时生成二氧化碳,氧气不足时生成一氧化碳,C错误;二氧化碳能和碳反应生成一氧化碳,此反应吸收热量,D错误。
9.C
10.B 点拨:一氧化碳是可燃性气体,点燃CO前要检验其纯度,防止发生爆炸,A正确;反应②,是一氧化碳与氧化铜反应生成铜和二氧化碳,固体减少的质量不等于生成CO2的质量,B不正确;反应③,是碳与氧化铜反应生成铜和二氧化碳,CuO提供氧,发生还原反应,是氧化剂,C正确;反应④,是碳与氧气反应,可能生成一氧化碳或二氧化碳,碳和氧气的质量比为12∶32=3∶8时生成二氧化碳;碳和氧气的质量比为(12×2) ∶32=3∶4时生成一氧化碳,参加反应的C和O2的质量比为3∶5时,丁中含CO和CO2,D正确。
11.D 点拨:由实验现象可知,将气体通过过量澄清石灰水,出现白色浑浊,证明气体中一定含有CO2;将剩余气体干燥后点燃,有水生成,证明气体中一定有H2或CH4中至少一种。对照选项,含CO2的选项只有D。
12.C 点拨:安装方法:d在a的台上,e固定在a上,c安装到e上。关闭c中的开关,盐酸从c中被压回烧杯中,固体与液体分离,反应停止。
二、13.(1)①②③ (2)③⑥ (3)④ (4)⑤ (5)③④⑤ (6)④
14.(1)常温下,碳的化学性质稳定
(2)O2(或CuO);C+O2CO2(或C+2CuO2Cu+CO2↑)
(3)CO+CuOCu+CO2(其他合理答案均可)
(4)水雾
15.(1)物理 (2)C+H2OCO+H2
(3)化合 (4)SO3
(5)原料全部转化为产品(或原子利用率100%,或实现“零排放”,或不对环境造成污染等)
16.(1)CO2 (2)B、C (3)CO2+H2O===H2CO3
(4)检验CO2 (5)放热 (6)CuO
三、17.(1)锥形瓶 (2)CaCO3+2HCl===CaCl2+H2O+CO2↑;B、C、D、G;铁架台 (3)二氧化碳的密度比空气大;由紫色变为红色;CO2+Ca(OH)2===
CaCO3↓+H2O
(4)2H2O22H2O+O2↑;氧气不易溶于水且不与水反应;集气瓶口有较大气泡冒出;2H2+O22H2O
四、18.解:(1)85% (2)1.2
(3)设反应生成的氯化钙的总质量为x。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 111
8 g-1.2 g x
= x=7.548 g
答:反应生成的氯化钙的总质量为7.548 g。
点拨:(1)8 g石灰石样品中含有1.2 g杂质,样品中碳酸钙的质量分数=×100%=85%;
(2)第3次加入10 g稀盐酸,充分反应后,碳酸钙完全反应,故n=1.2。
可能用到的相对原子质量:C—12 O—16 Cl—35.5 Ca—40
一、选择题(每题2分,共24分)
1.保护环境,共建美丽地球家园。以下践行“低碳”生活理念的做法不合理的是( )
A.加强新能源汽车的研发和推广应用
B.提高煤的开采水平,推广利用煤进行火力发电
C.废旧书籍、报纸分类回收再利用
D.减少使用化石燃料,开发利用太阳能、风能等
2.二氧化碳和二氧化硫都是由AB2型分子构成的物质,但分子中A原子和B原子的空间位置不同,其模型如图所示。根据此模型,下列叙述错误的是( )
A.两种物质都由两种元素组成
B.两种物质中碳元素和硫元素的化合价相同
C.两种物质的化学性质相同
D.分子中原子空间位置不同是因为A原子种类不同
3.下列物质的用途错误的是( )
A.用石油炼制汽油 B.C60用于超导领域
C.二氧化碳作化工产品的原料 D.炭黑用来制铅笔芯
4.自然界碳循环如图所示。下列说法正确的是( )
A.向空气中排放CO2会形成酸雨
B.无机物和有机物不可相互转化
C.植树造林有利于吸收CO2
D.煤、石油和天然气是可再生能源
5.石墨烯是由碳原子构成的单层片状结构的新材料(如图所示),即极薄的石墨。下列说法正确的是( )
A.石墨烯属于化合物
B.单层和双层石墨烯均有导电性
C.石墨烯叠加过程中有新物质产生
D.石墨烯中碳元素的化合价为+4价
6.下列实验现象描述正确的是( )
A.氢气在空气中燃烧:放热,产生黄色的火焰
B.一氧化碳还原氧化铜:黑色固体逐渐变为银白色
C.二氧化碳通入紫色石蕊溶液中:溶液由紫色变为红色
D.镁带在氧气中燃烧:火星四射,放出大量的热,生成黑色固体
7.熙蕾在学完二氧化碳和一氧化碳后,对有关知识进行了归纳和整理,其中不合理的是( )
A.CO2和CO都是由碳元素和氧元素组成的,在一定条件下可以相互转化
B.CO2通入紫色石蕊溶液中,溶液变为红色,说明二氧化碳具有酸性
C.CO有毒,CO2无毒
D.CO2和CO化学性质不同的原因是分子的构成不同
8.下列有关碳和碳的氧化物的说法正确的是( )
A.金刚石和石墨物理性质不同,是因为构成它们的原子的大小不同
B.C60表示1个C60分子由60个碳原子构成
C.碳在氧气中燃烧生成二氧化碳,在空气中燃烧生成一氧化碳
D.二氧化碳能和碳反应生成一氧化碳且放出热量
9.甲、乙、丙是某同学设计的三套制取二氧化碳的发生装置,对三套装置分析不正确的是( )
A.甲装置此时容器内右侧气压大于外界大气压
B.此时甲装置中的止水夹M处于关闭状态
C.乙装置N处添加止水夹可以与甲装置具有相同功能
D.甲装置和丙装置可使反应随时发生或停止
10.如图是常见物质间的转化关系,下列说法不正确的是( )
A.反应①,点燃CO前要检验其纯度,防止发生爆炸
B.反应②,固体减少的质量等于生成CO2的质量
C.反应③,CuO发生还原反应,是氧化剂
D.反应④,参加反应的C和O2的质量比为3∶5时,丁中含CO和CO2
11.某无色气体可能由H2、CH4、CO、CO2中的几种组成。将此混合气体通过过量的澄清石灰水,出现白色浑浊;将剩余气体导出,经干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成。该混合气体的可能组成是( )
A.H2、CH4 B.H2、CO
C.H2、CH4、CO D.CH4、CO、CO2
12.在没有现成的CO2气体发生器的情况下,请你选用下图的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生器,应选用的仪器是( )
A.abcd B.abdf C.acde D.abce
二、填空题(40分)
13.(12分)请将下列物质的序号填入相应空格中。
①煤 ②石油 ③天然气 ④氢气 ⑤一氧化碳 ⑥二氧化碳
(1)属于化石燃料的是____________。
(2)能导致温室效应的是____________。
(3)最理想的燃料是____________。
(4)有剧毒的气体是____________。
(5)点燃前一定要检验纯度的是____________。
(6)既能用排水法又能用向下排空气法收集的单质气体是____________。
14.(6分)木炭燃烧时能生成一氧化碳和二氧化碳。
(1)用墨书写、绘制的字画年深日久仍不掉色的原因是______________________。
(2)木炭和一氧化碳虽然是两种不同的物质,但它们的化学性质有许多相似之处,例如:它们都能与________反应,请写出木炭与其反应的化学方程式:________________________________________________________________。
(3)由于一氧化碳和二氧化碳的分子构成不同,所以其化学性质不同。请写出区分它们的化学方程式____________________________________________(写出一个即可)。
(4)一氧化碳和氢气都既有可燃性,又有还原性,鉴别它们的方法是:分别点燃两种气体,在火焰的上方各罩一个冷而干燥的烧杯,烧杯内壁出现________,则原气体为氢气。
15.(10分)煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源,煤气化和液化流程示意图如下:
(1)第①步操作发生的是________(填“物理”或“化学”)变化。
(2)第②步是精炼煤与水蒸气的反应,化学方程式为________________________。
(3)第③步反应的基本反应类型属于________________反应。
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:含硫化合物氧化得到SO2,SO2进一步氧化得到X,X与水反应得到H2SO4,则X的化学式为________。
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是_________________________________________________________________。
16.(12分)碳和碳的化合物间的部分转化关系如图所示。
(1)物质X的化学式为________。
(2)在物质的分类中,X属于________(填字母)。
A.单质 B.氧化物 C.化合物
(3)写出该图转化关系中①的化学方程式________________________。
(4)转化②在实验中常见的用途是________________________。
(5)转化③是________(填“吸热”或“放热”)反应。
(6)C和CO都能与CuO在一定条件下反应,反应中具有氧化性的物质是_______。
三、实验探究题(22分)
17.如图一中A~G是实验室常用的仪器,请据图回答问题:
(1)认识仪器:仪器A的名称是________。
(2)制取气体:实验室制取二氧化碳的化学方程式为________________________。利用上述仪器组装实验室制取二氧化碳的发生装置和收集装置时,若要实现随时控制反应的发生和停止,则必须选择的仪器是________________(填字母组合),还缺少的一种仪器的名称是__________。
(3)探究性质:实验一中,蜡烛由低到高依次熄灭,由此可知二氧化碳的物理性质是______________________________;实验二中,溶液颜色的变化是______________________;实验三中,澄清的石灰水变浑浊,反应的化学方程式是______________________________。
(4)拓展应用:将图甲所示装置倾斜使两种药品混合,即可制得气体。利用该装置制取氧气发生反应的化学方程式为______________________________,制得的氧气能用排水法收集,原因是______________________________,用排水法收集氧气时,判断氧气收集满的方法是____________________________。利用图甲装置还可制取氢气,制得的氢气点燃前需验纯,用化学方程式说明需验纯的原因____________________________________________________。
四、计算题(14分)
18.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8 g这种石灰石样品,把40 g稀盐酸分四次加入,测量过程所得数据见下表(提示:石灰石样品中含有的杂质不溶于水,不与盐酸反应),请计算:
序号 加入稀盐酸的质量/g 剩余固体质量/g
第一次 10 5.5
第二次 10 3.0
第三次 10 1.2
第四次 10 n
(1)样品中碳酸钙的质量分数为________。
(2)上表中n的数值为________。
(3)求反应生成的氯化钙的总质量。
答案
一、1.B 2.C 3.D 4.C 5.B
6.C 点拨:氢气在空气中燃烧产生淡蓝色火焰,A错误;一氧化碳具有还原性,与氧化铜反应生成紫红色的铜,黑色固体变红色,B错误;二氧化碳与水反应生成碳酸,碳酸可使石蕊变红,C正确;镁带在氧气中燃烧,发出耀眼的白光,放出大量的热,生成白色固体,D错误。
7.B 点拨:二氧化碳与水化合生成碳酸,碳酸使石蕊溶液变红色,二氧化碳不具有酸性,B不正确。
8.B 点拨:金刚石和石墨的物理性质有很大差异是因为碳原子的排列方式不同,A错误;C60可表示1个C60分子由60个碳原子构成,B正确;碳单质燃烧,氧气充足时生成二氧化碳,氧气不足时生成一氧化碳,C错误;二氧化碳能和碳反应生成一氧化碳,此反应吸收热量,D错误。
9.C
10.B 点拨:一氧化碳是可燃性气体,点燃CO前要检验其纯度,防止发生爆炸,A正确;反应②,是一氧化碳与氧化铜反应生成铜和二氧化碳,固体减少的质量不等于生成CO2的质量,B不正确;反应③,是碳与氧化铜反应生成铜和二氧化碳,CuO提供氧,发生还原反应,是氧化剂,C正确;反应④,是碳与氧气反应,可能生成一氧化碳或二氧化碳,碳和氧气的质量比为12∶32=3∶8时生成二氧化碳;碳和氧气的质量比为(12×2) ∶32=3∶4时生成一氧化碳,参加反应的C和O2的质量比为3∶5时,丁中含CO和CO2,D正确。
11.D 点拨:由实验现象可知,将气体通过过量澄清石灰水,出现白色浑浊,证明气体中一定含有CO2;将剩余气体干燥后点燃,有水生成,证明气体中一定有H2或CH4中至少一种。对照选项,含CO2的选项只有D。
12.C 点拨:安装方法:d在a的台上,e固定在a上,c安装到e上。关闭c中的开关,盐酸从c中被压回烧杯中,固体与液体分离,反应停止。
二、13.(1)①②③ (2)③⑥ (3)④ (4)⑤ (5)③④⑤ (6)④
14.(1)常温下,碳的化学性质稳定
(2)O2(或CuO);C+O2CO2(或C+2CuO2Cu+CO2↑)
(3)CO+CuOCu+CO2(其他合理答案均可)
(4)水雾
15.(1)物理 (2)C+H2OCO+H2
(3)化合 (4)SO3
(5)原料全部转化为产品(或原子利用率100%,或实现“零排放”,或不对环境造成污染等)
16.(1)CO2 (2)B、C (3)CO2+H2O===H2CO3
(4)检验CO2 (5)放热 (6)CuO
三、17.(1)锥形瓶 (2)CaCO3+2HCl===CaCl2+H2O+CO2↑;B、C、D、G;铁架台 (3)二氧化碳的密度比空气大;由紫色变为红色;CO2+Ca(OH)2===
CaCO3↓+H2O
(4)2H2O22H2O+O2↑;氧气不易溶于水且不与水反应;集气瓶口有较大气泡冒出;2H2+O22H2O
四、18.解:(1)85% (2)1.2
(3)设反应生成的氯化钙的总质量为x。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 111
8 g-1.2 g x
= x=7.548 g
答:反应生成的氯化钙的总质量为7.548 g。
点拨:(1)8 g石灰石样品中含有1.2 g杂质,样品中碳酸钙的质量分数=×100%=85%;
(2)第3次加入10 g稀盐酸,充分反应后,碳酸钙完全反应,故n=1.2。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
