10.1常见的酸和碱同步练习-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 10.1常见的酸和碱同步练习-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 113.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-24 00:00:00 | ||
图片预览



文档简介
10.1 常见的酸和碱 同步练习
一、单选题
1.下列关于酸、碱的说法错误的是
A.苛性钠、烧碱、火碱都是氢氧化钠
B.氢氧化钙可以用来改良酸性土壤
C.稀盐酸能够使酚酞溶液变红
D.生活中许多常见的物质(如柠檬、柑橘)中含有酸
2.衣服上沾了铁锈(主要成分是Fe2O3),直接用水很难洗净,要除去白色衬衣上的铁锈,你认为比较适宜的液体是
A.白醋 B.酱油 C.酒精 D.洗洁精
3.利用推理、归纳的方法得出以下结论,其中正确的是
A.金刚石、石墨是组成元素相同的单质,所以化学性质相似
B.氧化物中一定含有氧元素,所以含氧元素的化合物一定是氧化物
C.碱溶液pH>7,所以pH>7的溶液均为碱溶液
D.铁的金属活动性比铝弱,所以铁制品比铝制品更耐腐蚀
4.下列物质的用途仅与其物理性质有关的是( )
A.活性炭作吸附剂 B.稀盐酸作除锈剂
C.铁粉作脱氧剂 D.生石灰作干燥剂
5.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
6.如图所示,装置气密性良好,若想使∪形管中a端液面下降,b端液面上升,不能达到目的的选项是( )
选项 A B C D
X 水 水 稀盐酸 水
Y 氢氧化钠固体 生石灰 镁 硝酸铵
A.A B.B C.C D.D
7.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
8.生活中很多变化都伴随着热量变化,下列热量变化不是由化学变化引起的是
A.苹果腐烂发热 B.生石灰与水混合放热
C.灯管通电发热 D.暖宝宝贴(内含铁粉 活性炭 NaCl固体等)发热
9.下列关于物质用途的叙述错误的是
A.稀硫酸可用于除铁锈
B.氢氧化钙用于改良酸性土壤
C.氧气可用作燃料
D.明矾用于处理水中微小悬浮物
10.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
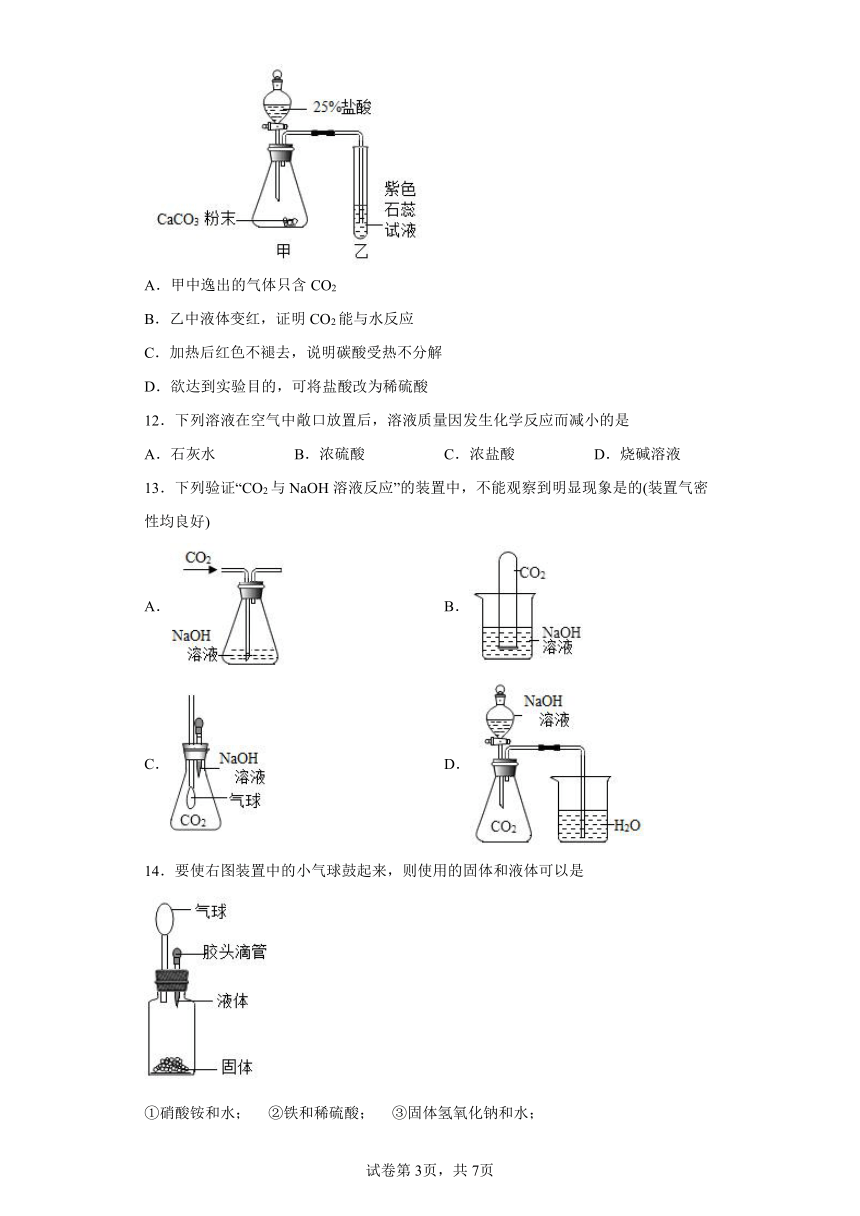
11.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
12.下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
13.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象是的(装置气密性均良好)
A. B.
C. D.
14.要使右图装置中的小气球鼓起来,则使用的固体和液体可以是
①硝酸铵和水; ②铁和稀硫酸; ③固体氢氧化钠和水;
④生石灰和水; ⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.②③⑤ D.②④⑤
15.中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是
A.食醋 B.烧碱 C.草木灰 D.生石灰
16.下列常用来改良酸性土壤的物质是
A.熟石灰
B.硫酸
C.烧碱
D.食盐
二、综合应用题
17.氢氧化钠、氢氧化钙是两种常见的碱
(1) 它们有一些相似的化学性质,其原因是溶液中都含有________
(2) 可作某些气体干燥剂的是________
(3) 用氢氧化钙溶液检验二氧化碳,反应的化学方程式为 __________。
(4) 根据化学方程式计算,用7.4kg氢氧化钙能中和硫酸厂排放的污水中硫酸的质量是多少________?
18.NaOH是重要的化工原料,研究其制备、检验、贮存及应用具有重要意义。
(1)某化学兴趣实验小组的同学在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液。小甲同学不小心将这两种溶液混合在-一起,结果产生__________________的现象,说明氢氧化钠溶液变质了,这是NaOH与空气中的__________反应的结果。
(2)小乙同学想用酚酞试液检验氢氧化钠溶液是否变质,你认为这种方法是否可行,为什么 ___________________。
(3)NaOH俗称“火碱”、“烧碱” ,有很强的腐蚀性,不小心洒到皮肤上,应立即用大量水冲洗,再涂上__________________溶液(写名称)。
(4)小丙同学欲用氢氧化钠固体与水配制50g溶质质量分数为10%的氢氧化钠溶液,下列选项错误的是_________________ (填“A”、“B”、“C”、“D”之一)。
①需称取氢氧化钠固体5.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,可将氢氧化钠放在纸上称量
④用量筒量取水的体积时,俯视读数
⑤溶解时用玻璃棒搅拌,玻璃棒的作用是引流
A只有①③④
B只有②④⑤
C只有③④⑤
D只有②③⑤
(5)小丁同学将10%的氢氧化钠溶液,逐滴加入到60g硫酸镁溶液中。当滴入10%氢氧化钠溶液40g时,恰好完全反应。试通过计算,求此时所得不饱和溶液的质量___________________ (计算结果精确至0.1g)。
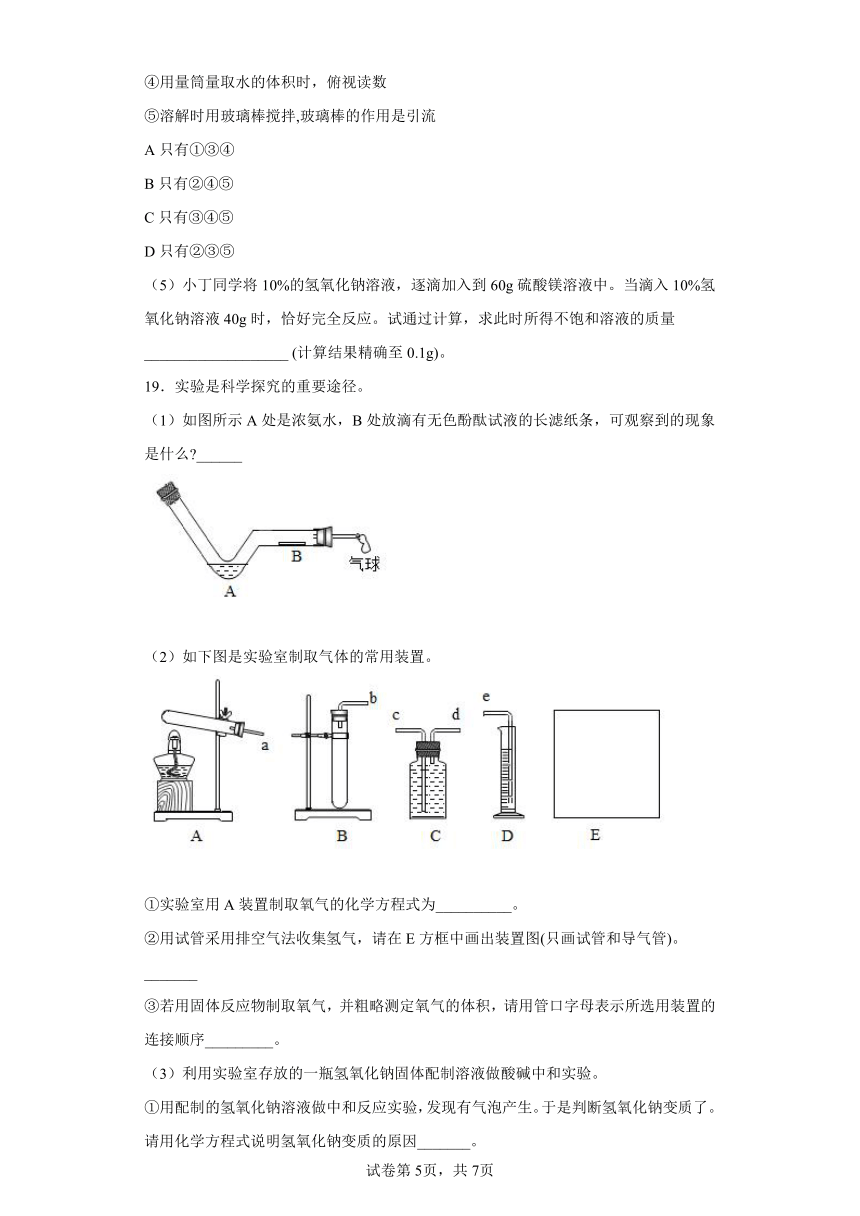
19.实验是科学探究的重要途径。
(1)如图所示A处是浓氨水,B处放滴有无色酚酞试液的长滤纸条,可观察到的现象是什么 ______
(2)如下图是实验室制取气体的常用装置。
①实验室用A装置制取氧气的化学方程式为__________。
②用试管采用排空气法收集氢气,请在E方框中画出装置图(只画试管和导气管)。_______
③若用固体反应物制取氧气,并粗略测定氧气的体积,请用管口字母表示所选用装置的连接顺序_________。
(3)利用实验室存放的一瓶氢氧化钠固体配制溶液做酸碱中和实验。
①用配制的氢氧化钠溶液做中和反应实验,发现有气泡产生。于是判断氢氧化钠变质了。请用化学方程式说明氢氧化钠变质的原因_______。
②为探究氢氧化钠是否完全变质,设计了两个实验方案。
方案1:取少量上述氢氧化钠溶液样品,滴加几滴酚酞溶液,溶液变成红色
方案2:取少量上述氢氧化钠溶液样品,加入饱和石灰水,静置,取上层清液,滴加几滴酚酞溶液。发现溶液变红色。
于是小明认为样品中还会有氢氧化钠,没有完全变质。
小红认为小明的两个实验方案都不能达到目的,她的理由是__________。
③请你设计一个方案来验证氢氧化钠是否完全变质___________。
(4)取10g变质的氢氧化钠固体样品溶于90g水中,向其中滴加过量饱和石灰水,对沉淀过滤洗涤、烘干后称量为0.5g。求样品中氢氧化钠的质量分数。______
20.波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成。
(1)硫酸铜所含阳离子的符号是_________,生石灰加水过程中会_________(填“放”或“吸”)热。
(2)波尔多液不能用铁质容器来配制的原因是(用化学方程式说明)____________。
(3)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO)。若要制取8.4t氧化钙,根据化学方程式计算需要加热分解碳酸钙的质量是多少_____?
21.化学兴趣小组的同学在老师的带领下,用如图装置来探究炼铁的化学反应原理,将混有CO2和H2O的CO通入盛有10g赤铁矿粉末(杂质不与酸反应)的硬质玻璃管中,充分加热至赤铁矿粉末完全反应,熄灭酒精喷灯,继续通入CO至硬质玻璃管冷却,把反应后的固体进行酸洗、干燥,称量剩余固体杂质的质量为1.2g。
(1)A装置的作用是______。
(2)根据实验数据计算化学兴趣小组的同学冶炼得到铁的质量(写出计算过程)。
(3)从环保角度考虑,请写出一种尾气处理方法:______。
22.(1)从a氮气、b金刚石、c石墨、d氢气、e 甲烷、f一氧化碳、g干冰七种物质中,选择与下列叙述相对应的物质的字母序号,填写在空白处。
①最清洁的燃料_____; ②可做电极的非金属单质_____。
③用作人工降雨剂的是_____;④可以用来裁玻璃、切割大理石的是_____。
⑤能与人体血红蛋白结合使人中毒的气体_____。
(2)现有初中化学常见的四种物质:氢气、一氧化碳、二氧化碳、甲烷,将它们分成两组:一组为一氧化碳、氢气、甲烷; 另一组为二氧化碳。其分组的依据是_____:(可能有一个或多个答案)
①是否为气体 ②是否有可燃性 ③是否为化合物 ④是否为单质
(3)能鉴别CO和CO2的方法有:_____(可能有一个或多个答案)。
①分别通入紫色石蕊溶液 ②分别点燃
③分别通入澄清石灰水 ④分别通入灼热的氧化铜
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.A
4.A
5.C
6.D
7.D
8.C
9.C
10.A
11.D
12.A
13.A
14.B
15.C
16.A
17. OH- 氢氧化钠固体 Ca(OH)2+CO2=CaCO3↓+H2O 9.8。
18. 白色沉淀(或沉淀、浑浊) CO2 (或“二氧化碳”) 不可行,氢氧化钠溶液变质生成的碳酸钠显碱性,同样能使无色酚酞变红 硼酸 C 97.1g
19. B处放滴有无色酚酞试液的长滤纸条变红色 a→d→c→e 方案1中,碳酸钠溶液也能使酚酞溶液变红;方案2中碳酸钠与氢氧化钙反应的生成物是氢氧化钠,也能使酚酞溶液变红 取少量上述氢氧化钠溶液样品,加入足量氯化钙溶液(或氯化钡溶液等),静置,取上层清液滴加几滴酚酞溶液,若溶液变成红色,则氢氧化钠没有完全变质;若溶液没有变成红色,则氢氧化钠全部变质 94.7%
20. Cu2+ 放 Fe+CuSO4=Cu+FeSO4
解:设若要制取8.4t氧化钙,需要加热分解碳酸钙的质量是x。
,x=15t
答:需要加热分解碳酸钙的质量为15t。
21.(1)除去CO中混有的CO2和H2O
(2)6.16g
解:10g赤铁矿粉末中含有氧化铁的质量为10g-1.2g=8.8g。设8.8g氧化铁被完全还原生成铁的质量为x,则:
(3)在尾部放一盏燃着的酒精灯/气球收集
22. d c g b f ② ①②③④
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列关于酸、碱的说法错误的是
A.苛性钠、烧碱、火碱都是氢氧化钠
B.氢氧化钙可以用来改良酸性土壤
C.稀盐酸能够使酚酞溶液变红
D.生活中许多常见的物质(如柠檬、柑橘)中含有酸
2.衣服上沾了铁锈(主要成分是Fe2O3),直接用水很难洗净,要除去白色衬衣上的铁锈,你认为比较适宜的液体是
A.白醋 B.酱油 C.酒精 D.洗洁精
3.利用推理、归纳的方法得出以下结论,其中正确的是
A.金刚石、石墨是组成元素相同的单质,所以化学性质相似
B.氧化物中一定含有氧元素,所以含氧元素的化合物一定是氧化物
C.碱溶液pH>7,所以pH>7的溶液均为碱溶液
D.铁的金属活动性比铝弱,所以铁制品比铝制品更耐腐蚀
4.下列物质的用途仅与其物理性质有关的是( )
A.活性炭作吸附剂 B.稀盐酸作除锈剂
C.铁粉作脱氧剂 D.生石灰作干燥剂
5.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
6.如图所示,装置气密性良好,若想使∪形管中a端液面下降,b端液面上升,不能达到目的的选项是( )
选项 A B C D
X 水 水 稀盐酸 水
Y 氢氧化钠固体 生石灰 镁 硝酸铵
A.A B.B C.C D.D
7.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
8.生活中很多变化都伴随着热量变化,下列热量变化不是由化学变化引起的是
A.苹果腐烂发热 B.生石灰与水混合放热
C.灯管通电发热 D.暖宝宝贴(内含铁粉 活性炭 NaCl固体等)发热
9.下列关于物质用途的叙述错误的是
A.稀硫酸可用于除铁锈
B.氢氧化钙用于改良酸性土壤
C.氧气可用作燃料
D.明矾用于处理水中微小悬浮物
10.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
11.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
12.下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
13.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象是的(装置气密性均良好)
A. B.
C. D.
14.要使右图装置中的小气球鼓起来,则使用的固体和液体可以是
①硝酸铵和水; ②铁和稀硫酸; ③固体氢氧化钠和水;
④生石灰和水; ⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.②③⑤ D.②④⑤
15.中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是
A.食醋 B.烧碱 C.草木灰 D.生石灰
16.下列常用来改良酸性土壤的物质是
A.熟石灰
B.硫酸
C.烧碱
D.食盐
二、综合应用题
17.氢氧化钠、氢氧化钙是两种常见的碱
(1) 它们有一些相似的化学性质,其原因是溶液中都含有________
(2) 可作某些气体干燥剂的是________
(3) 用氢氧化钙溶液检验二氧化碳,反应的化学方程式为 __________。
(4) 根据化学方程式计算,用7.4kg氢氧化钙能中和硫酸厂排放的污水中硫酸的质量是多少________?
18.NaOH是重要的化工原料,研究其制备、检验、贮存及应用具有重要意义。
(1)某化学兴趣实验小组的同学在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液。小甲同学不小心将这两种溶液混合在-一起,结果产生__________________的现象,说明氢氧化钠溶液变质了,这是NaOH与空气中的__________反应的结果。
(2)小乙同学想用酚酞试液检验氢氧化钠溶液是否变质,你认为这种方法是否可行,为什么 ___________________。
(3)NaOH俗称“火碱”、“烧碱” ,有很强的腐蚀性,不小心洒到皮肤上,应立即用大量水冲洗,再涂上__________________溶液(写名称)。
(4)小丙同学欲用氢氧化钠固体与水配制50g溶质质量分数为10%的氢氧化钠溶液,下列选项错误的是_________________ (填“A”、“B”、“C”、“D”之一)。
①需称取氢氧化钠固体5.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,可将氢氧化钠放在纸上称量
④用量筒量取水的体积时,俯视读数
⑤溶解时用玻璃棒搅拌,玻璃棒的作用是引流
A只有①③④
B只有②④⑤
C只有③④⑤
D只有②③⑤
(5)小丁同学将10%的氢氧化钠溶液,逐滴加入到60g硫酸镁溶液中。当滴入10%氢氧化钠溶液40g时,恰好完全反应。试通过计算,求此时所得不饱和溶液的质量___________________ (计算结果精确至0.1g)。
19.实验是科学探究的重要途径。
(1)如图所示A处是浓氨水,B处放滴有无色酚酞试液的长滤纸条,可观察到的现象是什么 ______
(2)如下图是实验室制取气体的常用装置。
①实验室用A装置制取氧气的化学方程式为__________。
②用试管采用排空气法收集氢气,请在E方框中画出装置图(只画试管和导气管)。_______
③若用固体反应物制取氧气,并粗略测定氧气的体积,请用管口字母表示所选用装置的连接顺序_________。
(3)利用实验室存放的一瓶氢氧化钠固体配制溶液做酸碱中和实验。
①用配制的氢氧化钠溶液做中和反应实验,发现有气泡产生。于是判断氢氧化钠变质了。请用化学方程式说明氢氧化钠变质的原因_______。
②为探究氢氧化钠是否完全变质,设计了两个实验方案。
方案1:取少量上述氢氧化钠溶液样品,滴加几滴酚酞溶液,溶液变成红色
方案2:取少量上述氢氧化钠溶液样品,加入饱和石灰水,静置,取上层清液,滴加几滴酚酞溶液。发现溶液变红色。
于是小明认为样品中还会有氢氧化钠,没有完全变质。
小红认为小明的两个实验方案都不能达到目的,她的理由是__________。
③请你设计一个方案来验证氢氧化钠是否完全变质___________。
(4)取10g变质的氢氧化钠固体样品溶于90g水中,向其中滴加过量饱和石灰水,对沉淀过滤洗涤、烘干后称量为0.5g。求样品中氢氧化钠的质量分数。______
20.波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成。
(1)硫酸铜所含阳离子的符号是_________,生石灰加水过程中会_________(填“放”或“吸”)热。
(2)波尔多液不能用铁质容器来配制的原因是(用化学方程式说明)____________。
(3)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO)。若要制取8.4t氧化钙,根据化学方程式计算需要加热分解碳酸钙的质量是多少_____?
21.化学兴趣小组的同学在老师的带领下,用如图装置来探究炼铁的化学反应原理,将混有CO2和H2O的CO通入盛有10g赤铁矿粉末(杂质不与酸反应)的硬质玻璃管中,充分加热至赤铁矿粉末完全反应,熄灭酒精喷灯,继续通入CO至硬质玻璃管冷却,把反应后的固体进行酸洗、干燥,称量剩余固体杂质的质量为1.2g。
(1)A装置的作用是______。
(2)根据实验数据计算化学兴趣小组的同学冶炼得到铁的质量(写出计算过程)。
(3)从环保角度考虑,请写出一种尾气处理方法:______。
22.(1)从a氮气、b金刚石、c石墨、d氢气、e 甲烷、f一氧化碳、g干冰七种物质中,选择与下列叙述相对应的物质的字母序号,填写在空白处。
①最清洁的燃料_____; ②可做电极的非金属单质_____。
③用作人工降雨剂的是_____;④可以用来裁玻璃、切割大理石的是_____。
⑤能与人体血红蛋白结合使人中毒的气体_____。
(2)现有初中化学常见的四种物质:氢气、一氧化碳、二氧化碳、甲烷,将它们分成两组:一组为一氧化碳、氢气、甲烷; 另一组为二氧化碳。其分组的依据是_____:(可能有一个或多个答案)
①是否为气体 ②是否有可燃性 ③是否为化合物 ④是否为单质
(3)能鉴别CO和CO2的方法有:_____(可能有一个或多个答案)。
①分别通入紫色石蕊溶液 ②分别点燃
③分别通入澄清石灰水 ④分别通入灼热的氧化铜
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.A
4.A
5.C
6.D
7.D
8.C
9.C
10.A
11.D
12.A
13.A
14.B
15.C
16.A
17. OH- 氢氧化钠固体 Ca(OH)2+CO2=CaCO3↓+H2O 9.8。
18. 白色沉淀(或沉淀、浑浊) CO2 (或“二氧化碳”) 不可行,氢氧化钠溶液变质生成的碳酸钠显碱性,同样能使无色酚酞变红 硼酸 C 97.1g
19. B处放滴有无色酚酞试液的长滤纸条变红色 a→d→c→e 方案1中,碳酸钠溶液也能使酚酞溶液变红;方案2中碳酸钠与氢氧化钙反应的生成物是氢氧化钠,也能使酚酞溶液变红 取少量上述氢氧化钠溶液样品,加入足量氯化钙溶液(或氯化钡溶液等),静置,取上层清液滴加几滴酚酞溶液,若溶液变成红色,则氢氧化钠没有完全变质;若溶液没有变成红色,则氢氧化钠全部变质 94.7%
20. Cu2+ 放 Fe+CuSO4=Cu+FeSO4
解:设若要制取8.4t氧化钙,需要加热分解碳酸钙的质量是x。
,x=15t
答:需要加热分解碳酸钙的质量为15t。
21.(1)除去CO中混有的CO2和H2O
(2)6.16g
解:10g赤铁矿粉末中含有氧化铁的质量为10g-1.2g=8.8g。设8.8g氧化铁被完全还原生成铁的质量为x,则:
(3)在尾部放一盏燃着的酒精灯/气球收集
22. d c g b f ② ①②③④
答案第1页,共2页
答案第1页,共2页
同课章节目录
