第九单元溶液检测卷--2021-2022学年九年级化学人教版下册(word版 含解析)
文档属性
| 名称 | 第九单元溶液检测卷--2021-2022学年九年级化学人教版下册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 70.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-24 00:00:00 | ||
图片预览



文档简介
第九单元《溶液》检测卷
一、单选题(共15小题)
1.如图是三种固体物质的溶解度曲线,下列说法正确的是( )
A. 物质c的溶解度随温度的升高而增大
B. 物质a的溶解度大于物质c的溶解度
C.t2℃时,60 g物质a与100 g水充分混合后所得溶液的总质量为160 g
D. 将t1℃ b、c两种物质的饱和溶液升温至t2℃,溶液中溶质质量分数不变的是b溶液
2.下列关于生理盐水的说法中,错误的是( )
A. 生理盐水的溶剂是水
B. 生理盐水各部分性质和密度都一样
C. 只要外界条件不改变,生理盐水的溶质和溶剂不会分离
D. 生理盐水中的氯化钠是由氯化钠分子构成的
3.下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列有关说法正确的是( )
A.t2℃时,在两个各盛有100 g水的烧杯中,分别加入50 g的甲、乙两种固体,充分搅拌,所得甲、乙溶液中溶质的质量不等
B.t1℃时,等质量甲、乙溶液中所含溶剂的质量甲等于乙
C. 乙中含有少量甲,可以用冷却热饱和溶液的方法提纯甲
D.t2℃时,将甲、乙的饱和溶液降温至t1℃,甲溶液析出晶体的质量大于乙
4.饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )
A. 溶质的质量
B. 溶剂的质量
C. 溶液的质量
D. 溶质与溶剂的质量比
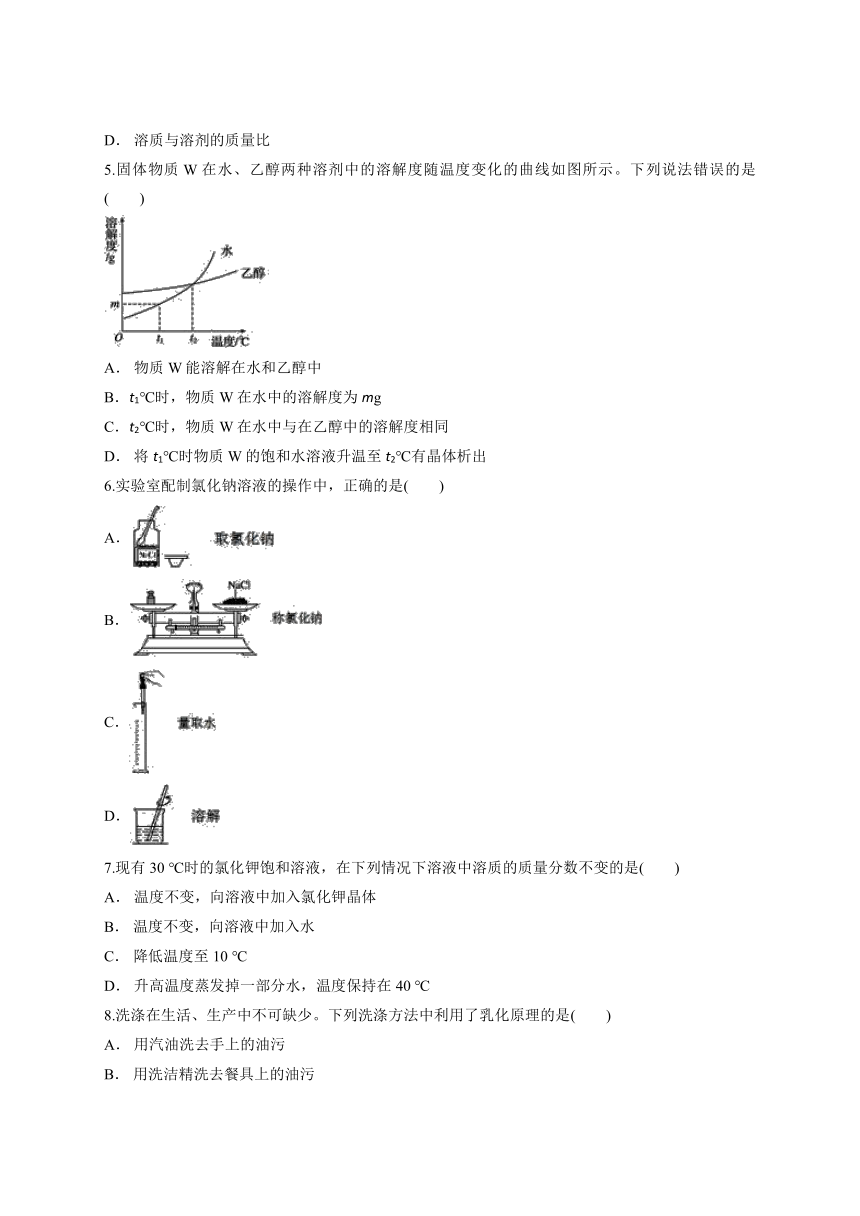
5.固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示。下列说法错误的是( )
A. 物质W能溶解在水和乙醇中
B.t1℃时,物质W在水中的溶解度为mg
C.t2℃时,物质W在水中与在乙醇中的溶解度相同
D. 将t1℃时物质W的饱和水溶液升温至t2℃有晶体析出
6.实验室配制氯化钠溶液的操作中,正确的是( )
A.
B.
C.
D.
7.现有30 ℃时的氯化钾饱和溶液,在下列情况下溶液中溶质的质量分数不变的是( )
A. 温度不变,向溶液中加入氯化钾晶体
B. 温度不变,向溶液中加入水
C. 降低温度至10 ℃
D. 升高温度蒸发掉一部分水,温度保持在40 ℃
8.洗涤在生活、生产中不可缺少。下列洗涤方法中利用了乳化原理的是( )
A. 用汽油洗去手上的油污
B. 用洗洁精洗去餐具上的油污
C. 用酒精洗去试管中的碘
D. 用水洗去手上的泥灰
9.下列关于生理盐水的说法中,错误的是( )
A. 生理盐水的溶剂是水
B. 各部分一样咸体现了溶液成分的均一性
C. 饮用生理盐水可以为人体补充无机盐
D. 水分子是保持NaCl性质的最小微粒
10.将60 ℃时的硝酸钾饱和溶液降温至20 ℃,不发生变化的是( )
A. 硝酸钾的溶解度
B. 溶液中溶质的质量
C. 溶液中溶剂的质量
D. 溶液中溶质的质量分数
11.对多数固体物质,使其不饱和溶液变为饱和溶液时,一般可采取的办法是( )
A. 增加压强
B. 升高温度
C. 加溶质或减少溶剂
D. 降低温度
12.下列关于溶液的说法正确的是( )
A. 溶液都是均一、稳定的纯净物
B. 饱和溶液的浓度一定大于不饱和溶液的浓度
C. 温度和溶剂的种类不会影响物质的溶解性
D. 配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解等步骤
13.下列说法正确的是( )
A. 水和冰块的共存物是悬浊液
B. 凡均一、稳定、透明、澄清的液体一定是溶液
C. 一定温度下,一定量溶剂里不能再溶解某物质的溶液就是该物质的饱和溶液
D. 在泥水里,泥是溶质,水是溶剂
14.下列关于溶液的说法正确的是( )
A. 溶液一定是无色、透明的混合物
B. 溶液加水稀释前后,溶质的质量一定不变
C. 溶剂量不变时,加入的溶质越多,溶液质量一定越大
D. 物质溶于水形成溶液时,溶液温度一定不变
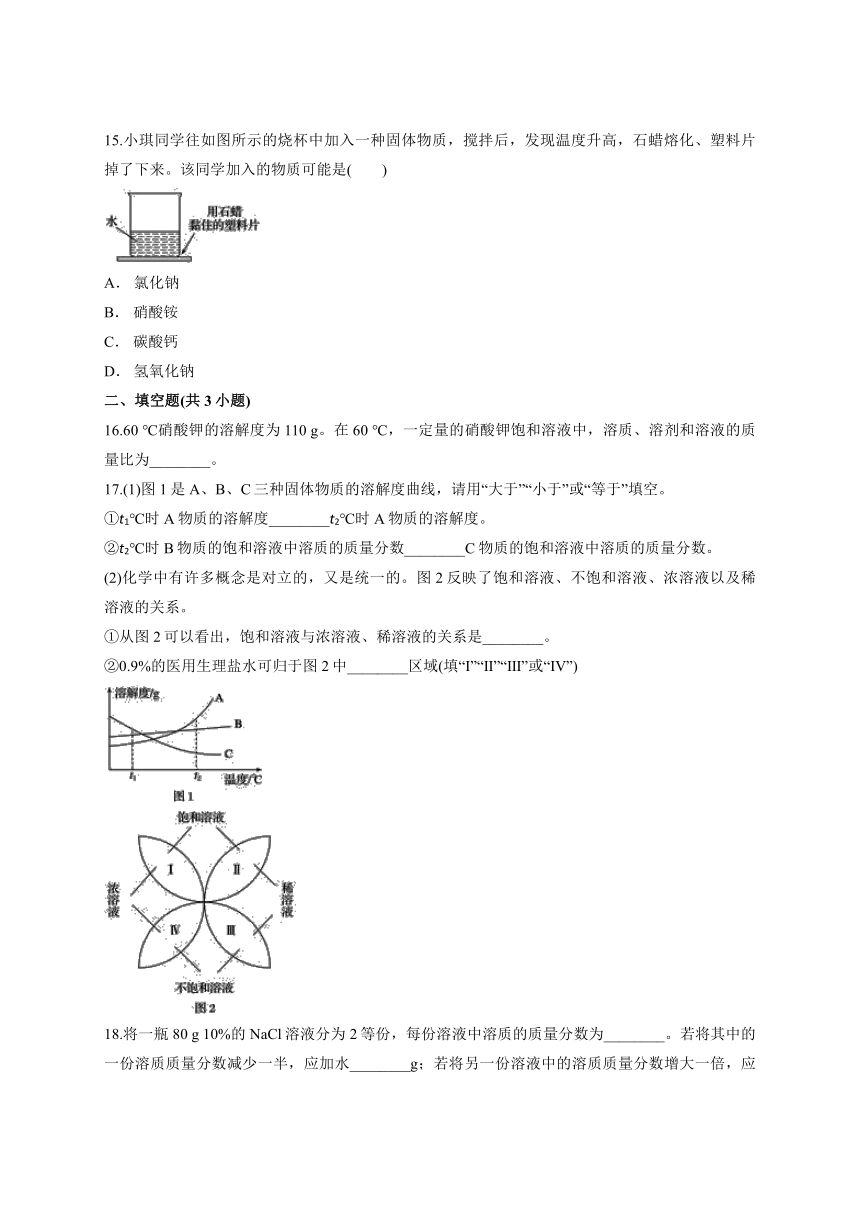
15.小琪同学往如图所示的烧杯中加入一种固体物质,搅拌后,发现温度升高,石蜡熔化、塑料片掉了下来。该同学加入的物质可能是( )
A. 氯化钠
B. 硝酸铵
C. 碳酸钙
D. 氢氧化钠
二、填空题(共3小题)
16.60 ℃硝酸钾的溶解度为110 g。在60 ℃,一定量的硝酸钾饱和溶液中,溶质、溶剂和溶液的质量比为________。
17.(1)图1是A、B、C三种固体物质的溶解度曲线,请用“大于”“小于”或“等于”填空。
①t1℃时A物质的溶解度________t2℃时A物质的溶解度。
②t2℃时B物质的饱和溶液中溶质的质量分数________C物质的饱和溶液中溶质的质量分数。
(2)化学中有许多概念是对立的,又是统一的。图2反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
①从图2可以看出,饱和溶液与浓溶液、稀溶液的关系是________。
②0.9%的医用生理盐水可归于图2中________区域(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)
18.将一瓶80 g 10%的NaCl溶液分为2等份,每份溶液中溶质的质量分数为________。若将其中的一份溶质质量分数减少一半,应加水________g;若将另一份溶液中的溶质质量分数增大一倍,应加入NaCl ________ g。
三、计算题(共3小题)
19.生理盐水是溶质质量分数约为0.9%的氯化钠溶液。现用500克生理盐水给患者输液,进入患者体内的氯化钠的质量约为多少克?若用溶质质量分数为18%的氯化钠溶液配制500克溶质质量分数为0.9%的生理盐水,需18%的氯化钠溶液多少克?需水多少克?(写出计算过程)
20.20 g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5 g,同时生成氢气0.4 g。试计算:
(1)样品中锌的质量分数;
(2)完全反应后生成溶液中溶质的质量分数;
(3)所用稀硫酸的质量分数 (计算结果保留到0.01%)。
21.某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25 g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8 g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:
(1)当加入212 g稀盐酸时,放出气体的质量为___________g。
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106 g稀盐酸(即A点)时烧杯中溶液的溶质质量分数为多少?(写出计算过程)
答案解析
1.【答案】D
【解析】A项,根据固体的溶解度曲线可知:c的溶解度随温度的升高而减小,错误;B项,要比较物质的溶解度大小,须限定温度,否则无法比较,错误;C项,t2℃时a的溶解度是50 g,即100 g水中最多溶解50 g的a,故60 g a物质加入到100 g水中,不会完全溶解,所得溶液为150 g,错误;D项,由图可知:b的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,将b、c两种物质的饱和溶液由t1℃升温至t2℃,b变为不饱和溶液,溶质和溶剂的质量不变,b物质的溶液中溶质质量分数不变,c析出晶体,溶质质量分数减小,正确。故选D。
2.【答案】D
【解析】溶液是均一的,也就是各部分的性质、密度是相同的,溶液是稳定的,也就是只要外界条件不改变,溶质和溶剂不会分离,氯化钠溶液是由氯化钠固体和水形成的,氯化钠是溶质,水是溶剂,氯化钠由氯离子和钠离子构成,溶解后仍然以离子形式分散在水分子中间。
3.【答案】A
【解析】A项,从溶解度曲线可看出,t2℃时,甲的溶解度=50 g,而乙的溶解度<50 g,故在两个各盛有100 g水的烧杯中,分别加入50 g的甲、乙两种固体,充分搅拌,甲能全部溶解,而乙有剩余,故所得甲、乙溶液中溶质的质量不等,正确;B项,t1℃时,甲、乙物质的溶解度相等,但没有指明是饱和溶液,故等质量甲、乙溶液中所含溶剂的质量甲不一定等于乙,错误;C项,从溶解度曲线可看出,甲的溶解度随温度的升高变化较大,而乙的溶解度随温度的升高变化较小,故乙中含有少量甲,可以用冷却热饱和溶液的方法提纯乙,错误;D项,没有指明高温时的溶液是否是等质量,故无法判断析出晶体量的多少,错误。故选A。
4.【答案】A
【解析】A项,饱和溶液用水稀释变成不饱和溶液的过程中,溶质的质量不变,正确;B项,饱和溶液用水稀释变成不饱和溶液的过程中,溶剂的质量增加,错误;C项,饱和溶液用水稀释变成不饱和溶液的过程中,溶液的质量增加,错误;D项,饱和溶液用水稀释变成不饱和溶液的过程中,溶质与溶剂的质量比发生改变,错误。
5.【答案】D
【解析】A项,从该物质在水和乙醇中的溶解度曲线不难看出,该物质既能溶于水,也能溶于乙醇,正确;B项,根据物质W在水中的溶解度曲线可知,在t1℃时,W在水的溶解度是mg,正确;C项,由于在t2℃时,物质W在两种溶剂中的溶解度曲线交于一点,说明该物质在这两种溶剂中的溶解度相等,正确;D项,由于物质W在水中的溶解度随温度的升高而增大,因此升温时,它的饱和水溶液不会有晶体析出,反而会变成不饱和溶液,错误。
6.【答案】D
【解析】A项,取用固体粉末状药品时,应用药匙取用,图中瓶塞没有倒放,错误;B项,托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,错误;C项,使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到量筒内或接触量筒内壁,应垂直悬空在量筒口上方滴加液体,防止污染胶头滴管,错误;D项,进行溶解操作时,在烧杯中进行,用玻璃棒进行搅拌,正确。故选D。
7.【答案】A
【解析】A项,因温度不变,虽向溶液中加入氯化钾晶体,但溶质及溶液的质量未变,溶质的质量分数也不变;B项,因溶液的质量变了,所以溶质的质量分数也相应发生变化;C项,降低温度有晶体析出,溶剂质量不变,其溶质的质量分数变小;D项,因溶液中溶剂质量减小,所以溶质的质量分数将增大。故本题正确答案为A。
8.【答案】B
【解析】A项,用汽油洗去手上的油污,是利用汽油能溶解油污来考虑,错误;B项,用洗洁精洗去餐具上的油污,符合乳化作用的特点,属于乳化作用,正确;C项,用酒精洗去试管中的碘,是利用酒精能溶解碘所以能洗去,错误;D项,用水洗去手上的泥灰是利用溶解原理洗去可溶性污物,利用悬浊液形成的原理洗去不溶性污物,错误。故选B。
9.【答案】D
【解析】A项,生理盐水是氯化钠溶于水形成的混合物,溶质是氯化钠,溶剂是水,正确;B项,溶液具有均一性即各部分性质相同,即各部分一样咸,正确;C项,生理盐水中的氯化钠属于无机盐,所以饮用生理盐水可以为人体补充无机盐,正确;D项,保持NaCl性质的最小微粒是钠离子和氯离子,错误。故选D。
10.【答案】C
【解析】A项,硝酸钾的溶解度随温度的降低而减小,因此将60 ℃时的硝酸钾饱和溶液降温至20 ℃,硝酸钾的溶解度会减小,正确;B项,将60 ℃时的硝酸钾饱和溶液降温至20 ℃,随硝酸钾溶解度的减小而析出硝酸钾晶体,溶液中溶质质量减小,错误;C项,降温时,饱和硝酸钾溶液析出硝酸钾晶体,而硝酸钾晶体中不含结晶水,因此析出晶体后的溶液中溶剂的质量不变,正确;D项,由于降温而使溶液中的溶质硝酸钾结晶析出,因此析出晶体后的溶液中溶质的质量分数减小,错误。故选C。
11.【答案】C
【解析】增加溶质或蒸发溶剂,都可使不饱和溶液变成饱和溶液(常用方法);大多数物质的溶解度随温度升高而增大,降温也可使不饱和溶液变成饱和溶液。故选C。
12.【答案】D
【解析】A项,溶液都是均一、稳定的混合物,错误;B项,饱和溶液比不饱和溶液浓的条件:同一温度、同一溶质,饱和溶液比不饱和溶液浓,错误;C项,影响物质溶解性的因素有温度、溶质的种类、溶剂的种类,错误;D项,配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解等步骤,正确。故选D。
13.【答案】C
【解析】A项,理解冰就是固态的水,冰水实际就是一种物质组成的,属于纯净物,错误;B项,溶液一定属于混合物,液体不一定就是混合物,水是最熟悉的液体属于纯净物,错误;C项,饱和溶液是一定温度下,一定量溶剂里不能再溶解某物质的溶液就是该物质的饱和溶液,正确;D项,泥水形成的是悬浊液,无法形成均一、稳定的混合物,溶质、溶剂是溶液的组成,错误。故选C。
14.【答案】B
【解析】A项,溶液不一定是无色、透明的。如糖水、茶水等;B项,溶液加水稀释前后,溶质的质量守恒;C项,溶剂量不变时,当加入的溶质达到饱和时,溶液质量不再增加;D项,物质溶于水形成溶液时,溶液温度可能升高、降低或不变。
15.【答案】D
【解析】氢氧化钠溶于水放热,硝酸铵溶于水吸热,氯化钠溶于水吸热放热不明显,碳酸钙不溶于水。
16.【答案】11∶10∶21
【解析】60 ℃硝酸钾的溶解度为110 g,说明在60 ℃ 100 g水中最多溶解110 g硝酸钾,所以溶液的质量为100 g+110 g=210 g,故溶质、溶剂和溶液的质量比=110 g∶100 g∶210 g=11∶10∶21。
17.【答案】(1)①小于 ②大于 (2)①饱和溶液可能是浓溶液,也可能是稀溶液 ②Ⅲ
【解析】①由图示可知A物质的溶解度随温度的升高而增大,所以t1℃时A物质的溶解度小于t2℃时A物质的溶解度;
②饱和溶液的溶质质量分数:,所以饱和溶液质量分数的大小取决于溶解度的大小,t2℃时B物质的溶解度大于C物质的溶解度,所以t2℃时B物质的饱和溶液中溶质的质量分数大于C物质的饱和溶液中溶质的质量分数;
(3)①由图示可知有的饱和溶液是浓溶液,有的饱和溶液是稀溶液,所以饱和溶液可能是浓溶液,也可能是稀溶液;
②含溶质较多的溶液属于浓溶液,含溶质较少的溶液属于稀溶液,0.9%的医用生理盐水属于稀溶液,还属于不饱和溶液。
18.【答案】10% 40 5
【解析】溶液具有均一性,因此其中每一份溶液的质量分数和原溶液相同,仍为10%;
将其中的一份溶质质量分数减少一半,即变为5%的溶液,设需要加水的质量为x
40 g×10%=(40 g+x)×5%x=40 g;
将另一份溶液中的溶质质量分数增大一倍,即变为20%的溶液,设需要加入氯化钠的质量为y,=20%,y=5 g。
19.【答案】4.5 g 475 g
【解析】溶质的质量=溶液的质量×溶质的质量分数;
⑴ 500 g×0.9%=4.5 g
⑵在稀释的过程中溶质的质量不变;
设需18%的氯化钠溶液的质量为X;
X×18%=500 g×0.9%或X×18%=4.5 g
解之得:X=25 g
需加水质量:500 g-25 g=475 g
20.【答案】(1)65% (2)40% (3)28.87%
【解析】样品中的锌能与稀硫酸反应生成硫酸锌和氢气,可利用化学方程式根据锌与生成的氢气的质量比求出锌的质量;反应后的溶液是硫酸锌溶液,利用化学方程式可计算出溶质硫酸锌的质量;
设样品中锌的质量为x;生成的硫酸锌的质量为y;硫酸中溶质的质量为z;
(1)x=13 g,W=×100%=65%
(2)y=32.2 g,W′=×100%=40%
(3)z=19.6 g,W′=×100%≈28.87%
21.【答案】(1)4.4 (2)80% (3)5.6%
【解析】(1)根据图像,可以看出当加入106 g稀盐酸的时候,反应就结束,产生气体质量为4.4 g,所以当加入212 g 稀盐酸时,放出气体的质量仍然为4.4 g。
(2)发生反应:Na2CO3+2HCl===2NaCl+H2O+CO2↑,根据方程式中碳酸钠与二氧化碳的质量关系可算出碳酸钠的质量,进而可以计算碳酸钠样品中碳酸钠的质量分数,反应后得到的是NaCl溶液,所以也可根据方程式中NaCl与二氧化碳的质量关系,求出溶液中溶质的质量,
解:设碳酸钠的质量为x,生成的NaCl质量为y
100∶44=x∶4.4 g,x=10.6 g
(2)碳酸钠样品中碳酸钠的质量分数=
117∶44=y∶4.4 g,y=11.7 g。
又由于反应后溶液质量=10.6 g+95.8 g+106 g-4.4 g=208 g。
(3)溶液的溶质质量分数=。
一、单选题(共15小题)
1.如图是三种固体物质的溶解度曲线,下列说法正确的是( )
A. 物质c的溶解度随温度的升高而增大
B. 物质a的溶解度大于物质c的溶解度
C.t2℃时,60 g物质a与100 g水充分混合后所得溶液的总质量为160 g
D. 将t1℃ b、c两种物质的饱和溶液升温至t2℃,溶液中溶质质量分数不变的是b溶液
2.下列关于生理盐水的说法中,错误的是( )
A. 生理盐水的溶剂是水
B. 生理盐水各部分性质和密度都一样
C. 只要外界条件不改变,生理盐水的溶质和溶剂不会分离
D. 生理盐水中的氯化钠是由氯化钠分子构成的
3.下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列有关说法正确的是( )
A.t2℃时,在两个各盛有100 g水的烧杯中,分别加入50 g的甲、乙两种固体,充分搅拌,所得甲、乙溶液中溶质的质量不等
B.t1℃时,等质量甲、乙溶液中所含溶剂的质量甲等于乙
C. 乙中含有少量甲,可以用冷却热饱和溶液的方法提纯甲
D.t2℃时,将甲、乙的饱和溶液降温至t1℃,甲溶液析出晶体的质量大于乙
4.饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )
A. 溶质的质量
B. 溶剂的质量
C. 溶液的质量
D. 溶质与溶剂的质量比
5.固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示。下列说法错误的是( )
A. 物质W能溶解在水和乙醇中
B.t1℃时,物质W在水中的溶解度为mg
C.t2℃时,物质W在水中与在乙醇中的溶解度相同
D. 将t1℃时物质W的饱和水溶液升温至t2℃有晶体析出
6.实验室配制氯化钠溶液的操作中,正确的是( )
A.
B.
C.
D.
7.现有30 ℃时的氯化钾饱和溶液,在下列情况下溶液中溶质的质量分数不变的是( )
A. 温度不变,向溶液中加入氯化钾晶体
B. 温度不变,向溶液中加入水
C. 降低温度至10 ℃
D. 升高温度蒸发掉一部分水,温度保持在40 ℃
8.洗涤在生活、生产中不可缺少。下列洗涤方法中利用了乳化原理的是( )
A. 用汽油洗去手上的油污
B. 用洗洁精洗去餐具上的油污
C. 用酒精洗去试管中的碘
D. 用水洗去手上的泥灰
9.下列关于生理盐水的说法中,错误的是( )
A. 生理盐水的溶剂是水
B. 各部分一样咸体现了溶液成分的均一性
C. 饮用生理盐水可以为人体补充无机盐
D. 水分子是保持NaCl性质的最小微粒
10.将60 ℃时的硝酸钾饱和溶液降温至20 ℃,不发生变化的是( )
A. 硝酸钾的溶解度
B. 溶液中溶质的质量
C. 溶液中溶剂的质量
D. 溶液中溶质的质量分数
11.对多数固体物质,使其不饱和溶液变为饱和溶液时,一般可采取的办法是( )
A. 增加压强
B. 升高温度
C. 加溶质或减少溶剂
D. 降低温度
12.下列关于溶液的说法正确的是( )
A. 溶液都是均一、稳定的纯净物
B. 饱和溶液的浓度一定大于不饱和溶液的浓度
C. 温度和溶剂的种类不会影响物质的溶解性
D. 配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解等步骤
13.下列说法正确的是( )
A. 水和冰块的共存物是悬浊液
B. 凡均一、稳定、透明、澄清的液体一定是溶液
C. 一定温度下,一定量溶剂里不能再溶解某物质的溶液就是该物质的饱和溶液
D. 在泥水里,泥是溶质,水是溶剂
14.下列关于溶液的说法正确的是( )
A. 溶液一定是无色、透明的混合物
B. 溶液加水稀释前后,溶质的质量一定不变
C. 溶剂量不变时,加入的溶质越多,溶液质量一定越大
D. 物质溶于水形成溶液时,溶液温度一定不变
15.小琪同学往如图所示的烧杯中加入一种固体物质,搅拌后,发现温度升高,石蜡熔化、塑料片掉了下来。该同学加入的物质可能是( )
A. 氯化钠
B. 硝酸铵
C. 碳酸钙
D. 氢氧化钠
二、填空题(共3小题)
16.60 ℃硝酸钾的溶解度为110 g。在60 ℃,一定量的硝酸钾饱和溶液中,溶质、溶剂和溶液的质量比为________。
17.(1)图1是A、B、C三种固体物质的溶解度曲线,请用“大于”“小于”或“等于”填空。
①t1℃时A物质的溶解度________t2℃时A物质的溶解度。
②t2℃时B物质的饱和溶液中溶质的质量分数________C物质的饱和溶液中溶质的质量分数。
(2)化学中有许多概念是对立的,又是统一的。图2反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
①从图2可以看出,饱和溶液与浓溶液、稀溶液的关系是________。
②0.9%的医用生理盐水可归于图2中________区域(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)
18.将一瓶80 g 10%的NaCl溶液分为2等份,每份溶液中溶质的质量分数为________。若将其中的一份溶质质量分数减少一半,应加水________g;若将另一份溶液中的溶质质量分数增大一倍,应加入NaCl ________ g。
三、计算题(共3小题)
19.生理盐水是溶质质量分数约为0.9%的氯化钠溶液。现用500克生理盐水给患者输液,进入患者体内的氯化钠的质量约为多少克?若用溶质质量分数为18%的氯化钠溶液配制500克溶质质量分数为0.9%的生理盐水,需18%的氯化钠溶液多少克?需水多少克?(写出计算过程)
20.20 g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5 g,同时生成氢气0.4 g。试计算:
(1)样品中锌的质量分数;
(2)完全反应后生成溶液中溶质的质量分数;
(3)所用稀硫酸的质量分数 (计算结果保留到0.01%)。
21.某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25 g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8 g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:
(1)当加入212 g稀盐酸时,放出气体的质量为___________g。
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106 g稀盐酸(即A点)时烧杯中溶液的溶质质量分数为多少?(写出计算过程)
答案解析
1.【答案】D
【解析】A项,根据固体的溶解度曲线可知:c的溶解度随温度的升高而减小,错误;B项,要比较物质的溶解度大小,须限定温度,否则无法比较,错误;C项,t2℃时a的溶解度是50 g,即100 g水中最多溶解50 g的a,故60 g a物质加入到100 g水中,不会完全溶解,所得溶液为150 g,错误;D项,由图可知:b的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,将b、c两种物质的饱和溶液由t1℃升温至t2℃,b变为不饱和溶液,溶质和溶剂的质量不变,b物质的溶液中溶质质量分数不变,c析出晶体,溶质质量分数减小,正确。故选D。
2.【答案】D
【解析】溶液是均一的,也就是各部分的性质、密度是相同的,溶液是稳定的,也就是只要外界条件不改变,溶质和溶剂不会分离,氯化钠溶液是由氯化钠固体和水形成的,氯化钠是溶质,水是溶剂,氯化钠由氯离子和钠离子构成,溶解后仍然以离子形式分散在水分子中间。
3.【答案】A
【解析】A项,从溶解度曲线可看出,t2℃时,甲的溶解度=50 g,而乙的溶解度<50 g,故在两个各盛有100 g水的烧杯中,分别加入50 g的甲、乙两种固体,充分搅拌,甲能全部溶解,而乙有剩余,故所得甲、乙溶液中溶质的质量不等,正确;B项,t1℃时,甲、乙物质的溶解度相等,但没有指明是饱和溶液,故等质量甲、乙溶液中所含溶剂的质量甲不一定等于乙,错误;C项,从溶解度曲线可看出,甲的溶解度随温度的升高变化较大,而乙的溶解度随温度的升高变化较小,故乙中含有少量甲,可以用冷却热饱和溶液的方法提纯乙,错误;D项,没有指明高温时的溶液是否是等质量,故无法判断析出晶体量的多少,错误。故选A。
4.【答案】A
【解析】A项,饱和溶液用水稀释变成不饱和溶液的过程中,溶质的质量不变,正确;B项,饱和溶液用水稀释变成不饱和溶液的过程中,溶剂的质量增加,错误;C项,饱和溶液用水稀释变成不饱和溶液的过程中,溶液的质量增加,错误;D项,饱和溶液用水稀释变成不饱和溶液的过程中,溶质与溶剂的质量比发生改变,错误。
5.【答案】D
【解析】A项,从该物质在水和乙醇中的溶解度曲线不难看出,该物质既能溶于水,也能溶于乙醇,正确;B项,根据物质W在水中的溶解度曲线可知,在t1℃时,W在水的溶解度是mg,正确;C项,由于在t2℃时,物质W在两种溶剂中的溶解度曲线交于一点,说明该物质在这两种溶剂中的溶解度相等,正确;D项,由于物质W在水中的溶解度随温度的升高而增大,因此升温时,它的饱和水溶液不会有晶体析出,反而会变成不饱和溶液,错误。
6.【答案】D
【解析】A项,取用固体粉末状药品时,应用药匙取用,图中瓶塞没有倒放,错误;B项,托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,错误;C项,使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到量筒内或接触量筒内壁,应垂直悬空在量筒口上方滴加液体,防止污染胶头滴管,错误;D项,进行溶解操作时,在烧杯中进行,用玻璃棒进行搅拌,正确。故选D。
7.【答案】A
【解析】A项,因温度不变,虽向溶液中加入氯化钾晶体,但溶质及溶液的质量未变,溶质的质量分数也不变;B项,因溶液的质量变了,所以溶质的质量分数也相应发生变化;C项,降低温度有晶体析出,溶剂质量不变,其溶质的质量分数变小;D项,因溶液中溶剂质量减小,所以溶质的质量分数将增大。故本题正确答案为A。
8.【答案】B
【解析】A项,用汽油洗去手上的油污,是利用汽油能溶解油污来考虑,错误;B项,用洗洁精洗去餐具上的油污,符合乳化作用的特点,属于乳化作用,正确;C项,用酒精洗去试管中的碘,是利用酒精能溶解碘所以能洗去,错误;D项,用水洗去手上的泥灰是利用溶解原理洗去可溶性污物,利用悬浊液形成的原理洗去不溶性污物,错误。故选B。
9.【答案】D
【解析】A项,生理盐水是氯化钠溶于水形成的混合物,溶质是氯化钠,溶剂是水,正确;B项,溶液具有均一性即各部分性质相同,即各部分一样咸,正确;C项,生理盐水中的氯化钠属于无机盐,所以饮用生理盐水可以为人体补充无机盐,正确;D项,保持NaCl性质的最小微粒是钠离子和氯离子,错误。故选D。
10.【答案】C
【解析】A项,硝酸钾的溶解度随温度的降低而减小,因此将60 ℃时的硝酸钾饱和溶液降温至20 ℃,硝酸钾的溶解度会减小,正确;B项,将60 ℃时的硝酸钾饱和溶液降温至20 ℃,随硝酸钾溶解度的减小而析出硝酸钾晶体,溶液中溶质质量减小,错误;C项,降温时,饱和硝酸钾溶液析出硝酸钾晶体,而硝酸钾晶体中不含结晶水,因此析出晶体后的溶液中溶剂的质量不变,正确;D项,由于降温而使溶液中的溶质硝酸钾结晶析出,因此析出晶体后的溶液中溶质的质量分数减小,错误。故选C。
11.【答案】C
【解析】增加溶质或蒸发溶剂,都可使不饱和溶液变成饱和溶液(常用方法);大多数物质的溶解度随温度升高而增大,降温也可使不饱和溶液变成饱和溶液。故选C。
12.【答案】D
【解析】A项,溶液都是均一、稳定的混合物,错误;B项,饱和溶液比不饱和溶液浓的条件:同一温度、同一溶质,饱和溶液比不饱和溶液浓,错误;C项,影响物质溶解性的因素有温度、溶质的种类、溶剂的种类,错误;D项,配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解等步骤,正确。故选D。
13.【答案】C
【解析】A项,理解冰就是固态的水,冰水实际就是一种物质组成的,属于纯净物,错误;B项,溶液一定属于混合物,液体不一定就是混合物,水是最熟悉的液体属于纯净物,错误;C项,饱和溶液是一定温度下,一定量溶剂里不能再溶解某物质的溶液就是该物质的饱和溶液,正确;D项,泥水形成的是悬浊液,无法形成均一、稳定的混合物,溶质、溶剂是溶液的组成,错误。故选C。
14.【答案】B
【解析】A项,溶液不一定是无色、透明的。如糖水、茶水等;B项,溶液加水稀释前后,溶质的质量守恒;C项,溶剂量不变时,当加入的溶质达到饱和时,溶液质量不再增加;D项,物质溶于水形成溶液时,溶液温度可能升高、降低或不变。
15.【答案】D
【解析】氢氧化钠溶于水放热,硝酸铵溶于水吸热,氯化钠溶于水吸热放热不明显,碳酸钙不溶于水。
16.【答案】11∶10∶21
【解析】60 ℃硝酸钾的溶解度为110 g,说明在60 ℃ 100 g水中最多溶解110 g硝酸钾,所以溶液的质量为100 g+110 g=210 g,故溶质、溶剂和溶液的质量比=110 g∶100 g∶210 g=11∶10∶21。
17.【答案】(1)①小于 ②大于 (2)①饱和溶液可能是浓溶液,也可能是稀溶液 ②Ⅲ
【解析】①由图示可知A物质的溶解度随温度的升高而增大,所以t1℃时A物质的溶解度小于t2℃时A物质的溶解度;
②饱和溶液的溶质质量分数:,所以饱和溶液质量分数的大小取决于溶解度的大小,t2℃时B物质的溶解度大于C物质的溶解度,所以t2℃时B物质的饱和溶液中溶质的质量分数大于C物质的饱和溶液中溶质的质量分数;
(3)①由图示可知有的饱和溶液是浓溶液,有的饱和溶液是稀溶液,所以饱和溶液可能是浓溶液,也可能是稀溶液;
②含溶质较多的溶液属于浓溶液,含溶质较少的溶液属于稀溶液,0.9%的医用生理盐水属于稀溶液,还属于不饱和溶液。
18.【答案】10% 40 5
【解析】溶液具有均一性,因此其中每一份溶液的质量分数和原溶液相同,仍为10%;
将其中的一份溶质质量分数减少一半,即变为5%的溶液,设需要加水的质量为x
40 g×10%=(40 g+x)×5%x=40 g;
将另一份溶液中的溶质质量分数增大一倍,即变为20%的溶液,设需要加入氯化钠的质量为y,=20%,y=5 g。
19.【答案】4.5 g 475 g
【解析】溶质的质量=溶液的质量×溶质的质量分数;
⑴ 500 g×0.9%=4.5 g
⑵在稀释的过程中溶质的质量不变;
设需18%的氯化钠溶液的质量为X;
X×18%=500 g×0.9%或X×18%=4.5 g
解之得:X=25 g
需加水质量:500 g-25 g=475 g
20.【答案】(1)65% (2)40% (3)28.87%
【解析】样品中的锌能与稀硫酸反应生成硫酸锌和氢气,可利用化学方程式根据锌与生成的氢气的质量比求出锌的质量;反应后的溶液是硫酸锌溶液,利用化学方程式可计算出溶质硫酸锌的质量;
设样品中锌的质量为x;生成的硫酸锌的质量为y;硫酸中溶质的质量为z;
(1)x=13 g,W=×100%=65%
(2)y=32.2 g,W′=×100%=40%
(3)z=19.6 g,W′=×100%≈28.87%
21.【答案】(1)4.4 (2)80% (3)5.6%
【解析】(1)根据图像,可以看出当加入106 g稀盐酸的时候,反应就结束,产生气体质量为4.4 g,所以当加入212 g 稀盐酸时,放出气体的质量仍然为4.4 g。
(2)发生反应:Na2CO3+2HCl===2NaCl+H2O+CO2↑,根据方程式中碳酸钠与二氧化碳的质量关系可算出碳酸钠的质量,进而可以计算碳酸钠样品中碳酸钠的质量分数,反应后得到的是NaCl溶液,所以也可根据方程式中NaCl与二氧化碳的质量关系,求出溶液中溶质的质量,
解:设碳酸钠的质量为x,生成的NaCl质量为y
100∶44=x∶4.4 g,x=10.6 g
(2)碳酸钠样品中碳酸钠的质量分数=
117∶44=y∶4.4 g,y=11.7 g。
又由于反应后溶液质量=10.6 g+95.8 g+106 g-4.4 g=208 g。
(3)溶液的溶质质量分数=。
同课章节目录
