2021-2022学年人教版初三化学下册第十单元课题2 酸和碱的中和反应 综合训练(word版有答案)
文档属性
| 名称 | 2021-2022学年人教版初三化学下册第十单元课题2 酸和碱的中和反应 综合训练(word版有答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 402.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-24 00:00:00 | ||
图片预览


文档简介
2021-2022学年人教版初三化学下册第十单元课题2 酸和碱的中和反应 综合训练
班级__________ 座号_____ 姓名__________ 分数__________
一、选择题
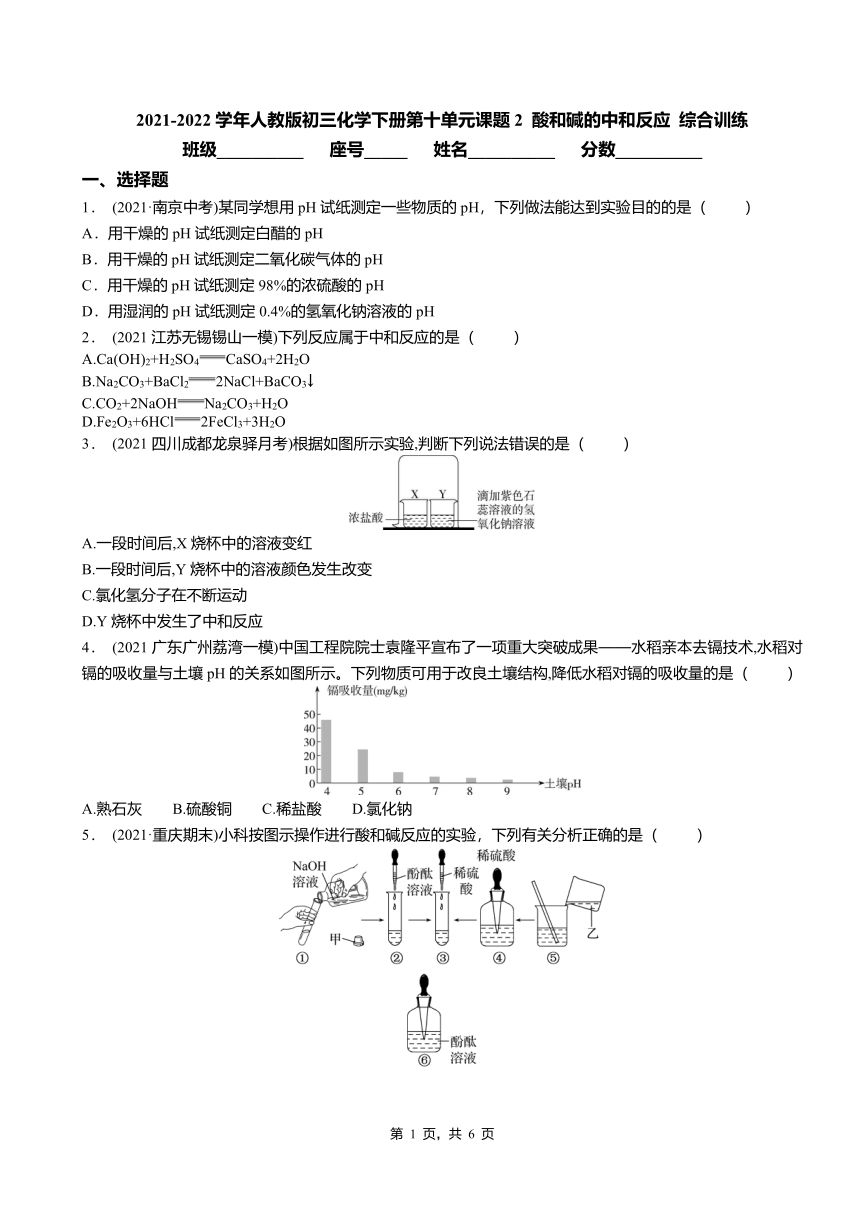
1. (2021·南京中考)某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )
A.用干燥的pH试纸测定白醋的pH
B.用干燥的pH试纸测定二氧化碳气体的pH
C.用干燥的pH试纸测定98%的浓硫酸的pH
D.用湿润的pH试纸测定0.4%的氢氧化钠溶液的pH
2. (2021江苏无锡锡山一模)下列反应属于中和反应的是( )
A.Ca(OH)2+H2SO4CaSO4+2H2O
B.Na2CO3+BaCl22NaCl+BaCO3↓
C.CO2+2NaOHNa2CO3+H2O
D.Fe2O3+6HCl2FeCl3+3H2O
3. (2021四川成都龙泉驿月考)根据如图所示实验,判断下列说法错误的是( )
A.一段时间后,X烧杯中的溶液变红
B.一段时间后,Y烧杯中的溶液颜色发生改变
C.氯化氢分子在不断运动
D.Y烧杯中发生了中和反应
4. (2021广东广州荔湾一模)中国工程院院士袁隆平宣布了一项重大突破成果——水稻亲本去镉技术,水稻对镉的吸收量与土壤pH的关系如图所示。下列物质可用于改良土壤结构,降低水稻对镉的吸收量的是( )
A.熟石灰 B.硫酸铜 C.稀盐酸 D.氯化钠
5. (2021·重庆期末)小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞
B.③中反应的实质是H+和OH-结合生成水
C.⑤中稀释浓硫酸时,倒入的乙物质是水
D.⑥中酚酞溶液用完后,滴管及时清洗
6. 几种适宜作物生长的PH范围如下:水稻6.0~7.0,棉花6.0~6.8,甘蔗6.0~8.0,茶树5.0~6.0。取某地土壤浸出液加几滴紫色石蕊试液,溶液略显蓝色,则这种土壤适宜种植的作物是( )
A.水稻 B.棉花 C.茶树 D.甘蔗
7. 下图表示的是身边一些物质在常温时的近似pH,有关这些物质的比较或判断不正确的是( )
A.草木灰水呈碱性 B.胃酸过多的病人宜吃鸡蛋清
C.橘子的酸性比柠檬的强 D.萝卜呈酸性
8. 下表是某酸碱指示剂在不同pH范围内显示的颜色,向滴有少量该指示剂的稀盐酸中,逐滴加入氢氧化钠溶液,出现的颜色变化可能是( )
颜色 红 橙 绿 蓝 紫
pH范围 1~3 4~5 6~7 8~10 11~14
A.由红到蓝 B.由绿到橙 C.由蓝到绿 D.由紫到红
9. 将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下。下列说法不正确的是( )
A.反应前后阴、阳离子的总数目不变
B.反应前后溶液的总质量不变
C.反应后溶液呈中性
D.反应前后元素种类不变
10.如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
A.X显酸性
B.Y可能是水
C.Z可能是某种盐溶液
D.Z可使紫色石蕊试液变红
二、填空题
11.为了探究盐酸和氢氧化钠是否发生反应,设计并进行了如图所示的实验。实验中可观察到的现象是________,该现象能证明盐酸和氢氧化钠发生了化学反应,其理由是________。
12.常温下,向pH=10的氢氧化钾溶液中滴加酚酞试液,溶液呈________色,再加入一定量的盐酸后溶液的pH=4,此时溶液中溶质的化学式是________,反应的化学方程式是___________________________________。
13.如图为某中和反应的示意图。图中的阴离子符号为__ __;写出一个符合如图反应的化学方程式:__ __;若将酸滴入加有酚酞的碱溶液中,至恰好中和时溶液由红色变为__ __。
14.(2021·泸州质检)某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降。经农场技术员测定:雨水pH约为4、土壤pH约为5。已知一些重要作物最适宜生长的土壤的pH为水稻6~7、小麦6.3~7.5、玉米6~7、油菜6~7、马铃薯4.8~5.5。
(1)根据以上数据,你认为这种土壤最适合种植的作物是__ __。
(2)继续种小麦,你认为最好选用以下__ __(填序号)试剂来改良该土壤。
A.工业盐酸 B.氢氧化钠 C.熟石灰
(3)该厂的下列整治措施不妥的是__ __(填序号)。
A.废气循环利用
B.将废气点燃后排放
C.废水用碱中和后排放
D.改进工艺,减少废气废水的产生
15.(2021吉林长春南关一模)某化学兴趣小组按如图所示操作进行酸碱中和反应的实验,回答下列问题:
(1)图E是稀释浓硫酸的操作示意图,乙烧杯中的物质应是 。
(2)某同学观察到图C中溶液颜色由 变为 ,认为氢氧化钠与硫酸恰好完全反应,化学方程式是 。
(3)另一位同学想用紫色石蕊溶液、铜粉、锌粒进一步确定反应后的无色溶液中溶质的成分,其中不能达到目的的是 。
三、实验探究题
16.在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:
加入盐酸体积V/mL 2 4 6 8 10 12 14 16 18 20
测得溶液温度t/℃ 15.2 19.6 22.0 26.0 28.2 26.7 25.7 24.7 23.7 22.9
(1)根据曲线讨论溶液温度变化的原因。 ①加入盐酸的量在2~10mL之间时:________;
②加入盐酸的量在10~20mL之间时:________。
(2)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?答:______ __。
17.(2021·上城区一模)小徐为判断酸碱中和反应是否进行完全,往20 g 10 %的氢氧化钠溶液中滴加10 %的盐酸,装置如图1。
图1实验中温度变化如表所示。
加入盐酸的体积V/mL 5 11 18 23 19
溶液温度t/℃ 28.7 34.1 37.8 35.3 33.4
(1)判断方法一:利用指示剂颜色变化判断。溶液红色消失,因为中和反应的结果是酸和碱各自的特性都消失,图2描述的是氢氧化钠与盐酸反应的微观实质,请用符号或文字表示酸碱反应的实质:__ __。
(2)根据表格数据分析,当温度为__ __℃时表明中和反应进行完全。由此得出判断方法二:利用__ __变化来判断是否完全中和。
(3)判断方法三:通过计算获取准确的数据来判断,当加入盐酸溶液的质量为__ __g时反应完全进行。
2021-2022学年人教版初三化学下册第十单元课题2 酸和碱的中和反应 综合训练(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 A A A A B D C A A D
二、填空题
11.
溶液由红色变为无色 氢氧化钠能使酚酞溶液变为红色,溶液由红色变为无色,说明氢氧化钠已反应完
12.红 KCl、HCl KOH+HCl==KCl+H2O
13.Cl-、OH- HCl+NaOH===NaCl+H2O 无色
14.马铃薯 C B
15. (1)水 (2)红色 无色 2NaOH+H2SO4Na2SO4+2H2O (3)铜粉
三、实验探究题
16.(1)随盐酸量增加,中和反应放出热量增多,溶液温度上升 完全反应后不再放热,过量盐酸起冷却降温作用,溶液温度降低
(2)不合理,因为固体氢氧化钠溶于水放热
17.H++OH-→H2O(或氢离子+氢氧根离子→水分子) 37.8 温度 18.25
PAGE
第 1 页,共 1 页
班级__________ 座号_____ 姓名__________ 分数__________
一、选择题
1. (2021·南京中考)某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )
A.用干燥的pH试纸测定白醋的pH
B.用干燥的pH试纸测定二氧化碳气体的pH
C.用干燥的pH试纸测定98%的浓硫酸的pH
D.用湿润的pH试纸测定0.4%的氢氧化钠溶液的pH
2. (2021江苏无锡锡山一模)下列反应属于中和反应的是( )
A.Ca(OH)2+H2SO4CaSO4+2H2O
B.Na2CO3+BaCl22NaCl+BaCO3↓
C.CO2+2NaOHNa2CO3+H2O
D.Fe2O3+6HCl2FeCl3+3H2O
3. (2021四川成都龙泉驿月考)根据如图所示实验,判断下列说法错误的是( )
A.一段时间后,X烧杯中的溶液变红
B.一段时间后,Y烧杯中的溶液颜色发生改变
C.氯化氢分子在不断运动
D.Y烧杯中发生了中和反应
4. (2021广东广州荔湾一模)中国工程院院士袁隆平宣布了一项重大突破成果——水稻亲本去镉技术,水稻对镉的吸收量与土壤pH的关系如图所示。下列物质可用于改良土壤结构,降低水稻对镉的吸收量的是( )
A.熟石灰 B.硫酸铜 C.稀盐酸 D.氯化钠
5. (2021·重庆期末)小科按图示操作进行酸和碱反应的实验,下列有关分析正确的是( )
A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞
B.③中反应的实质是H+和OH-结合生成水
C.⑤中稀释浓硫酸时,倒入的乙物质是水
D.⑥中酚酞溶液用完后,滴管及时清洗
6. 几种适宜作物生长的PH范围如下:水稻6.0~7.0,棉花6.0~6.8,甘蔗6.0~8.0,茶树5.0~6.0。取某地土壤浸出液加几滴紫色石蕊试液,溶液略显蓝色,则这种土壤适宜种植的作物是( )
A.水稻 B.棉花 C.茶树 D.甘蔗
7. 下图表示的是身边一些物质在常温时的近似pH,有关这些物质的比较或判断不正确的是( )
A.草木灰水呈碱性 B.胃酸过多的病人宜吃鸡蛋清
C.橘子的酸性比柠檬的强 D.萝卜呈酸性
8. 下表是某酸碱指示剂在不同pH范围内显示的颜色,向滴有少量该指示剂的稀盐酸中,逐滴加入氢氧化钠溶液,出现的颜色变化可能是( )
颜色 红 橙 绿 蓝 紫
pH范围 1~3 4~5 6~7 8~10 11~14
A.由红到蓝 B.由绿到橙 C.由蓝到绿 D.由紫到红
9. 将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下。下列说法不正确的是( )
A.反应前后阴、阳离子的总数目不变
B.反应前后溶液的总质量不变
C.反应后溶液呈中性
D.反应前后元素种类不变
10.如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
A.X显酸性
B.Y可能是水
C.Z可能是某种盐溶液
D.Z可使紫色石蕊试液变红
二、填空题
11.为了探究盐酸和氢氧化钠是否发生反应,设计并进行了如图所示的实验。实验中可观察到的现象是________,该现象能证明盐酸和氢氧化钠发生了化学反应,其理由是________。
12.常温下,向pH=10的氢氧化钾溶液中滴加酚酞试液,溶液呈________色,再加入一定量的盐酸后溶液的pH=4,此时溶液中溶质的化学式是________,反应的化学方程式是___________________________________。
13.如图为某中和反应的示意图。图中的阴离子符号为__ __;写出一个符合如图反应的化学方程式:__ __;若将酸滴入加有酚酞的碱溶液中,至恰好中和时溶液由红色变为__ __。
14.(2021·泸州质检)某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降。经农场技术员测定:雨水pH约为4、土壤pH约为5。已知一些重要作物最适宜生长的土壤的pH为水稻6~7、小麦6.3~7.5、玉米6~7、油菜6~7、马铃薯4.8~5.5。
(1)根据以上数据,你认为这种土壤最适合种植的作物是__ __。
(2)继续种小麦,你认为最好选用以下__ __(填序号)试剂来改良该土壤。
A.工业盐酸 B.氢氧化钠 C.熟石灰
(3)该厂的下列整治措施不妥的是__ __(填序号)。
A.废气循环利用
B.将废气点燃后排放
C.废水用碱中和后排放
D.改进工艺,减少废气废水的产生
15.(2021吉林长春南关一模)某化学兴趣小组按如图所示操作进行酸碱中和反应的实验,回答下列问题:
(1)图E是稀释浓硫酸的操作示意图,乙烧杯中的物质应是 。
(2)某同学观察到图C中溶液颜色由 变为 ,认为氢氧化钠与硫酸恰好完全反应,化学方程式是 。
(3)另一位同学想用紫色石蕊溶液、铜粉、锌粒进一步确定反应后的无色溶液中溶质的成分,其中不能达到目的的是 。
三、实验探究题
16.在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:
加入盐酸体积V/mL 2 4 6 8 10 12 14 16 18 20
测得溶液温度t/℃ 15.2 19.6 22.0 26.0 28.2 26.7 25.7 24.7 23.7 22.9
(1)根据曲线讨论溶液温度变化的原因。 ①加入盐酸的量在2~10mL之间时:________;
②加入盐酸的量在10~20mL之间时:________。
(2)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?答:______ __。
17.(2021·上城区一模)小徐为判断酸碱中和反应是否进行完全,往20 g 10 %的氢氧化钠溶液中滴加10 %的盐酸,装置如图1。
图1实验中温度变化如表所示。
加入盐酸的体积V/mL 5 11 18 23 19
溶液温度t/℃ 28.7 34.1 37.8 35.3 33.4
(1)判断方法一:利用指示剂颜色变化判断。溶液红色消失,因为中和反应的结果是酸和碱各自的特性都消失,图2描述的是氢氧化钠与盐酸反应的微观实质,请用符号或文字表示酸碱反应的实质:__ __。
(2)根据表格数据分析,当温度为__ __℃时表明中和反应进行完全。由此得出判断方法二:利用__ __变化来判断是否完全中和。
(3)判断方法三:通过计算获取准确的数据来判断,当加入盐酸溶液的质量为__ __g时反应完全进行。
2021-2022学年人教版初三化学下册第十单元课题2 酸和碱的中和反应 综合训练(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 A A A A B D C A A D
二、填空题
11.
溶液由红色变为无色 氢氧化钠能使酚酞溶液变为红色,溶液由红色变为无色,说明氢氧化钠已反应完
12.红 KCl、HCl KOH+HCl==KCl+H2O
13.Cl-、OH- HCl+NaOH===NaCl+H2O 无色
14.马铃薯 C B
15. (1)水 (2)红色 无色 2NaOH+H2SO4Na2SO4+2H2O (3)铜粉
三、实验探究题
16.(1)随盐酸量增加,中和反应放出热量增多,溶液温度上升 完全反应后不再放热,过量盐酸起冷却降温作用,溶液温度降低
(2)不合理,因为固体氢氧化钠溶于水放热
17.H++OH-→H2O(或氢离子+氢氧根离子→水分子) 37.8 温度 18.25
PAGE
第 1 页,共 1 页
同课章节目录
