第十一单元盐 化肥测试题-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第十一单元盐 化肥测试题-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 161.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览


文档简介
第十一单元《盐 化肥》测试题
一、单选题
1.下列物质不能与NaOH溶液反应的是
A.二氧化碳 B.硝酸
C.硫酸铜 D.氢氧化铁
2.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品 B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点 D.碳酸钾可用作化学肥料
3.下列化学反应属于置换反应的是( )
A.H2O+CaO═Ca(OH)2 B.Na2SO4+BaCl2═2NaCl+BaSO4↓
C.H2+CuOCu+H2O D.3CO+Fe2O32Fe+3CO2
4.可以把盐酸、氯化钙、氯化钠三种无色溶液一次区别开的试剂是 ( )
A.Na2CO3溶液 B.NaOH溶液 C.蒸馏水 D.硫酸溶液
5.下列做法正确的是
A.植树造林,防沙降尘 B.焚烧垃圾,净化环境
C.禁用农药,保护水源 D.深埋电池,消除污染
6.下列物质间不能发生反应的是( )
A.稀盐酸和镁条 B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁 D.稀盐酸和氢氧化铜
7.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
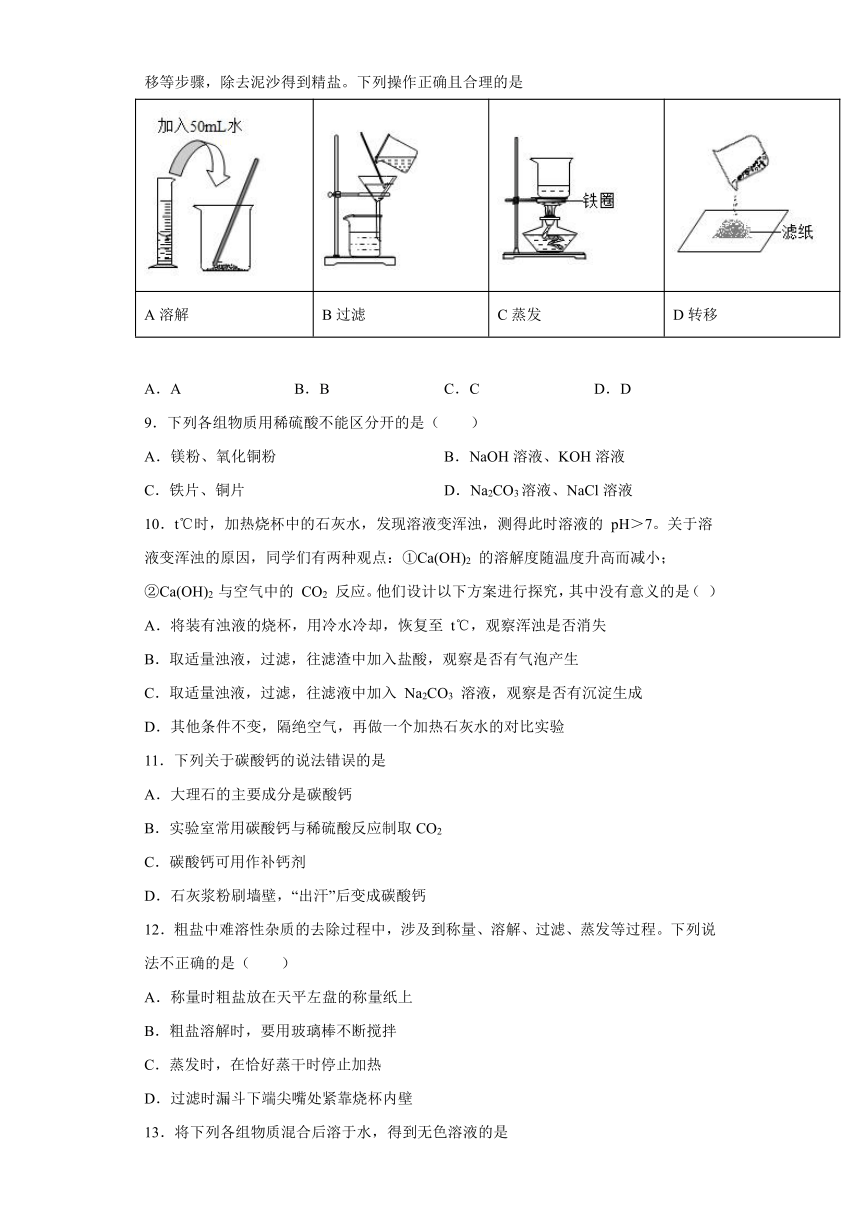
8.已知室温下NaCl的溶解度约为36g。现称取3.6g粗盐,经过溶解、过滤、蒸发、转移等步骤,除去泥沙得到精盐。下列操作正确且合理的是
A溶解 B过滤 C蒸发 D转移
A.A B.B C.C D.D
9.下列各组物质用稀硫酸不能区分开的是( )
A.镁粉、氧化铜粉 B.NaOH溶液、KOH溶液
C.铁片、铜片 D.Na2CO3溶液、NaCl溶液
10.t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH>7。关于溶液变浑浊的原因,同学们有两种观点:①Ca(OH)2 的溶解度随温度升高而减小;②Ca(OH)2 与空气中的 CO2 反应。他们设计以下方案进行探究,其中没有意义的是( )
A.将装有浊液的烧杯,用冷水冷却,恢复至 t℃,观察浑浊是否消失
B.取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C.取适量浊液,过滤,往滤液中加入 Na2CO3 溶液,观察是否有沉淀生成
D.其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
11.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
12.粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
13.将下列各组物质混合后溶于水,得到无色溶液的是
A.NaNO3、KCl、Na2SO4 B.FeCl3、NaOH、KNO3
C.CuSO4、CaCl2、KOH D.BaCl2、K2CO3、H2SO4
14.下列有关氢氧化钠的说法,错误的是( )
A.氢氧化钠俗称烧碱
B.氢氧化钠有强烈的腐蚀性
C.氢氧化钠固体可用于干燥二氧化碳气体
D.氢氧化钠可用于制肥皂、洗涤剂、造纸、纺织工业等
15.粗盐含有少量的MgCl2,CaCl2,Na2SO4等杂质,为了将杂质除干净,先向粗盐溶液中分别加入过量的①NaOH②Na2CO3③BaCl2溶液,过滤,再加入④稀盐酸使溶液的pH=7将最后所得溶液进行蒸发可得到精盐,加入溶液的先后顺序错误的是( )
A.②③①④ B.③②①④ C.①③②④ D.③①②④
二、填空题
16.化学就在我们身边。从①熟石灰②金刚石③氯化钠④干冰四种物质中,选择适当的物质填空(填序号)。
(1)用于炒菜调味的是_____;
(2)用于人工降雨的是_____;
(3)用来裁玻璃的是_____;
(4)用来改良酸性土壤的是_____。
17.化学肥料对农作物的增产具有十分重要的作用,俗话说:“庄稼一枝花,全靠肥当家”。下面是农业生产中广泛施用的几种化学肥料:①NH4NO3 ②KNO3 ③NH4Cl ④
请回答:
(1)属于复合肥料的是______(填序号,下同);
(2)属于铵态氮肥的是______,它们成分中都含有的离子是______(填符号)。
18.化学与我们的生产、生活息息相关。请回答下列问题。
(1)①食盐、②熟石灰、③小苏打、④石墨四种物质在生产、生活中用途广泛。其中可用于制铅笔芯的是_____(填数字序号,下同);可用作面点发酵剂的是_____;常用作食品加工调味的是______;常用于改良酸性土壤的是_____。
(2)农业上,碳酸钾(K2CO3)可用作_____(填“磷”或“钾”)肥。已知碳酸钾溶液呈碱性,则碳酸钾_____(填“能”或“不能”)与铵态氮肥混合施用。
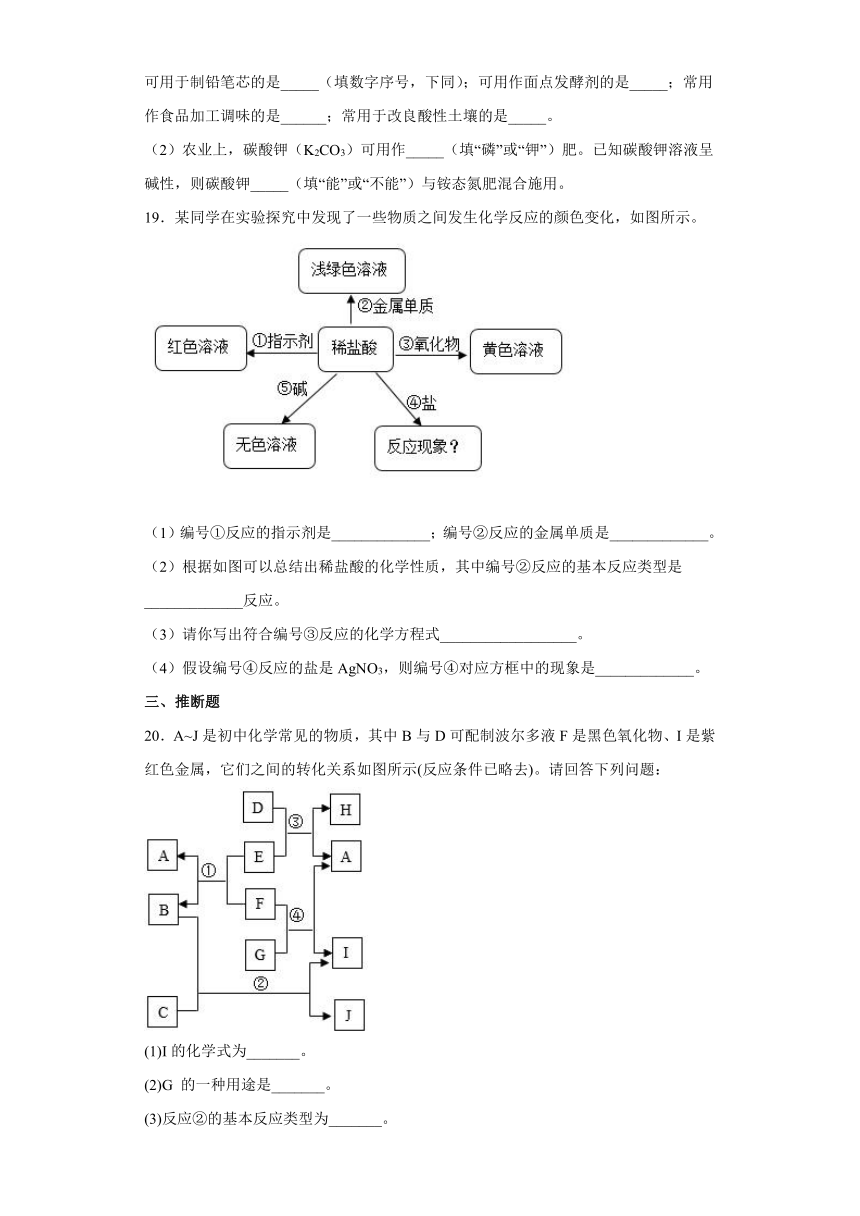
19.某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是_____________;编号②反应的金属单质是_____________。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是_____________反应。
(3)请你写出符合编号③反应的化学方程式__________________。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是_____________。
三、推断题
20.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
21.下图中的物质均为初中化学常见物质,其中A是常见的补钙剂,B是黑色粉末,H是蓝色沉淀。下图是它们之间的转化关系(部分生成物已经略去),请回答:
(1)写出B物质的化学式___________;
(2)写出F+G→H的化学方程式__________________;
(3)写出物质E的用途_________________。(一种即可)
四、实验题
22.依据下图回答问 题
去除粗盐中的泥沙。
(1)实验的步骤是溶解、过滤和______。
(2)过滤操作中用到的玻璃仪器有______。
配制 150 克 10%的氢氧化钠溶液。
(1)称取氢氧化钠的质量为______克。
(2)量取时仰视读数会使实际质量分数______(填“大于”或“小于”)10%。
23.为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳能发生反应。如图所示进行实验(装置气密性良好,实验前弹簧夹K1、K2处于关闭状态)。
资料:CaCl2+Na2CO3═CaCO3↓+2NaCl
实验一:氢氧化钙溶液与稀盐酸恰好完全反应。
(1)实验过程中需缓缓通入氮气,其作用是什么____________?
(2)写出氢氧化钙溶液与稀盐酸恰好完全反应的实验操作及现象__________。
实验二:氢氧化钠溶液与二氧化碳反应。
(3)打开活塞Ⅱ,将足量氢氧化钠溶液加入锥形瓶中,立即关闭活塞Ⅱ,写出利用图示装置证明氢氧化钠溶液与二氧化碳反应的实验操作及现象_______________。
(4)实验后,取B中锥形瓶内的溶液,倒入烧杯中,若溶液呈红色,设计实验方案,探究该溶液中是否有氢氧化钠,写出实验操作、预期现象和结论_______________。
五、计算题
24.我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了杰出贡献。在实际生产的产品碳酸钠中会混有少量的氯化钠,现有纯碱样品,为测定该样品中碳酸钠的质量分数,称取样品6 g,放入20 g水中使其完全溶解,再加入稀盐酸26. 2 g,恰好完全反应,气体全部逸出,得到不饱和氯化钠溶液,溶液的总质量为50 g。试计算:
(1)生成二氧化碳的质量为多少g。
(2)样品中碳酸钠的质量。
(3)反应后所得溶液中溶质的质量分数。
25.有一定质量的BaCl2和BaCO3固体混合物,加入50g稀盐酸,恰好完全反应,生成的2.2g气体全部逸出,再向反应后所得溶液中加入150g水形成不饱和溶液,测得该溶液中含7.1g氯元素。请计算:
(1)原固体混合物的质量;
(2)所加盐酸溶液中溶质质量分数;
(3)反应后所得溶液中溶质的质量分数(计算结果精确至0.1%)。
试卷第1页,共3页
参考答案:
1.D 2.B 3.C 4.A 5.A 6.B 7.B 8.B 9.B 10.C 11.B 12.C 13.A 14.C 15.A
16. ③ ④ ② ①
17. ②④ ①③④
18. ④ ③ ① ② 钾 不能
19. 石蕊试剂 Fe 置换反应 产生白色沉淀
20. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
21. CuO 2NaOH+CuSO4= Na2SO4+Cu(OH)2↓ 改良酸性土壤(合理即可)
22. 蒸发 ①③⑤ 15 小于
23. 搅拌,使氢氧化钙溶液和盐酸充分反应 打开活塞Ⅰ和弹簧夹K1,逐滴滴加稀盐酸,同时鼓入氮气,直至A中溶液恰好由红色变成无色 打开活塞Ⅱ,将足量氢氧化钠溶液加入锥形瓶中,立即关闭活塞Ⅱ,打开K2。锥形瓶中的二氧化碳与氢氧化钠反应生成碳酸钠,压强变小,A装置中的压强大,就会将锥形瓶内的氯化钙流入B中,然后氯化钙与反应生成的碳酸钠反应,生成碳酸钙白色沉淀。因此有白色沉淀生成 取反应后的溶液,滴加氯化钡溶液(或氯化钙溶液)至不再产生沉淀为止,溶液仍为变红,说明该溶液中有氢氧化钠
24.(1)2.2(2)5.3g(3)13.1%
25.解:设固体混合物中BaCO3的质量为x,消耗HCl的质量为y,生成BaCl2的质量为z
(1)氯元素质量7.1g,故所得溶液中BaCl2的质量:
原固体混合物的质量:
(2)所加盐酸溶液中溶质质量分数:
(3)滤液的质量:
所得滤液中溶质的质量分数:
答:原固体混合物的质量20.25g,加入的稀硫酸中溶质的质量分数为7.3%,反应后所得溶液中溶质的质量分数9.5%。
答案第1页,共2页
一、单选题
1.下列物质不能与NaOH溶液反应的是
A.二氧化碳 B.硝酸
C.硫酸铜 D.氢氧化铁
2.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品 B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点 D.碳酸钾可用作化学肥料
3.下列化学反应属于置换反应的是( )
A.H2O+CaO═Ca(OH)2 B.Na2SO4+BaCl2═2NaCl+BaSO4↓
C.H2+CuOCu+H2O D.3CO+Fe2O32Fe+3CO2
4.可以把盐酸、氯化钙、氯化钠三种无色溶液一次区别开的试剂是 ( )
A.Na2CO3溶液 B.NaOH溶液 C.蒸馏水 D.硫酸溶液
5.下列做法正确的是
A.植树造林,防沙降尘 B.焚烧垃圾,净化环境
C.禁用农药,保护水源 D.深埋电池,消除污染
6.下列物质间不能发生反应的是( )
A.稀盐酸和镁条 B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁 D.稀盐酸和氢氧化铜
7.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
8.已知室温下NaCl的溶解度约为36g。现称取3.6g粗盐,经过溶解、过滤、蒸发、转移等步骤,除去泥沙得到精盐。下列操作正确且合理的是
A溶解 B过滤 C蒸发 D转移
A.A B.B C.C D.D
9.下列各组物质用稀硫酸不能区分开的是( )
A.镁粉、氧化铜粉 B.NaOH溶液、KOH溶液
C.铁片、铜片 D.Na2CO3溶液、NaCl溶液
10.t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH>7。关于溶液变浑浊的原因,同学们有两种观点:①Ca(OH)2 的溶解度随温度升高而减小;②Ca(OH)2 与空气中的 CO2 反应。他们设计以下方案进行探究,其中没有意义的是( )
A.将装有浊液的烧杯,用冷水冷却,恢复至 t℃,观察浑浊是否消失
B.取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C.取适量浊液,过滤,往滤液中加入 Na2CO3 溶液,观察是否有沉淀生成
D.其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
11.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
12.粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
13.将下列各组物质混合后溶于水,得到无色溶液的是
A.NaNO3、KCl、Na2SO4 B.FeCl3、NaOH、KNO3
C.CuSO4、CaCl2、KOH D.BaCl2、K2CO3、H2SO4
14.下列有关氢氧化钠的说法,错误的是( )
A.氢氧化钠俗称烧碱
B.氢氧化钠有强烈的腐蚀性
C.氢氧化钠固体可用于干燥二氧化碳气体
D.氢氧化钠可用于制肥皂、洗涤剂、造纸、纺织工业等
15.粗盐含有少量的MgCl2,CaCl2,Na2SO4等杂质,为了将杂质除干净,先向粗盐溶液中分别加入过量的①NaOH②Na2CO3③BaCl2溶液,过滤,再加入④稀盐酸使溶液的pH=7将最后所得溶液进行蒸发可得到精盐,加入溶液的先后顺序错误的是( )
A.②③①④ B.③②①④ C.①③②④ D.③①②④
二、填空题
16.化学就在我们身边。从①熟石灰②金刚石③氯化钠④干冰四种物质中,选择适当的物质填空(填序号)。
(1)用于炒菜调味的是_____;
(2)用于人工降雨的是_____;
(3)用来裁玻璃的是_____;
(4)用来改良酸性土壤的是_____。
17.化学肥料对农作物的增产具有十分重要的作用,俗话说:“庄稼一枝花,全靠肥当家”。下面是农业生产中广泛施用的几种化学肥料:①NH4NO3 ②KNO3 ③NH4Cl ④
请回答:
(1)属于复合肥料的是______(填序号,下同);
(2)属于铵态氮肥的是______,它们成分中都含有的离子是______(填符号)。
18.化学与我们的生产、生活息息相关。请回答下列问题。
(1)①食盐、②熟石灰、③小苏打、④石墨四种物质在生产、生活中用途广泛。其中可用于制铅笔芯的是_____(填数字序号,下同);可用作面点发酵剂的是_____;常用作食品加工调味的是______;常用于改良酸性土壤的是_____。
(2)农业上,碳酸钾(K2CO3)可用作_____(填“磷”或“钾”)肥。已知碳酸钾溶液呈碱性,则碳酸钾_____(填“能”或“不能”)与铵态氮肥混合施用。
19.某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是_____________;编号②反应的金属单质是_____________。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是_____________反应。
(3)请你写出符合编号③反应的化学方程式__________________。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是_____________。
三、推断题
20.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
21.下图中的物质均为初中化学常见物质,其中A是常见的补钙剂,B是黑色粉末,H是蓝色沉淀。下图是它们之间的转化关系(部分生成物已经略去),请回答:
(1)写出B物质的化学式___________;
(2)写出F+G→H的化学方程式__________________;
(3)写出物质E的用途_________________。(一种即可)
四、实验题
22.依据下图回答问 题
去除粗盐中的泥沙。
(1)实验的步骤是溶解、过滤和______。
(2)过滤操作中用到的玻璃仪器有______。
配制 150 克 10%的氢氧化钠溶液。
(1)称取氢氧化钠的质量为______克。
(2)量取时仰视读数会使实际质量分数______(填“大于”或“小于”)10%。
23.为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳能发生反应。如图所示进行实验(装置气密性良好,实验前弹簧夹K1、K2处于关闭状态)。
资料:CaCl2+Na2CO3═CaCO3↓+2NaCl
实验一:氢氧化钙溶液与稀盐酸恰好完全反应。
(1)实验过程中需缓缓通入氮气,其作用是什么____________?
(2)写出氢氧化钙溶液与稀盐酸恰好完全反应的实验操作及现象__________。
实验二:氢氧化钠溶液与二氧化碳反应。
(3)打开活塞Ⅱ,将足量氢氧化钠溶液加入锥形瓶中,立即关闭活塞Ⅱ,写出利用图示装置证明氢氧化钠溶液与二氧化碳反应的实验操作及现象_______________。
(4)实验后,取B中锥形瓶内的溶液,倒入烧杯中,若溶液呈红色,设计实验方案,探究该溶液中是否有氢氧化钠,写出实验操作、预期现象和结论_______________。
五、计算题
24.我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了杰出贡献。在实际生产的产品碳酸钠中会混有少量的氯化钠,现有纯碱样品,为测定该样品中碳酸钠的质量分数,称取样品6 g,放入20 g水中使其完全溶解,再加入稀盐酸26. 2 g,恰好完全反应,气体全部逸出,得到不饱和氯化钠溶液,溶液的总质量为50 g。试计算:
(1)生成二氧化碳的质量为多少g。
(2)样品中碳酸钠的质量。
(3)反应后所得溶液中溶质的质量分数。
25.有一定质量的BaCl2和BaCO3固体混合物,加入50g稀盐酸,恰好完全反应,生成的2.2g气体全部逸出,再向反应后所得溶液中加入150g水形成不饱和溶液,测得该溶液中含7.1g氯元素。请计算:
(1)原固体混合物的质量;
(2)所加盐酸溶液中溶质质量分数;
(3)反应后所得溶液中溶质的质量分数(计算结果精确至0.1%)。
试卷第1页,共3页
参考答案:
1.D 2.B 3.C 4.A 5.A 6.B 7.B 8.B 9.B 10.C 11.B 12.C 13.A 14.C 15.A
16. ③ ④ ② ①
17. ②④ ①③④
18. ④ ③ ① ② 钾 不能
19. 石蕊试剂 Fe 置换反应 产生白色沉淀
20. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
21. CuO 2NaOH+CuSO4= Na2SO4+Cu(OH)2↓ 改良酸性土壤(合理即可)
22. 蒸发 ①③⑤ 15 小于
23. 搅拌,使氢氧化钙溶液和盐酸充分反应 打开活塞Ⅰ和弹簧夹K1,逐滴滴加稀盐酸,同时鼓入氮气,直至A中溶液恰好由红色变成无色 打开活塞Ⅱ,将足量氢氧化钠溶液加入锥形瓶中,立即关闭活塞Ⅱ,打开K2。锥形瓶中的二氧化碳与氢氧化钠反应生成碳酸钠,压强变小,A装置中的压强大,就会将锥形瓶内的氯化钙流入B中,然后氯化钙与反应生成的碳酸钠反应,生成碳酸钙白色沉淀。因此有白色沉淀生成 取反应后的溶液,滴加氯化钡溶液(或氯化钙溶液)至不再产生沉淀为止,溶液仍为变红,说明该溶液中有氢氧化钠
24.(1)2.2(2)5.3g(3)13.1%
25.解:设固体混合物中BaCO3的质量为x,消耗HCl的质量为y,生成BaCl2的质量为z
(1)氯元素质量7.1g,故所得溶液中BaCl2的质量:
原固体混合物的质量:
(2)所加盐酸溶液中溶质质量分数:
(3)滤液的质量:
所得滤液中溶质的质量分数:
答:原固体混合物的质量20.25g,加入的稀硫酸中溶质的质量分数为7.3%,反应后所得溶液中溶质的质量分数9.5%。
答案第1页,共2页
同课章节目录
