第八章常见的酸碱盐基础训练-2021-2022学年九年级化学科粤版(2012)下册(word版 含答案)
文档属性
| 名称 | 第八章常见的酸碱盐基础训练-2021-2022学年九年级化学科粤版(2012)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 147.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览



文档简介
第八章《常见的酸碱盐》基础训练
一、单选题
1.下列事实与解释不相符的是( )
A.浓氨水挥发﹣﹣分子不断运动
B.干冰升华﹣﹣分子间的间隔变大
C.稀盐酸、稀硫酸均显酸性﹣﹣溶液中都含有氢元素
D.金刚石和石墨的物理性质不同﹣﹣碳原子的排列方式不同
2.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
3.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性 B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质 D.固体氢氧化钠能吸收水蒸气而潮解
4.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
5.下列各组离子能在指定溶液中大量共存的一组是
A.在稀硫酸中:Ba2+、CO3 2—、Zn2+ B.在氢氧化钙溶液中:H+、Mg2+、Cl—
C.在氯化钠溶液中:K+、Ca2+、NO3— D.在氯化铵溶液中:Na+、Cu2+、OH—
6.向烧杯中逐渐加入x溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
选项 烧杯中的物质 x溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
A.A B.B C.C D.D
7.某校化学小组在利用硫酸和氢氧化钾两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。下列说法正确的是
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4
C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸溶液的烧杯中
D.由c点到d点的变化过程中没有发生化学反应
8.在下列各组物质中,每组的3种物质两两之间都能发生化学反应的是
①Cu、稀硫酸、CuO ②稀盐酸、Ca(OH)2溶液、Na2CO3溶液 ③C、CO、Fe2O3
A.①② B.①③ C.② D.①②③
9.物质的性质与用途密切相关。 下列做法不合理的是
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
10.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如下图所示,则X可能是
A.水
B.纯碱溶液
C.澄清石灰水
D.稀盐酸
二、简答题
11.用化学方程式说明问题:
(1)用盐酸除铁锈________________
(2)烧水的铝壶中常结有一层水垢(水垢的主要成分是CaCO3),用适量的稀盐酸可以将它除去,反应的化学方程式是_______________若盐酸的用量过多,会损坏铝壶,反应的化学方程式是___________
(3)同时生成两种沉淀的复分解反应________________
12.三位学生设计了下述三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确证试液中有。
(已知:)
方案甲:
方案乙:
方案丙:
试评价上述各种方案是否严密,并分别说明理由。
(1)方案甲:______;
(2)方案乙:______;
(3)方案丙:______;
三、推断题
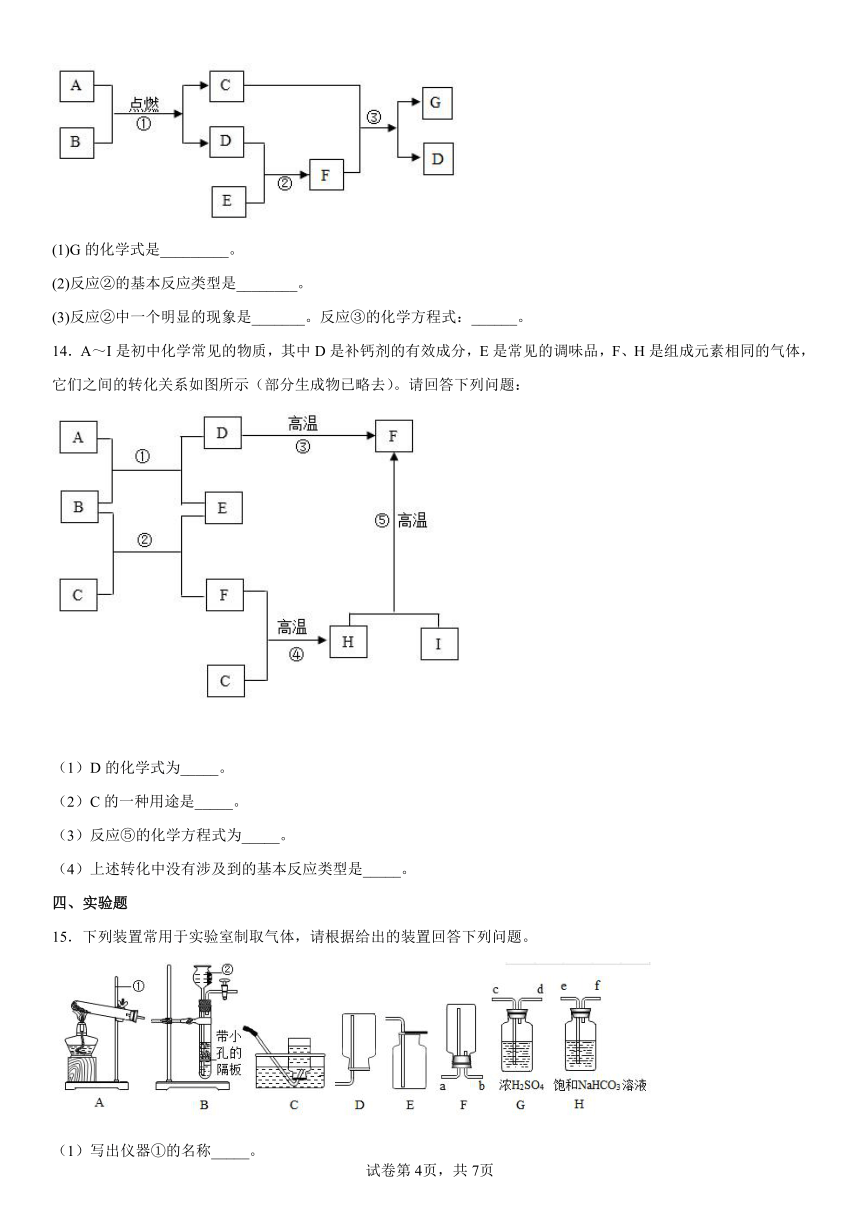
13.如图中A~E是初中化学常见的物质,已知A是天然气的主要成分,G是石灰石的主要成分。请分析回答:
(1)G的化学式是_________。
(2)反应②的基本反应类型是________。
(3)反应②中一个明显的现象是_______。反应③的化学方程式:______。
14.A~I是初中化学常见的物质,其中D是补钙剂的有效成分,E是常见的调味品,F、H是组成元素相同的气体,它们之间的转化关系如图所示(部分生成物已略去)。请回答下列问题:
(1)D的化学式为_____。
(2)C的一种用途是_____。
(3)反应⑤的化学方程式为_____。
(4)上述转化中没有涉及到的基本反应类型是_____。
四、实验题
15.下列装置常用于实验室制取气体,请根据给出的装置回答下列问题。
(1)写出仪器①的名称_____。
(2)实验室用氯酸钾制取氧气,应选用的发生装置是_____(填序号),化学方程式_____。
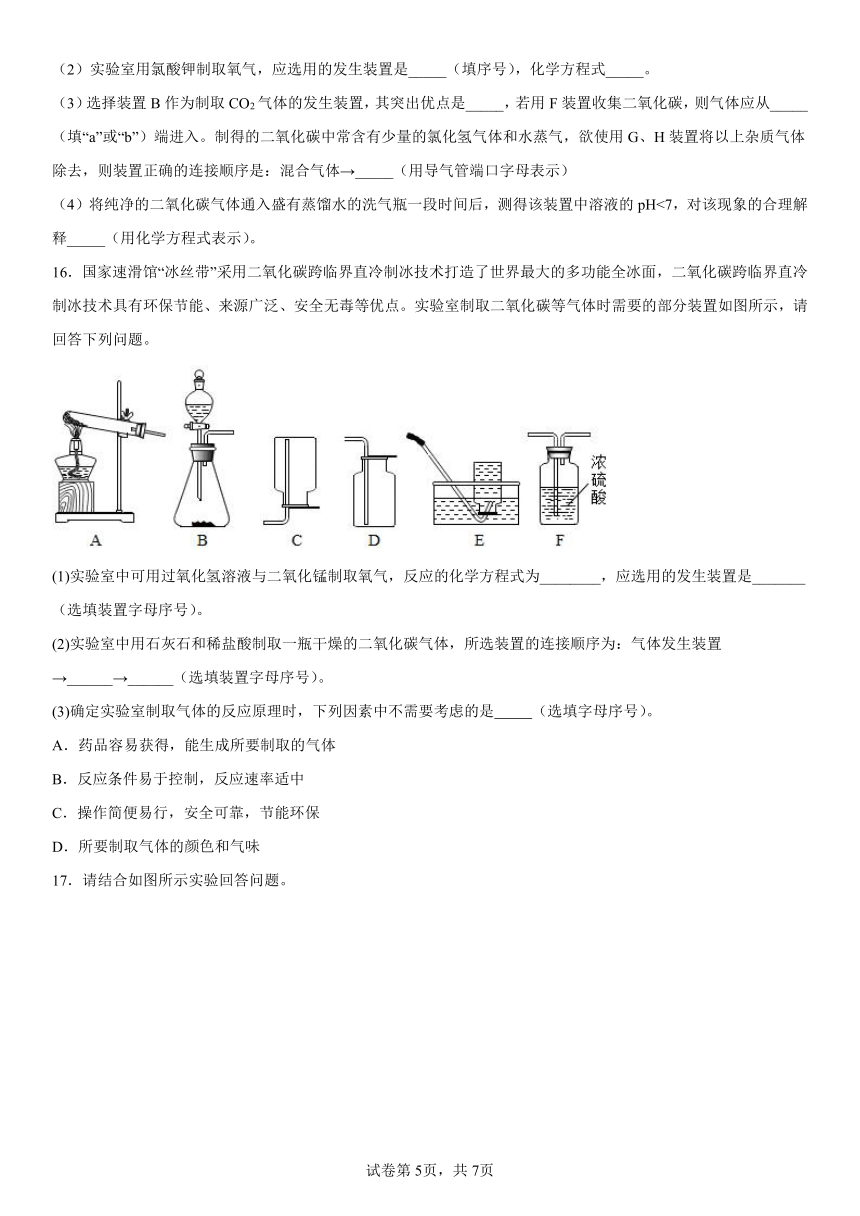
(3)选择装置B作为制取CO2气体的发生装置,其突出优点是_____,若用F装置收集二氧化碳,则气体应从_____(填“a”或“b”)端进入。制得的二氧化碳中常含有少量的氯化氢气体和水蒸气,欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→_____(用导气管端口字母表示)
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH<7,对该现象的合理解释_____(用化学方程式表示)。
16.国家速滑馆“冰丝带”采用二氧化碳跨临界直冷制冰技术打造了世界最大的多功能全冰面,二氧化碳跨临界直冷制冰技术具有环保节能、来源广泛、安全无毒等优点。实验室制取二氧化碳等气体时需要的部分装置如图所示,请回答下列问题。
(1)实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为________,应选用的发生装置是_______(选填装置字母序号)。
(2)实验室中用石灰石和稀盐酸制取一瓶干燥的二氧化碳气体,所选装置的连接顺序为:气体发生装置→______→______(选填装置字母序号)。
(3)确定实验室制取气体的反应原理时,下列因素中不需要考虑的是 (选填字母序号)。
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
17.请结合如图所示实验回答问题。
(1)A实验中用玻璃棒搅拌的目的是_____。
(2)B实验中错误操作造成的后果是_____。
(3)C实验正、负极产生的气体体积比约为_____。此实验说明水是由_____组成的。
五、计算题
18.尿素〔CO(NH2)2〕是化肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。
(1)尿素属于化肥中的______肥(填“氮”“钾”或“复合”)。
(2)CO(NH2)2中共含有______(写数字)种元素;
(3)CO(NH2)2的相对分子质量是______
(4)CO(NH2)2中C、H、N、O元素的质量比为______。
19.课外活动小组为测定某未知稀硫酸的质量分数,进行了下面实验:
①取10g稀硫酸于烧杯中,逐滴滴加BaCl2溶液,至不再产生白色沉淀止,经过滤、洗涤,干燥后,称得沉淀物的质量为4.71g
②为保障测定结果的精确性,按实验①操作又连续进行了四次相同的实验。几次实验所得数据见下表:
第一次 第二次 第三次 第四次 第五次
固体质量/g 4.71 4.63 4.64 4.66 4.66
分析实验与表中数据后,回答:
(1)第一次实验测得数据明显偏高,可能的原因是______;
(2)五次测定结果的平均值是______;
(3)请利用(2)中数据计算:未知稀硫酸的质量分数是______。(不要求计算过程,计算结果精确到0.01)
20.下图是某种化肥广告内容,请根据相关信息回答下列问题。
(1)硝酸铵的相对分子质量为 。
(2)硝酸铵中氮、氢元素的质量比为 。
(3)通过计算判断该广告是否属于虚假广告?(写出计算过程)结论:该广告_____(“是”或“不是”)虚假广告。
(4)40千克NH4NO3与多少千克NH4HCO3(碳酸氢铵)的肥效相同(即含氮元素质量相等)?(写出计算过程)
21.硝酸溶解废旧CPU所得溶液中含有Cu2+和Ag+,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如下方法回收Cu和Ag(图中标注的试剂均不同)。
(1)加入过量Fe粉发生的主要反应为______(写化学方程式)。
(2)试剂1和试剂3的名称依次是______。
(3)若向66g物质1中加入100g试剂2后,恰好完全反应,剩余固体质量为60.4g,求所得溶液中溶质的质量分数(写出计算过程,计算结果精确到0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.B
4.B
5.C
6.C
7.D
8.C
9.D
10.B
11. Fe2O3 + 6HCl === 2FeCl3 + 3H2O CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 2Al + 6HCl == 2AlCl3 + 3H2↑ CuSO4+ Ba(OH)2 === Cu(OH)2↓+BaSO4↓
12. 不严密,因为含有而不含的无色溶液也会出现此方案的现象 严密,因为只有含有的无色溶液才会出现此方案的现象 不严密,因为含有而不含的无色溶液也会出现此方案的现象
13.(1)CaCO3
(2)化合反应
(3) 放出热量
14. CaCO3 金属除锈(合理即可) (合理即可) 置换反应
15. 铁架台 A 可以控制反应随时发生随时停止 b e→f→c→d CO2+H2O=H2CO3
16.(1) B
(2) F D
(3)D
17. 防止因局部温度过高造成液滴飞溅 水沸腾使酸滴向四周飞溅 1:2 氢元素和氧元素
18.(1)尿素中含有氮元素,属于化肥中的氮肥。
(2)CO(NH2)2中共含有C、O、N、H,4种元素;
(3)CO(NH2)2的相对分子质量是12+16+(14+1×2)×2=60;
(4)CO(NH2)2中C、H、N、O元素的质量比为12:(1×4):(14×2):16=3:1:7:4。
19.(1)第一次产生的沉淀未充分干燥
(2)五次测定结果的平均值=;
(3)设:未知稀硫酸的质量分数为x。
x=19.60%
20.(1)硝酸铵的相对分子质量为:14×2+1×4+16×3=80;
答:硝酸铵的相对分子质量为80。
(2)硝酸铵中氮、氢元素的质量比为(14×2):(1×4)=7:1;
答:硝酸铵中氮、氢元素的质量比为7:1。
(3)纯净硝酸铵中氮元素的质量分数为×100%=35%,35%<38%,
答:该广告属于虚假广告。
(4)设与40kgNH4NO3肥效相同的NH4HCO3的质量为x,则
x××100%=40kg××100%
x=79kg。
答:40千克NH4NO3与79千克NH4HCO3(碳酸氢铵)的肥效相同。
21.(1)
(2)氯化钠溶液、氨水
(3)剩余固体的质量为铜的质量,故物质1中铁的质量为:66g-60.4g=5.6g
解:设反应生成氯化亚铁的质量为x,生成氢气的质量为y
x=12.7g
y=0.2g
故所得溶液中溶质的质量分数:
答:所得溶液中溶质的质量分数为12.0%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列事实与解释不相符的是( )
A.浓氨水挥发﹣﹣分子不断运动
B.干冰升华﹣﹣分子间的间隔变大
C.稀盐酸、稀硫酸均显酸性﹣﹣溶液中都含有氢元素
D.金刚石和石墨的物理性质不同﹣﹣碳原子的排列方式不同
2.下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸二氢铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
3.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性 B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质 D.固体氢氧化钠能吸收水蒸气而潮解
4.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
5.下列各组离子能在指定溶液中大量共存的一组是
A.在稀硫酸中:Ba2+、CO3 2—、Zn2+ B.在氢氧化钙溶液中:H+、Mg2+、Cl—
C.在氯化钠溶液中:K+、Ca2+、NO3— D.在氯化铵溶液中:Na+、Cu2+、OH—
6.向烧杯中逐渐加入x溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
选项 烧杯中的物质 x溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
A.A B.B C.C D.D
7.某校化学小组在利用硫酸和氢氧化钾两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。下列说法正确的是
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4
C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸溶液的烧杯中
D.由c点到d点的变化过程中没有发生化学反应
8.在下列各组物质中,每组的3种物质两两之间都能发生化学反应的是
①Cu、稀硫酸、CuO ②稀盐酸、Ca(OH)2溶液、Na2CO3溶液 ③C、CO、Fe2O3
A.①② B.①③ C.② D.①②③
9.物质的性质与用途密切相关。 下列做法不合理的是
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
10.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如下图所示,则X可能是
A.水
B.纯碱溶液
C.澄清石灰水
D.稀盐酸
二、简答题
11.用化学方程式说明问题:
(1)用盐酸除铁锈________________
(2)烧水的铝壶中常结有一层水垢(水垢的主要成分是CaCO3),用适量的稀盐酸可以将它除去,反应的化学方程式是_______________若盐酸的用量过多,会损坏铝壶,反应的化学方程式是___________
(3)同时生成两种沉淀的复分解反应________________
12.三位学生设计了下述三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确证试液中有。
(已知:)
方案甲:
方案乙:
方案丙:
试评价上述各种方案是否严密,并分别说明理由。
(1)方案甲:______;
(2)方案乙:______;
(3)方案丙:______;
三、推断题
13.如图中A~E是初中化学常见的物质,已知A是天然气的主要成分,G是石灰石的主要成分。请分析回答:
(1)G的化学式是_________。
(2)反应②的基本反应类型是________。
(3)反应②中一个明显的现象是_______。反应③的化学方程式:______。
14.A~I是初中化学常见的物质,其中D是补钙剂的有效成分,E是常见的调味品,F、H是组成元素相同的气体,它们之间的转化关系如图所示(部分生成物已略去)。请回答下列问题:
(1)D的化学式为_____。
(2)C的一种用途是_____。
(3)反应⑤的化学方程式为_____。
(4)上述转化中没有涉及到的基本反应类型是_____。
四、实验题
15.下列装置常用于实验室制取气体,请根据给出的装置回答下列问题。
(1)写出仪器①的名称_____。
(2)实验室用氯酸钾制取氧气,应选用的发生装置是_____(填序号),化学方程式_____。
(3)选择装置B作为制取CO2气体的发生装置,其突出优点是_____,若用F装置收集二氧化碳,则气体应从_____(填“a”或“b”)端进入。制得的二氧化碳中常含有少量的氯化氢气体和水蒸气,欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→_____(用导气管端口字母表示)
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH<7,对该现象的合理解释_____(用化学方程式表示)。
16.国家速滑馆“冰丝带”采用二氧化碳跨临界直冷制冰技术打造了世界最大的多功能全冰面,二氧化碳跨临界直冷制冰技术具有环保节能、来源广泛、安全无毒等优点。实验室制取二氧化碳等气体时需要的部分装置如图所示,请回答下列问题。
(1)实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为________,应选用的发生装置是_______(选填装置字母序号)。
(2)实验室中用石灰石和稀盐酸制取一瓶干燥的二氧化碳气体,所选装置的连接顺序为:气体发生装置→______→______(选填装置字母序号)。
(3)确定实验室制取气体的反应原理时,下列因素中不需要考虑的是 (选填字母序号)。
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
17.请结合如图所示实验回答问题。
(1)A实验中用玻璃棒搅拌的目的是_____。
(2)B实验中错误操作造成的后果是_____。
(3)C实验正、负极产生的气体体积比约为_____。此实验说明水是由_____组成的。
五、计算题
18.尿素〔CO(NH2)2〕是化肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。
(1)尿素属于化肥中的______肥(填“氮”“钾”或“复合”)。
(2)CO(NH2)2中共含有______(写数字)种元素;
(3)CO(NH2)2的相对分子质量是______
(4)CO(NH2)2中C、H、N、O元素的质量比为______。
19.课外活动小组为测定某未知稀硫酸的质量分数,进行了下面实验:
①取10g稀硫酸于烧杯中,逐滴滴加BaCl2溶液,至不再产生白色沉淀止,经过滤、洗涤,干燥后,称得沉淀物的质量为4.71g
②为保障测定结果的精确性,按实验①操作又连续进行了四次相同的实验。几次实验所得数据见下表:
第一次 第二次 第三次 第四次 第五次
固体质量/g 4.71 4.63 4.64 4.66 4.66
分析实验与表中数据后,回答:
(1)第一次实验测得数据明显偏高,可能的原因是______;
(2)五次测定结果的平均值是______;
(3)请利用(2)中数据计算:未知稀硫酸的质量分数是______。(不要求计算过程,计算结果精确到0.01)
20.下图是某种化肥广告内容,请根据相关信息回答下列问题。
(1)硝酸铵的相对分子质量为 。
(2)硝酸铵中氮、氢元素的质量比为 。
(3)通过计算判断该广告是否属于虚假广告?(写出计算过程)结论:该广告_____(“是”或“不是”)虚假广告。
(4)40千克NH4NO3与多少千克NH4HCO3(碳酸氢铵)的肥效相同(即含氮元素质量相等)?(写出计算过程)
21.硝酸溶解废旧CPU所得溶液中含有Cu2+和Ag+,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如下方法回收Cu和Ag(图中标注的试剂均不同)。
(1)加入过量Fe粉发生的主要反应为______(写化学方程式)。
(2)试剂1和试剂3的名称依次是______。
(3)若向66g物质1中加入100g试剂2后,恰好完全反应,剩余固体质量为60.4g,求所得溶液中溶质的质量分数(写出计算过程,计算结果精确到0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.B
4.B
5.C
6.C
7.D
8.C
9.D
10.B
11. Fe2O3 + 6HCl === 2FeCl3 + 3H2O CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 2Al + 6HCl == 2AlCl3 + 3H2↑ CuSO4+ Ba(OH)2 === Cu(OH)2↓+BaSO4↓
12. 不严密,因为含有而不含的无色溶液也会出现此方案的现象 严密,因为只有含有的无色溶液才会出现此方案的现象 不严密,因为含有而不含的无色溶液也会出现此方案的现象
13.(1)CaCO3
(2)化合反应
(3) 放出热量
14. CaCO3 金属除锈(合理即可) (合理即可) 置换反应
15. 铁架台 A 可以控制反应随时发生随时停止 b e→f→c→d CO2+H2O=H2CO3
16.(1) B
(2) F D
(3)D
17. 防止因局部温度过高造成液滴飞溅 水沸腾使酸滴向四周飞溅 1:2 氢元素和氧元素
18.(1)尿素中含有氮元素,属于化肥中的氮肥。
(2)CO(NH2)2中共含有C、O、N、H,4种元素;
(3)CO(NH2)2的相对分子质量是12+16+(14+1×2)×2=60;
(4)CO(NH2)2中C、H、N、O元素的质量比为12:(1×4):(14×2):16=3:1:7:4。
19.(1)第一次产生的沉淀未充分干燥
(2)五次测定结果的平均值=;
(3)设:未知稀硫酸的质量分数为x。
x=19.60%
20.(1)硝酸铵的相对分子质量为:14×2+1×4+16×3=80;
答:硝酸铵的相对分子质量为80。
(2)硝酸铵中氮、氢元素的质量比为(14×2):(1×4)=7:1;
答:硝酸铵中氮、氢元素的质量比为7:1。
(3)纯净硝酸铵中氮元素的质量分数为×100%=35%,35%<38%,
答:该广告属于虚假广告。
(4)设与40kgNH4NO3肥效相同的NH4HCO3的质量为x,则
x××100%=40kg××100%
x=79kg。
答:40千克NH4NO3与79千克NH4HCO3(碳酸氢铵)的肥效相同。
21.(1)
(2)氯化钠溶液、氨水
(3)剩余固体的质量为铜的质量,故物质1中铁的质量为:66g-60.4g=5.6g
解:设反应生成氯化亚铁的质量为x,生成氢气的质量为y
x=12.7g
y=0.2g
故所得溶液中溶质的质量分数:
答:所得溶液中溶质的质量分数为12.0%。
答案第1页,共2页
答案第1页,共2页
