第四单元盐 化肥单元测试题—2021-2022学年九年级化学人教版(五四学制)全一册(word版 含答案)
文档属性
| 名称 | 第四单元盐 化肥单元测试题—2021-2022学年九年级化学人教版(五四学制)全一册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 126.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览


文档简介
第四单元《盐化肥》单元测试题—2021-2022学年九年级化学人教版(五四学制)全一册
一、单选题
1.下列化肥从外观即可与其他化肥相区别的是( )
A.硝酸钾 B.氯化铵 C.磷矿粉 D.氯化钾
2.氮肥能促进植物的枝叶繁茂,叶色浓绿。下列属于氮肥的是
A.KH2PO4 B.K2SO4 C.NH4NO3 D.Ca3(PO4)2
3.下列各组固体物质,不能用水鉴别的是( )
A.KNO3、KCl
B.CaCO3、CaCl2
C.CuSO4、Na2SO4
D.NH4NO3、CaO
4.下列各组物质的溶液中,不另加试剂则无法鉴别出来的是
A.H2SO4 NaOH CuSO4
B.HCl NaOH NaCl
C.H2SO4 Ca(OH)2 FeCl3
D.HCl Ca(OH)2 Na2CO3
5.2020年世界水日的主题是“水与气候变化”。下列关于水的说法正确的是
A.生活中硬水转化为软水的方法是煮沸
B.电解水实验中产生氢气和氧气的体积比为1:8
C.化合物之间有水生成的反应一定是复分解反应
D.过滤后的河水为纯净水
6.下列各组离子在无色透明溶液中能大量共存的是
A.Cu2+、Na+、SO42-、Cl- B.K+、Na+、CO32—、NO3-
C.OH-、CO32-、Ca2+、Na+ D.Mg2+、Na+、OH-、CO32-
7.党的十九大提出要加快生态文明体制改革,建设美丽中国。下列做法正确的是
A.为保护环境,把废旧电池深埋处理
B.为增加粮食产量,大量使用农药、化肥
C.为节约水资源,用工业废水直接灌溉农田
D.为节约资源,大力开发新能源替代化石燃料
8.下列各组溶液混合后能发生反应且无明显现象的一组是
A.NaNO3、NaCl、AgNO3 B.CuSO4、H2SO4、BaCl2
C.HCl、Na2SO4、NaOH D.HCl、NaHCO3、NaNO3
9.现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有
A.② B.②③ C.①②③ D.②③④
10.下表物质中含有少量杂质,其中除杂方法正确的是
物质 杂质 除去杂质的方法
A CaCl2溶液 HCl 滴入碳酸钠溶液
B CO2 O2 通过灼热的铜网
C NaOH Na2CO3 加入稀盐酸至不再产生气泡
D CuO Cu 加足量稀盐酸,充分搅拌后再过滤
A.A B.B C.C D.D
二、简答题
11.某园林工人配制波尔多液时,将胆矾(CuSO4·5H2O)晶体、生石灰(CaO)分别与水按1∶50的质量比混合(胆矾溶于水得到CuSO4溶液),然后把得到的两种液体在木桶里混合并充分搅拌。
(1)配制波尔多液不用铁桶的原因:__________________________________________。
(2)两种液体在木桶里反应的化学方程式:____________________________________________________。
(3)若要检验所配的波尔多液中是否还含有CuSO4,实验方法是_________________________________。
12.某同学设计了下图所示的装置进行实验,观察到紫色石蕊溶液变成红色,从而得出二氧化碳和水反应生成了酸。而此实验存在一个明显的不足,影响结论的得出,请回答:
(1)此实验的不足是什么?
(2)如果在原装置基础上加一个装置就可以得出正确结论,则要加的装置是什么,装置内加入的药品是什么?
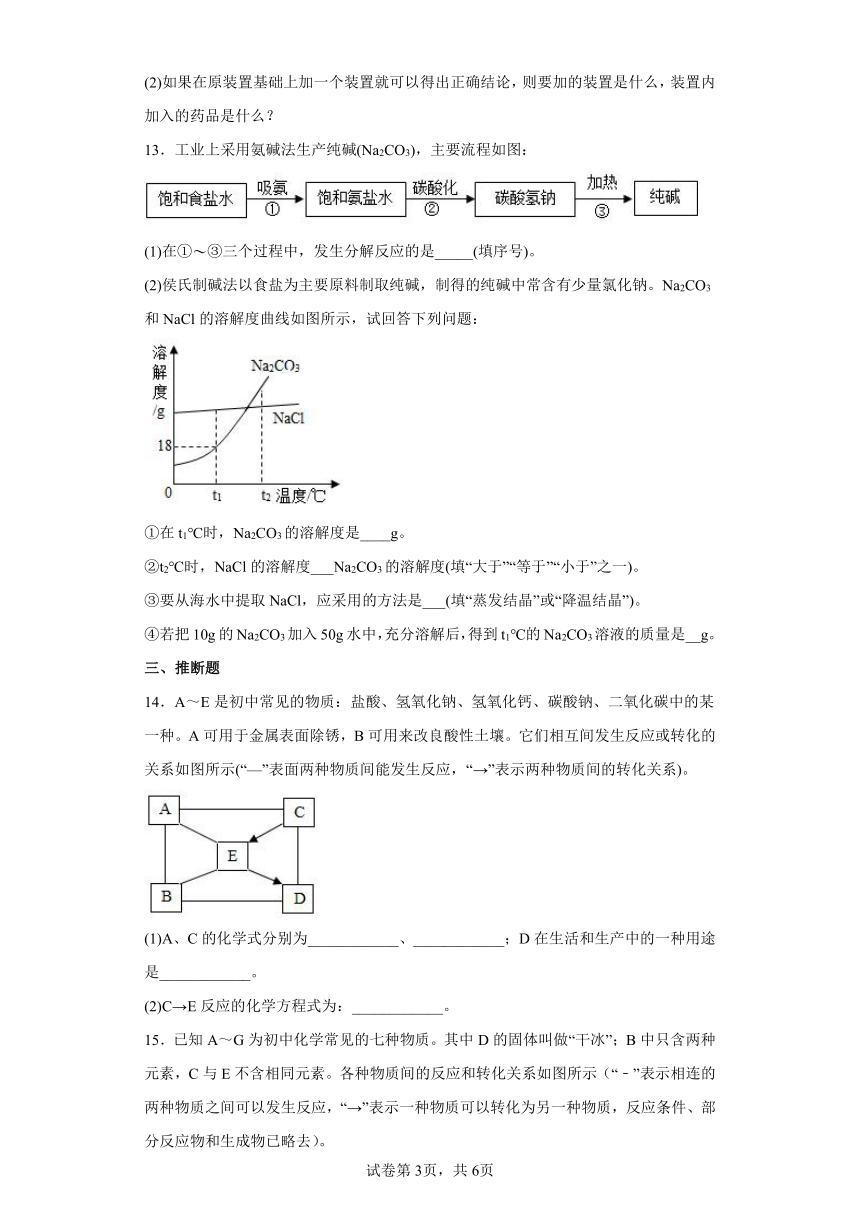
13.工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:
(1)在① ③三个过程中,发生分解反应的是_____(填序号)。
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:
①在t1℃时,Na2CO3的溶解度是____g。
②t2℃时,NaCl的溶解度___Na2CO3的溶解度(填“大于”“等于”“小于”之一)。
③要从海水中提取NaCl,应采用的方法是___(填“蒸发结晶”或“降温结晶”)。
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是__g。
三、推断题
14.A~E是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种。A可用于金属表面除锈,B可用来改良酸性土壤。它们相互间发生反应或转化的关系如图所示(“—”表面两种物质间能发生反应,“→”表示两种物质间的转化关系)。
(1)A、C的化学式分别为____________、____________;D在生活和生产中的一种用途是____________。
(2)C→E反应的化学方程式为:____________。
15.已知A~G为初中化学常见的七种物质。其中D的固体叫做“干冰”;B中只含两种元素,C与E不含相同元素。各种物质间的反应和转化关系如图所示(“﹣”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
请分析后回答:
(1)D的化学式_____。
(2)B与G反应的化学方程式_____。
四、实验题
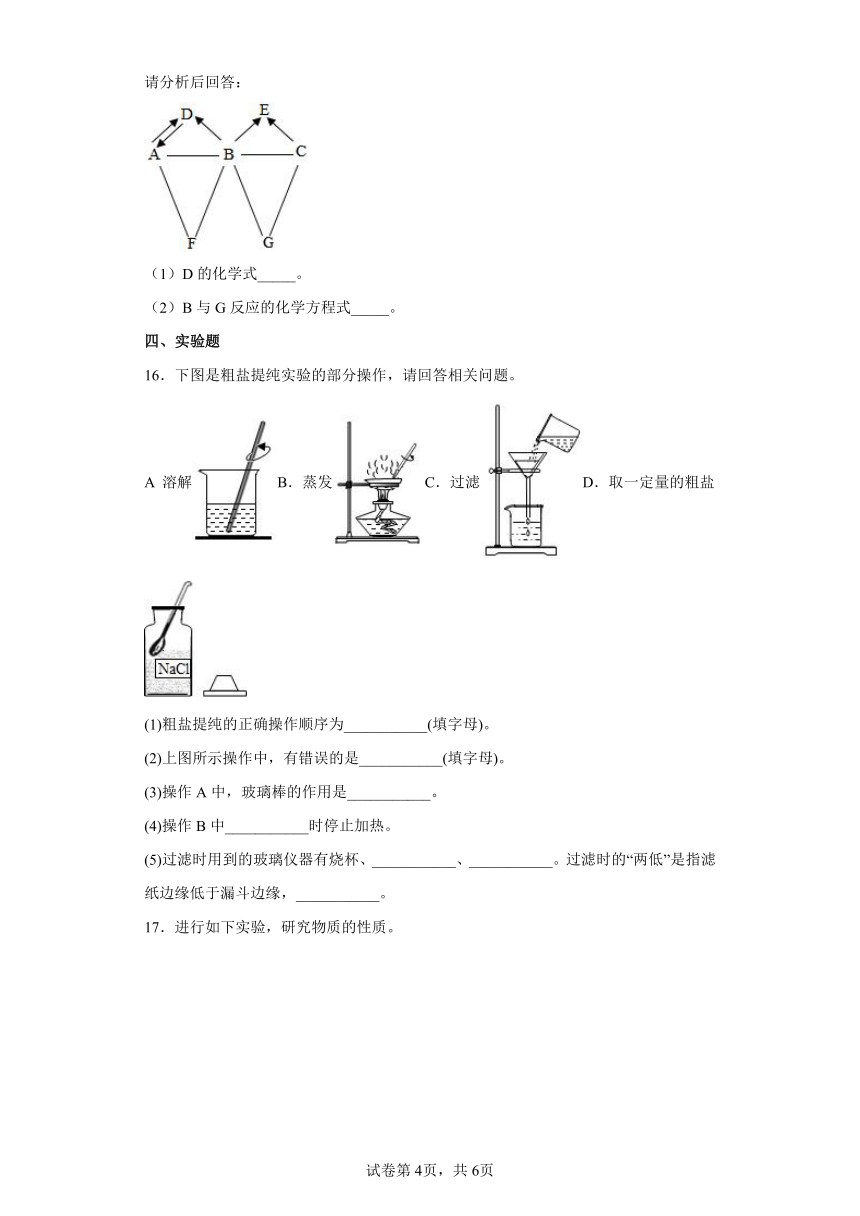
16.下图是粗盐提纯实验的部分操作,请回答相关问题。
A 溶解B.蒸发C.过滤D.取一定量的粗盐
(1)粗盐提纯的正确操作顺序为___________(填字母)。
(2)上图所示操作中,有错误的是___________(填字母)。
(3)操作A中,玻璃棒的作用是___________。
(4)操作B中___________时停止加热。
(5)过滤时用到的玻璃仪器有烧杯、___________、___________。过滤时的“两低”是指滤纸边缘低于漏斗边缘,___________。
17.进行如下实验,研究物质的性质。
(1)A中有气泡产生,证明黄铜为_______合金(填序号)。
a 铜锌 b 铜银 c 铜碳
(2)B中反应的化学方程式为_______。
(3)验证鸡蛋壳中含有碳酸盐,应补充的操作及观察到现象是________。
五、计算题
18.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
19.磷酸氢二铵[(NH4)2HPO4]是一种化肥,它对提高农作物的产量具有重要作用.填空:
(1)(NH4)2HPO4_____(填“属于”或“不属于”)复合肥料,它由_____(写数字)种元素组成.
(2)(NH4)2HPO4的相对分子质量是_____;
(3)(NH4)2HPO4中氮元素的质量分数为_____(精确到0.1%)
20.为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如右表:根据实验及有关数据进行分析与计算:
第Ⅰ组 第Ⅱ组 第Ⅲ组
稀硫酸的质量/g 50 100 150
溶解固体的质量/g 10 16 16
(1)20g样品中含氧化铜的质量为______g。
(2)根据第I组数据计算所用稀硫酸的溶质质量分数是多少?(写出计算过程)
(3)求第I组实验所得溶液中溶质的质量分数______(精确到0.1%)。
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,在图中画出滤液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图。
21.厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如下图所示。
计算:该食用碱中碳酸钠的质量分数是__________ (计算结果精确至0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.A
4.B
5.A
6.B
7.D
8.C
9.B
10.B
11. 铁能与硫酸铜发生置换反应(或Fe+CuSO4===Cu+FeSO4) Ca(OH)2+CuSO4===CaSO4+Cu(OH)2↓ 将一根光亮的铁丝插入波尔多液中,观察铁丝表面是否变红
12.(1)反应中所用的酸为浓盐酸,会挥发出氯化氢气体溶于水也能使石蕊变红
(2)在甲乙之间加一个吸收氯化氢气体的装置,药品为饱和的碳酸氢钠溶液
13. ③ 18 小于 蒸发结晶 59
14.(1) HCl NaOH 灭火
(2)2NaOH+CO2=Na2CO3+H2O
15. CO2 HCl+AgNO3=HNO3+AgCl↓
16.(1)DACB
(2)C
(3)加速溶解
(4)大量固体
(5) 漏斗(或玻璃棒) 玻璃棒(或漏斗) 液面低于滤纸边缘
17. a Ca(OH)2+2HCl=CaCl2+2H2O 将产生的气体通入澄清的石灰水中,石灰水变浑浊
18.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
19. 属于 4 132 21.2%
20.(1)16
(2)解:由第I组合第II组实验数据可知,第I组实验中硫酸完全反应
设50g稀硫酸中H2SO4的质量为x,生成硫酸铜的质量为y
= x=12.25g
= y=20g
稀硫酸的溶质质量分数=×100%=24.5%
答:稀硫酸的溶质质量分数为24.5%。
(3)解:反应后溶液的质量=50g+10g=60g
反应后所得溶液中溶质的质量分数=×100%≈33.3%
答:反应后所得溶液中溶质的质量分数为33.3%。
(4)解:设和16g氧化铜反应的硫酸的质量为x,生成硫酸铜的质量为y
= x=19.6g
= y=32g
第Ⅱ组实验后溶液中剩余硫酸的质量=100g×24.5% 19.6g=4.9g
设与溶液中剩余的硫酸反应的氢氧化钠溶液的质量为z
= z=40g
设与32g硫酸铜反应的氢氧化钠溶液的质量为m,生成氢氧化铜沉淀的质量为n
= m=160g
= n=19.6g
所以将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图画为
答:将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图画为。
21.88.3%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列化肥从外观即可与其他化肥相区别的是( )
A.硝酸钾 B.氯化铵 C.磷矿粉 D.氯化钾
2.氮肥能促进植物的枝叶繁茂,叶色浓绿。下列属于氮肥的是
A.KH2PO4 B.K2SO4 C.NH4NO3 D.Ca3(PO4)2
3.下列各组固体物质,不能用水鉴别的是( )
A.KNO3、KCl
B.CaCO3、CaCl2
C.CuSO4、Na2SO4
D.NH4NO3、CaO
4.下列各组物质的溶液中,不另加试剂则无法鉴别出来的是
A.H2SO4 NaOH CuSO4
B.HCl NaOH NaCl
C.H2SO4 Ca(OH)2 FeCl3
D.HCl Ca(OH)2 Na2CO3
5.2020年世界水日的主题是“水与气候变化”。下列关于水的说法正确的是
A.生活中硬水转化为软水的方法是煮沸
B.电解水实验中产生氢气和氧气的体积比为1:8
C.化合物之间有水生成的反应一定是复分解反应
D.过滤后的河水为纯净水
6.下列各组离子在无色透明溶液中能大量共存的是
A.Cu2+、Na+、SO42-、Cl- B.K+、Na+、CO32—、NO3-
C.OH-、CO32-、Ca2+、Na+ D.Mg2+、Na+、OH-、CO32-
7.党的十九大提出要加快生态文明体制改革,建设美丽中国。下列做法正确的是
A.为保护环境,把废旧电池深埋处理
B.为增加粮食产量,大量使用农药、化肥
C.为节约水资源,用工业废水直接灌溉农田
D.为节约资源,大力开发新能源替代化石燃料
8.下列各组溶液混合后能发生反应且无明显现象的一组是
A.NaNO3、NaCl、AgNO3 B.CuSO4、H2SO4、BaCl2
C.HCl、Na2SO4、NaOH D.HCl、NaHCO3、NaNO3
9.现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有
A.② B.②③ C.①②③ D.②③④
10.下表物质中含有少量杂质,其中除杂方法正确的是
物质 杂质 除去杂质的方法
A CaCl2溶液 HCl 滴入碳酸钠溶液
B CO2 O2 通过灼热的铜网
C NaOH Na2CO3 加入稀盐酸至不再产生气泡
D CuO Cu 加足量稀盐酸,充分搅拌后再过滤
A.A B.B C.C D.D
二、简答题
11.某园林工人配制波尔多液时,将胆矾(CuSO4·5H2O)晶体、生石灰(CaO)分别与水按1∶50的质量比混合(胆矾溶于水得到CuSO4溶液),然后把得到的两种液体在木桶里混合并充分搅拌。
(1)配制波尔多液不用铁桶的原因:__________________________________________。
(2)两种液体在木桶里反应的化学方程式:____________________________________________________。
(3)若要检验所配的波尔多液中是否还含有CuSO4,实验方法是_________________________________。
12.某同学设计了下图所示的装置进行实验,观察到紫色石蕊溶液变成红色,从而得出二氧化碳和水反应生成了酸。而此实验存在一个明显的不足,影响结论的得出,请回答:
(1)此实验的不足是什么?
(2)如果在原装置基础上加一个装置就可以得出正确结论,则要加的装置是什么,装置内加入的药品是什么?
13.工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:
(1)在① ③三个过程中,发生分解反应的是_____(填序号)。
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:
①在t1℃时,Na2CO3的溶解度是____g。
②t2℃时,NaCl的溶解度___Na2CO3的溶解度(填“大于”“等于”“小于”之一)。
③要从海水中提取NaCl,应采用的方法是___(填“蒸发结晶”或“降温结晶”)。
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是__g。
三、推断题
14.A~E是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种。A可用于金属表面除锈,B可用来改良酸性土壤。它们相互间发生反应或转化的关系如图所示(“—”表面两种物质间能发生反应,“→”表示两种物质间的转化关系)。
(1)A、C的化学式分别为____________、____________;D在生活和生产中的一种用途是____________。
(2)C→E反应的化学方程式为:____________。
15.已知A~G为初中化学常见的七种物质。其中D的固体叫做“干冰”;B中只含两种元素,C与E不含相同元素。各种物质间的反应和转化关系如图所示(“﹣”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
请分析后回答:
(1)D的化学式_____。
(2)B与G反应的化学方程式_____。
四、实验题
16.下图是粗盐提纯实验的部分操作,请回答相关问题。
A 溶解B.蒸发C.过滤D.取一定量的粗盐
(1)粗盐提纯的正确操作顺序为___________(填字母)。
(2)上图所示操作中,有错误的是___________(填字母)。
(3)操作A中,玻璃棒的作用是___________。
(4)操作B中___________时停止加热。
(5)过滤时用到的玻璃仪器有烧杯、___________、___________。过滤时的“两低”是指滤纸边缘低于漏斗边缘,___________。
17.进行如下实验,研究物质的性质。
(1)A中有气泡产生,证明黄铜为_______合金(填序号)。
a 铜锌 b 铜银 c 铜碳
(2)B中反应的化学方程式为_______。
(3)验证鸡蛋壳中含有碳酸盐,应补充的操作及观察到现象是________。
五、计算题
18.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
19.磷酸氢二铵[(NH4)2HPO4]是一种化肥,它对提高农作物的产量具有重要作用.填空:
(1)(NH4)2HPO4_____(填“属于”或“不属于”)复合肥料,它由_____(写数字)种元素组成.
(2)(NH4)2HPO4的相对分子质量是_____;
(3)(NH4)2HPO4中氮元素的质量分数为_____(精确到0.1%)
20.为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如右表:根据实验及有关数据进行分析与计算:
第Ⅰ组 第Ⅱ组 第Ⅲ组
稀硫酸的质量/g 50 100 150
溶解固体的质量/g 10 16 16
(1)20g样品中含氧化铜的质量为______g。
(2)根据第I组数据计算所用稀硫酸的溶质质量分数是多少?(写出计算过程)
(3)求第I组实验所得溶液中溶质的质量分数______(精确到0.1%)。
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,在图中画出滤液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图。
21.厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如下图所示。
计算:该食用碱中碳酸钠的质量分数是__________ (计算结果精确至0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.A
4.B
5.A
6.B
7.D
8.C
9.B
10.B
11. 铁能与硫酸铜发生置换反应(或Fe+CuSO4===Cu+FeSO4) Ca(OH)2+CuSO4===CaSO4+Cu(OH)2↓ 将一根光亮的铁丝插入波尔多液中,观察铁丝表面是否变红
12.(1)反应中所用的酸为浓盐酸,会挥发出氯化氢气体溶于水也能使石蕊变红
(2)在甲乙之间加一个吸收氯化氢气体的装置,药品为饱和的碳酸氢钠溶液
13. ③ 18 小于 蒸发结晶 59
14.(1) HCl NaOH 灭火
(2)2NaOH+CO2=Na2CO3+H2O
15. CO2 HCl+AgNO3=HNO3+AgCl↓
16.(1)DACB
(2)C
(3)加速溶解
(4)大量固体
(5) 漏斗(或玻璃棒) 玻璃棒(或漏斗) 液面低于滤纸边缘
17. a Ca(OH)2+2HCl=CaCl2+2H2O 将产生的气体通入澄清的石灰水中,石灰水变浑浊
18.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
19. 属于 4 132 21.2%
20.(1)16
(2)解:由第I组合第II组实验数据可知,第I组实验中硫酸完全反应
设50g稀硫酸中H2SO4的质量为x,生成硫酸铜的质量为y
= x=12.25g
= y=20g
稀硫酸的溶质质量分数=×100%=24.5%
答:稀硫酸的溶质质量分数为24.5%。
(3)解:反应后溶液的质量=50g+10g=60g
反应后所得溶液中溶质的质量分数=×100%≈33.3%
答:反应后所得溶液中溶质的质量分数为33.3%。
(4)解:设和16g氧化铜反应的硫酸的质量为x,生成硫酸铜的质量为y
= x=19.6g
= y=32g
第Ⅱ组实验后溶液中剩余硫酸的质量=100g×24.5% 19.6g=4.9g
设与溶液中剩余的硫酸反应的氢氧化钠溶液的质量为z
= z=40g
设与32g硫酸铜反应的氢氧化钠溶液的质量为m,生成氢氧化铜沉淀的质量为n
= m=160g
= n=19.6g
所以将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图画为
答:将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图画为。
21.88.3%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
