科粤版九年级化学下册7.2物质溶解的量同步练习(word版有答案)
文档属性
| 名称 | 科粤版九年级化学下册7.2物质溶解的量同步练习(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 167.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览



文档简介
科粤版九年级化学下册 7.2 物质溶解的量 同步练习
一、单选题
1.将下列调味剂加入水中,不能形成溶液的是
A.芝麻油 B.蔗糖 C.味精 D.食盐
2.夏季暴雨前,常出现“闷热”天气,此时鱼塘中鱼儿往往有“浮头”(浮出水面)现象。说明气体在水中的溶解度与压强、温度有关。以下关于气体溶解度的说法正确的是( )
A.压强增大,气体溶解度不变 B.压强减小,气体溶解度增大
C.温度降低,气体溶解度减小 D.温度升高,气体溶解度减小
3.一定温度下,向烧杯中加入一定质量的水,仅有部分晶体溶解,所得溶液与原溶液相比,说法正确的是( )
A.溶剂的质量增加,溶液颜色变浅 B.溶质溶解度不变,溶液颜色变深
C.溶质的质量增加,溶液颜色变深 D.溶质溶解度不变,溶液颜色不变
4.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.a物质的溶解度一定小于b的溶解度
B.40℃时,a、b两种物质的饱和溶液中溶质的质量分数相同
C.c物质一定是氢氧化钙的溶解度曲线
D.三种物质的饱和溶液分别从40℃降温到20℃,a、b析出的晶体质量相等
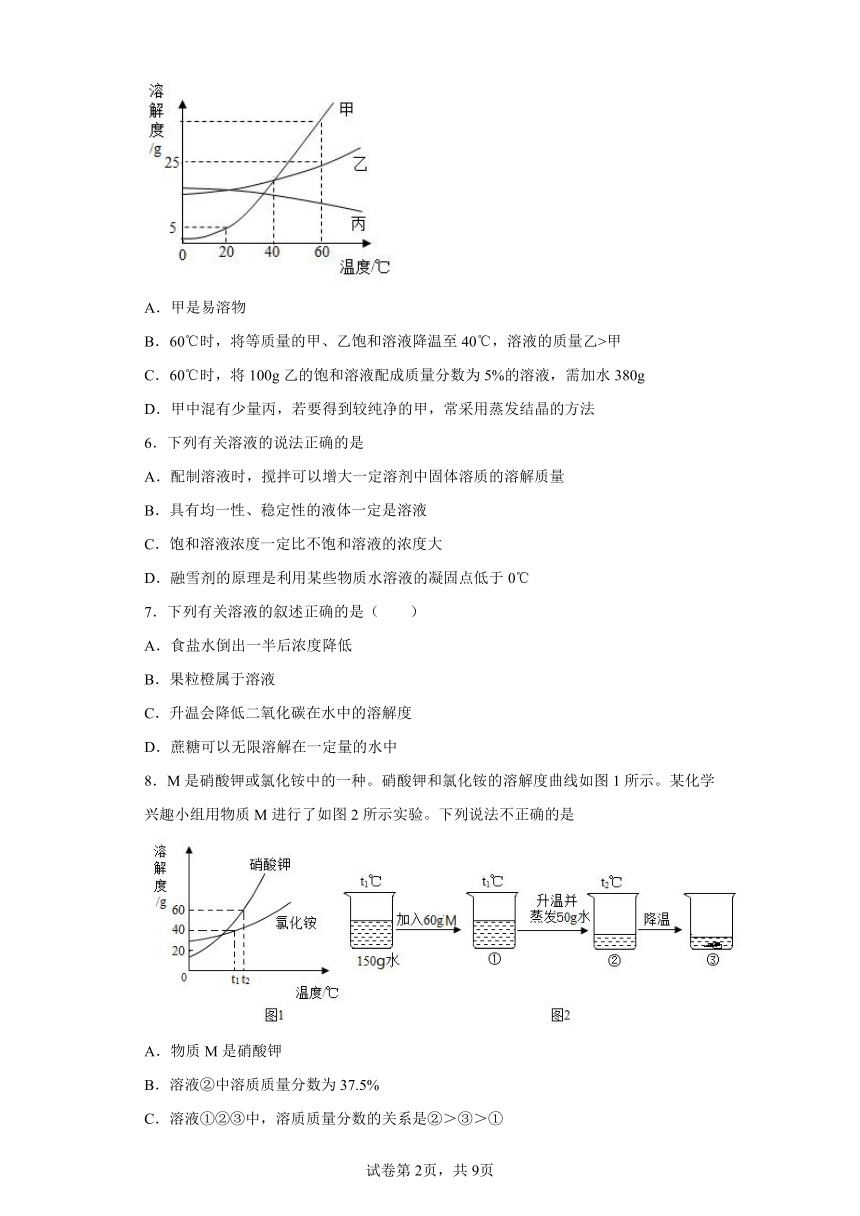
5.甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是
A.甲是易溶物
B.60℃时,将等质量的甲、乙饱和溶液降温至40℃,溶液的质量乙>甲
C.60℃时,将100g乙的饱和溶液配成质量分数为5%的溶液,需加水380g
D.甲中混有少量丙,若要得到较纯净的甲,常采用蒸发结晶的方法
6.下列有关溶液的说法正确的是
A.配制溶液时,搅拌可以增大一定溶剂中固体溶质的溶解质量
B.具有均一性、稳定性的液体一定是溶液
C.饱和溶液浓度一定比不饱和溶液的浓度大
D.融雪剂的原理是利用某些物质水溶液的凝固点低于0℃
7.下列有关溶液的叙述正确的是( )
A.食盐水倒出一半后浓度降低
B.果粒橙属于溶液
C.升温会降低二氧化碳在水中的溶解度
D.蔗糖可以无限溶解在一定量的水中
8.M是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组用物质M进行了如图2所示实验。下列说法不正确的是
A.物质M是硝酸钾
B.溶液②中溶质质量分数为37.5%
C.溶液①②③中,溶质质量分数的关系是②>③>①
D.溶液①为不饱和溶液,溶液②和③为饱和溶液
9.在装有水的烧杯中分别加入以下物质,其中形成的溶液温度降低的是
A.生石灰 B.氢氧化钠 C.氯化钠 D.硝酸铵
10.甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是
A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
11.下列关于饱和溶液与不饱和溶液的叙述,正确的是
A.稀溶液一定是不饱和溶液 B.浓溶液一定是饱和溶液
C.在一定温度下,同种溶质的饱和溶液一定比不饱和溶液要浓 D.浓溶液不一定是饱和溶液,稀溶液一定是不饱和溶液
12.某兴趣小组同学用下列实验装置进行相应实验,不能达到实验目的的是
A.用甲所示装置验证铁、铜两种金属的活动性顺序
B.用乙所示装置验证氢氧化钠溶解的热效应
C.用丙所示装置可证明大理石粉尘不能发生爆炸
D.用丁所示装置配制1%的Ca(OH)2溶液
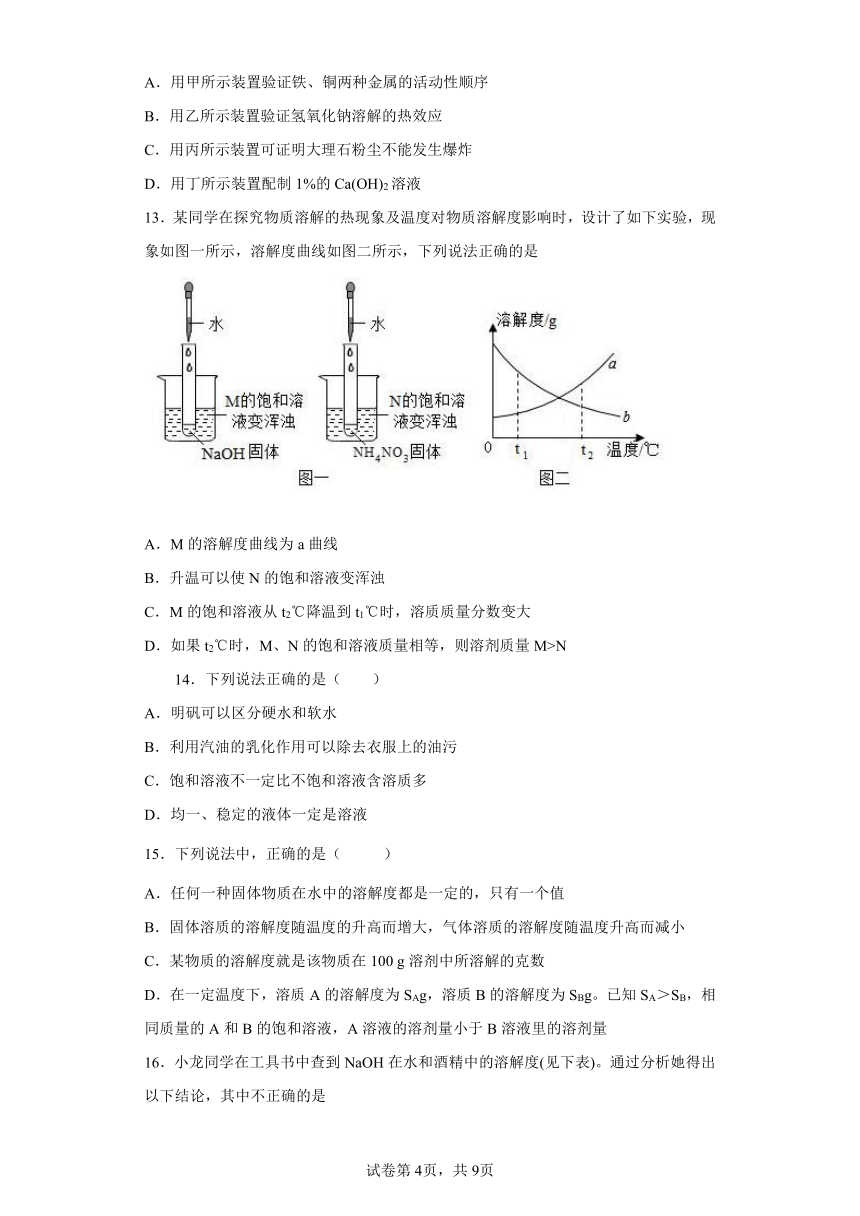
13.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
14.下列说法正确的是( )
A.明矾可以区分硬水和软水
B.利用汽油的乳化作用可以除去衣服上的油污
C.饱和溶液不一定比不饱和溶液含溶质多
D.均一、稳定的液体一定是溶液
15.下列说法中,正确的是( )
A.任何一种固体物质在水中的溶解度都是一定的,只有一个值
B.固体溶质的溶解度随温度的升高而增大,气体溶质的溶解度随温度升高而减小
C.某物质的溶解度就是该物质在100 g溶剂中所溶解的克数
D.在一定温度下,溶质A的溶解度为SAg,溶质B的溶解度为SBg。已知SA>SB,相同质量的A和B的饱和溶液,A溶液的溶剂量小于B溶液里的溶剂量
16.小龙同学在工具书中查到NaOH在水和酒精中的溶解度(见下表)。通过分析她得出以下结论,其中不正确的是
20 ℃ 40 ℃
水 109 g 129 g
酒精 17.3 g 40 g
A.温度和溶剂种类对NaOH的溶解度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40 ℃,40 g NaOH溶解在100 g酒精中达到饱和
D.将等质量40 ℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20 ℃,析出的晶体前者比后者多
二、综合应用题
17.某品牌可乐汽水、白砂糖、焦糖色素(使可乐显黑褐色)、磷酸(H3PO4)等按一定比例混合并压入二氧化碳配制而成。
(1)磷酸中H、P、O三种元素的质量比为_______________。
(2)某同学为了定量测定可乐中磷酸的含量,进行如下实验
步骤1:取可乐样品25mL,加入活性炭,浸泡、过滤、洗涤。
步骤2:将滤液煮沸10min,冷却,加入适量蒸馏水。
步骤3:继续往滤液中加几滴某指示剂,再逐滴滴入0.1%的NaOH溶液20g,恰好完全反应。(测定原理: H3PO4+NaOH=NaH2PO4+H2O)
①步骤1中活性炭的作用是_____________________
②步骤2中“煮沸10min"能除尽滤液中CO2的原因之一是当温度升高时,气体的溶解度_______(填“变大”“变小”或“不变”)。
③计算1L可乐中磷酸的含量_____________。
18.(1)回答有关燃料的问题:
①三大矿物燃料包括:煤、石油和______;
②天然气的主要成分甲烷完全燃烧的化学方程式是______。
③燃烧发电时,将煤块粉碎成煤粉,目的是______,使燃料充分燃烧;化石燃料燃烧都会产生温室气体二氧化碳,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,生成水和甲烷。该反应化学方程式为______。
(2)溶液及物质的溶解性对我们的生产生活有重要意义、如图是三种物质的溶解度曲线,请回答:
①三种物质中,______的溶解度受温度影响最大。
②80℃时硝酸钠的溶解度是______g。
③将70℃时三种物质的饱和溶液分别降温至30℃,所得溶液为不饱和溶液的是______溶液。
④硝酸钾属于复合肥料,所含营养元素有______,溶质质量分数为3%的硝酸钾溶液常用作无土栽培的营养液,配制这种营养液150kg,需要硝酸钾固体的质量______kg。
19.种学家发出警钟称,到本世纪末,全球平均温度可能比工业革命之前上升4℃以上,要防止这个局面的出现,必须降低未来几十年全球的温室气体排放量,2015年的巴黎气候变化大会上也达成了这一全球性协议,旨在实现碳中和——让地球排放的温室气体与其吸纳能力相当。请你回答下列问题:
(1)为保护人类赖以生存的地球,我们应采取有效措施以防止大气中二氧化碳含量的大量增加,以下建议中行之有效的措施是______(填序号)。
a开发太阳能、水能、风能、地热等新能源
b.禁止使用煤、石油、天然气等矿物燃料
c.大量植树造林绿化环境,禁止乱砍乱伐
(2)将空气中的二氧化碳输送到水冷的深海中贮藏可以减少空气中二氧化碳含量。但科学家担心这样做会增加海水的酸度,导致海洋生物死亡。二氧化碳使海水酸度增加的原因是_____(用化学方程式表示)。
(3)实验室常用石灰石和稀盐酸制取二氧化碳,某化学兴趣小组现取含碳酸钙的石灰石25g于烧杯中缓慢加入稀盐酸(石灰石中的杂质不溶于水,也不与加入稀盐酸的反应)剩余固体质量于加入的稀盐酸的质量关系如图所示。请根据要求回答问题:
①在滴入稀盐酸的过程中,观察到的明显现象是______(一条即可)
②当加入稀盐酸240g时,烧杯中溶液里含有的溶质是_______(写化学式)
③计算恰好完全反应时所得不饱和溶液的质量______(计算结果精确到0.1g)。
20.t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
(1)烧杯②中的上层清液是否达到饱和状态?_______(填“是”、“否”或“无法判断”);
(2)烧杯②中溶解的溶质是________(写化学式);
(3)t1℃时200g硝酸钾的饱和溶液中硝酸钾的质量______g;
(4)关于图1中烧杯内的物质,下列说法正确的是_________
A烧杯①内溶液中溶质的质量分数<烧杯②内上层清液中溶质的质量分数
B烧杯②中加热蒸发少量水时,同时一定还有固体析出
C将两个烧杯中的溶液混合,充分搅拌后,烧杯中可能还有氯化钾没有溶解
D将温度升高到t2℃,烧杯②中固体一定全溶解,并成为不饱和溶液(不考虑水的蒸发)
E将温度升高到t2℃,烧杯①内溶液的质量=烧杯②内溶液的质量(不考虑水的蒸发)
21.(1)回答有关燃料的问题:
①三大矿物燃料包括:煤、石油和___;
②天然气的主要成分甲烷完全燃烧的化学方程式是_______。
③燃烧发电时,将煤块粉碎成煤粉,目的是_______,使燃料充分燃烧;化石燃料燃烧都会产生温室气体二氧化碳,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,生成水和甲烷。该反应化学方程式为______。
(2)如图是甲、乙、丙三种物质的溶解度曲线。请根据图中信息回答下列问题:
①甲、乙两种物质在_____℃时溶解度相等;
②t3℃时,把30克甲充分溶解在50克水中,所得溶液质量是_____g。
③t3℃时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是_____。
④若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是_____。
22.水与溶液在生产生活中有广泛的用途。请结合所学知识回答下列问题:
(1)崂山是中国海岸线第一高峰第,有着海上“第一名山”之称。“五.一”期间小明家去崂山踏青。
①小明带去“自热米饭”的加热原理是饭盒夹层中的水与生石灰反应生成氢氧化钙,放出大量的热,该反应的化学方程式为 _____ 。
②小明从北九水带回一瓶山泉水,为检验这瓶水的硬度,可向水中加入 _____ 。
(2)如图是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。
①M点表示的含义是 _____ 。
②t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是 _____ 。
③t3℃时,将35g甲物质加入到50g水中,充分溶解后所得溶液的质量是 _____ 。
④t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶质质量分数由大到小的顺序是 _____ 。
(3)下图是初中化学中常见的实验。相关说法错误的是 _____ (填序号)。
A实验的目的是测定空气中氧气的体积分数
B实验,水中的白磷没有燃烧,是因为温度没有达到着火点
C实验看到的实验现象是软塑料瓶变瘪,可证明二氧化碳与水发生了化学反应
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.D
3.D
4.B
5.B
6.D
7.C
8.C
9.D
10.D
11.C
12.D
13.D
14.C
15.D
16.D
17. 3:31:64 吸附色素 变小 1.96g/L
18. 天然气 CH4+2O2CO2+2H2O 增大与氧气的接触面积 CO2+4H22H2O+CH4 硝酸钾 150 硫酸铈 氮元素、钾元素 4.5
19.(1)AC(2)CO2+H2O=H2CO3(3)产生大量的气泡或固体减少;CaCl2和HCl;200g
20. 是 KNO3 40g DE
21. 天然气 CH4+2O2CO2+2H2O 增大与氧气的接触面积 CO2+4H22H2O+CH4 t2 75 丙 冷却热饱和溶液
22. 肥皂水 t2℃时,甲、丙两种物质的溶解度均为30g 丙>乙>甲 80g 乙>甲>丙 C
答案第1页,共2页
答案第1页,共2页
一、单选题
1.将下列调味剂加入水中,不能形成溶液的是
A.芝麻油 B.蔗糖 C.味精 D.食盐
2.夏季暴雨前,常出现“闷热”天气,此时鱼塘中鱼儿往往有“浮头”(浮出水面)现象。说明气体在水中的溶解度与压强、温度有关。以下关于气体溶解度的说法正确的是( )
A.压强增大,气体溶解度不变 B.压强减小,气体溶解度增大
C.温度降低,气体溶解度减小 D.温度升高,气体溶解度减小
3.一定温度下,向烧杯中加入一定质量的水,仅有部分晶体溶解,所得溶液与原溶液相比,说法正确的是( )
A.溶剂的质量增加,溶液颜色变浅 B.溶质溶解度不变,溶液颜色变深
C.溶质的质量增加,溶液颜色变深 D.溶质溶解度不变,溶液颜色不变
4.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.a物质的溶解度一定小于b的溶解度
B.40℃时,a、b两种物质的饱和溶液中溶质的质量分数相同
C.c物质一定是氢氧化钙的溶解度曲线
D.三种物质的饱和溶液分别从40℃降温到20℃,a、b析出的晶体质量相等
5.甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是
A.甲是易溶物
B.60℃时,将等质量的甲、乙饱和溶液降温至40℃,溶液的质量乙>甲
C.60℃时,将100g乙的饱和溶液配成质量分数为5%的溶液,需加水380g
D.甲中混有少量丙,若要得到较纯净的甲,常采用蒸发结晶的方法
6.下列有关溶液的说法正确的是
A.配制溶液时,搅拌可以增大一定溶剂中固体溶质的溶解质量
B.具有均一性、稳定性的液体一定是溶液
C.饱和溶液浓度一定比不饱和溶液的浓度大
D.融雪剂的原理是利用某些物质水溶液的凝固点低于0℃
7.下列有关溶液的叙述正确的是( )
A.食盐水倒出一半后浓度降低
B.果粒橙属于溶液
C.升温会降低二氧化碳在水中的溶解度
D.蔗糖可以无限溶解在一定量的水中
8.M是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组用物质M进行了如图2所示实验。下列说法不正确的是
A.物质M是硝酸钾
B.溶液②中溶质质量分数为37.5%
C.溶液①②③中,溶质质量分数的关系是②>③>①
D.溶液①为不饱和溶液,溶液②和③为饱和溶液
9.在装有水的烧杯中分别加入以下物质,其中形成的溶液温度降低的是
A.生石灰 B.氢氧化钠 C.氯化钠 D.硝酸铵
10.甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是
A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
11.下列关于饱和溶液与不饱和溶液的叙述,正确的是
A.稀溶液一定是不饱和溶液 B.浓溶液一定是饱和溶液
C.在一定温度下,同种溶质的饱和溶液一定比不饱和溶液要浓 D.浓溶液不一定是饱和溶液,稀溶液一定是不饱和溶液
12.某兴趣小组同学用下列实验装置进行相应实验,不能达到实验目的的是
A.用甲所示装置验证铁、铜两种金属的活动性顺序
B.用乙所示装置验证氢氧化钠溶解的热效应
C.用丙所示装置可证明大理石粉尘不能发生爆炸
D.用丁所示装置配制1%的Ca(OH)2溶液
13.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
14.下列说法正确的是( )
A.明矾可以区分硬水和软水
B.利用汽油的乳化作用可以除去衣服上的油污
C.饱和溶液不一定比不饱和溶液含溶质多
D.均一、稳定的液体一定是溶液
15.下列说法中,正确的是( )
A.任何一种固体物质在水中的溶解度都是一定的,只有一个值
B.固体溶质的溶解度随温度的升高而增大,气体溶质的溶解度随温度升高而减小
C.某物质的溶解度就是该物质在100 g溶剂中所溶解的克数
D.在一定温度下,溶质A的溶解度为SAg,溶质B的溶解度为SBg。已知SA>SB,相同质量的A和B的饱和溶液,A溶液的溶剂量小于B溶液里的溶剂量
16.小龙同学在工具书中查到NaOH在水和酒精中的溶解度(见下表)。通过分析她得出以下结论,其中不正确的是
20 ℃ 40 ℃
水 109 g 129 g
酒精 17.3 g 40 g
A.温度和溶剂种类对NaOH的溶解度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40 ℃,40 g NaOH溶解在100 g酒精中达到饱和
D.将等质量40 ℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20 ℃,析出的晶体前者比后者多
二、综合应用题
17.某品牌可乐汽水、白砂糖、焦糖色素(使可乐显黑褐色)、磷酸(H3PO4)等按一定比例混合并压入二氧化碳配制而成。
(1)磷酸中H、P、O三种元素的质量比为_______________。
(2)某同学为了定量测定可乐中磷酸的含量,进行如下实验
步骤1:取可乐样品25mL,加入活性炭,浸泡、过滤、洗涤。
步骤2:将滤液煮沸10min,冷却,加入适量蒸馏水。
步骤3:继续往滤液中加几滴某指示剂,再逐滴滴入0.1%的NaOH溶液20g,恰好完全反应。(测定原理: H3PO4+NaOH=NaH2PO4+H2O)
①步骤1中活性炭的作用是_____________________
②步骤2中“煮沸10min"能除尽滤液中CO2的原因之一是当温度升高时,气体的溶解度_______(填“变大”“变小”或“不变”)。
③计算1L可乐中磷酸的含量_____________。
18.(1)回答有关燃料的问题:
①三大矿物燃料包括:煤、石油和______;
②天然气的主要成分甲烷完全燃烧的化学方程式是______。
③燃烧发电时,将煤块粉碎成煤粉,目的是______,使燃料充分燃烧;化石燃料燃烧都会产生温室气体二氧化碳,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,生成水和甲烷。该反应化学方程式为______。
(2)溶液及物质的溶解性对我们的生产生活有重要意义、如图是三种物质的溶解度曲线,请回答:
①三种物质中,______的溶解度受温度影响最大。
②80℃时硝酸钠的溶解度是______g。
③将70℃时三种物质的饱和溶液分别降温至30℃,所得溶液为不饱和溶液的是______溶液。
④硝酸钾属于复合肥料,所含营养元素有______,溶质质量分数为3%的硝酸钾溶液常用作无土栽培的营养液,配制这种营养液150kg,需要硝酸钾固体的质量______kg。
19.种学家发出警钟称,到本世纪末,全球平均温度可能比工业革命之前上升4℃以上,要防止这个局面的出现,必须降低未来几十年全球的温室气体排放量,2015年的巴黎气候变化大会上也达成了这一全球性协议,旨在实现碳中和——让地球排放的温室气体与其吸纳能力相当。请你回答下列问题:
(1)为保护人类赖以生存的地球,我们应采取有效措施以防止大气中二氧化碳含量的大量增加,以下建议中行之有效的措施是______(填序号)。
a开发太阳能、水能、风能、地热等新能源
b.禁止使用煤、石油、天然气等矿物燃料
c.大量植树造林绿化环境,禁止乱砍乱伐
(2)将空气中的二氧化碳输送到水冷的深海中贮藏可以减少空气中二氧化碳含量。但科学家担心这样做会增加海水的酸度,导致海洋生物死亡。二氧化碳使海水酸度增加的原因是_____(用化学方程式表示)。
(3)实验室常用石灰石和稀盐酸制取二氧化碳,某化学兴趣小组现取含碳酸钙的石灰石25g于烧杯中缓慢加入稀盐酸(石灰石中的杂质不溶于水,也不与加入稀盐酸的反应)剩余固体质量于加入的稀盐酸的质量关系如图所示。请根据要求回答问题:
①在滴入稀盐酸的过程中,观察到的明显现象是______(一条即可)
②当加入稀盐酸240g时,烧杯中溶液里含有的溶质是_______(写化学式)
③计算恰好完全反应时所得不饱和溶液的质量______(计算结果精确到0.1g)。
20.t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
(1)烧杯②中的上层清液是否达到饱和状态?_______(填“是”、“否”或“无法判断”);
(2)烧杯②中溶解的溶质是________(写化学式);
(3)t1℃时200g硝酸钾的饱和溶液中硝酸钾的质量______g;
(4)关于图1中烧杯内的物质,下列说法正确的是_________
A烧杯①内溶液中溶质的质量分数<烧杯②内上层清液中溶质的质量分数
B烧杯②中加热蒸发少量水时,同时一定还有固体析出
C将两个烧杯中的溶液混合,充分搅拌后,烧杯中可能还有氯化钾没有溶解
D将温度升高到t2℃,烧杯②中固体一定全溶解,并成为不饱和溶液(不考虑水的蒸发)
E将温度升高到t2℃,烧杯①内溶液的质量=烧杯②内溶液的质量(不考虑水的蒸发)
21.(1)回答有关燃料的问题:
①三大矿物燃料包括:煤、石油和___;
②天然气的主要成分甲烷完全燃烧的化学方程式是_______。
③燃烧发电时,将煤块粉碎成煤粉,目的是_______,使燃料充分燃烧;化石燃料燃烧都会产生温室气体二氧化碳,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,生成水和甲烷。该反应化学方程式为______。
(2)如图是甲、乙、丙三种物质的溶解度曲线。请根据图中信息回答下列问题:
①甲、乙两种物质在_____℃时溶解度相等;
②t3℃时,把30克甲充分溶解在50克水中,所得溶液质量是_____g。
③t3℃时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是_____。
④若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是_____。
22.水与溶液在生产生活中有广泛的用途。请结合所学知识回答下列问题:
(1)崂山是中国海岸线第一高峰第,有着海上“第一名山”之称。“五.一”期间小明家去崂山踏青。
①小明带去“自热米饭”的加热原理是饭盒夹层中的水与生石灰反应生成氢氧化钙,放出大量的热,该反应的化学方程式为 _____ 。
②小明从北九水带回一瓶山泉水,为检验这瓶水的硬度,可向水中加入 _____ 。
(2)如图是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。
①M点表示的含义是 _____ 。
②t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是 _____ 。
③t3℃时,将35g甲物质加入到50g水中,充分溶解后所得溶液的质量是 _____ 。
④t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶质质量分数由大到小的顺序是 _____ 。
(3)下图是初中化学中常见的实验。相关说法错误的是 _____ (填序号)。
A实验的目的是测定空气中氧气的体积分数
B实验,水中的白磷没有燃烧,是因为温度没有达到着火点
C实验看到的实验现象是软塑料瓶变瘪,可证明二氧化碳与水发生了化学反应
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.D
3.D
4.B
5.B
6.D
7.C
8.C
9.D
10.D
11.C
12.D
13.D
14.C
15.D
16.D
17. 3:31:64 吸附色素 变小 1.96g/L
18. 天然气 CH4+2O2CO2+2H2O 增大与氧气的接触面积 CO2+4H22H2O+CH4 硝酸钾 150 硫酸铈 氮元素、钾元素 4.5
19.(1)AC(2)CO2+H2O=H2CO3(3)产生大量的气泡或固体减少;CaCl2和HCl;200g
20. 是 KNO3 40g DE
21. 天然气 CH4+2O2CO2+2H2O 增大与氧气的接触面积 CO2+4H22H2O+CH4 t2 75 丙 冷却热饱和溶液
22. 肥皂水 t2℃时,甲、丙两种物质的溶解度均为30g 丙>乙>甲 80g 乙>甲>丙 C
答案第1页,共2页
答案第1页,共2页
