科粤版九年级化学下册8.2常见的酸和碱同步练习(word版有答案)
文档属性
| 名称 | 科粤版九年级化学下册8.2常见的酸和碱同步练习(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 258.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览




文档简介
科粤版九年级化学下册 8.2 常见的酸和碱 同步练习
一、单选题
1.下列各图所示变化中,属于物理变化的是( )
A.制作叶脉书签 B.钻木取火
C.比较硬度 D.酸雨的腐蚀
2.下列图示实验操作中,正确的是
A.取用液体 B.稀释浓硫酸
C.收集氧气 D.蒸发结晶
3.下图所示实验操作正确的是( )
A. 点燃酒精灯 B.滴加液体
C. 稀释浓硫酸 D. 读出液体的体积
4.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性 B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质 D.固体氢氧化钠能吸收水蒸气而潮解
5.下列实验基本操作不正确的是( )
A.稀释浓硫酸
B.溶解氯化钠
C.滴加酚酞溶液
D.加热水
6.下列变化中,与其他三种变化有本质区别的是( )
A.浓盐酸敞口放置在空气中质量减少
B.抹在墙壁上的石灰浆逐渐变硬
C.生石灰溶于水成熟石灰
D.NaOH溶液遇酚酞变红色
7.下列说法正确的是
A.不同种元素最本质的区别是相对原子质量的不同
B.空气质量指数级别越高,空气质量越差
C.饱和澄清石灰水变浑浊一定是发生了化学变化
D.敞口放置一段时间的浓盐酸和浓硫酸,溶质的质量分数和溶液的质量都会减小
8.下列对实验现象的描述错误的是( )
A.硫在氧气中燃烧产生淡蓝色的火焰,生成有刺激性气味的气体
B.将二氧化碳通入紫色石蕊试液中,溶液变红
C.打开盛有浓盐酸的试剂瓶,瓶口产生大量白雾
D.镁和稀盐酸反应产生大量气泡,放出热量
9.下列变化属于化学变化的是
A.分离液态空气制氧气 B.食品久置发生霉变
C.活性炭吸附除异味 D.浓盐酸敞口产生大量白雾
10.下列物质露置于空气中,因发生化学变化而使质量增加的是
A.浓硫酸 B.烧碱溶液 C.浓盐酸 D.双氧水溶液
11.下列说法不正确的是( )
A.稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水里,并不断搅拌
B.一定温度下,某固态物质的饱和溶液一定不能再溶解其他物质
C.洗涤剂去除油污利用了洗涤剂的乳化功能
D.打开汽水瓶盖时,汽水会自动喷出来,这说明气体在水中的溶解度与压强有关
12.如图中所有物质的类别均不同,连线两端的物质常温下均能反应。下列说法正确的是
A.X、Y、Z分别属于碱、盐、酸
B.X和Z可以是Al2O3和CaCl2
C.Y和Z可以是Na2CO3和Ca(OH)2
D.X和Y可以是NaCl和NaOH
13.下列说法正确的是
①酸和碱中都含氢元素,所以含氢元素的化合物一定是酸或碱
②我们把pH小于5.6的降雨称为酸雨
③书写化学方程式时,生成物中有气体生成就必须注明“↑”符号
④红热的铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体物质
⑤燃烧都伴随有发光、放热现象,有发光、放热现象的变化一定是燃烧
⑥分子原子都是不显电性的粒子,不显电性的粒子不一定是分子或原子
⑦现有Al、Cu、Ag三种金属,只用CuSO4溶液不能确定其金属活动性顺序
A.①③⑦ B.①②⑥ C.③④⑤ D.②④⑥
14.下列有关氢氧化钠的说法,错误的是( )
A.氢氧化钠俗称烧碱
B.氢氧化钠有强烈的腐蚀性
C.氢氧化钠固体可用于干燥二氧化碳气体
D.氢氧化钠可用于制肥皂、洗涤剂、造纸、纺织工业等
15.盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是
A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀
16.NaOH可用于造纸和印染工业,NaOH属于
A.单质 B.酸 C.碱 D.盐
二、综合应用题
17.实验是科学探究的重要途径。
(1)结合下列化学实验装置,回答有关问题。
①写出一个用A装置制取O2的化学方程式_____。
②若用B装置制取能使澄清的石灰水变浑浊的气体,则实验室制取该气体的化学方程式是__。与B相比较,C的主要优点是什么______。
③用试管采用排空气法收集氢气,请在D方框中画出装置图(只画试管和导气管)______。
(2)用实验室存放的氢氧化钠溶液做中和反应实验,发现有气泡产生。于是红红判断氢氧化钠变质了。请用化学方程式说明氢氧化钠变质的原因______。
为探究氢氧化钠是否完全变质,红红设计了两个实验方案。
方案1:取少量上述氢氧化钠溶液样品,滴加几滴酚酞溶液,溶液变成红色
方案2:取少量上述氢氧化钠溶液样品,加入饱和石灰水,静置,取上层清液,滴加几滴酚酞溶液。发现溶红色。于是明明认为样品中还会有氢氧化钠,没有完全变质。
①康康认为红红的两个实验方案都不能达到目的,他的理由是____。
②请你设计一个方案来验证氢氧化钠是否完全变质。______。
(3)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。请计算废水中氯化氢的质量分数__。
18.家庭厨房就是一个化学小世界,包含着许多的化学知识。请回答问题。
一、厨房里离不开水。
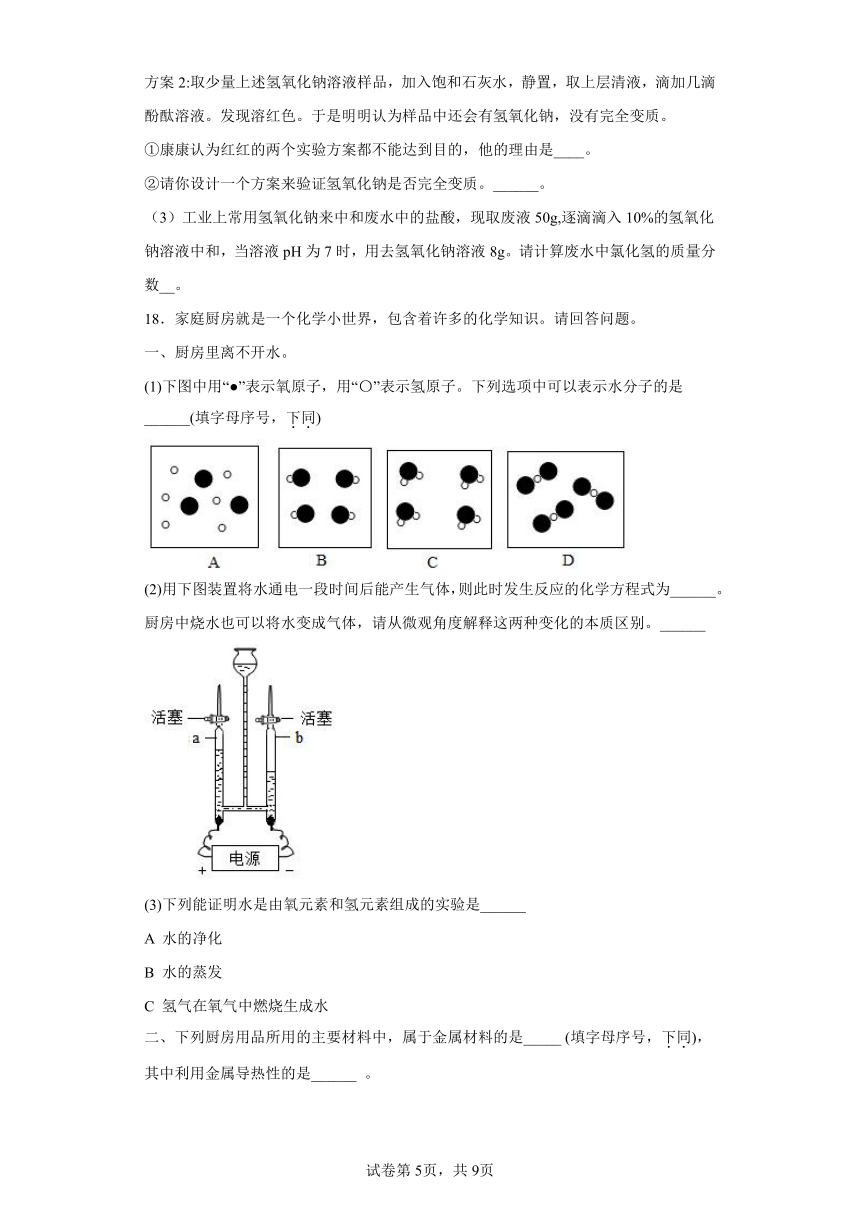
(1)下图中用“●”表示氧原子,用“〇”表示氢原子。下列选项中可以表示水分子的是______(填字母序号,下同)
(2)用下图装置将水通电一段时间后能产生气体,则此时发生反应的化学方程式为______。厨房中烧水也可以将水变成气体,请从微观角度解释这两种变化的本质区别。______
(3)下列能证明水是由氧元素和氢元素组成的实验是______
A 水的净化
B 水的蒸发
C 氢气在氧气中燃烧生成水
二、下列厨房用品所用的主要材料中,属于金属材料的是_____ (填字母序号,下同),其中利用金属导热性的是______ 。
三、厨房里离不开燃料,燃料燃烧产生热量为我们所用。
(1) 化石燃料是当前人类的主要燃料,包括煤、______和天然气。
(2) 写出天然气燃烧的化学方程式。______
(3)化石能源是有限的,我们在合理利用的同时,要努力开发新能源。请写出一种你所知道的新能源_______。
(4) 炒菜时,油锅着火,盖上锅盖即可灭火,原因是______。
四、下表列出了两种家用清洁剂的功能、有效成分和注意事项。
名称 洁厕灵 漂白精
功能 有效清除污垢,除异味 快速漂除衣物污渍
有效成分 HC1 NaCIO
注意事项 勿用于铁、铝等金属制品清洁 勿与酸性制品或其他清洁产品混合使用
据表回答下列问题:
(1) “洁厕灵”勿用于铁制品清洁的理由是 ______ (用化学方程式表示)。
(2)“洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为NaClO + 2HC1 = NaCl + X个+ H2O,则X的化学式为______ ;NaC1O中氯元素的化合价为______ 。
19.在化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂,为了确定其成分,同学们进行了如下的探究活动:
【查阅资料】
Ⅰ.石灰干燥剂的有效成分为生石灰(CaO)
Ⅱ.Ca(OH)2是一种微溶于水的白色固体,其水溶液(俗称石灰水)具有如下性质:能使无色酚酞(一种化学指示剂)溶液变红,与CO2气体反应出现浑浊,能与盐酸反应但无明显现象。
【方案设计】
小组成员设计了如下实验方案以期得到相应推论:取样滴加稀盐酸,有气泡产生,则白色固体为CaCO3;若无气泡产生,则白色固体为Ca(OH)2
(1)请简要说明上述方案中不合理之处:___________。
(2)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你设计一种实验方案予以证明。
实验步骤 实验现象 结论
______________ _____________ 含CaCO3
______________ _____________ 含Ca(OH)2
【数据分析】
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学向10克样品中加入足量的稀盐酸,测得CO2气体的质量如图所示。
(3)根据题给信息猜想一下,实验开始时的一段时间没有CO2气体产生的原因是_______;计算该混合物中CaCO3的质量分数_____________(请写出过程)。
【反思与评价】
实验中,如有部分二氧化碳气体因溶解于水而没有全部逸出,则测得的混合物中CaCO3的质量分数________(填写“偏大”、 “偏小”或“不变”)。
20.实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,设计了实验,实验过程如下:
【实验一】取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是______________(用化学方程式表 示)。
【实验二】如图过程进行实验
通过实验二,能进一步推算出氢氧化钠变质的程度,请写出计算过程(反应的化学方程式是Na2CO3+CaC12=CaCO3↓+2NaC1)
【结论】该样品属于___________ (填“全部”、“部分”)变质。
【拓展】若要获得氢氧化钠溶液,应先取一定量的固体加入足量水中充分溶解,再加入___________,后进行_____。
21.化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)某化学兴趣小组的同学利用如图微型实验装置进行探究实验。
①写出一个双球管中可能反应的化学方程式___________。
②挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,由此可说明燃烧需要什么条件?___________。
③相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是___________。
(2)实验室可利用如图实验装置制取纯净、干燥的CO,然后用CO还原Fe2O3并检验气体产物。已知CO发生装置中的反应为:H2C2O4H2O+CO2↑+CO↑。
①A装置中能观察到什么现象?___________。
②写出B装置中反应的化学方程式:___________。
③要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接___________、___________接___________、___________接___________、___________接___________。
④从环保角度考虑,还需对以上装置进行改进,请简述改进措施___________。
(3)锌和盐酸(HCl)反应生成氢气和氯化锌。现实验室用13g锌与足量的盐酸反应,可制得氢气和氯化锌的质量各是多少?
22.如图所示,A~I是初中化学常见的物质,A的水溶液显碱性,D为大理石的主要成份,F为生活中最常见的调味剂,Y为红色固体,G与I组成元素相同,请根据图示回答下列问题(部分产物或反应条件省略):
⑴A的俗名为_____;
⑵反应③的化学方程式为_____;
⑶反应④的可能化学方程式为_____;
⑷Y属于是_____(选填“混合物”、“单质”或“氧化物”);
⑸某化学兴趣小组对①反应的废液过滤后的成份产生了兴趣.进行了实验探究:
【提出问题】将废液过滤后,滤液中的溶质含有哪些物质?
【猜想与假设】猜想I:滤液中的溶质只有氯化钙;
猜想Ⅱ:滤液中的溶质有_____
【进行实验】①甲小组的同学从下面A-E五种药品中选择合适的一种进行实验,证明了猜想Ⅱ是正确的。他们选择的药品不可能是_____。
A 紫色石蕊试液 B无色酚酞试液 C 锌粒 D 氧化铁粉末 E 氢氧化钠溶液
②乙小组选用一种钠盐溶液进行实验,也证明了猜想Ⅱ是确的,请完成下面的实验报告。
实验操作 实验现象 实验结论
取少量滤液于试管中,加入足量_____(填化学式)溶液,振荡。 _____ 猜想Ⅱ正确
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.D
4.B
5.B
6.A
7.B
8.A
9.B
10.B
11.B
12.C
13.D
14.C
15.B
16.C
17. 可以控制反应速度 方案1中,碳酸钠溶液也能使酚酞溶液变红,方案2中碳酸钠与氢氧化钙反应的生成物是氢氧化钠,也能使酚酞溶液变红 取少量上述氢氧化钠溶液样品,加入足量氯化钙溶液(或氯化钡溶液等),静置,取上层清液滴加几滴酚酞溶液,若溶液变成红色,则氢氧化钠没有完全变质;若溶液没有变成红色,则氢氧化钠全部变质 1.46%
18. C 2H2O2H2↑+O2↑ 水蒸发时分子本身不变,只是间隙发生变化,水电解时分子变成了其它分子 C BD B 石油 CH4 +2O2CO2 +2H2O 风能 隔绝氧气 Fe+2HCl=H2↑+FeCl2 Cl2 +1
19. 若白色固体为CaCO3和Ca(OH)2的混合物,加入盐酸也有气泡产生 取少量样品向其中滴加稀盐酸 有气泡产生 另取少量样品加入适量的水溶解、静置,取上层清液通入CO2气体 溶液变浑浊 盐酸先与氢氧化钠反应,还未与碳酸钠反应 50% 偏小
20. 解:设样品中碳酸钠的质量为x。
x=10.6g
,
因为样品中碳酸钠的质量分数为70.67%,所以部分变质,故填部分变质。 适量氢氧化钙溶液 过滤
21.(1) 或 温度达到可燃物着火点 磷##P
(2) Ca(OH)2溶液变浑浊
h g e f c##d d##c a 在A装置后加一个燃着的酒精灯或在A装置后绑一个气球
(3)解:设生成氢气的质量为x,生成氯化锌的质量为y
x=0.4g
y=27.2g
答:可制得氢气的质量为0.4g,生成氯化锌的质量为27.2g
22. 纯碱 氧化物 氯化钙和氯化氢 BE 冒气泡,生成白色沉淀
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列各图所示变化中,属于物理变化的是( )
A.制作叶脉书签 B.钻木取火
C.比较硬度 D.酸雨的腐蚀
2.下列图示实验操作中,正确的是
A.取用液体 B.稀释浓硫酸
C.收集氧气 D.蒸发结晶
3.下图所示实验操作正确的是( )
A. 点燃酒精灯 B.滴加液体
C. 稀释浓硫酸 D. 读出液体的体积
4.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性 B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质 D.固体氢氧化钠能吸收水蒸气而潮解
5.下列实验基本操作不正确的是( )
A.稀释浓硫酸
B.溶解氯化钠
C.滴加酚酞溶液
D.加热水
6.下列变化中,与其他三种变化有本质区别的是( )
A.浓盐酸敞口放置在空气中质量减少
B.抹在墙壁上的石灰浆逐渐变硬
C.生石灰溶于水成熟石灰
D.NaOH溶液遇酚酞变红色
7.下列说法正确的是
A.不同种元素最本质的区别是相对原子质量的不同
B.空气质量指数级别越高,空气质量越差
C.饱和澄清石灰水变浑浊一定是发生了化学变化
D.敞口放置一段时间的浓盐酸和浓硫酸,溶质的质量分数和溶液的质量都会减小
8.下列对实验现象的描述错误的是( )
A.硫在氧气中燃烧产生淡蓝色的火焰,生成有刺激性气味的气体
B.将二氧化碳通入紫色石蕊试液中,溶液变红
C.打开盛有浓盐酸的试剂瓶,瓶口产生大量白雾
D.镁和稀盐酸反应产生大量气泡,放出热量
9.下列变化属于化学变化的是
A.分离液态空气制氧气 B.食品久置发生霉变
C.活性炭吸附除异味 D.浓盐酸敞口产生大量白雾
10.下列物质露置于空气中,因发生化学变化而使质量增加的是
A.浓硫酸 B.烧碱溶液 C.浓盐酸 D.双氧水溶液
11.下列说法不正确的是( )
A.稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水里,并不断搅拌
B.一定温度下,某固态物质的饱和溶液一定不能再溶解其他物质
C.洗涤剂去除油污利用了洗涤剂的乳化功能
D.打开汽水瓶盖时,汽水会自动喷出来,这说明气体在水中的溶解度与压强有关
12.如图中所有物质的类别均不同,连线两端的物质常温下均能反应。下列说法正确的是
A.X、Y、Z分别属于碱、盐、酸
B.X和Z可以是Al2O3和CaCl2
C.Y和Z可以是Na2CO3和Ca(OH)2
D.X和Y可以是NaCl和NaOH
13.下列说法正确的是
①酸和碱中都含氢元素,所以含氢元素的化合物一定是酸或碱
②我们把pH小于5.6的降雨称为酸雨
③书写化学方程式时,生成物中有气体生成就必须注明“↑”符号
④红热的铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体物质
⑤燃烧都伴随有发光、放热现象,有发光、放热现象的变化一定是燃烧
⑥分子原子都是不显电性的粒子,不显电性的粒子不一定是分子或原子
⑦现有Al、Cu、Ag三种金属,只用CuSO4溶液不能确定其金属活动性顺序
A.①③⑦ B.①②⑥ C.③④⑤ D.②④⑥
14.下列有关氢氧化钠的说法,错误的是( )
A.氢氧化钠俗称烧碱
B.氢氧化钠有强烈的腐蚀性
C.氢氧化钠固体可用于干燥二氧化碳气体
D.氢氧化钠可用于制肥皂、洗涤剂、造纸、纺织工业等
15.盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是
A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀
16.NaOH可用于造纸和印染工业,NaOH属于
A.单质 B.酸 C.碱 D.盐
二、综合应用题
17.实验是科学探究的重要途径。
(1)结合下列化学实验装置,回答有关问题。
①写出一个用A装置制取O2的化学方程式_____。
②若用B装置制取能使澄清的石灰水变浑浊的气体,则实验室制取该气体的化学方程式是__。与B相比较,C的主要优点是什么______。
③用试管采用排空气法收集氢气,请在D方框中画出装置图(只画试管和导气管)______。
(2)用实验室存放的氢氧化钠溶液做中和反应实验,发现有气泡产生。于是红红判断氢氧化钠变质了。请用化学方程式说明氢氧化钠变质的原因______。
为探究氢氧化钠是否完全变质,红红设计了两个实验方案。
方案1:取少量上述氢氧化钠溶液样品,滴加几滴酚酞溶液,溶液变成红色
方案2:取少量上述氢氧化钠溶液样品,加入饱和石灰水,静置,取上层清液,滴加几滴酚酞溶液。发现溶红色。于是明明认为样品中还会有氢氧化钠,没有完全变质。
①康康认为红红的两个实验方案都不能达到目的,他的理由是____。
②请你设计一个方案来验证氢氧化钠是否完全变质。______。
(3)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。请计算废水中氯化氢的质量分数__。
18.家庭厨房就是一个化学小世界,包含着许多的化学知识。请回答问题。
一、厨房里离不开水。
(1)下图中用“●”表示氧原子,用“〇”表示氢原子。下列选项中可以表示水分子的是______(填字母序号,下同)
(2)用下图装置将水通电一段时间后能产生气体,则此时发生反应的化学方程式为______。厨房中烧水也可以将水变成气体,请从微观角度解释这两种变化的本质区别。______
(3)下列能证明水是由氧元素和氢元素组成的实验是______
A 水的净化
B 水的蒸发
C 氢气在氧气中燃烧生成水
二、下列厨房用品所用的主要材料中,属于金属材料的是_____ (填字母序号,下同),其中利用金属导热性的是______ 。
三、厨房里离不开燃料,燃料燃烧产生热量为我们所用。
(1) 化石燃料是当前人类的主要燃料,包括煤、______和天然气。
(2) 写出天然气燃烧的化学方程式。______
(3)化石能源是有限的,我们在合理利用的同时,要努力开发新能源。请写出一种你所知道的新能源_______。
(4) 炒菜时,油锅着火,盖上锅盖即可灭火,原因是______。
四、下表列出了两种家用清洁剂的功能、有效成分和注意事项。
名称 洁厕灵 漂白精
功能 有效清除污垢,除异味 快速漂除衣物污渍
有效成分 HC1 NaCIO
注意事项 勿用于铁、铝等金属制品清洁 勿与酸性制品或其他清洁产品混合使用
据表回答下列问题:
(1) “洁厕灵”勿用于铁制品清洁的理由是 ______ (用化学方程式表示)。
(2)“洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为NaClO + 2HC1 = NaCl + X个+ H2O,则X的化学式为______ ;NaC1O中氯元素的化合价为______ 。
19.在化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂,为了确定其成分,同学们进行了如下的探究活动:
【查阅资料】
Ⅰ.石灰干燥剂的有效成分为生石灰(CaO)
Ⅱ.Ca(OH)2是一种微溶于水的白色固体,其水溶液(俗称石灰水)具有如下性质:能使无色酚酞(一种化学指示剂)溶液变红,与CO2气体反应出现浑浊,能与盐酸反应但无明显现象。
【方案设计】
小组成员设计了如下实验方案以期得到相应推论:取样滴加稀盐酸,有气泡产生,则白色固体为CaCO3;若无气泡产生,则白色固体为Ca(OH)2
(1)请简要说明上述方案中不合理之处:___________。
(2)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你设计一种实验方案予以证明。
实验步骤 实验现象 结论
______________ _____________ 含CaCO3
______________ _____________ 含Ca(OH)2
【数据分析】
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学向10克样品中加入足量的稀盐酸,测得CO2气体的质量如图所示。
(3)根据题给信息猜想一下,实验开始时的一段时间没有CO2气体产生的原因是_______;计算该混合物中CaCO3的质量分数_____________(请写出过程)。
【反思与评价】
实验中,如有部分二氧化碳气体因溶解于水而没有全部逸出,则测得的混合物中CaCO3的质量分数________(填写“偏大”、 “偏小”或“不变”)。
20.实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,设计了实验,实验过程如下:
【实验一】取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是______________(用化学方程式表 示)。
【实验二】如图过程进行实验
通过实验二,能进一步推算出氢氧化钠变质的程度,请写出计算过程(反应的化学方程式是Na2CO3+CaC12=CaCO3↓+2NaC1)
【结论】该样品属于___________ (填“全部”、“部分”)变质。
【拓展】若要获得氢氧化钠溶液,应先取一定量的固体加入足量水中充分溶解,再加入___________,后进行_____。
21.化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)某化学兴趣小组的同学利用如图微型实验装置进行探究实验。
①写出一个双球管中可能反应的化学方程式___________。
②挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,由此可说明燃烧需要什么条件?___________。
③相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是___________。
(2)实验室可利用如图实验装置制取纯净、干燥的CO,然后用CO还原Fe2O3并检验气体产物。已知CO发生装置中的反应为:H2C2O4H2O+CO2↑+CO↑。
①A装置中能观察到什么现象?___________。
②写出B装置中反应的化学方程式:___________。
③要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接___________、___________接___________、___________接___________、___________接___________。
④从环保角度考虑,还需对以上装置进行改进,请简述改进措施___________。
(3)锌和盐酸(HCl)反应生成氢气和氯化锌。现实验室用13g锌与足量的盐酸反应,可制得氢气和氯化锌的质量各是多少?
22.如图所示,A~I是初中化学常见的物质,A的水溶液显碱性,D为大理石的主要成份,F为生活中最常见的调味剂,Y为红色固体,G与I组成元素相同,请根据图示回答下列问题(部分产物或反应条件省略):
⑴A的俗名为_____;
⑵反应③的化学方程式为_____;
⑶反应④的可能化学方程式为_____;
⑷Y属于是_____(选填“混合物”、“单质”或“氧化物”);
⑸某化学兴趣小组对①反应的废液过滤后的成份产生了兴趣.进行了实验探究:
【提出问题】将废液过滤后,滤液中的溶质含有哪些物质?
【猜想与假设】猜想I:滤液中的溶质只有氯化钙;
猜想Ⅱ:滤液中的溶质有_____
【进行实验】①甲小组的同学从下面A-E五种药品中选择合适的一种进行实验,证明了猜想Ⅱ是正确的。他们选择的药品不可能是_____。
A 紫色石蕊试液 B无色酚酞试液 C 锌粒 D 氧化铁粉末 E 氢氧化钠溶液
②乙小组选用一种钠盐溶液进行实验,也证明了猜想Ⅱ是确的,请完成下面的实验报告。
实验操作 实验现象 实验结论
取少量滤液于试管中,加入足量_____(填化学式)溶液,振荡。 _____ 猜想Ⅱ正确
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.D
4.B
5.B
6.A
7.B
8.A
9.B
10.B
11.B
12.C
13.D
14.C
15.B
16.C
17. 可以控制反应速度 方案1中,碳酸钠溶液也能使酚酞溶液变红,方案2中碳酸钠与氢氧化钙反应的生成物是氢氧化钠,也能使酚酞溶液变红 取少量上述氢氧化钠溶液样品,加入足量氯化钙溶液(或氯化钡溶液等),静置,取上层清液滴加几滴酚酞溶液,若溶液变成红色,则氢氧化钠没有完全变质;若溶液没有变成红色,则氢氧化钠全部变质 1.46%
18. C 2H2O2H2↑+O2↑ 水蒸发时分子本身不变,只是间隙发生变化,水电解时分子变成了其它分子 C BD B 石油 CH4 +2O2CO2 +2H2O 风能 隔绝氧气 Fe+2HCl=H2↑+FeCl2 Cl2 +1
19. 若白色固体为CaCO3和Ca(OH)2的混合物,加入盐酸也有气泡产生 取少量样品向其中滴加稀盐酸 有气泡产生 另取少量样品加入适量的水溶解、静置,取上层清液通入CO2气体 溶液变浑浊 盐酸先与氢氧化钠反应,还未与碳酸钠反应 50% 偏小
20. 解:设样品中碳酸钠的质量为x。
x=10.6g
,
因为样品中碳酸钠的质量分数为70.67%,所以部分变质,故填部分变质。 适量氢氧化钙溶液 过滤
21.(1) 或 温度达到可燃物着火点 磷##P
(2) Ca(OH)2溶液变浑浊
h g e f c##d d##c a 在A装置后加一个燃着的酒精灯或在A装置后绑一个气球
(3)解:设生成氢气的质量为x,生成氯化锌的质量为y
x=0.4g
y=27.2g
答:可制得氢气的质量为0.4g,生成氯化锌的质量为27.2g
22. 纯碱 氧化物 氯化钙和氯化氢 BE 冒气泡,生成白色沉淀
答案第1页,共2页
答案第1页,共2页
