科粤版九年级化学下册8.5化学肥料同步练习(word版有答案)
文档属性
| 名称 | 科粤版九年级化学下册8.5化学肥料同步练习(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 159.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览




文档简介
科粤版九年级化学下册 8.5 化学肥料 同步练习
一、单选题
1.下列物质可用作氮肥的是
A.K2SO4 B.Ca3(PO4)2 C.NH4HCO3 D.NaCl
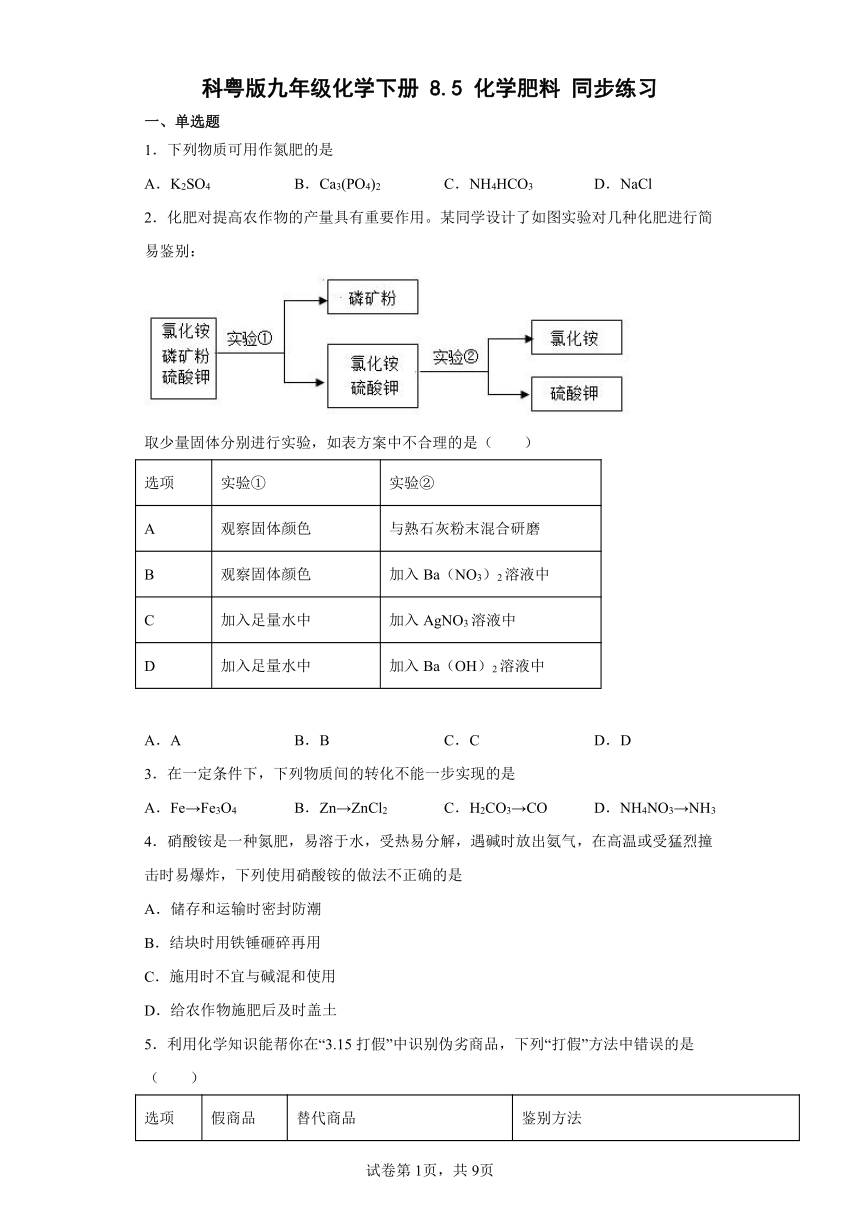
2.化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
选项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
A.A B.B C.C D.D
3.在一定条件下,下列物质间的转化不能一步实现的是
A.Fe→Fe3O4 B.Zn→ZnCl2 C.H2CO3→CO D.NH4NO3→NH3
4.硝酸铵是一种氮肥,易溶于水,受热易分解,遇碱时放出氨气,在高温或受猛烈撞击时易爆炸,下列使用硝酸铵的做法不正确的是
A.储存和运输时密封防潮
B.结块时用铁锤砸碎再用
C.施用时不宜与碱混和使用
D.给农作物施肥后及时盖土
5.利用化学知识能帮你在“3.15打假”中识别伪劣商品,下列“打假”方法中错误的是( )
选项 假商品 替代商品 鉴别方法
A 假化肥 用NH4Cl代替尿素[CO(NH2)2] 与氢氧化钠溶液混合后加热,闻气味
B 假黄金 用铜锌合金代替金首饰 放入稀盐酸中,观察是否有气泡冒出
C 假纯水 用自来水(含有Cl-)代替纯水 加硝酸银溶液,观察是否产生白色沉淀
D 假药 用BaCO3代替BaSO4做钡餐 加水观察两种钡盐是否溶解
A.A B.B C.C D.D
6.下列实验中无明显现象的是
A.向H2SO4溶液中滴加Ba(OH)2溶液
B.向Mg(NO3)2溶液中滴加Na2SO4溶液
C.将浓硫酸加入蒸馏水中并不断搅拌
D.将(NH4)2SO4和熟石灰混合研磨
7.下表用甲试剂鉴别乙中的两种化肥,难以实现的是
甲 乙 甲 乙
A Ca(OH)2 CO(NH2)2、NH4HCO3 B Ba(NO3)2 KCl、(NH4)2SO4
C AgNO3 NH4Cl、NH4NO3 D NaCl K2SO4、KNO3
A.A
B.B
C.C
D.D
8.今年我市部分地区的小麦得了“软骨病”,出现倒伏现象,为预防这种现象的发生,应提前施用的化肥是
A.NH4H2PO4 B.CO(NH2)2 C.K2CO3 D.NH4HCO3
9.下列肥料中,属于复合肥料的是
A.(NH4)2HPO4
B.CO(NH2)2
C.CaHPO4
D.KCl
10.小明家的甘蔗茎杆细弱,需要追施钾肥,应选择( )
A.KOH B.Ca3(PO4)2 C.K2CO3 D.CO(NH2)2
11.碳酸氢铵是白色固体,在生产生活中应用广泛。它稍微受热就能快速分解: 。下列有关叙述错误的是
A.碳酸氢铵要密封保存在阴凉干燥处
B.加热碳酸氢铵时,白色固体会逐渐消失
C.食品工业上常用碳酸氢铵作膨松剂
D.碳酸氢铵与草木灰混合施用能提高肥效
12.小美发现荔枝园旁边的水稻叶子发黄,并倒下了一片,你认为应该向稻田施用的复合肥是( )
A.CO(NH2)2 B.KCl C.Ca3(PO4)2 D.KNO3
13.某农用物资店的货架上待售的化肥有(NH4)2SO4、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是
A.氮肥
B.磷肥
C.钾肥
D.复合肥料
14.下列对化肥的认识不正确的是
A.KNO3是一种复合肥 B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用 D.化肥能提高粮食产量,施用越多越好
15.化肥碳酸氢铵具有以下性质:易溶于水,受潮时在常温下即能分解放出氨气,温度越高分解越快,遇碱性物质时也会放出氨气。该花费在运输、贮存和施用中做法错误的是
A.运输时注意密封 B.贮存时不能受潮或暴晒
C.与草木灰混合施用 D.施用后立即盖上
16.硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
二、综合应用题
17.我国拥有地球上7%的耕地,但化肥使用量却占全球总量的35%,认识化肥,科学施肥至关重要.
(1)下列物质中,可用作磷肥的是_______________:
A.K2SO4 B.CO(NH2)2 C.KNO3 D.Ca(H2PO4)
(2)NH4Cl是常见的氮肥,不能与碱性物质混用,否则会因释放出________而损失肥效;
(3)过度使用化肥造成的后果有:①____________________;②水体富营养化等;
(4)“雷雨发庄稼”现象涉及的化学反应较为复杂,其中一个反应是NO3与H2O反应生成HNO2和NO,写出该反应的化学方程式:__________________________;该反应中.化合价发生改变的元素是________(填元素符号).
18.(1)下列关于酸、碱、盐的生产或应用中的说法合理的是_________。
A将氯化铵与草木灰混合施用
B用小苏打治疗胃酸过多
C烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
D高温煅烧生石灰可以得到熟石灰
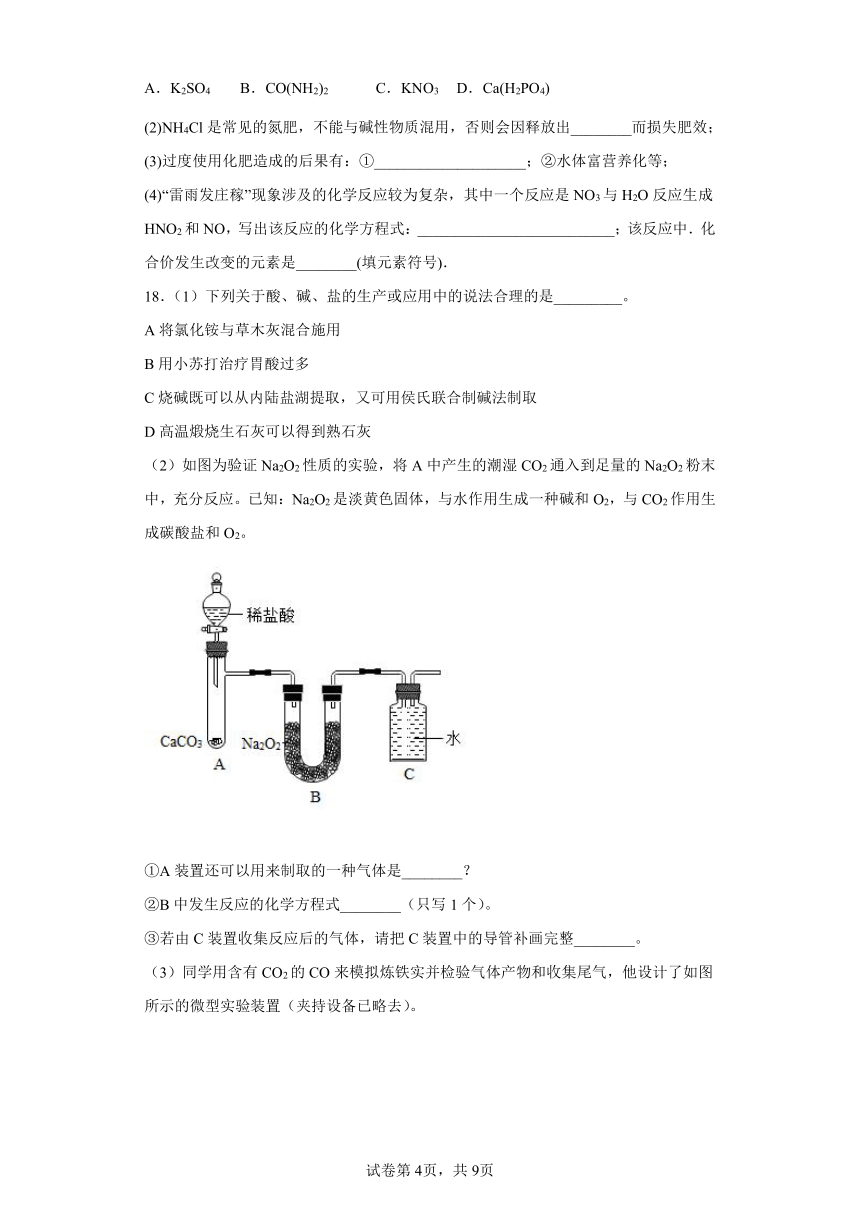
(2)如图为验证Na2O2性质的实验,将A中产生的潮湿CO2通入到足量的Na2O2粉末中,充分反应。已知:Na2O2是淡黄色固体,与水作用生成一种碱和O2,与CO2作用生成碳酸盐和O2。
①A装置还可以用来制取的一种气体是________?
②B中发生反应的化学方程式________(只写1个)。
③若由C装置收集反应后的气体,请把C装置中的导管补画完整________。
(3)同学用含有CO2的CO来模拟炼铁实并检验气体产物和收集尾气,他设计了如图所示的微型实验装置(夹持设备已略去)。
①装置A的作用是什么________?
②写出B处玻璃管中发生反应的化学方程________。
③实验结束后,D中有部分溶液进入E处量筒中,请设计实验方案,确定该溶液中含有哪些溶质________?(写出实验步骤、现象和结论)
(4)某小组按下图实验进行操作,计算E装置中Na2CO3的质量分数________。
19.普通干电池在生活中的用途很广。
(1)普通干电池照明时化学能转化为____。
(2)目前,废旧电池对环境的污染已越来越引起人们的重视。为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术。如图为普通电池(锌锰电池)示意图,请你根据图示分析:将回收的废旧电池进行分离,可以得到的金属单质有(用化学式表示,下同)____,氧化物有___,盐有____,有机物有__(写名称)。
(3)小明同学想得到⑤中纯净干燥的二氧化锰和氯化铵溶液,并检验氯化铵中的铵根离子。设计了如下实验步骤,请你帮他完成。
实验步骤 实验现象 结论或解释
①剥开干电池,取出碳棒周围的黑色粉末
②溶解、___(填操作名称)、洗涤 得到黑色粉末和无色澄清液体 黑色粉末的成分为__。
③对黑色粉末进行__ 得到纯净的MnO2固体
④检验第②步中得到的无色澄清液体中是否含铵根离子的方法是:_____ _____ 化学方程式为:______
(4)对分离回收的铜帽净化处理,放入硝酸银溶液中,一段时间以后,可观察到的现象是__,反应的化学方程式是_____,其基本反应类型为___反应。
20.空气是人类最宝贵的自然资源。空气中氮气的含量最多,氮气在高温、高压条件下可与某些物质发生反应,图1是以空气和其他必要的原料合成碳酸氢铵(NH4HCO3)的流程.请按要求回答下列问题:
(1)步骤①中可利用氮气和氧气的__________不同分离出氮气和氧气。
(2)写出步骤②中发生反应的化学方程式是_______。
(3)图2是化肥碳酸氢铵包装袋上的部分说明,碳酸氢铵具有的性质是____(填字母)。
A 易溶于水 B 有挥发性 C 受热易分解
(4)这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少 带着这些问题,兴趣小组的同学取了一些化肥样品,进入实验室。
【查找资料】①碱石灰能够吸收水和二氧化碳,但是不吸收氨气。②浓硫酸能吸收氨气
【性质探究】兴趣小组的同学设计了如下的实验装置:
①用A装置给碳酸氢铵加热,装药品前,必进行的一步作是______,加热,E中的现象是_____。
③连接A、B装置,继续加热,观察到试管口的现象是____,B中发生反应的化学方程式是___。
【含量分析】将装置A、C、D依次连接,加入20g化肥样品,加热至A中固体完全消失。兴趣小组的同学称量装置D的质量如表:
实验前D装置的质量 149g
实验后D装置的质量 152.4g
④由此分析得知:反应中产生氨气的质量为_____g。
⑤通过反应的化学方程式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮元素质量分数为_____。
⑥纯净的碳酸氢铵中氮元素质量分数为______(小数点后面保留1位)。
⑦31.6克碳酸氢铵和_____克的硝酸铵(NH4NO3)含氮元素质量相等。
21.化学竞赛周之前小胖想对所学知识进行总结,请你和他一起完成如下总结:
A.工业炼铁
(1)工业炼铁是利用一氧化碳将铁矿石中的铁还原出来,如下图是实验室模拟炼铁原理。实验过程中可以观察到的现象是:__________,硬质玻璃管中发生的化学反应方程式是_________________。小胖说应该在酒精灯上加一个灯罩,酒精灯罩的作用是_______________。
(2)实验过程中应该先______________(填“点燃酒精灯”或“通入CO”),其目的是 ______________。实验结束后,小胖说应该先关闭硬质玻璃管和澄清石灰水之间的止水夹,否则石灰水倒吸使试管炸裂,小华觉得他分析的不正确,其理由是______________________________。
(3)从环保的角度来分析,该装置存在的不足是____________,应做出的改进是______________。
(4)实验完成后,发现过量的澄清石灰水增重4.4g,则通入装置的CO气体质量肯定大于_______g,其理由是________________________________________________________ 。
B.侯氏制碱法
我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:
(1)请写出食盐水、氨气、二氧化碳反应的化学方程式______________。 分析下表,反应后能得到碳酸氢钠的晶体的原因是________________________________________。
物质 氯化钠 氯化铵 碳酸氢钠 碳酸氢铵
溶解度(20℃) 36g 37.2g 8.5g 29.8g
(2)写出反应I的化学方程式 ___________________________;该反应的基本类型为 __________。
(3)操作a的过程是蒸发浓缩、___________ 、过滤、干燥。
(4)老师告诉小胖在通二氧化碳的时候最好采用加压的方法,小胖百思不得其解,你觉得这样做的 目的是:___________________。
(5)上述工艺流程中可循环利用的物质是______________ 。得到的氯化铵可以用作_____________。
22.酸、碱、盐是九年级化学学习的重要知识,并且它们具有广泛的用途。
(1)下列关于酸、碱、盐的生产或应用中的说法合理的是( )
A 将氯化铵与草木灰混合施用
B 烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
C 用小苏打治疗胃酸过多
D 高温煅烧生石灰可以得到熟石灰
(2)随着新能源汽车的发展,动力电池领域对氢氧化锂的需求量越来越大。氢氧化锂(LiOH)与氢氧化钠化学性质相似,其原因是溶液中都有_______(填离子符号)。
(3)盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式_______。
(4)粗盐中含有泥沙、MgCl2、CaCl2、Na2SO4等杂质,为了得到纯净的氯化钠,化学兴趣小组设计如下实验:
Ⅰ.在操作①、操作②、操作③中都会用到同一种玻璃仪器,该仪器在操作③中的作用是什么?____
Ⅱ.写出一个加入Na2CO3溶液时所发生反应的化学方程式_______。
Ⅲ.上述流程中若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含有哪些杂质?_____(BaSO4不溶于水也不溶于酸)。
Ⅳ.如何判断加入盐酸达到适量_____。
(5)10g碳酸钙与100g稀盐酸恰好完全反应,生成4.4g二氧化碳,则反应所得氯化钙溶液的溶质质量分数为______(准确到0.1%)?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.B
5.D
6.B
7.D
8.C
9.A
10.C
11.D
12.D
13.C
14.D
15.C
16.A
17. D 氨气(或NH3) 土壤污染(或大气污染,土壤退化等) 3NO2+H2O=== 2HNO3+NO N
18. B H2 吸收二氧化碳气体 取少量溶液于试管中,滴加足量氯化钡(或氯化钙)溶液,静置,再向上层清液中滴加酚酞溶液,若无沉淀产生,溶液变红,说明溶质为氢氧化钠;若有白色沉淀产生,溶液变红,说明溶质为碳酸钠和氢氧化钠;若有白色沉淀产生,溶液不变红,说明溶质为碳酸钠 21.2%
19. 电能 Cu、Zn MnO2 NH4Cl、ZnCl2 淀粉 过滤 二氧化锰和炭粉 灼烧(或暴露在空气中加强热) 取样于试管中,加入氢氧化钠溶液并加热,把湿润的红色石蕊试纸放在试管口 产生强烈刺激性气味气体,湿润的红色石蕊试纸变蓝色 NH4Cl+NaOHNaCl+H2O+NH3↑ 铜表面有银白色固体析出,溶液由无色变为蓝色 Cu+2AgNO3=2Ag+Cu(NO3)2 置换
20. 沸点 AC 检查装置气密性 酚酞溶液变红 有水珠出现 3.4 14% 17.7% 16
21. 红色粉末逐渐变黑,澄清石灰水变浑浊 3CO+Fe2O3 2Fe +3CO2 集中火焰,提高温度 通入CO 排尽空气,防止加热时发生爆炸 实验结束会一直通一氧化碳至装置冷却,石灰水不会倒吸 未处理尾气,污染空气 在石灰水后用酒精灯点燃尾气或用气球收集尾气 2.8 部分一氧化碳没有参加反应 NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl 20℃时碳酸氢钠的溶解度最小,先饱和析出固体 2NaHCO3Na2CO3+CO2↑+H2O↑ 分解反应 冷却结晶 压强增大,二氧化碳气体溶解度增大 CO2和H2O 氮肥
22. C OH- 搅拌,防止因局部温度过高造成液滴飞溅 (或) 氯化钙、氯化钡、氯化镁 当不再有气泡出时停止滴加稀盐酸 解:设反应后生成氯化钙质量为x
x=11.1g
答:滤液中氯化钙的质量分数是10.5%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质可用作氮肥的是
A.K2SO4 B.Ca3(PO4)2 C.NH4HCO3 D.NaCl
2.化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
选项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
A.A B.B C.C D.D
3.在一定条件下,下列物质间的转化不能一步实现的是
A.Fe→Fe3O4 B.Zn→ZnCl2 C.H2CO3→CO D.NH4NO3→NH3
4.硝酸铵是一种氮肥,易溶于水,受热易分解,遇碱时放出氨气,在高温或受猛烈撞击时易爆炸,下列使用硝酸铵的做法不正确的是
A.储存和运输时密封防潮
B.结块时用铁锤砸碎再用
C.施用时不宜与碱混和使用
D.给农作物施肥后及时盖土
5.利用化学知识能帮你在“3.15打假”中识别伪劣商品,下列“打假”方法中错误的是( )
选项 假商品 替代商品 鉴别方法
A 假化肥 用NH4Cl代替尿素[CO(NH2)2] 与氢氧化钠溶液混合后加热,闻气味
B 假黄金 用铜锌合金代替金首饰 放入稀盐酸中,观察是否有气泡冒出
C 假纯水 用自来水(含有Cl-)代替纯水 加硝酸银溶液,观察是否产生白色沉淀
D 假药 用BaCO3代替BaSO4做钡餐 加水观察两种钡盐是否溶解
A.A B.B C.C D.D
6.下列实验中无明显现象的是
A.向H2SO4溶液中滴加Ba(OH)2溶液
B.向Mg(NO3)2溶液中滴加Na2SO4溶液
C.将浓硫酸加入蒸馏水中并不断搅拌
D.将(NH4)2SO4和熟石灰混合研磨
7.下表用甲试剂鉴别乙中的两种化肥,难以实现的是
甲 乙 甲 乙
A Ca(OH)2 CO(NH2)2、NH4HCO3 B Ba(NO3)2 KCl、(NH4)2SO4
C AgNO3 NH4Cl、NH4NO3 D NaCl K2SO4、KNO3
A.A
B.B
C.C
D.D
8.今年我市部分地区的小麦得了“软骨病”,出现倒伏现象,为预防这种现象的发生,应提前施用的化肥是
A.NH4H2PO4 B.CO(NH2)2 C.K2CO3 D.NH4HCO3
9.下列肥料中,属于复合肥料的是
A.(NH4)2HPO4
B.CO(NH2)2
C.CaHPO4
D.KCl
10.小明家的甘蔗茎杆细弱,需要追施钾肥,应选择( )
A.KOH B.Ca3(PO4)2 C.K2CO3 D.CO(NH2)2
11.碳酸氢铵是白色固体,在生产生活中应用广泛。它稍微受热就能快速分解: 。下列有关叙述错误的是
A.碳酸氢铵要密封保存在阴凉干燥处
B.加热碳酸氢铵时,白色固体会逐渐消失
C.食品工业上常用碳酸氢铵作膨松剂
D.碳酸氢铵与草木灰混合施用能提高肥效
12.小美发现荔枝园旁边的水稻叶子发黄,并倒下了一片,你认为应该向稻田施用的复合肥是( )
A.CO(NH2)2 B.KCl C.Ca3(PO4)2 D.KNO3
13.某农用物资店的货架上待售的化肥有(NH4)2SO4、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是
A.氮肥
B.磷肥
C.钾肥
D.复合肥料
14.下列对化肥的认识不正确的是
A.KNO3是一种复合肥 B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用 D.化肥能提高粮食产量,施用越多越好
15.化肥碳酸氢铵具有以下性质:易溶于水,受潮时在常温下即能分解放出氨气,温度越高分解越快,遇碱性物质时也会放出氨气。该花费在运输、贮存和施用中做法错误的是
A.运输时注意密封 B.贮存时不能受潮或暴晒
C.与草木灰混合施用 D.施用后立即盖上
16.硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
二、综合应用题
17.我国拥有地球上7%的耕地,但化肥使用量却占全球总量的35%,认识化肥,科学施肥至关重要.
(1)下列物质中,可用作磷肥的是_______________:
A.K2SO4 B.CO(NH2)2 C.KNO3 D.Ca(H2PO4)
(2)NH4Cl是常见的氮肥,不能与碱性物质混用,否则会因释放出________而损失肥效;
(3)过度使用化肥造成的后果有:①____________________;②水体富营养化等;
(4)“雷雨发庄稼”现象涉及的化学反应较为复杂,其中一个反应是NO3与H2O反应生成HNO2和NO,写出该反应的化学方程式:__________________________;该反应中.化合价发生改变的元素是________(填元素符号).
18.(1)下列关于酸、碱、盐的生产或应用中的说法合理的是_________。
A将氯化铵与草木灰混合施用
B用小苏打治疗胃酸过多
C烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
D高温煅烧生石灰可以得到熟石灰
(2)如图为验证Na2O2性质的实验,将A中产生的潮湿CO2通入到足量的Na2O2粉末中,充分反应。已知:Na2O2是淡黄色固体,与水作用生成一种碱和O2,与CO2作用生成碳酸盐和O2。
①A装置还可以用来制取的一种气体是________?
②B中发生反应的化学方程式________(只写1个)。
③若由C装置收集反应后的气体,请把C装置中的导管补画完整________。
(3)同学用含有CO2的CO来模拟炼铁实并检验气体产物和收集尾气,他设计了如图所示的微型实验装置(夹持设备已略去)。
①装置A的作用是什么________?
②写出B处玻璃管中发生反应的化学方程________。
③实验结束后,D中有部分溶液进入E处量筒中,请设计实验方案,确定该溶液中含有哪些溶质________?(写出实验步骤、现象和结论)
(4)某小组按下图实验进行操作,计算E装置中Na2CO3的质量分数________。
19.普通干电池在生活中的用途很广。
(1)普通干电池照明时化学能转化为____。
(2)目前,废旧电池对环境的污染已越来越引起人们的重视。为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术。如图为普通电池(锌锰电池)示意图,请你根据图示分析:将回收的废旧电池进行分离,可以得到的金属单质有(用化学式表示,下同)____,氧化物有___,盐有____,有机物有__(写名称)。
(3)小明同学想得到⑤中纯净干燥的二氧化锰和氯化铵溶液,并检验氯化铵中的铵根离子。设计了如下实验步骤,请你帮他完成。
实验步骤 实验现象 结论或解释
①剥开干电池,取出碳棒周围的黑色粉末
②溶解、___(填操作名称)、洗涤 得到黑色粉末和无色澄清液体 黑色粉末的成分为__。
③对黑色粉末进行__ 得到纯净的MnO2固体
④检验第②步中得到的无色澄清液体中是否含铵根离子的方法是:_____ _____ 化学方程式为:______
(4)对分离回收的铜帽净化处理,放入硝酸银溶液中,一段时间以后,可观察到的现象是__,反应的化学方程式是_____,其基本反应类型为___反应。
20.空气是人类最宝贵的自然资源。空气中氮气的含量最多,氮气在高温、高压条件下可与某些物质发生反应,图1是以空气和其他必要的原料合成碳酸氢铵(NH4HCO3)的流程.请按要求回答下列问题:
(1)步骤①中可利用氮气和氧气的__________不同分离出氮气和氧气。
(2)写出步骤②中发生反应的化学方程式是_______。
(3)图2是化肥碳酸氢铵包装袋上的部分说明,碳酸氢铵具有的性质是____(填字母)。
A 易溶于水 B 有挥发性 C 受热易分解
(4)这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少 带着这些问题,兴趣小组的同学取了一些化肥样品,进入实验室。
【查找资料】①碱石灰能够吸收水和二氧化碳,但是不吸收氨气。②浓硫酸能吸收氨气
【性质探究】兴趣小组的同学设计了如下的实验装置:
①用A装置给碳酸氢铵加热,装药品前,必进行的一步作是______,加热,E中的现象是_____。
③连接A、B装置,继续加热,观察到试管口的现象是____,B中发生反应的化学方程式是___。
【含量分析】将装置A、C、D依次连接,加入20g化肥样品,加热至A中固体完全消失。兴趣小组的同学称量装置D的质量如表:
实验前D装置的质量 149g
实验后D装置的质量 152.4g
④由此分析得知:反应中产生氨气的质量为_____g。
⑤通过反应的化学方程式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮元素质量分数为_____。
⑥纯净的碳酸氢铵中氮元素质量分数为______(小数点后面保留1位)。
⑦31.6克碳酸氢铵和_____克的硝酸铵(NH4NO3)含氮元素质量相等。
21.化学竞赛周之前小胖想对所学知识进行总结,请你和他一起完成如下总结:
A.工业炼铁
(1)工业炼铁是利用一氧化碳将铁矿石中的铁还原出来,如下图是实验室模拟炼铁原理。实验过程中可以观察到的现象是:__________,硬质玻璃管中发生的化学反应方程式是_________________。小胖说应该在酒精灯上加一个灯罩,酒精灯罩的作用是_______________。
(2)实验过程中应该先______________(填“点燃酒精灯”或“通入CO”),其目的是 ______________。实验结束后,小胖说应该先关闭硬质玻璃管和澄清石灰水之间的止水夹,否则石灰水倒吸使试管炸裂,小华觉得他分析的不正确,其理由是______________________________。
(3)从环保的角度来分析,该装置存在的不足是____________,应做出的改进是______________。
(4)实验完成后,发现过量的澄清石灰水增重4.4g,则通入装置的CO气体质量肯定大于_______g,其理由是________________________________________________________ 。
B.侯氏制碱法
我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:
(1)请写出食盐水、氨气、二氧化碳反应的化学方程式______________。 分析下表,反应后能得到碳酸氢钠的晶体的原因是________________________________________。
物质 氯化钠 氯化铵 碳酸氢钠 碳酸氢铵
溶解度(20℃) 36g 37.2g 8.5g 29.8g
(2)写出反应I的化学方程式 ___________________________;该反应的基本类型为 __________。
(3)操作a的过程是蒸发浓缩、___________ 、过滤、干燥。
(4)老师告诉小胖在通二氧化碳的时候最好采用加压的方法,小胖百思不得其解,你觉得这样做的 目的是:___________________。
(5)上述工艺流程中可循环利用的物质是______________ 。得到的氯化铵可以用作_____________。
22.酸、碱、盐是九年级化学学习的重要知识,并且它们具有广泛的用途。
(1)下列关于酸、碱、盐的生产或应用中的说法合理的是( )
A 将氯化铵与草木灰混合施用
B 烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
C 用小苏打治疗胃酸过多
D 高温煅烧生石灰可以得到熟石灰
(2)随着新能源汽车的发展,动力电池领域对氢氧化锂的需求量越来越大。氢氧化锂(LiOH)与氢氧化钠化学性质相似,其原因是溶液中都有_______(填离子符号)。
(3)盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式_______。
(4)粗盐中含有泥沙、MgCl2、CaCl2、Na2SO4等杂质,为了得到纯净的氯化钠,化学兴趣小组设计如下实验:
Ⅰ.在操作①、操作②、操作③中都会用到同一种玻璃仪器,该仪器在操作③中的作用是什么?____
Ⅱ.写出一个加入Na2CO3溶液时所发生反应的化学方程式_______。
Ⅲ.上述流程中若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含有哪些杂质?_____(BaSO4不溶于水也不溶于酸)。
Ⅳ.如何判断加入盐酸达到适量_____。
(5)10g碳酸钙与100g稀盐酸恰好完全反应,生成4.4g二氧化碳,则反应所得氯化钙溶液的溶质质量分数为______(准确到0.1%)?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.B
5.D
6.B
7.D
8.C
9.A
10.C
11.D
12.D
13.C
14.D
15.C
16.A
17. D 氨气(或NH3) 土壤污染(或大气污染,土壤退化等) 3NO2+H2O=== 2HNO3+NO N
18. B H2 吸收二氧化碳气体 取少量溶液于试管中,滴加足量氯化钡(或氯化钙)溶液,静置,再向上层清液中滴加酚酞溶液,若无沉淀产生,溶液变红,说明溶质为氢氧化钠;若有白色沉淀产生,溶液变红,说明溶质为碳酸钠和氢氧化钠;若有白色沉淀产生,溶液不变红,说明溶质为碳酸钠 21.2%
19. 电能 Cu、Zn MnO2 NH4Cl、ZnCl2 淀粉 过滤 二氧化锰和炭粉 灼烧(或暴露在空气中加强热) 取样于试管中,加入氢氧化钠溶液并加热,把湿润的红色石蕊试纸放在试管口 产生强烈刺激性气味气体,湿润的红色石蕊试纸变蓝色 NH4Cl+NaOHNaCl+H2O+NH3↑ 铜表面有银白色固体析出,溶液由无色变为蓝色 Cu+2AgNO3=2Ag+Cu(NO3)2 置换
20. 沸点 AC 检查装置气密性 酚酞溶液变红 有水珠出现 3.4 14% 17.7% 16
21. 红色粉末逐渐变黑,澄清石灰水变浑浊 3CO+Fe2O3 2Fe +3CO2 集中火焰,提高温度 通入CO 排尽空气,防止加热时发生爆炸 实验结束会一直通一氧化碳至装置冷却,石灰水不会倒吸 未处理尾气,污染空气 在石灰水后用酒精灯点燃尾气或用气球收集尾气 2.8 部分一氧化碳没有参加反应 NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl 20℃时碳酸氢钠的溶解度最小,先饱和析出固体 2NaHCO3Na2CO3+CO2↑+H2O↑ 分解反应 冷却结晶 压强增大,二氧化碳气体溶解度增大 CO2和H2O 氮肥
22. C OH- 搅拌,防止因局部温度过高造成液滴飞溅 (或) 氯化钙、氯化钡、氯化镁 当不再有气泡出时停止滴加稀盐酸 解:设反应后生成氯化钙质量为x
x=11.1g
答:滤液中氯化钙的质量分数是10.5%。
答案第1页,共2页
答案第1页,共2页
