九年级化学沪教版(上海)第二学期第六单元 常用的金属和盐章末练习题(word版有答案)
文档属性
| 名称 | 九年级化学沪教版(上海)第二学期第六单元 常用的金属和盐章末练习题(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 240.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 23:51:47 | ||
图片预览



文档简介
第6章常用的金属和盐章末练习题2021-2022学年九年级化学沪教版(上海)第二学期
一、单选题
1.下列金属活动性最强的是
A.Cu B.Zn C.Fe D.Mg
2.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是
A.NH4NO3 B.KNO3
C.Ca3(PO4)2 D.KCl
3.下列应用、对应的化学方程式及基本反应类型都正确的是
A.用一氧化碳还原氧化铁: 置换反应
B.用氢氧化钠溶液吸收二氧化碳: 复分解反应
C.用铁桶盛装农药波尔多液: 置换反应
D.用生石灰制熟石灰: 化合反应
4.如图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
A.开始时应先预热玻璃管,后通入一氧化碳
B.实验中玻璃管里粉末由黑色逐渐变成红棕色
C.参加反应的氧化铁和一氧化碳质量比为40:7
D.将尾气点燃或收集,可防止一氧化碳污染空气
5.饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,下列药剂不适宜的是
A.氢氧化铝 B.氯化钠 C.碳酸镁 D.碳酸氢钠
6.如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
7.将X、Z两种金属分别放入Y(NO3)2的溶液中,仅X的表面有Y单质析出,则X、Y、Z三种金属的活动性顺序是
A.Z>X>Y B.Y>Z>X C.X>Y>Z D.Y>X>Z
8.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 分离KCl和MnO2的固体混合物 加足量的水溶解,过滤
B 鉴别NaNO3和NH4HCO3两种氮肥 取样,闻气味
C 除去CO中的CO2 将混合气体通过红热的铜
D 探究铁钉生锈的条件 将两根铁钉分别密封在盛有干燥空气和盛满水的试管中一周并观察现象
A.A B.B C.C D.D
9.将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
10.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
A.紫色石蕊溶液 B.氯化钠溶液 C.铁粉 D.pH试纸
11.现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有
A.② B.②③ C.①②③ D.②③④
二、简答题
12.化学与人类生活密不可分。请用所学知识解释下列现象。
(1)用洗洁精可以除去餐具上的油污。
(2)铝的化学性质活泼,为什么铝制品却具有很好的抗腐蚀性能?(用化学方程式表示)。
13.怎样鉴别石灰水和氢氧化钠溶液?
14.解释下述现象。
(1)鸡蛋壳的主要成分是碳酸钙。将一个新鲜的鸡蛋放在盛有足量稀盐酸的玻璃杯中,可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
(2)馒头、面包等发面食品的一个特点是面团中有许多小孔(如图),它们使发面食品松软可口。根据发酵粉(含碳酸氢钠和有机酸等)可与面粉、水混合直接制作发面食品的事实,说明碳酸氢钠在其中的作用。
三、推断题
15.五个圆分别表示A(二氧化碳)、B(澄清石灰水)、C(稀硫酸)、D(铁)、E(碳酸钠溶液)五种物质(两圆相切表示两种物质可以发生反应),如图2所示。请回答下列问题:
(1)将B、C、D、E三种物质名称或化学式填入图2的4个圆中。
(2)写出B物质与E物质反应的现象_______。
(3)写出上述反应中有气泡生成的一个化学方程式_______。
(4)图2中的稀硫酸与各物质间的反应情况,可以体现出的酸的通性有:
①
②_______。
③_______。
16.A、B、C、D、E均含有同一种金属元素,它们之间的转化关系如右图所示(“→”表示反应可一步实现,部分物质和反应条件略去)。已知A为氧化物,其中金属元素显+3价,且其质量分数为70%;B为单质,E为难溶性碱;A→B是工业制取B的主要原理, A的化学式为______;D→E的化学方程式为______;C与B可发生化合反应生成D,该反应的化学方程式为______。
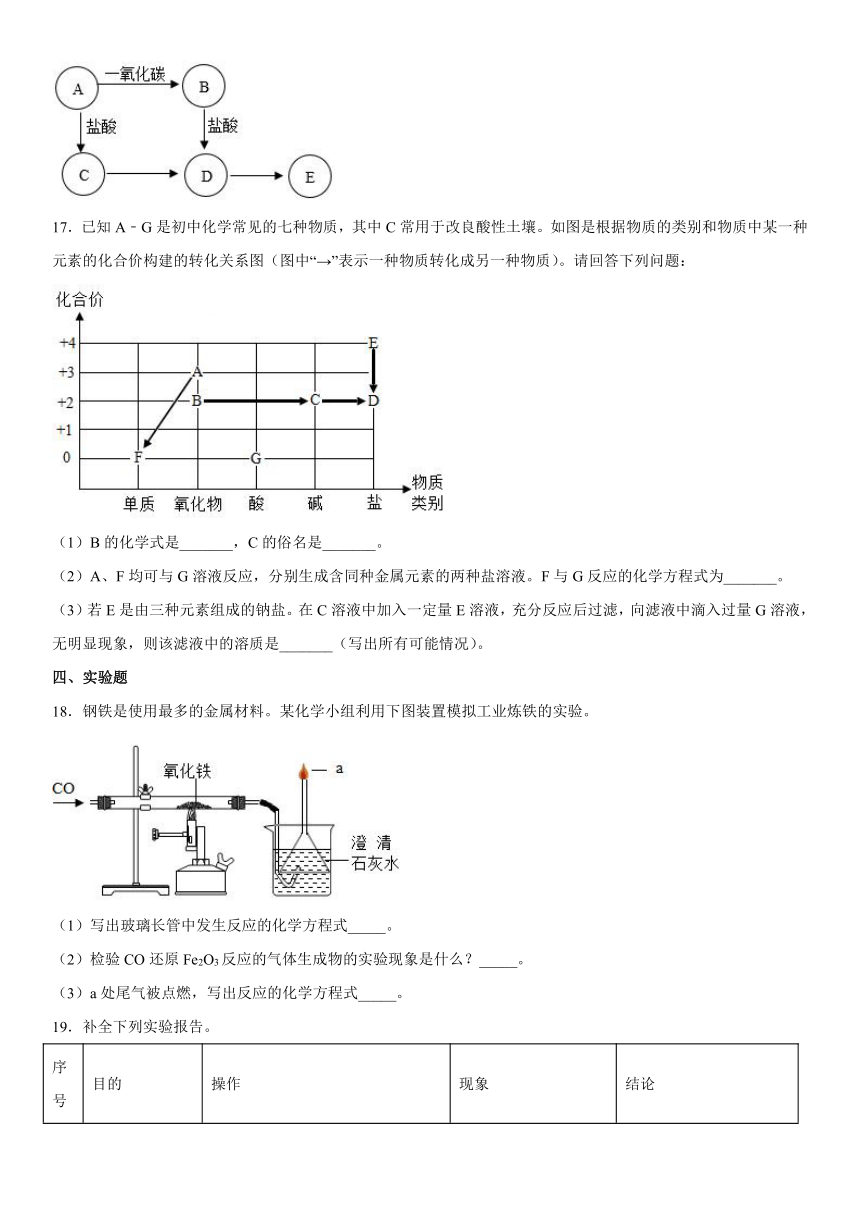
17.已知A﹣G是初中化学常见的七种物质,其中C常用于改良酸性土壤。如图是根据物质的类别和物质中某一种元素的化合价构建的转化关系图(图中“→”表示一种物质转化成另一种物质)。请回答下列问题:
(1)B的化学式是_______,C的俗名是_______。
(2)A、F均可与G溶液反应,分别生成含同种金属元素的两种盐溶液。F与G反应的化学方程式为_______。
(3)若E是由三种元素组成的钠盐。在C溶液中加入一定量E溶液,充分反应后过滤,向滤液中滴入过量G溶液,无明显现象,则该滤液中的溶质是_______(写出所有可能情况)。
四、实验题
18.钢铁是使用最多的金属材料。某化学小组利用下图装置模拟工业炼铁的实验。
(1)写出玻璃长管中发生反应的化学方程式_____。
(2)检验CO还原Fe2O3反应的气体生成物的实验现象是什么?_____。
(3)a处尾气被点燃,写出反应的化学方程式_____。
19.补全下列实验报告。
序号 目的 操作 现象 结论
(1) 验证NaCl不能无限溶解 ____ (已知:20℃时,NaC1的溶解度为36g) ①中固体完全溶解,②中固体未完全溶解 一定温度时,NaCl在一定量水中不能无限溶解
(2) 比较铁、铜的金属活动性 _______ 铁的金属活动性比铜强
(3) 测定空气中氧气含量 瓶中液面最终升至刻度1处 _______
(4) _______ 分别向集气瓶内伸入燃着的木条 右侧集气瓶中木条先熄灭 呼出气体中氧气含量比空气中的低
五、计算题
20.为测定实验室中某硫酸铜样品中硫酸铜的质量分数(所含杂质溶于水,但不参与反应),进行了图所示的实验。请计算:
(1)a=______。
(2)该样品中硫酸铜的质量分数。
21.某化学实验小组欲测定一块Cu-Zn合金中铜的质量分数,他们进行了以下实验。取该合金的粉末32.5g放入烧杯中,向烧杯内加入足量稀硫酸,测定反应过程中烧杯内的总质量随时间的变化,记录如下表:
时间/min t1 t2 t3 t4 t5 t6
烧杯内总质量减少/g 0.1 0.2 0.3 0.4 0.4 0.4
请计算:
(1)反应过程中生成氢气的质量是 g。
(2)该合金中铜的质量分数。
22.常见的化肥的①尿素〔CO(NH2)2〕、②硝酸钾(KNO3)、③碳酸氢铵(NH4HCO3)、④硫酸钾(K2SO4)、⑤磷酸二氢钾(KH2PO4)等。
(1)以上五种肥料中属于复合肥的是_______(填数字序号)。
(2)工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应方程式为: ;要合成 90 吨尿素,需要二氧化碳多少吨?
23.实验室用金属锌和稀硫酸制备氢气,若需要制备4.4g氢气,至少需要金属锌多少克?
参考答案:
1.D
2.B
3.D
4.D
5.B
6.B
7.C
8.B
9.B
10.B
11.B
12.(1)洗洁精具有乳化作用
(2)
13.取少量溶液于试管中,加入适量碳酸钠溶液,产生白色沉淀,则是石灰水,无明显现象,则是氢氧化钠溶液。
14.(1)鸡蛋壳主要成分是碳酸钙,会与盐酸反应产生二氧化碳气体,产生气泡,一开始鸡蛋的重力大于鸡蛋受到的浮力,鸡蛋下沉,随着蛋壳表面的气体越快越多,鸡蛋受到的浮力增大,浮力大于重力,鸡蛋上浮,当浮出液面一定程度时,气体逸出,鸡蛋的重力大于受到的浮力,鸡蛋又将下沉;
(2)碳酸氢钠受热能分解生成二氧化碳,碳酸氢钠也能与有机酸反应生成二氧化碳,可使面包等松软可口,且可除去发酵过程中产生的酸
15.(1)
(2)产生白色沉淀或浑浊
(3)或
(4)
16. Fe2O3
17. CaO 熟石灰、消石灰 Fe+2HCl=FeCl2+H2↑ NaOH和Ca(OH)2
18. 烧杯中澄清的石灰水变浑浊
19. 大于16g 铁丝表面有红色物质析出 氧气约占空气总体积的1/5 比较呼出气体和空气中氧气的含量
20.(1)10
(2)96%
解:由题意知,硫酸铜样品中所含杂质溶于水,所以滤渣的质量为氢氧化铜的质量,
设参加反应的硫酸铜质量为x,
样品中硫酸铜的质量分数为×100%=96%;
答:样品中硫酸铜的质量分数为96%。
21.(1)0.4
(2)解:设锌的质量为x,
x=13g
该合金中铜的质量分数为×100%=60%
答:该合金中铜的质量分数为60%。
22.(1)②⑤
(2)设要合成 90 吨尿素,需要二氧化碳的质量为x,
x=66t
答:要合成 90 吨尿素,需要二氧化碳的质量为66t。
23.143g
一、单选题
1.下列金属活动性最强的是
A.Cu B.Zn C.Fe D.Mg
2.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是
A.NH4NO3 B.KNO3
C.Ca3(PO4)2 D.KCl
3.下列应用、对应的化学方程式及基本反应类型都正确的是
A.用一氧化碳还原氧化铁: 置换反应
B.用氢氧化钠溶液吸收二氧化碳: 复分解反应
C.用铁桶盛装农药波尔多液: 置换反应
D.用生石灰制熟石灰: 化合反应
4.如图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
A.开始时应先预热玻璃管,后通入一氧化碳
B.实验中玻璃管里粉末由黑色逐渐变成红棕色
C.参加反应的氧化铁和一氧化碳质量比为40:7
D.将尾气点燃或收集,可防止一氧化碳污染空气
5.饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,下列药剂不适宜的是
A.氢氧化铝 B.氯化钠 C.碳酸镁 D.碳酸氢钠
6.如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
7.将X、Z两种金属分别放入Y(NO3)2的溶液中,仅X的表面有Y单质析出,则X、Y、Z三种金属的活动性顺序是
A.Z>X>Y B.Y>Z>X C.X>Y>Z D.Y>X>Z
8.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 分离KCl和MnO2的固体混合物 加足量的水溶解,过滤
B 鉴别NaNO3和NH4HCO3两种氮肥 取样,闻气味
C 除去CO中的CO2 将混合气体通过红热的铜
D 探究铁钉生锈的条件 将两根铁钉分别密封在盛有干燥空气和盛满水的试管中一周并观察现象
A.A B.B C.C D.D
9.将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
10.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
A.紫色石蕊溶液 B.氯化钠溶液 C.铁粉 D.pH试纸
11.现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有
A.② B.②③ C.①②③ D.②③④
二、简答题
12.化学与人类生活密不可分。请用所学知识解释下列现象。
(1)用洗洁精可以除去餐具上的油污。
(2)铝的化学性质活泼,为什么铝制品却具有很好的抗腐蚀性能?(用化学方程式表示)。
13.怎样鉴别石灰水和氢氧化钠溶液?
14.解释下述现象。
(1)鸡蛋壳的主要成分是碳酸钙。将一个新鲜的鸡蛋放在盛有足量稀盐酸的玻璃杯中,可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
(2)馒头、面包等发面食品的一个特点是面团中有许多小孔(如图),它们使发面食品松软可口。根据发酵粉(含碳酸氢钠和有机酸等)可与面粉、水混合直接制作发面食品的事实,说明碳酸氢钠在其中的作用。
三、推断题
15.五个圆分别表示A(二氧化碳)、B(澄清石灰水)、C(稀硫酸)、D(铁)、E(碳酸钠溶液)五种物质(两圆相切表示两种物质可以发生反应),如图2所示。请回答下列问题:
(1)将B、C、D、E三种物质名称或化学式填入图2的4个圆中。
(2)写出B物质与E物质反应的现象_______。
(3)写出上述反应中有气泡生成的一个化学方程式_______。
(4)图2中的稀硫酸与各物质间的反应情况,可以体现出的酸的通性有:
①
②_______。
③_______。
16.A、B、C、D、E均含有同一种金属元素,它们之间的转化关系如右图所示(“→”表示反应可一步实现,部分物质和反应条件略去)。已知A为氧化物,其中金属元素显+3价,且其质量分数为70%;B为单质,E为难溶性碱;A→B是工业制取B的主要原理, A的化学式为______;D→E的化学方程式为______;C与B可发生化合反应生成D,该反应的化学方程式为______。
17.已知A﹣G是初中化学常见的七种物质,其中C常用于改良酸性土壤。如图是根据物质的类别和物质中某一种元素的化合价构建的转化关系图(图中“→”表示一种物质转化成另一种物质)。请回答下列问题:
(1)B的化学式是_______,C的俗名是_______。
(2)A、F均可与G溶液反应,分别生成含同种金属元素的两种盐溶液。F与G反应的化学方程式为_______。
(3)若E是由三种元素组成的钠盐。在C溶液中加入一定量E溶液,充分反应后过滤,向滤液中滴入过量G溶液,无明显现象,则该滤液中的溶质是_______(写出所有可能情况)。
四、实验题
18.钢铁是使用最多的金属材料。某化学小组利用下图装置模拟工业炼铁的实验。
(1)写出玻璃长管中发生反应的化学方程式_____。
(2)检验CO还原Fe2O3反应的气体生成物的实验现象是什么?_____。
(3)a处尾气被点燃,写出反应的化学方程式_____。
19.补全下列实验报告。
序号 目的 操作 现象 结论
(1) 验证NaCl不能无限溶解 ____ (已知:20℃时,NaC1的溶解度为36g) ①中固体完全溶解,②中固体未完全溶解 一定温度时,NaCl在一定量水中不能无限溶解
(2) 比较铁、铜的金属活动性 _______ 铁的金属活动性比铜强
(3) 测定空气中氧气含量 瓶中液面最终升至刻度1处 _______
(4) _______ 分别向集气瓶内伸入燃着的木条 右侧集气瓶中木条先熄灭 呼出气体中氧气含量比空气中的低
五、计算题
20.为测定实验室中某硫酸铜样品中硫酸铜的质量分数(所含杂质溶于水,但不参与反应),进行了图所示的实验。请计算:
(1)a=______。
(2)该样品中硫酸铜的质量分数。
21.某化学实验小组欲测定一块Cu-Zn合金中铜的质量分数,他们进行了以下实验。取该合金的粉末32.5g放入烧杯中,向烧杯内加入足量稀硫酸,测定反应过程中烧杯内的总质量随时间的变化,记录如下表:
时间/min t1 t2 t3 t4 t5 t6
烧杯内总质量减少/g 0.1 0.2 0.3 0.4 0.4 0.4
请计算:
(1)反应过程中生成氢气的质量是 g。
(2)该合金中铜的质量分数。
22.常见的化肥的①尿素〔CO(NH2)2〕、②硝酸钾(KNO3)、③碳酸氢铵(NH4HCO3)、④硫酸钾(K2SO4)、⑤磷酸二氢钾(KH2PO4)等。
(1)以上五种肥料中属于复合肥的是_______(填数字序号)。
(2)工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应方程式为: ;要合成 90 吨尿素,需要二氧化碳多少吨?
23.实验室用金属锌和稀硫酸制备氢气,若需要制备4.4g氢气,至少需要金属锌多少克?
参考答案:
1.D
2.B
3.D
4.D
5.B
6.B
7.C
8.B
9.B
10.B
11.B
12.(1)洗洁精具有乳化作用
(2)
13.取少量溶液于试管中,加入适量碳酸钠溶液,产生白色沉淀,则是石灰水,无明显现象,则是氢氧化钠溶液。
14.(1)鸡蛋壳主要成分是碳酸钙,会与盐酸反应产生二氧化碳气体,产生气泡,一开始鸡蛋的重力大于鸡蛋受到的浮力,鸡蛋下沉,随着蛋壳表面的气体越快越多,鸡蛋受到的浮力增大,浮力大于重力,鸡蛋上浮,当浮出液面一定程度时,气体逸出,鸡蛋的重力大于受到的浮力,鸡蛋又将下沉;
(2)碳酸氢钠受热能分解生成二氧化碳,碳酸氢钠也能与有机酸反应生成二氧化碳,可使面包等松软可口,且可除去发酵过程中产生的酸
15.(1)
(2)产生白色沉淀或浑浊
(3)或
(4)
16. Fe2O3
17. CaO 熟石灰、消石灰 Fe+2HCl=FeCl2+H2↑ NaOH和Ca(OH)2
18. 烧杯中澄清的石灰水变浑浊
19. 大于16g 铁丝表面有红色物质析出 氧气约占空气总体积的1/5 比较呼出气体和空气中氧气的含量
20.(1)10
(2)96%
解:由题意知,硫酸铜样品中所含杂质溶于水,所以滤渣的质量为氢氧化铜的质量,
设参加反应的硫酸铜质量为x,
样品中硫酸铜的质量分数为×100%=96%;
答:样品中硫酸铜的质量分数为96%。
21.(1)0.4
(2)解:设锌的质量为x,
x=13g
该合金中铜的质量分数为×100%=60%
答:该合金中铜的质量分数为60%。
22.(1)②⑤
(2)设要合成 90 吨尿素,需要二氧化碳的质量为x,
x=66t
答:要合成 90 吨尿素,需要二氧化碳的质量为66t。
23.143g
