九年级化学京改版(2013)下册 第12章盐随堂练习题(word版有答案)
文档属性
| 名称 | 九年级化学京改版(2013)下册 第12章盐随堂练习题(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 244.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 00:00:00 | ||
图片预览



文档简介
第12章盐随堂练习题2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.氢氧化钠的俗称是
A.纯碱 B.小苏打 C.熟石灰 D.烧碱
2.糕点制作时所用的发酵粉中含有小苏打,小苏打的化学式是( )
A.NaCl B.NaHCO3 C.Na2CO3 D.CaCO3
3.物质的俗称和化学式对应正确的是
A.胆矾CuSO4 B.食盐NaCl C.水银Ag D.熟石灰CaCO3
4.下列实验现象的描述中正确的是
A.红磷燃烧,产生大量白烟,生成五氧化二磷
B.将铁丝伸入盛有氧气的集气瓶中,铁丝剧烈燃烧,火星四射,生成黑色固体
C.将氢氧化钠溶液滴加入硫酸铜溶液中,生成白色沉淀
D.碳酸钠固体和稀盐酸反应,生成能使澄清石灰水变浑浊的气体
5.兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。应选用的药品是
A.铁粉和稀盐酸液体中
B.硝酸钾晶体和水
C.碳酸钡粉末和稀硫酸
D.铜粉和硝酸银溶液
6.下列化学反应属于置换反应的是( )
A.H2O+CaO═Ca(OH)2
B.Na2SO4+BaCl2═2NaCl+BaSO4↓
C.H2+CuOCu+H2O
D.3CO+Fe2O32Fe+3CO2
7.下列各组溶液混合后能发生反应且无明显现象的一组是
A.NaNO3、NaCl、AgNO3 B.CuSO4、H2SO4、BaCl2
C.HCl、Na2SO4、NaOH D.HCl、NaHCO3、NaNO3
8.下列知识归纳完全正确的是
A.性质与用途 B.化学与环保
①氧气可用于炼钢,是由于氧气具有可燃性 ②CO可用于炼铁,是由于CO具有还原性 ①大力发展化石能源,满足工业生产需求 ②二氧化硫是造成酸雨的主要气体
C.化学与生活 D.物质分类
①生石灰可用作食品干燥剂 ②如果庄稼的叶子发黄,可施用氮肥 ①烧碱、纯碱都属于碱 ②二氧化锰、氧化铝都属于氧化物
A.A B.B C.C D.D
9.下图是某反应前后的微观示意图,“”和“”表示两种不同元素的原子。下列有关说法正确的是
A.该反应没有单质生成
B.该反应属于复分解反应
C.该反应中,原子个数发生了改变
D.参加反应的两种分子(和)的个数比为1:1
10.物质的性质与用途密切相关。 下列做法不合理的是
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
11.把 CaCO3、NaCl、MgCl2三种固体物质组成的混合物逐一分离所需要的试剂依次是
A.H2ONaOHHCl
B.H2O KOH HCl
C.H2O NaOH H2SO4
D.H2O KOH H2SO4
12.下列各物物质在同一溶液中可以大量共存的是
A.NaOH、FeCl3、K2SO4 B.NaCl、HNO3、AgNO3
C.NaCl、K2CO3、Ca(OH)2 D.KNO3、NaCl、Ba(OH)2
二、简答题
13.某小组同学利用传感器对碳酸氢钠、碳酸钠的某些性质进行以下探究。
25℃时,向等体积、含有等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的盐酸,利用pH传感器测得pH变化与时间的关系如图1、图2所示,将图1、图2的阴影部分进行叠加,发现两者基本重合。
回答下列问题:
(1)等体积、含有等碳原子数的碳酸氢钠和碳酸钠溶液均呈碱性,两种溶液中碱性较强的是_____。
(2)a点的溶质为_____,b点前发生反应的化学方程式为_____。
(3)含有等碳原子数的碳酸氢钠和碳酸钠溶液,加入足量的盐酸,产生二氧化碳的质量_____。
A 碳酸氢钠多 B 碳酸钠多 C 两者一样多 D 不能确定哪个多
14.某兴趣小组用一定量的碳酸钠溶液和石灰水反应制取氢氧化钠,并对反应后溶液的成分进行探究。
(1)反应后的溶液中除了氢氧化钠,还可能含有哪些溶质_______?
(2)请设计实验方案(包括实验步骤、现象和结论)验证你的猜想_________。
三、推断题
15.如图是几种常见物质之间的反应及转化关系,其中B、C、D都是由两种元素组成的化合物,A是一种常用的建筑材料,也可用来配制波尔多液。则A的化学式是__________;B和C反应的化学方程式为______;D和铁单质反应的现象为______________。
16.踩高跷是客家传统的娱乐项目。小莹用初中常见的化学物质组建了一对高跷(如图所示),相邻物质之间能发生化学反应。已知A是最轻的气体,B、D是黑色固体,C的浓溶液可用来做干燥剂,F可用于改良酸性土壤。
(1)物质C的化学式:______
(2)C和D反应的基本反应类型:______
(3)若G是纯碱,则F和G反应的化学方程式:______,为了搭好这对“高跷”,物质X可能是______
A.H2O B.HNO3 C.NaCl D.BaCl2
四、实验题
17.物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后总质量不变。
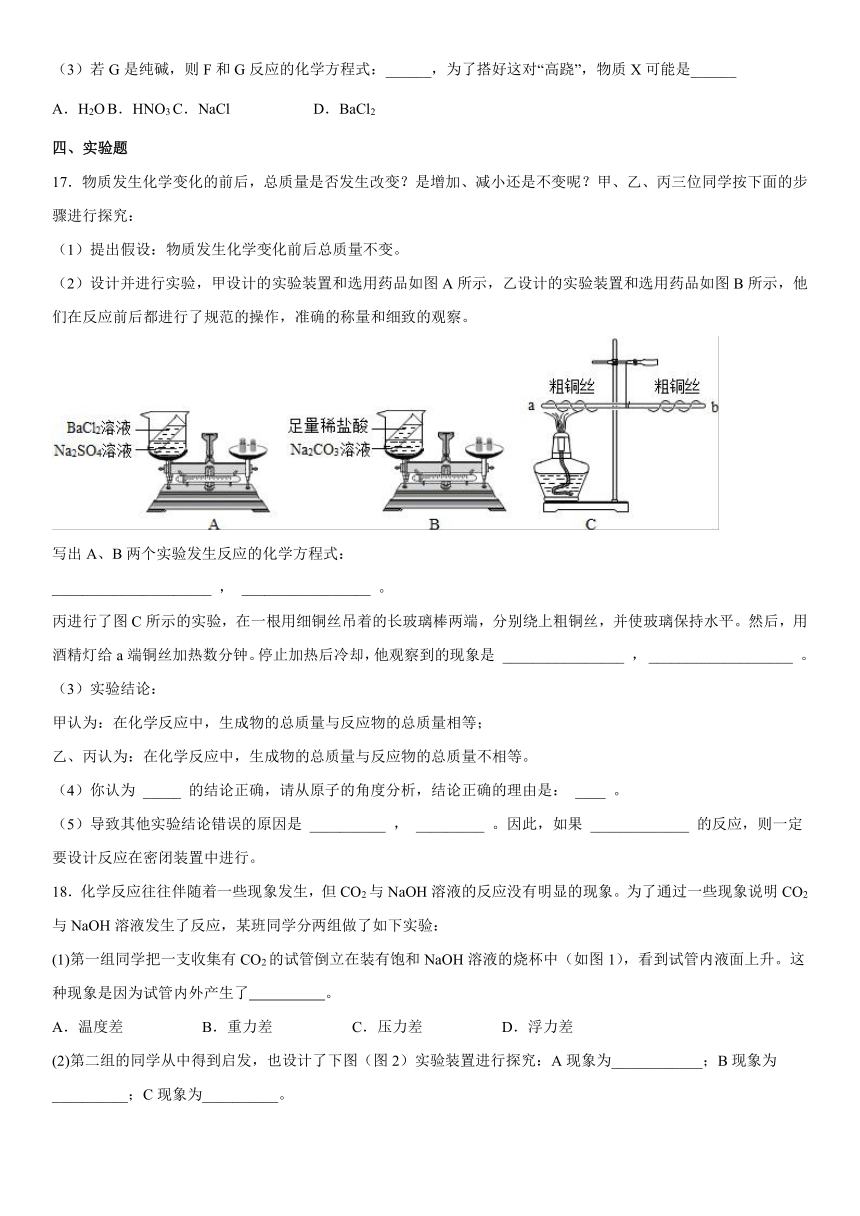
(2)设计并进行实验,甲设计的实验装置和选用药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
写出A、B两个实验发生反应的化学方程式:
_____________________ , _________________ 。
丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃保持水平。然后,用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是 ________________ , ___________________ 。
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙、丙认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
(4)你认为 _____ 的结论正确,请从原子的角度分析,结论正确的理由是: ____ 。
(5)导致其他实验结论错误的原因是 __________ , _________ 。因此,如果 _____________ 的反应,则一定要设计反应在密闭装置中进行。
18.化学反应往往伴随着一些现象发生,但CO2与NaOH溶液的反应没有明显的现象。为了通过一些现象说明CO2与NaOH溶液发生了反应,某班同学分两组做了如下实验:
(1)第一组同学把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中(如图1),看到试管内液面上升。这种现象是因为试管内外产生了 。
A.温度差 B.重力差 C.压力差 D.浮力差
(2)第二组的同学从中得到启发,也设计了下图(图2)实验装置进行探究:A现象为____________;B现象为__________;C现象为__________。
(3)同学们经过分析讨论,认为第一组的实验中液面上升现象的原因可能有两种。一种是因为CO2与溶液中NaOH的反应,消耗了CO2,你认为另一种原因是___________。
(4)为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液;第一组同学滴加_________,现象为_____________;第二组同学滴加____________,现象为____________。他们虽然看到的现象不同,但都可以证实CO2与NaOH溶液已经发生了反应。
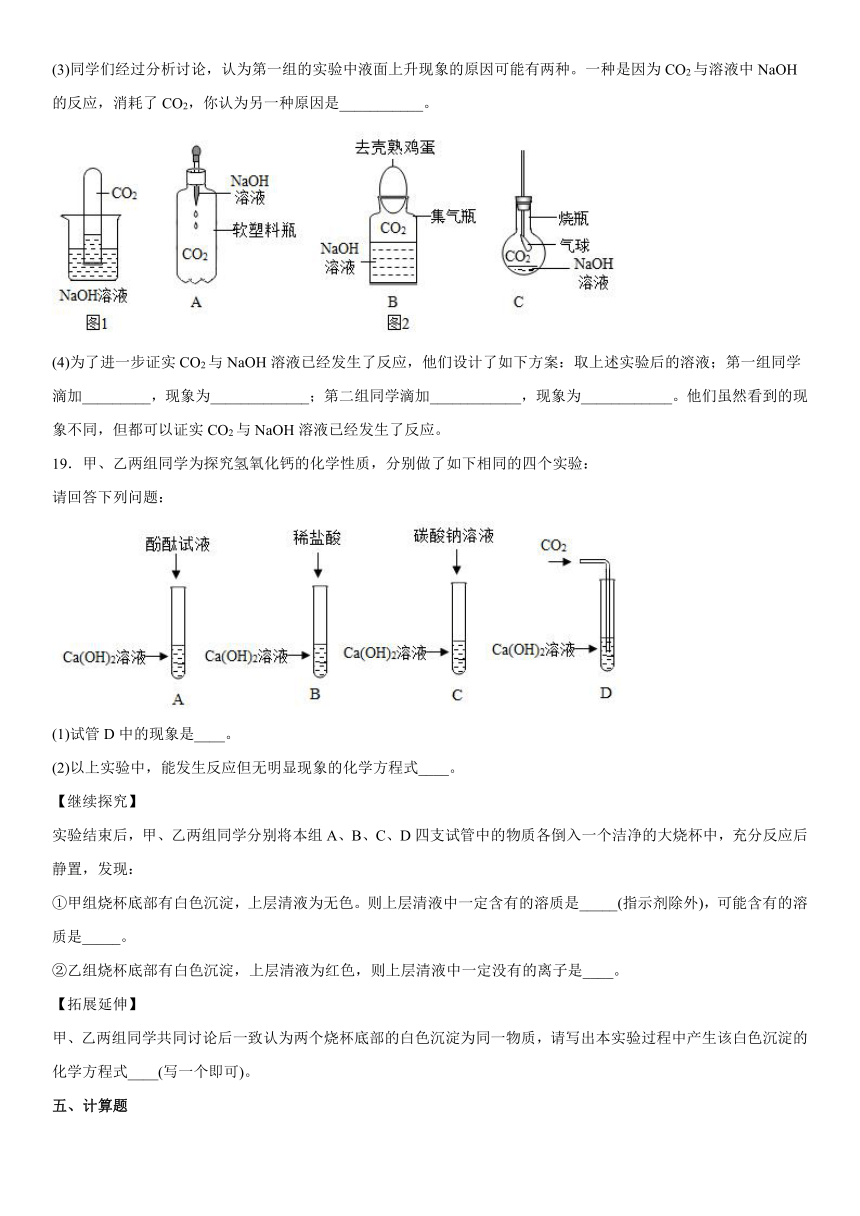
19.甲、乙两组同学为探究氢氧化钙的化学性质,分别做了如下相同的四个实验:
请回答下列问题:
(1)试管D中的现象是____。
(2)以上实验中,能发生反应但无明显现象的化学方程式____。
【继续探究】
实验结束后,甲、乙两组同学分别将本组A、B、C、D四支试管中的物质各倒入一个洁净的大烧杯中,充分反应后静置,发现:
①甲组烧杯底部有白色沉淀,上层清液为无色。则上层清液中一定含有的溶质是_____(指示剂除外),可能含有的溶质是_____。
②乙组烧杯底部有白色沉淀,上层清液为红色,则上层清液中一定没有的离子是____。
【拓展延伸】
甲、乙两组同学共同讨论后一致认为两个烧杯底部的白色沉淀为同一物质,请写出本实验过程中产生该白色沉淀的化学方程式____(写一个即可)。
五、计算题
20.纯碱(主要成分为碳酸钠)中常含有少量氯化钠。化学兴趣小组的同学为了测定实验室中某盐酸的溶质质量分数,称取了某品牌纯碱样品12g进行了以下实验:将样品置于烧杯中,取50g此稀盐酸分五次加入其中,测得的有关数据如下表所示。
第一次 第二次 第三次 第四次 第五次
加入稀盐酸质量/ 10 10 10 10 10
烧杯中剩余物的质量/ 20.9 29.8 47.6 57.6
试计算:
(1)表中a的值为______。
(2)实验中产生二氧化碳的总质量为______。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程,计算结果保留一位小数)
21.为测定某纯碱样品杂质为氯化钠中碳酸钠的含量,某小组同学进行了如图所示的实验,请回答问题:
写出反应的化学方程式______;
列出求解混合物中参加反应的物质质量的比例式______;
样品中碳酸钠的含量为______最终结果保留整数;
最终所得溶液的溶质质量分数为______;
若用质量分数的浓盐酸配制实验所需稀盐酸,需要浓盐酸和水的质量比为______。
22.施肥是农业增产的重要手段,CO(NH2)2、(NH4)2HPO4是常用的化学肥料。
回答下列问题:
(1)(NH4)2HPO4中N和H原子的个数比为______ 。
(2)CO(NH2)2的相对分子质量______ 。
(3)经农科所技术人员检测,某农户的农作物缺磷和氮。若需补充磷3.1kg和氮7.0kg,则至少需要施用_________ kg(NH4)2HPO4和__________kg CO(NH2)2。
23.如图1是复方龙胆碳酸氢钠片合的侧面上说明文字,
小明同学为了测定该胃药每片含有碳酸氢钠的质量,(若其它成分不溶于水,也不与酸反应)取20片该胃药,并做如图2实验,请回答问题:
(1)该胃药中每片含碳酸氢钠多少g。______
(2)则所用盐酸的溶质质量分数为多少。______
参考答案:
1.D
2.B
3.B
4.D
5.D
6.C
7.C
8.C
9.A
10.D
11.A
12.D
13. 碳酸钠(或Na2CO3) NaCl、HCl Na2CO3+HCl=NaCl+NaHCO3 C
14. 碳酸钠或氢氧化钙; 取少量反应后的溶液,加入BaCl2溶液,若有白色沉淀生成,说明含有碳酸钠;另取少量反应后的溶液,加入碳酸钠溶液,若有白色沉淀生成,说明含有氢氧化钙。
15. Ca(OH)2 有红色固体生成,溶液由蓝色变为浅绿色
16. H2SO4 置换反应
BD
17. a端上铜丝变黑 玻璃棒a端下沉 甲 在化学反应前后,原子的种类没有改变,数目没有增减,原子的质量也没有改变 B实验反应后生成的气体逸散到空气中去了 C实验a端铜丝增加了氧元素的质量 有气体参与反应或者生成物中有气体
18.(1)C
(2) 软塑料瓶变瘪 去壳的熟鸡蛋被吸入集气瓶中 烧瓶中的气球胀大
(3)氧化碳能溶于水且与水反应
(4) 足量的稀盐酸 有气泡产生 CaCl2溶液 产生白色沉淀
19. 溶液变浑浊 氯化钙 氯化钠
氢离子
20.(1)38.7;(2)4.4g
(3)根据反应生成二氧化碳的质量,可求出稀盐酸中溶质的质量,根据溶质质量分数的计算公式计算稀盐酸中溶质的质量分数。
设参加反应的HCl的总质量为x。
x=7.3g
稀盐酸中溶质的质量分数为(其他解法合理即可)
答:所用稀盐酸中溶质的质量分数为。
21.(1);(2);(3);(4);(5)1:4
22.(1)2:9(2)60(3)13.2;9
23.(1)20片胃药的质量为:20×0.5g=10g
生成二氧化碳的质量为:10g+25g-32.8g=2.2g
解:设20片胃药中含碳酸氢钠的质量为x
x=4.2g
每片胃药中含碳酸氢钠的质量为:4.2g÷20=0.21g;
(2)解:设所用盐酸的溶质质量分数为y
y=7.3%
答:所用盐酸的溶质质量分数为7.3%。
一、单选题
1.氢氧化钠的俗称是
A.纯碱 B.小苏打 C.熟石灰 D.烧碱
2.糕点制作时所用的发酵粉中含有小苏打,小苏打的化学式是( )
A.NaCl B.NaHCO3 C.Na2CO3 D.CaCO3
3.物质的俗称和化学式对应正确的是
A.胆矾CuSO4 B.食盐NaCl C.水银Ag D.熟石灰CaCO3
4.下列实验现象的描述中正确的是
A.红磷燃烧,产生大量白烟,生成五氧化二磷
B.将铁丝伸入盛有氧气的集气瓶中,铁丝剧烈燃烧,火星四射,生成黑色固体
C.将氢氧化钠溶液滴加入硫酸铜溶液中,生成白色沉淀
D.碳酸钠固体和稀盐酸反应,生成能使澄清石灰水变浑浊的气体
5.兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。应选用的药品是
A.铁粉和稀盐酸液体中
B.硝酸钾晶体和水
C.碳酸钡粉末和稀硫酸
D.铜粉和硝酸银溶液
6.下列化学反应属于置换反应的是( )
A.H2O+CaO═Ca(OH)2
B.Na2SO4+BaCl2═2NaCl+BaSO4↓
C.H2+CuOCu+H2O
D.3CO+Fe2O32Fe+3CO2
7.下列各组溶液混合后能发生反应且无明显现象的一组是
A.NaNO3、NaCl、AgNO3 B.CuSO4、H2SO4、BaCl2
C.HCl、Na2SO4、NaOH D.HCl、NaHCO3、NaNO3
8.下列知识归纳完全正确的是
A.性质与用途 B.化学与环保
①氧气可用于炼钢,是由于氧气具有可燃性 ②CO可用于炼铁,是由于CO具有还原性 ①大力发展化石能源,满足工业生产需求 ②二氧化硫是造成酸雨的主要气体
C.化学与生活 D.物质分类
①生石灰可用作食品干燥剂 ②如果庄稼的叶子发黄,可施用氮肥 ①烧碱、纯碱都属于碱 ②二氧化锰、氧化铝都属于氧化物
A.A B.B C.C D.D
9.下图是某反应前后的微观示意图,“”和“”表示两种不同元素的原子。下列有关说法正确的是
A.该反应没有单质生成
B.该反应属于复分解反应
C.该反应中,原子个数发生了改变
D.参加反应的两种分子(和)的个数比为1:1
10.物质的性质与用途密切相关。 下列做法不合理的是
A.工业上用稀盐酸除铁锈
B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
11.把 CaCO3、NaCl、MgCl2三种固体物质组成的混合物逐一分离所需要的试剂依次是
A.H2ONaOHHCl
B.H2O KOH HCl
C.H2O NaOH H2SO4
D.H2O KOH H2SO4
12.下列各物物质在同一溶液中可以大量共存的是
A.NaOH、FeCl3、K2SO4 B.NaCl、HNO3、AgNO3
C.NaCl、K2CO3、Ca(OH)2 D.KNO3、NaCl、Ba(OH)2
二、简答题
13.某小组同学利用传感器对碳酸氢钠、碳酸钠的某些性质进行以下探究。
25℃时,向等体积、含有等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的盐酸,利用pH传感器测得pH变化与时间的关系如图1、图2所示,将图1、图2的阴影部分进行叠加,发现两者基本重合。
回答下列问题:
(1)等体积、含有等碳原子数的碳酸氢钠和碳酸钠溶液均呈碱性,两种溶液中碱性较强的是_____。
(2)a点的溶质为_____,b点前发生反应的化学方程式为_____。
(3)含有等碳原子数的碳酸氢钠和碳酸钠溶液,加入足量的盐酸,产生二氧化碳的质量_____。
A 碳酸氢钠多 B 碳酸钠多 C 两者一样多 D 不能确定哪个多
14.某兴趣小组用一定量的碳酸钠溶液和石灰水反应制取氢氧化钠,并对反应后溶液的成分进行探究。
(1)反应后的溶液中除了氢氧化钠,还可能含有哪些溶质_______?
(2)请设计实验方案(包括实验步骤、现象和结论)验证你的猜想_________。
三、推断题
15.如图是几种常见物质之间的反应及转化关系,其中B、C、D都是由两种元素组成的化合物,A是一种常用的建筑材料,也可用来配制波尔多液。则A的化学式是__________;B和C反应的化学方程式为______;D和铁单质反应的现象为______________。
16.踩高跷是客家传统的娱乐项目。小莹用初中常见的化学物质组建了一对高跷(如图所示),相邻物质之间能发生化学反应。已知A是最轻的气体,B、D是黑色固体,C的浓溶液可用来做干燥剂,F可用于改良酸性土壤。
(1)物质C的化学式:______
(2)C和D反应的基本反应类型:______
(3)若G是纯碱,则F和G反应的化学方程式:______,为了搭好这对“高跷”,物质X可能是______
A.H2O B.HNO3 C.NaCl D.BaCl2
四、实验题
17.物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后总质量不变。
(2)设计并进行实验,甲设计的实验装置和选用药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
写出A、B两个实验发生反应的化学方程式:
_____________________ , _________________ 。
丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃保持水平。然后,用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是 ________________ , ___________________ 。
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙、丙认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
(4)你认为 _____ 的结论正确,请从原子的角度分析,结论正确的理由是: ____ 。
(5)导致其他实验结论错误的原因是 __________ , _________ 。因此,如果 _____________ 的反应,则一定要设计反应在密闭装置中进行。
18.化学反应往往伴随着一些现象发生,但CO2与NaOH溶液的反应没有明显的现象。为了通过一些现象说明CO2与NaOH溶液发生了反应,某班同学分两组做了如下实验:
(1)第一组同学把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中(如图1),看到试管内液面上升。这种现象是因为试管内外产生了 。
A.温度差 B.重力差 C.压力差 D.浮力差
(2)第二组的同学从中得到启发,也设计了下图(图2)实验装置进行探究:A现象为____________;B现象为__________;C现象为__________。
(3)同学们经过分析讨论,认为第一组的实验中液面上升现象的原因可能有两种。一种是因为CO2与溶液中NaOH的反应,消耗了CO2,你认为另一种原因是___________。
(4)为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液;第一组同学滴加_________,现象为_____________;第二组同学滴加____________,现象为____________。他们虽然看到的现象不同,但都可以证实CO2与NaOH溶液已经发生了反应。
19.甲、乙两组同学为探究氢氧化钙的化学性质,分别做了如下相同的四个实验:
请回答下列问题:
(1)试管D中的现象是____。
(2)以上实验中,能发生反应但无明显现象的化学方程式____。
【继续探究】
实验结束后,甲、乙两组同学分别将本组A、B、C、D四支试管中的物质各倒入一个洁净的大烧杯中,充分反应后静置,发现:
①甲组烧杯底部有白色沉淀,上层清液为无色。则上层清液中一定含有的溶质是_____(指示剂除外),可能含有的溶质是_____。
②乙组烧杯底部有白色沉淀,上层清液为红色,则上层清液中一定没有的离子是____。
【拓展延伸】
甲、乙两组同学共同讨论后一致认为两个烧杯底部的白色沉淀为同一物质,请写出本实验过程中产生该白色沉淀的化学方程式____(写一个即可)。
五、计算题
20.纯碱(主要成分为碳酸钠)中常含有少量氯化钠。化学兴趣小组的同学为了测定实验室中某盐酸的溶质质量分数,称取了某品牌纯碱样品12g进行了以下实验:将样品置于烧杯中,取50g此稀盐酸分五次加入其中,测得的有关数据如下表所示。
第一次 第二次 第三次 第四次 第五次
加入稀盐酸质量/ 10 10 10 10 10
烧杯中剩余物的质量/ 20.9 29.8 47.6 57.6
试计算:
(1)表中a的值为______。
(2)实验中产生二氧化碳的总质量为______。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程,计算结果保留一位小数)
21.为测定某纯碱样品杂质为氯化钠中碳酸钠的含量,某小组同学进行了如图所示的实验,请回答问题:
写出反应的化学方程式______;
列出求解混合物中参加反应的物质质量的比例式______;
样品中碳酸钠的含量为______最终结果保留整数;
最终所得溶液的溶质质量分数为______;
若用质量分数的浓盐酸配制实验所需稀盐酸,需要浓盐酸和水的质量比为______。
22.施肥是农业增产的重要手段,CO(NH2)2、(NH4)2HPO4是常用的化学肥料。
回答下列问题:
(1)(NH4)2HPO4中N和H原子的个数比为______ 。
(2)CO(NH2)2的相对分子质量______ 。
(3)经农科所技术人员检测,某农户的农作物缺磷和氮。若需补充磷3.1kg和氮7.0kg,则至少需要施用_________ kg(NH4)2HPO4和__________kg CO(NH2)2。
23.如图1是复方龙胆碳酸氢钠片合的侧面上说明文字,
小明同学为了测定该胃药每片含有碳酸氢钠的质量,(若其它成分不溶于水,也不与酸反应)取20片该胃药,并做如图2实验,请回答问题:
(1)该胃药中每片含碳酸氢钠多少g。______
(2)则所用盐酸的溶质质量分数为多少。______
参考答案:
1.D
2.B
3.B
4.D
5.D
6.C
7.C
8.C
9.A
10.D
11.A
12.D
13. 碳酸钠(或Na2CO3) NaCl、HCl Na2CO3+HCl=NaCl+NaHCO3 C
14. 碳酸钠或氢氧化钙; 取少量反应后的溶液,加入BaCl2溶液,若有白色沉淀生成,说明含有碳酸钠;另取少量反应后的溶液,加入碳酸钠溶液,若有白色沉淀生成,说明含有氢氧化钙。
15. Ca(OH)2 有红色固体生成,溶液由蓝色变为浅绿色
16. H2SO4 置换反应
BD
17. a端上铜丝变黑 玻璃棒a端下沉 甲 在化学反应前后,原子的种类没有改变,数目没有增减,原子的质量也没有改变 B实验反应后生成的气体逸散到空气中去了 C实验a端铜丝增加了氧元素的质量 有气体参与反应或者生成物中有气体
18.(1)C
(2) 软塑料瓶变瘪 去壳的熟鸡蛋被吸入集气瓶中 烧瓶中的气球胀大
(3)氧化碳能溶于水且与水反应
(4) 足量的稀盐酸 有气泡产生 CaCl2溶液 产生白色沉淀
19. 溶液变浑浊 氯化钙 氯化钠
氢离子
20.(1)38.7;(2)4.4g
(3)根据反应生成二氧化碳的质量,可求出稀盐酸中溶质的质量,根据溶质质量分数的计算公式计算稀盐酸中溶质的质量分数。
设参加反应的HCl的总质量为x。
x=7.3g
稀盐酸中溶质的质量分数为(其他解法合理即可)
答:所用稀盐酸中溶质的质量分数为。
21.(1);(2);(3);(4);(5)1:4
22.(1)2:9(2)60(3)13.2;9
23.(1)20片胃药的质量为:20×0.5g=10g
生成二氧化碳的质量为:10g+25g-32.8g=2.2g
解:设20片胃药中含碳酸氢钠的质量为x
x=4.2g
每片胃药中含碳酸氢钠的质量为:4.2g÷20=0.21g;
(2)解:设所用盐酸的溶质质量分数为y
y=7.3%
答:所用盐酸的溶质质量分数为7.3%。
