第四单元盐化肥基础练习题—2021-2022学年九年级化学人教版(五四学制)全一册(word版有答案)
文档属性
| 名称 | 第四单元盐化肥基础练习题—2021-2022学年九年级化学人教版(五四学制)全一册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 112.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-26 00:00:00 | ||
图片预览


文档简介
第四单元盐化肥基础练习题2021-2022学年九年级化学人教版(五四学制)全一册
一、单选题
1.下列做法不符合“节能降耗、保护环境”这一主题的是( )
A.合理和综合利用煤和石油
B.研制太阳能电池、海洋电池等
C.大量使用农药化肥提高粮食产量
D.推广垃圾分类、回收和处理
2.下列物质的名称、俗称、化学式对应不一致的是
A.碳酸钠—纯碱—Na2CO3
B.氯化钠—食盐—NaCl
C.碳酸氢钠—小苏打—NaHCO3
D.碳酸钠—小苏打—NaHCO3
3.草木灰是一种碱性农家肥,下列肥料不能与草木灰混合使用的是
A.KNO3 B.NH4HCO3 C.KCl D.Ca3(PO4)2
4.下列属于置换反应的是
A.
B.
C.NaOH+HCl=NaCl+H2O
D.2Al+6HCl=2AlCl3+3H2↑
5.下列各组离子在水中能大量共存,并形成无色溶液的是
A.Ba2+、SO、NO
B.Fe2+、SO、OH-
C.Na+、NO、OH-
D.Ag+、NO、Cl-
6.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
7.氯化铵(NH4Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化铵的说法正确的是
A.氯化铵属于酸 B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效 D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
8.除去下列物质中的杂质,选用试剂和方法均正确的是
选项 物质 杂质(少量) 试剂和方法
A 氯化钾 氯酸钾 加入少量二氧化锰粉末,加热
B 稀硫酸 稀盐酸 加入适量的氯化钡溶液,过滤
C 氯化钙溶液 氢氧化钙 加入稍微过量的稀盐酸,加热
D 硝酸钾溶液 硫酸钾 加入过量的硝酸钡溶液,过滤
A.A B.B C.C D.D
9.下列化肥,属于磷肥的是( )
A.KNO3 B.NH4NO3 C.CO(NH2)2 D.Ca(H2PO4)2
10.下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
11.对已变质的NaOH溶液进行如下实验,其中实验方案能达到实验目的的是
选项 实验目的 实验方案
A 证明溶液中存在Na2CO3 取样滴加无色酚酞溶液
B 除去溶液中的Na2CO3 加入一定量的氯化钙溶液,然后过滤
C 证明溶液部分变质 取样加入过量呈中性的氯化钡溶液,振荡后滴加无色酚酞溶液
D 测溶液的PH 用玻璃棒蘸取少量溶液涂在湿润的PH试纸上,与标准比色卡对比
A.A B.B C.C D.D
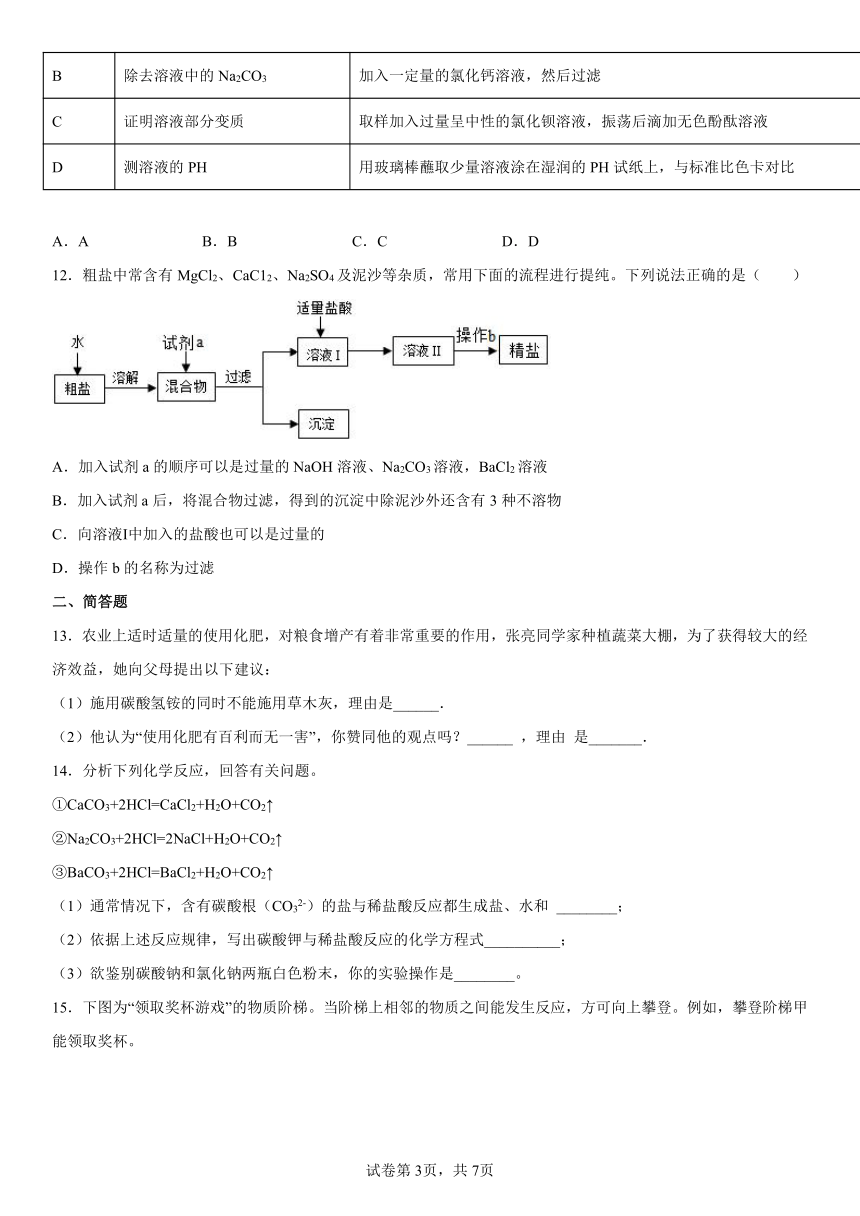
12.粗盐中常含有MgCl2、CaC12、Na2SO4及泥沙等杂质,常用下面的流程进行提纯。下列说法正确的是( )
A.加入试剂a的顺序可以是过量的NaOH溶液、Na2CO3溶液,BaCl2溶液
B.加入试剂a后,将混合物过滤,得到的沉淀中除泥沙外还含有3种不溶物
C.向溶液Ⅰ中加入的盐酸也可以是过量的
D.操作b的名称为过滤
二、简答题
13.农业上适时适量的使用化肥,对粮食增产有着非常重要的作用,张亮同学家种植蔬菜大棚,为了获得较大的经济效益,她向父母提出以下建议:
(1)施用碳酸氢铵的同时不能施用草木灰,理由是______.
(2)他认为“使用化肥有百利而无一害”,你赞同他的观点吗?______ ,理由 是_______.
14.分析下列化学反应,回答有关问题。
①CaCO3+2HCl=CaCl2+H2O+CO2↑
②Na2CO3+2HCl=2NaCl+H2O+CO2↑
③BaCO3+2HCl=BaCl2+H2O+CO2↑
(1)通常情况下,含有碳酸根(CO32-)的盐与稀盐酸反应都生成盐、水和 ________;
(2)依据上述反应规律,写出碳酸钾与稀盐酸反应的化学方程式__________;
(3)欲鉴别碳酸钠和氯化钠两瓶白色粉末,你的实验操作是________。
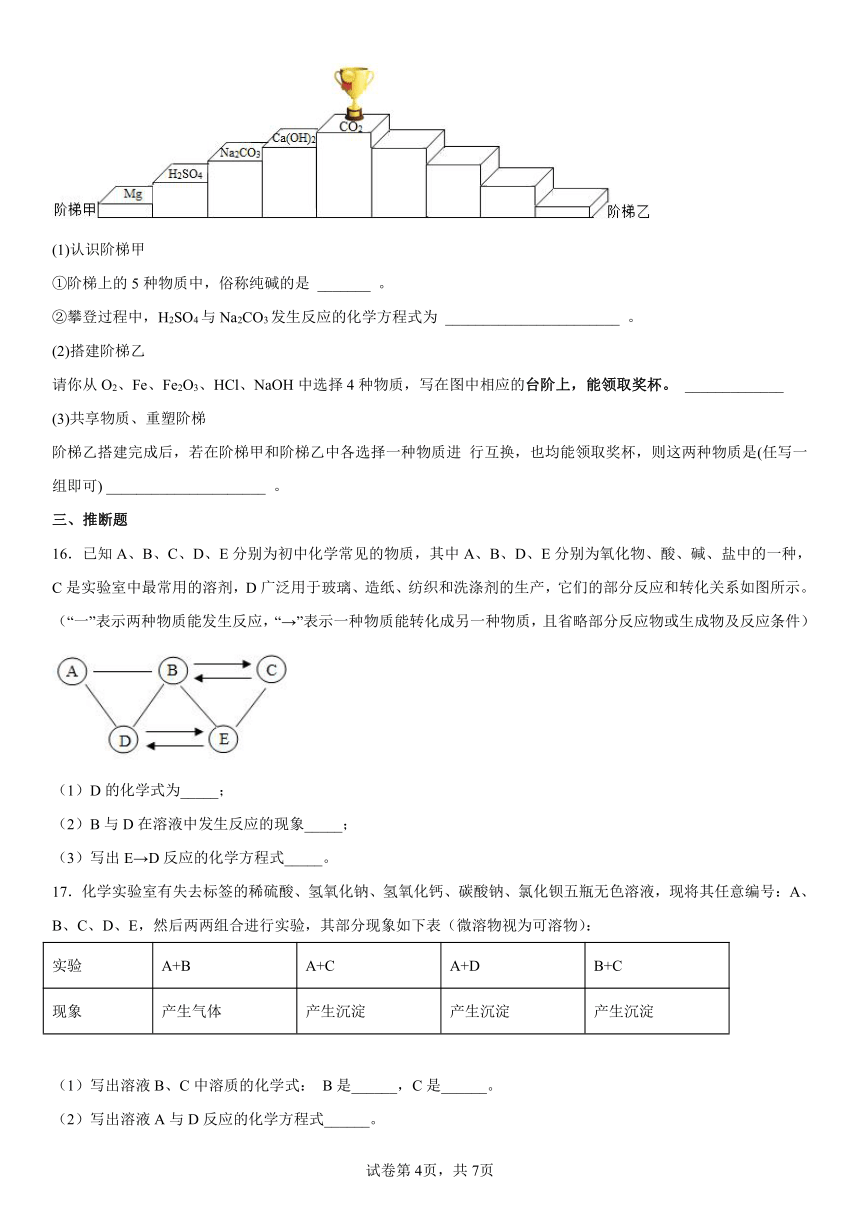
15.下图为“领取奖杯游戏”的物质阶梯。当阶梯上相邻的物质之间能发生反应,方可向上攀登。例如,攀登阶梯甲能领取奖杯。
(1)认识阶梯甲
①阶梯上的5种物质中,俗称纯碱的是 _______ 。
②攀登过程中,H2SO4与Na2CO3发生反应的化学方程式为 _______________________ 。
(2)搭建阶梯乙
请你从O2、Fe、Fe2O3、HCl、NaOH中选择4种物质,写在图中相应的台阶上,能领取奖杯。 _____________
(3)共享物质、重塑阶梯
阶梯乙搭建完成后,若在阶梯甲和阶梯乙中各选择一种物质进 行互换,也均能领取奖杯,则这两种物质是(任写一组即可) _____________________ 。
三、推断题
16.已知A、B、C、D、E分别为初中化学常见的物质,其中A、B、D、E分别为氧化物、酸、碱、盐中的一种,C是实验室中最常用的溶剂,D广泛用于玻璃、造纸、纺织和洗涤剂的生产,它们的部分反应和转化关系如图所示。(“一”表示两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物或生成物及反应条件)
(1)D的化学式为_____;
(2)B与D在溶液中发生反应的现象_____;
(3)写出E→D反应的化学方程式_____。
17.化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可溶物):
实验 A+B A+C A+D B+C
现象 产生气体 产生沉淀 产生沉淀 产生沉淀
(1)写出溶液B、C中溶质的化学式: B是______,C是______。
(2)写出溶液A与D反应的化学方程式______。
四、实验题
18.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
19.下图为初中化学常见的仪器装置,请回答下列问题。
(1)写出仪器名称:a为______,b为______。
(2)实验室可选用______(填字母)和D装置制取CO2气体:实验室检验CO2化学方程式为______。
(3)实验室用KMnO4粉末制取O2的化学方程式为______;发生装置中需在试管口放一团蓬松的棉花,以防止KMnO4粉末______。
(4)实验室用过氧化氢溶液及少量MnO2制取O2,收集O2可选用______装置(填字母);MnO2起______作用。
(5)实验室用FeS和稀H2SO4反应制取H2S。H2S是有毒气体,能溶于水,其水溶液为氢硫酸。
① 制取H2S的化学方程式为______。
② 图中“防倒吸装置”应选择______。(填“甲”或“乙”)
③ NaOH溶液的作用是______。化学方程式为______。
20.某化学兴趣小组的同学在对稀盐酸、氢氧化钠、碳酸钠的化学性质进行探究的过程中遇到“异常”现象。
现象一:向试管中加入2mL某浓度的氢氧化钠溶液,再滴入2~3滴酚酞溶液,氢氧化钠溶液变红色;然后振荡试管,发现红色消失。
【提出问题】红色为什么会消失?
【猜想】(1)氢氧化钠溶液的量少了;(2)酚酞溶液的量少了;(3)_____。
【查阅资料】酚酞是一种弱有机酸,在pH<8.2的溶液里为无色的内酯式结构,当pH>8.2时为红色的锟式结构;在碱性介质中很不稳定,它会慢慢地转化成无色羧酸盐。
【实验探究】根据上述“猜想”进行如下探究
(1)取4mL同浓度氢氧化钠溶液,滴入2~3滴酚酞溶液,振荡后红色消失;
(2)取2mL同浓度氢氧化钠溶液,滴入4~5滴酚酞溶液,振荡后红色消失;
(3)取2mL同浓度氢氧化钠溶液,加适量水稀释,滴入2~3滴酚酞溶液,振荡后红色没有消失。
结论:猜想_____正确。
【继续实验】取一定体积的稀氢氧化钠溶液,滴入2~3滴酚酞溶液,逐滴加入一定浓度的稀盐酸直至红色消失,写出反应的化学方程式_____。微观角度分析,该反应的实质是_____。
现象二:向碳酸钠粉末中逐滴加入稀盐酸,立即产生气泡;而向碳酸钠溶液中逐滴加入稀盐酸时,开始没有气泡,过一段时间后才有气泡产生。
【提出问题】碳酸钠溶液刚开始与稀盐酸是否发生了化学反应?
【实验探究】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的稀盐酸。
【收集证据】分别收集实验过程中不同阶段消耗盐酸的质量与生成CO2的质量,得到两者之间的关系如图1、图2所示。(忽略CO2在水中的溶解)
【合作交流】
(1)图1中A点时溶液中的溶质有_____(填化学式);
(2)图2中从B点开始的变化关系与图1完全重合,据此我们可以判断碳酸钠溶液刚开始和稀盐酸确实发生了化学反应(如图OB段所示),请你写出该反应的化学方程式_____。
【反思与评价】基于以上“异常”现象,你能提出的有价值的见解是_____(任写一点)。
五、计算题
21.厨房用泡打粉是一种复合膨松剂,又称为发泡粉,可作为快速发面剂用于制作面食。某种泡打粉的主要成分是碳酸氢钠,某化学探究小组为了测定其中碳酸氢钠的含量,他们准确称取泡打粉样品10g,向其中加入100g溶质质量分数为10%的稀盐酸,充分反应后再次称量,得溶液105.6g。忽略散失掉的水蒸气和氯化氢气体,试计算该泡打粉样品中NaHCO3的质量分数。
22.向CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,生成沉淀的质量变化与加入Na2CO3溶液质量关系如图所示;请回答问题:
(1)生成沉淀质量为____g;
(2)所用Na2CO3溶液的溶质质量分数为____。(计算结果保留一位小数)
23.某氯化钠溶液中含有氯化镁(MgCl2),学习小组为测定其中氯化镁的质量分数,在50.0g该溶液中加入50.0g氢氧化钠溶液恰好完全反应,经测定生成沉淀的质量为2.9g。请回答下列问题:
(1)反应后溶液的质量为 g。
(2)求原氯化钠溶液中氯化镁的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.B
4.D
5.C
6.B
7.D
8.C
9.D
10.A
11.C
12.C
13. 草木灰显碱性,二者能发 生化学反应生成氨气,使化肥肥效降低 不赞同 如果无限量使用化肥,会造成土壤板结;也会对水体造成污染,引起“赤 潮”“水华”等现象
14. 二氧化碳 K2CO3+2HCl=2KCl+H2O+CO2↑ 加盐酸看是否有气体生成
15. Na2CO3 Na2CO3 + H2SO4 = Na2SO4+H2O +CO2↑ 从高到低: NaOH HCl Fe O2 H2SO4和HCl(或 Fe 和Mg)
16. Na2CO3 产生白色沉淀 2NaOH+CO2=Na2CO3+H2O
17. H2SO4 BaCl2
18. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
19.(1) 长颈漏斗 水槽
(2) A##C
(3) 进入导管
(4) D##F 催化
(5) 乙 吸收尾气
20. 可能与氢氧化钠溶液浓度有关 (3) NaOH+HCl═NaCl+H2O 氢离子和氢氧根离子反应生成水分子 NaCl、NaHCO3 Na2CO3+HCl═NaCl+NaHCO3 有些化学反应是分步进行的
21.解:生成二氧化碳质量:10g+100g-105.6g=4.4g
设泡打粉样品中NaHCO3的质量为x
x=8.4g
答:该泡打粉样品中NaHCO3的质量分数为84%。
22.(1) 向CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,盐酸先和碳酸钠反应,然后氯化钙和碳酸钠反应生成碳酸钙和氯化钠,由图可知生成沉淀质量为10g。
(2)设所用Na2CO3溶液的溶质质量分数为x
由图可知,氯化钙和碳酸钠完全反应消耗的碳酸钠的质量为
答:所用Na2CO3溶液的溶质质量分数为23.6%。
23.(1)97.1
(2)解:设原氯化钠溶液中氯化镁的质量分数为x
得x=9.5%
答:原氯化钠溶液中氯化镁的质量分数为9.5%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列做法不符合“节能降耗、保护环境”这一主题的是( )
A.合理和综合利用煤和石油
B.研制太阳能电池、海洋电池等
C.大量使用农药化肥提高粮食产量
D.推广垃圾分类、回收和处理
2.下列物质的名称、俗称、化学式对应不一致的是
A.碳酸钠—纯碱—Na2CO3
B.氯化钠—食盐—NaCl
C.碳酸氢钠—小苏打—NaHCO3
D.碳酸钠—小苏打—NaHCO3
3.草木灰是一种碱性农家肥,下列肥料不能与草木灰混合使用的是
A.KNO3 B.NH4HCO3 C.KCl D.Ca3(PO4)2
4.下列属于置换反应的是
A.
B.
C.NaOH+HCl=NaCl+H2O
D.2Al+6HCl=2AlCl3+3H2↑
5.下列各组离子在水中能大量共存,并形成无色溶液的是
A.Ba2+、SO、NO
B.Fe2+、SO、OH-
C.Na+、NO、OH-
D.Ag+、NO、Cl-
6.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
7.氯化铵(NH4Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化铵的说法正确的是
A.氯化铵属于酸 B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效 D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
8.除去下列物质中的杂质,选用试剂和方法均正确的是
选项 物质 杂质(少量) 试剂和方法
A 氯化钾 氯酸钾 加入少量二氧化锰粉末,加热
B 稀硫酸 稀盐酸 加入适量的氯化钡溶液,过滤
C 氯化钙溶液 氢氧化钙 加入稍微过量的稀盐酸,加热
D 硝酸钾溶液 硫酸钾 加入过量的硝酸钡溶液,过滤
A.A B.B C.C D.D
9.下列化肥,属于磷肥的是( )
A.KNO3 B.NH4NO3 C.CO(NH2)2 D.Ca(H2PO4)2
10.下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
11.对已变质的NaOH溶液进行如下实验,其中实验方案能达到实验目的的是
选项 实验目的 实验方案
A 证明溶液中存在Na2CO3 取样滴加无色酚酞溶液
B 除去溶液中的Na2CO3 加入一定量的氯化钙溶液,然后过滤
C 证明溶液部分变质 取样加入过量呈中性的氯化钡溶液,振荡后滴加无色酚酞溶液
D 测溶液的PH 用玻璃棒蘸取少量溶液涂在湿润的PH试纸上,与标准比色卡对比
A.A B.B C.C D.D
12.粗盐中常含有MgCl2、CaC12、Na2SO4及泥沙等杂质,常用下面的流程进行提纯。下列说法正确的是( )
A.加入试剂a的顺序可以是过量的NaOH溶液、Na2CO3溶液,BaCl2溶液
B.加入试剂a后,将混合物过滤,得到的沉淀中除泥沙外还含有3种不溶物
C.向溶液Ⅰ中加入的盐酸也可以是过量的
D.操作b的名称为过滤
二、简答题
13.农业上适时适量的使用化肥,对粮食增产有着非常重要的作用,张亮同学家种植蔬菜大棚,为了获得较大的经济效益,她向父母提出以下建议:
(1)施用碳酸氢铵的同时不能施用草木灰,理由是______.
(2)他认为“使用化肥有百利而无一害”,你赞同他的观点吗?______ ,理由 是_______.
14.分析下列化学反应,回答有关问题。
①CaCO3+2HCl=CaCl2+H2O+CO2↑
②Na2CO3+2HCl=2NaCl+H2O+CO2↑
③BaCO3+2HCl=BaCl2+H2O+CO2↑
(1)通常情况下,含有碳酸根(CO32-)的盐与稀盐酸反应都生成盐、水和 ________;
(2)依据上述反应规律,写出碳酸钾与稀盐酸反应的化学方程式__________;
(3)欲鉴别碳酸钠和氯化钠两瓶白色粉末,你的实验操作是________。
15.下图为“领取奖杯游戏”的物质阶梯。当阶梯上相邻的物质之间能发生反应,方可向上攀登。例如,攀登阶梯甲能领取奖杯。
(1)认识阶梯甲
①阶梯上的5种物质中,俗称纯碱的是 _______ 。
②攀登过程中,H2SO4与Na2CO3发生反应的化学方程式为 _______________________ 。
(2)搭建阶梯乙
请你从O2、Fe、Fe2O3、HCl、NaOH中选择4种物质,写在图中相应的台阶上,能领取奖杯。 _____________
(3)共享物质、重塑阶梯
阶梯乙搭建完成后,若在阶梯甲和阶梯乙中各选择一种物质进 行互换,也均能领取奖杯,则这两种物质是(任写一组即可) _____________________ 。
三、推断题
16.已知A、B、C、D、E分别为初中化学常见的物质,其中A、B、D、E分别为氧化物、酸、碱、盐中的一种,C是实验室中最常用的溶剂,D广泛用于玻璃、造纸、纺织和洗涤剂的生产,它们的部分反应和转化关系如图所示。(“一”表示两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物或生成物及反应条件)
(1)D的化学式为_____;
(2)B与D在溶液中发生反应的现象_____;
(3)写出E→D反应的化学方程式_____。
17.化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可溶物):
实验 A+B A+C A+D B+C
现象 产生气体 产生沉淀 产生沉淀 产生沉淀
(1)写出溶液B、C中溶质的化学式: B是______,C是______。
(2)写出溶液A与D反应的化学方程式______。
四、实验题
18.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
19.下图为初中化学常见的仪器装置,请回答下列问题。
(1)写出仪器名称:a为______,b为______。
(2)实验室可选用______(填字母)和D装置制取CO2气体:实验室检验CO2化学方程式为______。
(3)实验室用KMnO4粉末制取O2的化学方程式为______;发生装置中需在试管口放一团蓬松的棉花,以防止KMnO4粉末______。
(4)实验室用过氧化氢溶液及少量MnO2制取O2,收集O2可选用______装置(填字母);MnO2起______作用。
(5)实验室用FeS和稀H2SO4反应制取H2S。H2S是有毒气体,能溶于水,其水溶液为氢硫酸。
① 制取H2S的化学方程式为______。
② 图中“防倒吸装置”应选择______。(填“甲”或“乙”)
③ NaOH溶液的作用是______。化学方程式为______。
20.某化学兴趣小组的同学在对稀盐酸、氢氧化钠、碳酸钠的化学性质进行探究的过程中遇到“异常”现象。
现象一:向试管中加入2mL某浓度的氢氧化钠溶液,再滴入2~3滴酚酞溶液,氢氧化钠溶液变红色;然后振荡试管,发现红色消失。
【提出问题】红色为什么会消失?
【猜想】(1)氢氧化钠溶液的量少了;(2)酚酞溶液的量少了;(3)_____。
【查阅资料】酚酞是一种弱有机酸,在pH<8.2的溶液里为无色的内酯式结构,当pH>8.2时为红色的锟式结构;在碱性介质中很不稳定,它会慢慢地转化成无色羧酸盐。
【实验探究】根据上述“猜想”进行如下探究
(1)取4mL同浓度氢氧化钠溶液,滴入2~3滴酚酞溶液,振荡后红色消失;
(2)取2mL同浓度氢氧化钠溶液,滴入4~5滴酚酞溶液,振荡后红色消失;
(3)取2mL同浓度氢氧化钠溶液,加适量水稀释,滴入2~3滴酚酞溶液,振荡后红色没有消失。
结论:猜想_____正确。
【继续实验】取一定体积的稀氢氧化钠溶液,滴入2~3滴酚酞溶液,逐滴加入一定浓度的稀盐酸直至红色消失,写出反应的化学方程式_____。微观角度分析,该反应的实质是_____。
现象二:向碳酸钠粉末中逐滴加入稀盐酸,立即产生气泡;而向碳酸钠溶液中逐滴加入稀盐酸时,开始没有气泡,过一段时间后才有气泡产生。
【提出问题】碳酸钠溶液刚开始与稀盐酸是否发生了化学反应?
【实验探究】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的稀盐酸。
【收集证据】分别收集实验过程中不同阶段消耗盐酸的质量与生成CO2的质量,得到两者之间的关系如图1、图2所示。(忽略CO2在水中的溶解)
【合作交流】
(1)图1中A点时溶液中的溶质有_____(填化学式);
(2)图2中从B点开始的变化关系与图1完全重合,据此我们可以判断碳酸钠溶液刚开始和稀盐酸确实发生了化学反应(如图OB段所示),请你写出该反应的化学方程式_____。
【反思与评价】基于以上“异常”现象,你能提出的有价值的见解是_____(任写一点)。
五、计算题
21.厨房用泡打粉是一种复合膨松剂,又称为发泡粉,可作为快速发面剂用于制作面食。某种泡打粉的主要成分是碳酸氢钠,某化学探究小组为了测定其中碳酸氢钠的含量,他们准确称取泡打粉样品10g,向其中加入100g溶质质量分数为10%的稀盐酸,充分反应后再次称量,得溶液105.6g。忽略散失掉的水蒸气和氯化氢气体,试计算该泡打粉样品中NaHCO3的质量分数。
22.向CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,生成沉淀的质量变化与加入Na2CO3溶液质量关系如图所示;请回答问题:
(1)生成沉淀质量为____g;
(2)所用Na2CO3溶液的溶质质量分数为____。(计算结果保留一位小数)
23.某氯化钠溶液中含有氯化镁(MgCl2),学习小组为测定其中氯化镁的质量分数,在50.0g该溶液中加入50.0g氢氧化钠溶液恰好完全反应,经测定生成沉淀的质量为2.9g。请回答下列问题:
(1)反应后溶液的质量为 g。
(2)求原氯化钠溶液中氯化镁的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.B
4.D
5.C
6.B
7.D
8.C
9.D
10.A
11.C
12.C
13. 草木灰显碱性,二者能发 生化学反应生成氨气,使化肥肥效降低 不赞同 如果无限量使用化肥,会造成土壤板结;也会对水体造成污染,引起“赤 潮”“水华”等现象
14. 二氧化碳 K2CO3+2HCl=2KCl+H2O+CO2↑ 加盐酸看是否有气体生成
15. Na2CO3 Na2CO3 + H2SO4 = Na2SO4+H2O +CO2↑ 从高到低: NaOH HCl Fe O2 H2SO4和HCl(或 Fe 和Mg)
16. Na2CO3 产生白色沉淀 2NaOH+CO2=Na2CO3+H2O
17. H2SO4 BaCl2
18. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
19.(1) 长颈漏斗 水槽
(2) A##C
(3) 进入导管
(4) D##F 催化
(5) 乙 吸收尾气
20. 可能与氢氧化钠溶液浓度有关 (3) NaOH+HCl═NaCl+H2O 氢离子和氢氧根离子反应生成水分子 NaCl、NaHCO3 Na2CO3+HCl═NaCl+NaHCO3 有些化学反应是分步进行的
21.解:生成二氧化碳质量:10g+100g-105.6g=4.4g
设泡打粉样品中NaHCO3的质量为x
x=8.4g
答:该泡打粉样品中NaHCO3的质量分数为84%。
22.(1) 向CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,盐酸先和碳酸钠反应,然后氯化钙和碳酸钠反应生成碳酸钙和氯化钠,由图可知生成沉淀质量为10g。
(2)设所用Na2CO3溶液的溶质质量分数为x
由图可知,氯化钙和碳酸钠完全反应消耗的碳酸钠的质量为
答:所用Na2CO3溶液的溶质质量分数为23.6%。
23.(1)97.1
(2)解:设原氯化钠溶液中氯化镁的质量分数为x
得x=9.5%
答:原氯化钠溶液中氯化镁的质量分数为9.5%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
