科粤版(2012)第八章常见的酸、碱、盐单元测试(word版有答案)
文档属性
| 名称 | 科粤版(2012)第八章常见的酸、碱、盐单元测试(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 227.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-28 00:00:00 | ||
图片预览




文档简介
科粤版(2012)第八章 常见的酸、碱、盐
一、单选题
1.下列除去杂质的方法中,正确的是( )
选项 物质(括号内为杂质) 除去杂质的方法
A FeSO4溶液(CuSO4) 加入过量Fe粉、过滤
B CaO(CaCO3) 加水溶解、过滤
C CO2(CO) 通入适量氧气、点燃
D 盐酸(硫酸) 先加入适量的Ba(NO3)2溶液、再过滤
A.A B.B C.C D.D
2.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
3.下列有关溶液的说法正确的是( )
A.均一、稳定的液体一定是溶液
B.稀释浓硫酸时,会放出大量的热
C.降低温度,不饱和溶液一定能变成饱和溶液
D.实验室利用氯化钠固体和水配制50g质量分数为6%的氯化钠溶液的步骤是:计算、量取、溶解、贮存
4.下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D.用pH试纸测得该氢氧化钠溶液的
5.小东同学家的西红柿植株生长不茂盛,叶色淡绿需要施加的肥料是
A.尿素
B.磷矿粉
C.碳酸钾
D.磷酸二氢钾
6.下列物质间的转化一步就能实现的是
A.CaCO3→Na2CO3 B. C.CO2→O2 D.H2O2→H2
7.下列物质属于盐的是
A.NaOH B.CaO C.Cu D.CaCO3
8.中和反应在生活中有广泛应用。下列应用不属于中和反应的是
A.用盐酸除铁锈 B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤 D.用硫酸处理印染厂含碱废水
9.下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是
A.NaCl
B.NaOH
C.NaHCO3
D.Na2SO4
10.下列做法中一定发生化学变化的是( )
A.用石油分馏制得汽油、柴油等 B.用柠檬酸和小苏打、白糖配置汽水
C.用钢丝球擦除灶具上的污渍 D.用汽油清洗衣服上的油污
11.将20g质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法中不正确的是
A.实验步骤:计算、量取、混匀、装瓶贴标签
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
12.某无色混合气体可能由CH4、H2、CO、CO2和HCl中的若干种气体组成,将此混合气体通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使白色CuSO4粉末变蓝色。则原混合气体中一定含有
A.HCl和CO B.HC1、H2和CO2 C.CH4和H2 D.CO和CO2
13.小深同学用思维导图梳理了Na2CO3 的相关知识,其中描述错误的是( )
A.A B.B C.C D.D
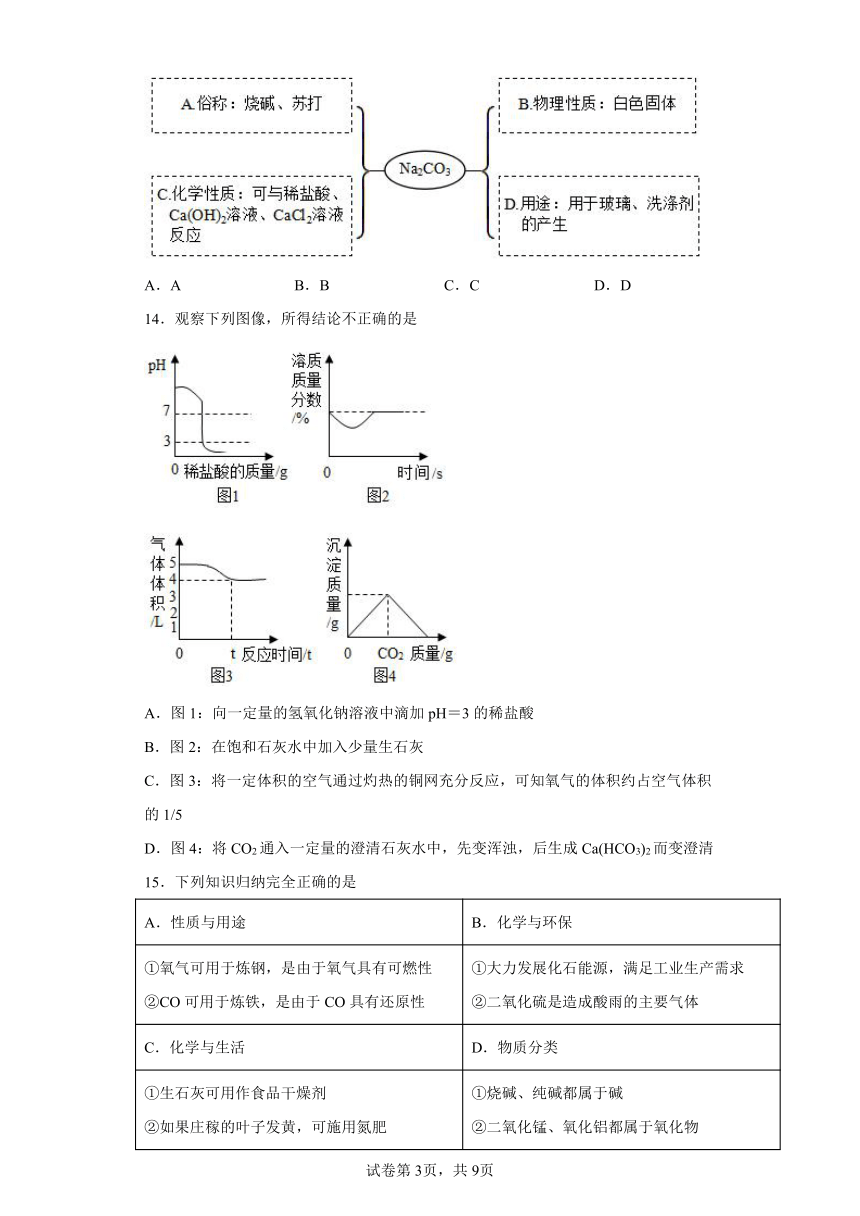
14.观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
15.下列知识归纳完全正确的是
A.性质与用途 B.化学与环保
①氧气可用于炼钢,是由于氧气具有可燃性 ②CO可用于炼铁,是由于CO具有还原性 ①大力发展化石能源,满足工业生产需求 ②二氧化硫是造成酸雨的主要气体
C.化学与生活 D.物质分类
①生石灰可用作食品干燥剂 ②如果庄稼的叶子发黄,可施用氮肥 ①烧碱、纯碱都属于碱 ②二氧化锰、氧化铝都属于氧化物
A.A B.B C.C D.D
二、填空题
16.纯净的浓盐酸是____色的液体,有_____气味,它是_____的水溶液.常用浓盐酸的质量分数是_____,浓盐酸在空气里会形成_____,这是因为浓盐酸具有挥发性,挥发出来的____气体跟空气里的____接触,形成盐酸的_____缘故.
17.化学肥料对农作物的增产具有十分重要的作用,俗话说:“庄稼一枝花,全靠肥当家”。下面是农业生产中广泛施用的几种化学肥料:①NH4NO3 ②KNO3 ③NH4Cl ④
请回答:
(1)属于复合肥料的是______(填序号,下同);
(2)属于铵态氮肥的是______,它们成分中都含有的离子是______(填符号)。
18.二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活中,有着重要的应用。
(1)二氧化碳用于制汽水,这是利用了二氧化碳____________________________的性质。
(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为________(用化学方程式表示)。
(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有______________,利用其能与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强________(选填“酸”或“碱”)性,能达到消毒杀菌的效果。
(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为______________________________________________。
19.我们的胃液中含有盐酸,它有助于消化,但胃酸过多会引起胃部不适。有时可以用小苏打治疗,反应的方程式为________________,化学反应前后一定没有变化的离子是________________(离子符号表示)。
三、综合应用题
20.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式_____.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由_____.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有_____.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如表三组探究实验.
实验方案 ①测溶液pH ②滴加Na2CO3溶液 ③滴加BaCl2溶液
实验操作
实验现象 试纸变色,与标准比色卡比照,得pH<7 _____ 产生白色沉淀
实验结论 溶液中有H2SO4 溶液中有H2SO4 溶液中有H2SO4
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定.同时也指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是_____;
(2)实验方案探究中也有一个是不合理的,这个方案是_____(选填①、②、③),不合理的原因是_____.
【剖析本质】实验后,老师又带领大家从微观的角度来理解此反应的实质,请你和同学们一起在如图反应后的方框中补画未画全的微粒____.
II.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如图实验:
试计算上述【演示实验】反应后溶液中Na2SO4的质量分数是___________?(列出计算过程)
21.现有HCl与CaCl2的混合溶液,为了分析混合溶液中HCl与CaCl2的质量分数,设计了如图所示实验方案:
【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH溶液质量增加4.4g。
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g。
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中HCl的质量分数为______(只写结果)。
(2)混合溶液中CaCl2的质量分数为_____(写出计算过程)?
(3)实验中混合溶液与Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为____(不考虑过滤中的损失。只写结果,保留小数点后一位)。
(4)若在100g混合溶液中不断加入溶质质量分数为10.6%的Na2CO3的溶液,请你在图上画出加入Na2CO3溶液的质量与产生沉淀的质量的关系图。____
22.(1)海洋中蕴藏着丰富的化学资源,从海水中提取金属镁的主要步骤如下:资料:海滩贝壳的主要成分是CaCO3
①为节约资源,试剂A常用海滩贝壳为原料制得,则试剂A为______(填化学式)。
②操作Y的名称为_______。
(2)在熔融状态下的MgCl2,通电后会生成镁与一种气体单质,该反应的化学方程式为_______;
(3)某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示(BaCl2溶液呈中性)。求:
①完全反应后生成沉淀的质量为____g;
②计算20g混合溶液中HCl的质量为多少_____?
23.2010年春我国西南大部分地区发生严重的旱灾,我们在抗旱救灾的同时,更应倡导保护水环境、珍惜水资源。请回答下列问题:
(1)不论是自来水还是纯净水,你认为保持水的化学性质的最小微粒是___________。下列选项中能确认水是由氢元素和氧元素组成的实验是_________(填序号)。
A.水的蒸馏 B.水的蒸发 C.水的电解 D.水的净化
(2)下图是我国部分地区人均水量图,从中可以看出河北是极度缺水的省。下列做法符合节约用水的是____________(填序号)。
A.使用节水龙头
B.用淘米水洗碗
C.用喷灌、滴灌方法给农作物浇水
D.使用不间断地边注水边冲淋、排水的用水量为165L/次的家用洗衣机
(3)实验室中有一杯含有MgCl2和CaCl2的硬水,下表是某兴趣小组设计软化硬水的实验方案,请你一起来完成下表。
可选用的药品有:Ca(OH)2溶液、NaOH溶液、Na2CO3溶液、肥皂水。
实验操作 现象 结论或化学方程式
①取少量硬水样品于试管中,向其中滴加Ca(OH)2溶液,直到不再产生沉淀 有白色沉淀产生 MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
②再向上述试管中滴加 ,直到不再产生沉淀 有白色沉淀产生 化学方程式:
③过滤 滤出沉淀 得到澄清滤液
④用两试管分别取等量的上述滤液和原硬水样品,分别滴加 ,振荡 盛有滤液的试管中 证明硬水已软化
____________ ____________ ____________ ____________
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.C
3.B
4.C
5.A
6.C
7.D
8.A
9.C
10.B
11.C
12.A
13.A
14.A
15.C
16. 无 刺激性 氯化氢 37% 白雾 氯化氢 水蒸气 小液滴
17. ②④ ①③④
18. 可与水反应生成碳酸 Ca(OH)2+CO2=CaCO3↓+H2O 氢氧化钠 酸 2NaCl+2H2O2NaOH+H2↑+Cl2↑
19. NaHCO3+HCl=NaCl+H2O+CO2↑ Na+ 、Cl-
20. H2SO4+2NaOH=Na2SO4 +2H2O 猜想四不合理,H2SO4和NaOH会继续反应,不可能共存 NaOH 有气泡产生 将pH试纸直接放入待测液测pH ③ 生成的Na2SO4也会与BaCl2反应产生白色沉淀,不一定是由过量H2SO4引起的 10.65%
21. 7.3% 11.1% 8.2%
22. Ca(OH)2 过滤 MgCl2Mg+Cl2↑ 4.66 2.92g
23. 水分子 C ABC Na2CO3溶液 CaCl2+Na2CO3═2NaCl+CaCO3↓ 等量的肥皂水 产生较多泡沫
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列除去杂质的方法中,正确的是( )
选项 物质(括号内为杂质) 除去杂质的方法
A FeSO4溶液(CuSO4) 加入过量Fe粉、过滤
B CaO(CaCO3) 加水溶解、过滤
C CO2(CO) 通入适量氧气、点燃
D 盐酸(硫酸) 先加入适量的Ba(NO3)2溶液、再过滤
A.A B.B C.C D.D
2.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
3.下列有关溶液的说法正确的是( )
A.均一、稳定的液体一定是溶液
B.稀释浓硫酸时,会放出大量的热
C.降低温度,不饱和溶液一定能变成饱和溶液
D.实验室利用氯化钠固体和水配制50g质量分数为6%的氯化钠溶液的步骤是:计算、量取、溶解、贮存
4.下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D.用pH试纸测得该氢氧化钠溶液的
5.小东同学家的西红柿植株生长不茂盛,叶色淡绿需要施加的肥料是
A.尿素
B.磷矿粉
C.碳酸钾
D.磷酸二氢钾
6.下列物质间的转化一步就能实现的是
A.CaCO3→Na2CO3 B. C.CO2→O2 D.H2O2→H2
7.下列物质属于盐的是
A.NaOH B.CaO C.Cu D.CaCO3
8.中和反应在生活中有广泛应用。下列应用不属于中和反应的是
A.用盐酸除铁锈 B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤 D.用硫酸处理印染厂含碱废水
9.下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是
A.NaCl
B.NaOH
C.NaHCO3
D.Na2SO4
10.下列做法中一定发生化学变化的是( )
A.用石油分馏制得汽油、柴油等 B.用柠檬酸和小苏打、白糖配置汽水
C.用钢丝球擦除灶具上的污渍 D.用汽油清洗衣服上的油污
11.将20g质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法中不正确的是
A.实验步骤:计算、量取、混匀、装瓶贴标签
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
12.某无色混合气体可能由CH4、H2、CO、CO2和HCl中的若干种气体组成,将此混合气体通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使白色CuSO4粉末变蓝色。则原混合气体中一定含有
A.HCl和CO B.HC1、H2和CO2 C.CH4和H2 D.CO和CO2
13.小深同学用思维导图梳理了Na2CO3 的相关知识,其中描述错误的是( )
A.A B.B C.C D.D
14.观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
15.下列知识归纳完全正确的是
A.性质与用途 B.化学与环保
①氧气可用于炼钢,是由于氧气具有可燃性 ②CO可用于炼铁,是由于CO具有还原性 ①大力发展化石能源,满足工业生产需求 ②二氧化硫是造成酸雨的主要气体
C.化学与生活 D.物质分类
①生石灰可用作食品干燥剂 ②如果庄稼的叶子发黄,可施用氮肥 ①烧碱、纯碱都属于碱 ②二氧化锰、氧化铝都属于氧化物
A.A B.B C.C D.D
二、填空题
16.纯净的浓盐酸是____色的液体,有_____气味,它是_____的水溶液.常用浓盐酸的质量分数是_____,浓盐酸在空气里会形成_____,这是因为浓盐酸具有挥发性,挥发出来的____气体跟空气里的____接触,形成盐酸的_____缘故.
17.化学肥料对农作物的增产具有十分重要的作用,俗话说:“庄稼一枝花,全靠肥当家”。下面是农业生产中广泛施用的几种化学肥料:①NH4NO3 ②KNO3 ③NH4Cl ④
请回答:
(1)属于复合肥料的是______(填序号,下同);
(2)属于铵态氮肥的是______,它们成分中都含有的离子是______(填符号)。
18.二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活中,有着重要的应用。
(1)二氧化碳用于制汽水,这是利用了二氧化碳____________________________的性质。
(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为________(用化学方程式表示)。
(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有______________,利用其能与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强________(选填“酸”或“碱”)性,能达到消毒杀菌的效果。
(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为______________________________________________。
19.我们的胃液中含有盐酸,它有助于消化,但胃酸过多会引起胃部不适。有时可以用小苏打治疗,反应的方程式为________________,化学反应前后一定没有变化的离子是________________(离子符号表示)。
三、综合应用题
20.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式_____.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由_____.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有_____.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如表三组探究实验.
实验方案 ①测溶液pH ②滴加Na2CO3溶液 ③滴加BaCl2溶液
实验操作
实验现象 试纸变色,与标准比色卡比照,得pH<7 _____ 产生白色沉淀
实验结论 溶液中有H2SO4 溶液中有H2SO4 溶液中有H2SO4
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定.同时也指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是_____;
(2)实验方案探究中也有一个是不合理的,这个方案是_____(选填①、②、③),不合理的原因是_____.
【剖析本质】实验后,老师又带领大家从微观的角度来理解此反应的实质,请你和同学们一起在如图反应后的方框中补画未画全的微粒____.
II.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如图实验:
试计算上述【演示实验】反应后溶液中Na2SO4的质量分数是___________?(列出计算过程)
21.现有HCl与CaCl2的混合溶液,为了分析混合溶液中HCl与CaCl2的质量分数,设计了如图所示实验方案:
【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH溶液质量增加4.4g。
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g。
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中HCl的质量分数为______(只写结果)。
(2)混合溶液中CaCl2的质量分数为_____(写出计算过程)?
(3)实验中混合溶液与Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为____(不考虑过滤中的损失。只写结果,保留小数点后一位)。
(4)若在100g混合溶液中不断加入溶质质量分数为10.6%的Na2CO3的溶液,请你在图上画出加入Na2CO3溶液的质量与产生沉淀的质量的关系图。____
22.(1)海洋中蕴藏着丰富的化学资源,从海水中提取金属镁的主要步骤如下:资料:海滩贝壳的主要成分是CaCO3
①为节约资源,试剂A常用海滩贝壳为原料制得,则试剂A为______(填化学式)。
②操作Y的名称为_______。
(2)在熔融状态下的MgCl2,通电后会生成镁与一种气体单质,该反应的化学方程式为_______;
(3)某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示(BaCl2溶液呈中性)。求:
①完全反应后生成沉淀的质量为____g;
②计算20g混合溶液中HCl的质量为多少_____?
23.2010年春我国西南大部分地区发生严重的旱灾,我们在抗旱救灾的同时,更应倡导保护水环境、珍惜水资源。请回答下列问题:
(1)不论是自来水还是纯净水,你认为保持水的化学性质的最小微粒是___________。下列选项中能确认水是由氢元素和氧元素组成的实验是_________(填序号)。
A.水的蒸馏 B.水的蒸发 C.水的电解 D.水的净化
(2)下图是我国部分地区人均水量图,从中可以看出河北是极度缺水的省。下列做法符合节约用水的是____________(填序号)。
A.使用节水龙头
B.用淘米水洗碗
C.用喷灌、滴灌方法给农作物浇水
D.使用不间断地边注水边冲淋、排水的用水量为165L/次的家用洗衣机
(3)实验室中有一杯含有MgCl2和CaCl2的硬水,下表是某兴趣小组设计软化硬水的实验方案,请你一起来完成下表。
可选用的药品有:Ca(OH)2溶液、NaOH溶液、Na2CO3溶液、肥皂水。
实验操作 现象 结论或化学方程式
①取少量硬水样品于试管中,向其中滴加Ca(OH)2溶液,直到不再产生沉淀 有白色沉淀产生 MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
②再向上述试管中滴加 ,直到不再产生沉淀 有白色沉淀产生 化学方程式:
③过滤 滤出沉淀 得到澄清滤液
④用两试管分别取等量的上述滤液和原硬水样品,分别滴加 ,振荡 盛有滤液的试管中 证明硬水已软化
____________ ____________ ____________ ____________
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.C
3.B
4.C
5.A
6.C
7.D
8.A
9.C
10.B
11.C
12.A
13.A
14.A
15.C
16. 无 刺激性 氯化氢 37% 白雾 氯化氢 水蒸气 小液滴
17. ②④ ①③④
18. 可与水反应生成碳酸 Ca(OH)2+CO2=CaCO3↓+H2O 氢氧化钠 酸 2NaCl+2H2O2NaOH+H2↑+Cl2↑
19. NaHCO3+HCl=NaCl+H2O+CO2↑ Na+ 、Cl-
20. H2SO4+2NaOH=Na2SO4 +2H2O 猜想四不合理,H2SO4和NaOH会继续反应,不可能共存 NaOH 有气泡产生 将pH试纸直接放入待测液测pH ③ 生成的Na2SO4也会与BaCl2反应产生白色沉淀,不一定是由过量H2SO4引起的 10.65%
21. 7.3% 11.1% 8.2%
22. Ca(OH)2 过滤 MgCl2Mg+Cl2↑ 4.66 2.92g
23. 水分子 C ABC Na2CO3溶液 CaCl2+Na2CO3═2NaCl+CaCO3↓ 等量的肥皂水 产生较多泡沫
答案第1页,共2页
答案第1页,共2页
