粤教版化学九年级下册同步提优训练 6.4 珍惜和保护金属资源(word版有答案)
文档属性
| 名称 | 粤教版化学九年级下册同步提优训练 6.4 珍惜和保护金属资源(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 108.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-29 00:00:00 | ||
图片预览

文档简介
数学
化学
6.4 珍惜和保护金属资源
核心点拨
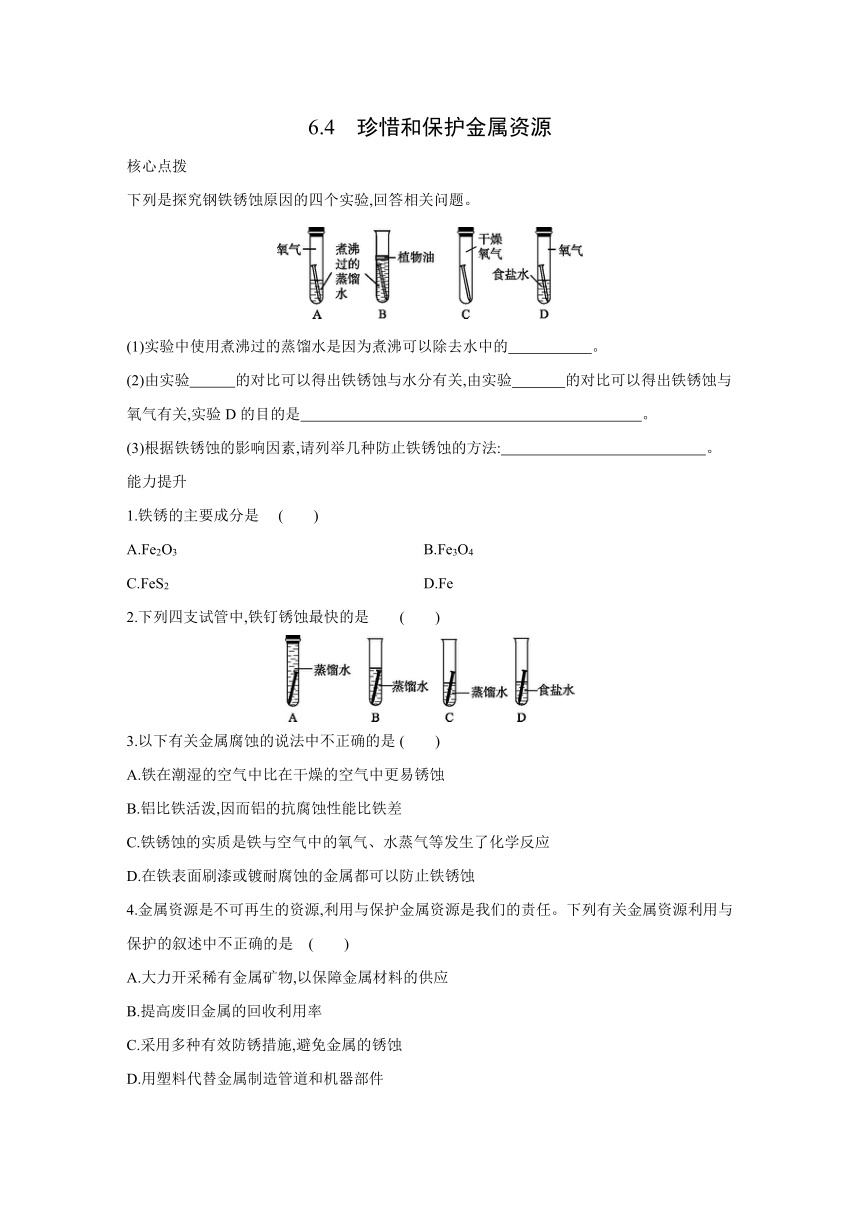
下列是探究钢铁锈蚀原因的四个实验,回答相关问题。
(1)实验中使用煮沸过的蒸馏水是因为煮沸可以除去水中的 。
(2)由实验 的对比可以得出铁锈蚀与水分有关,由实验 的对比可以得出铁锈蚀与氧气有关,实验D的目的是 。
(3)根据铁锈蚀的影响因素,请列举几种防止铁锈蚀的方法: 。
能力提升
1.铁锈的主要成分是 ( )
A.Fe2O3 B.Fe3O4
C.FeS2 D.Fe
2.下列四支试管中,铁钉锈蚀最快的是 ( )
3.以下有关金属腐蚀的说法中不正确的是 ( )
A.铁在潮湿的空气中比在干燥的空气中更易锈蚀
B.铝比铁活泼,因而铝的抗腐蚀性能比铁差
C.铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学反应
D.在铁表面刷漆或镀耐腐蚀的金属都可以防止铁锈蚀
4.金属资源是不可再生的资源,利用与保护金属资源是我们的责任。下列有关金属资源利用与保护的叙述中不正确的是 ( )
A.大力开采稀有金属矿物,以保障金属材料的供应
B.提高废旧金属的回收利用率
C.采用多种有效防锈措施,避免金属的锈蚀
D.用塑料代替金属制造管道和机器部件
5.[2020·宜昌] 线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如图所示实验,探究铁生锈的条件。下列说法错误的是 ( )
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙、丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
6.[2020·怀化] “雪龙2号”的船身等主要由金属材料制成,下列金属防护措施不正确的是 ( )
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
7.化学源于生活,生活中蕴含着许多化学知识,请回答下列问题。
(1)铁制品涂油能防锈的原理是 。回收利用废旧金属的目的之一是 。
(2)铝的金属活动性较强,但可以制成铝制品长期使用,原因是 。
(3)“双吸剂”的主要成分之一为铁粉,常用于食品保鲜,其原理是 。
8.暖贴发热是利用了铁粉生锈放出热量的原理,某小组同学设计并进行实验,探究铁生锈的条件及影响铁生锈速率的因素。
Ⅰ.探究铁生锈的条件
(1)由实验B和C得出铁生锈需要与水接触,画出实验C的实验装置图。
(2)证明铁生锈需要与氧气接触的实验现象是 。
Ⅱ.探究影响铁生锈速率的因素
[查阅资料] 暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
[猜想假设]
①活性炭能加快铁生锈的速率。
②食盐能加快铁生锈的速率。
[进行实验] 下表是2 g铁粉、5 g水与不同量活性炭、食盐均匀混合后,在10 min内温度上升的实验记录。
实验编号 活性炭质量/g 食盐质量/g 温度上升值/℃
1 0 0 0.1
2 0.2 0 22.0
3 x 0.1 3.1
4 0.2 0.1 56.3
[解释与结论]
(3)表中x的值为 。
(4)对比实验1和3,得出的结论是 。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,需要对比 (填实验编号)。
[反思与评价]
(6)下列说法正确的是 (填字母)。
A.暖贴在使用前要密封保存
B.暖贴使用后剩余物可以回收利用
C.利用铁生锈的原理,铁粉还可用于食品保鲜
9.改革开放以来,我国钢铁工业飞速发展,近年来钢铁产量已稳居世界首位。某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,反应原理为Fe2O3+3CO2Fe+3CO2。若该厂日产含铁1.4×104 t的生铁,至少需要含Fe2O3 80%的赤铁矿的质量是多少 (要求写出计算过程)
10.电镀是利用镀层金属或其他不溶性材料作为阳极,待镀金属作为阴极,镀层金属的阳离子在待镀金属表面被还原形成镀层。我国第5套人民币中的一元硬币材料为钢芯镀镍,依据你所理解的电镀原理,你认为在制作硬币时,阳极是 ,阴极是 。
6.4 珍惜和保护金属资源
核心点拨
(1)氧气 (2)A、C A、B 探究食盐对铁生锈的影响
(3)喷漆、涂油、烤蓝、搪瓷、镀上一层耐腐蚀的金属、制成合金等(合理即可)
能力提升
1.A 2.D
3.B 铝比铁活泼,但是铝在常温下能够与空气中的氧气反应,从而在表面形成一层致密的氧化膜,阻止铝进一步被氧化,因而铝的抗腐蚀性能比铁强。
4.A 5.C
6.D 在金属制品表面镀保护层、刷漆或是涂油,能使金属和空气或水隔绝,防止金属生锈;合金往往具有良好的抗腐蚀性,制成合金后使用,能防止生锈;稀盐酸是酸性物质,用稀盐酸定期清洗金属制品,会加速锈蚀。
7.(1)隔绝氧气和水 能节约有限的金属资源(或减少环境污染)
(2)铝表面易形成一层致密的氧化物膜
(3)铁常温下能和氧气、水反应
8.(1)如图所示(合理即可)
(2)A中铁钉不生锈,B中铁钉生锈
(3)0
(4)食盐能加快铁生锈的速率 (5)1、2、3、4(或2、3、4)
(6)ABC
9.解:设需要含Fe2O3 80%的赤铁矿的质量是x。
Fe2O3+3CO2Fe+3CO2
160 112
x×80% 1.4×104 t
=
x=2.5×104 t
答:需要含Fe2O3 80%的赤铁矿的质量是2.5×104 t。
10.镍 钢芯
根据题给信息可知镀层金属作为阳极,待镀金属作为阴极,则用钢芯镀镍材料制作一元硬币时,阳极为镍,阴极为钢芯。
化学
6.4 珍惜和保护金属资源
核心点拨
下列是探究钢铁锈蚀原因的四个实验,回答相关问题。
(1)实验中使用煮沸过的蒸馏水是因为煮沸可以除去水中的 。
(2)由实验 的对比可以得出铁锈蚀与水分有关,由实验 的对比可以得出铁锈蚀与氧气有关,实验D的目的是 。
(3)根据铁锈蚀的影响因素,请列举几种防止铁锈蚀的方法: 。
能力提升
1.铁锈的主要成分是 ( )
A.Fe2O3 B.Fe3O4
C.FeS2 D.Fe
2.下列四支试管中,铁钉锈蚀最快的是 ( )
3.以下有关金属腐蚀的说法中不正确的是 ( )
A.铁在潮湿的空气中比在干燥的空气中更易锈蚀
B.铝比铁活泼,因而铝的抗腐蚀性能比铁差
C.铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学反应
D.在铁表面刷漆或镀耐腐蚀的金属都可以防止铁锈蚀
4.金属资源是不可再生的资源,利用与保护金属资源是我们的责任。下列有关金属资源利用与保护的叙述中不正确的是 ( )
A.大力开采稀有金属矿物,以保障金属材料的供应
B.提高废旧金属的回收利用率
C.采用多种有效防锈措施,避免金属的锈蚀
D.用塑料代替金属制造管道和机器部件
5.[2020·宜昌] 线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如图所示实验,探究铁生锈的条件。下列说法错误的是 ( )
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙、丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
6.[2020·怀化] “雪龙2号”的船身等主要由金属材料制成,下列金属防护措施不正确的是 ( )
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
7.化学源于生活,生活中蕴含着许多化学知识,请回答下列问题。
(1)铁制品涂油能防锈的原理是 。回收利用废旧金属的目的之一是 。
(2)铝的金属活动性较强,但可以制成铝制品长期使用,原因是 。
(3)“双吸剂”的主要成分之一为铁粉,常用于食品保鲜,其原理是 。
8.暖贴发热是利用了铁粉生锈放出热量的原理,某小组同学设计并进行实验,探究铁生锈的条件及影响铁生锈速率的因素。
Ⅰ.探究铁生锈的条件
(1)由实验B和C得出铁生锈需要与水接触,画出实验C的实验装置图。
(2)证明铁生锈需要与氧气接触的实验现象是 。
Ⅱ.探究影响铁生锈速率的因素
[查阅资料] 暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
[猜想假设]
①活性炭能加快铁生锈的速率。
②食盐能加快铁生锈的速率。
[进行实验] 下表是2 g铁粉、5 g水与不同量活性炭、食盐均匀混合后,在10 min内温度上升的实验记录。
实验编号 活性炭质量/g 食盐质量/g 温度上升值/℃
1 0 0 0.1
2 0.2 0 22.0
3 x 0.1 3.1
4 0.2 0.1 56.3
[解释与结论]
(3)表中x的值为 。
(4)对比实验1和3,得出的结论是 。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,需要对比 (填实验编号)。
[反思与评价]
(6)下列说法正确的是 (填字母)。
A.暖贴在使用前要密封保存
B.暖贴使用后剩余物可以回收利用
C.利用铁生锈的原理,铁粉还可用于食品保鲜
9.改革开放以来,我国钢铁工业飞速发展,近年来钢铁产量已稳居世界首位。某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,反应原理为Fe2O3+3CO2Fe+3CO2。若该厂日产含铁1.4×104 t的生铁,至少需要含Fe2O3 80%的赤铁矿的质量是多少 (要求写出计算过程)
10.电镀是利用镀层金属或其他不溶性材料作为阳极,待镀金属作为阴极,镀层金属的阳离子在待镀金属表面被还原形成镀层。我国第5套人民币中的一元硬币材料为钢芯镀镍,依据你所理解的电镀原理,你认为在制作硬币时,阳极是 ,阴极是 。
6.4 珍惜和保护金属资源
核心点拨
(1)氧气 (2)A、C A、B 探究食盐对铁生锈的影响
(3)喷漆、涂油、烤蓝、搪瓷、镀上一层耐腐蚀的金属、制成合金等(合理即可)
能力提升
1.A 2.D
3.B 铝比铁活泼,但是铝在常温下能够与空气中的氧气反应,从而在表面形成一层致密的氧化膜,阻止铝进一步被氧化,因而铝的抗腐蚀性能比铁强。
4.A 5.C
6.D 在金属制品表面镀保护层、刷漆或是涂油,能使金属和空气或水隔绝,防止金属生锈;合金往往具有良好的抗腐蚀性,制成合金后使用,能防止生锈;稀盐酸是酸性物质,用稀盐酸定期清洗金属制品,会加速锈蚀。
7.(1)隔绝氧气和水 能节约有限的金属资源(或减少环境污染)
(2)铝表面易形成一层致密的氧化物膜
(3)铁常温下能和氧气、水反应
8.(1)如图所示(合理即可)
(2)A中铁钉不生锈,B中铁钉生锈
(3)0
(4)食盐能加快铁生锈的速率 (5)1、2、3、4(或2、3、4)
(6)ABC
9.解:设需要含Fe2O3 80%的赤铁矿的质量是x。
Fe2O3+3CO2Fe+3CO2
160 112
x×80% 1.4×104 t
=
x=2.5×104 t
答:需要含Fe2O3 80%的赤铁矿的质量是2.5×104 t。
10.镍 钢芯
根据题给信息可知镀层金属作为阳极,待镀金属作为阴极,则用钢芯镀镍材料制作一元硬币时,阳极为镍,阴极为钢芯。
