9.1认识溶液 基础夯实(含解析)—2021_2022学年九年级化学京改版(2013)下册
文档属性
| 名称 | 9.1认识溶液 基础夯实(含解析)—2021_2022学年九年级化学京改版(2013)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 111.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-30 00:00:00 | ||
图片预览




文档简介
9.1认识溶液
一、选择题(共16题)
1.把少量下列物质分别放入水中充分搅拌,可以得到溶液的是
A.面粉 B.白糖 C.花生油 D.辣椒粉
2.下列关于溶液的说法正确的是
A.溶液一定是混合物 B.饱和溶液一定是浓溶液
C.溶液都是无色的 D.均一、稳定的液体一定是溶液
3.关于溶液的说法正确的是
A.溶液中的溶质可以是一种或多种
B.溶液上层的密度小,下层的密度大
C.长期放置不分层的液体就是溶液
D.溶液一定是无色、澄清的
4.下列有关溶液的说法中,错误的是( )
A.溶液具有均一性和稳定性
B.物质的溶解过程通常会伴随着能量的变化
C.饱和溶液一定是浓溶液
D.改变条件,能够使饱和溶液与不饱和溶液相互转化
5.下列叙述正确的是
A.不同种元素最本质的区别是质子数不同
B.核电荷数少于核外电子数的一定是阳离子
C.粗盐经溶解、过滤、蒸发提纯后的盐是纯净物
D.凡是均一、稳定的液体一定是溶液
6.下列措施中,不能加快蔗糖在水中溶解速度的是
A.升高温度 B.用玻璃棒搅拌
C.将颗粒磨碎 D.多加蔗糖
7.生活中的下列物质,溶于水形成溶液的是
A.面粉 B.蔗糖 C.植物油 D.木炭
8.下列有关溶液的说法,正确的是
A.溶液通常是液体,溶质一定是固体
B.凡是溶液一定是混合物
C.一种物质分散到另一种物质中,形成的液体是溶液
D.无色透明的液体是溶液
9.某学生利用身边常见的物质解决日常生活中的有关问题,下列方法中不正确的是( )
A.用木炭除去冰箱中的异味 B.用汽油清洗衣服上的油污
C.用明矾净化浑浊的生活用水 D.用食盐水除水瓶中的水垢
10.下列物质放入水中,能形成溶液的是
A.白糖 B.牛奶 C.面粉 D.花生油
11.下列物质分散到水中能形成溶液的是
A.面粉 B.葡萄糖 C.山茶油 D.汽油
12.下列方法中,利用了乳化功能的是
A.用汽油清洗沾有碘的试管
B.用洗洁精清洗餐具上的油污
C.用水冲洗杯子上的蔗糖
D.用明矾净化黄泥水
13.下列物质放入水中,不能形成溶液的是
A.食盐 B.植物油 C.硝酸钾 D.白酒
14.已知:20℃时,NaCl和NaNO3的溶解度分别为36 g和88 g。
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
上表是20℃时实验得出的数据,根据该数据,则下列关于①~⑤所得溶液的说法不正确的是A.溶质质量:②=④ B.溶液质量: ①<②
C.溶质质量分数:①=③ D.⑤中溶质与溶剂的质量比为22:25
15.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是
A.面粉 B.氯化钠 C.泥土 D.乳胶漆
16.2018年世界水日的主题是“借自然之力,护绿水青山”。下列有关水的说法,正确的是
A.水是由氢气和氧气组成的
B.含可溶性钙、镁化合物较多的水叫做软水
C.冰水混合物是纯净物
D.油脂在水中融化后形成溶液
二、综合题(共6题)
17.化学使世界更美好。请用所学化学知识回答下列问题。
Ⅰ.现有氢气、氦气、二氧化碳、食盐、金刚石、生石灰等物质,请按要求用化学式填写:
①飞艇中充入的气体是________; ②切割玻璃的是________;
③用作干燥剂的是_________; ④用作调味品的是_______。
Ⅱ.回答下列与含碳物质有关的问题
①石墨能用于制作干电池电极,说明石墨能__________;
②制糖工业中利用活性炭的__________性脱色制白糖;
③CO2通入汽水中可制作碳酸饮料,反应的化学方程式______________;
④炼铁时发生反应:,其中____做还原剂;
⑤在2Mg+CO22MgO+C中,反应前后碳元素的存在形态由_____(填编号)。
A.游离态到化合态 B. 化合态到游离态
Ⅲ. 某病人注射用的生理盐水(含0.85~0.90%的氯化钠)中添加了适量的葡萄糖(C6H12O6)以补充能量。该注射液中的溶质为_____;葡萄糖分子中碳,氢,氧元素的质量之比是______;1个葡萄糖分子中共含___________个原子;葡萄糖中质量分数最高是____元素;1mol 该葡萄糖中约含有___________个葡萄糖分子;
18.水是常用溶剂,某同学进行如图实验。
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是______。
(2)实验可知,溶质状态可以是______。
(3)实验结束后,用洗涤剂洗净B试管,原理是______。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知: ,X的化学式为______。
(5)询问老师得知用可处理Cl2,根据化学方程式计算,处理0.142gCl2至少需NaOH的质量是多少______?
19.水是人类宝贵的资源。
(1)下列物质加入水中能形成溶液的是________(填序号,下同),能形成乳浊液的是________。
a.植物油 b.蔗糖 c.粉笔灰
(2)NaCl能溶于水,难溶于植物油;NaCl在热水中溶解的质量比在等质量的冷水中溶解的质量大。这说明,物质的溶解能力与_____________________和__________有关。
(3)净化水常用方法有沉降、过滤、吸附和蒸馏,活性炭在净水器中起到过滤和______的作用,从盐水中获得饮用水,可采取的方法是______。
20.水是生命的源泉,是人类最宝贵的资源
(1)自来水净化天然水的主要步骤如图所示:试剂X可以用_____,净化后的水是_____(选填“纯净物”或“混合物”)
(2)水是一种最常用的溶剂,将下列生活中的物质分别放入水中,能形成溶液的是_____
A面粉 B冰块 C冰糖 D花生油
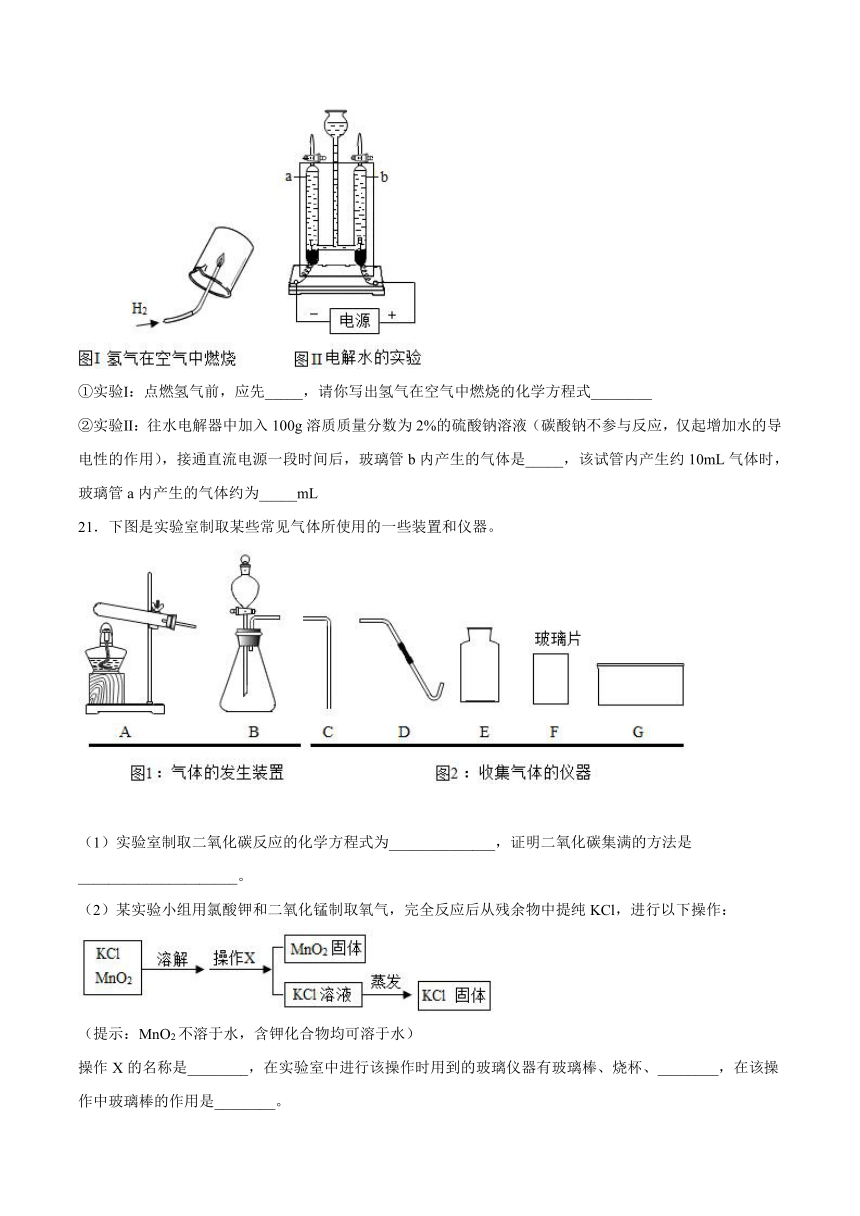
(3)某化学兴趣小组的同学利用以下两个实验验证水的组成
①实验Ⅰ:点燃氢气前,应先_____,请你写出氢气在空气中燃烧的化学方程式________
②实验Ⅱ:往水电解器中加入100g溶质质量分数为2%的硫酸钠溶液(碳酸钠不参与反应,仅起增加水的导电性的作用),接通直流电源一段时间后,玻璃管b内产生的气体是_____,该试管内产生约10mL气体时,玻璃管a内产生的气体约为_____mL
21.下图是实验室制取某些常见气体所使用的一些装置和仪器。
(1)实验室制取二氧化碳反应的化学方程式为______________,证明二氧化碳集满的方法是_____________________。
(2)某实验小组用氯酸钾和二氧化锰制取氧气,完全反应后从残余物中提纯KCl,进行以下操作:
(提示:MnO2不溶于水,含钾化合物均可溶于水)
操作X的名称是________,在实验室中进行该操作时用到的玻璃仪器有玻璃棒、烧杯、________,在该操作中玻璃棒的作用是________。
22.根据下列仪器装置,回答有关问题。
(1)制取氧气。实验室选用装置A制取氧气时,用到的化学药品是______(用化学式表示);收集氧气可以选用的装置是______填装置序号)。实验结束熄灭酒精灯的操作为______。
(2)制取二氧化碳。用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为______。为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为____→H→____→干燥、纯净CO2 (在括号内填装置序号)。
(3)进一步探究二氧化碳与氢氧化钠溶液的反应。
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3。向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3=Na2CO3+H2O;Ca(HCO3)2溶于水。
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④______。
【实验】请你参与下列验证猜想③的实验,完成探究报告。
步骤和方法 现象 分析
取少量反应后的溶液,加入足量的CaCl2溶液 ______ 发生反应的方程式:______
______ 产生白色沉淀 结论:猜想③正确
【讨论】二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素是______。
试卷第1页,共3页
参考答案:
1.B
【详解】
A、面粉是一种不溶于水的粉末,与水混合后形成悬浊液,选项错误;
B、白糖是一种能够溶于水的固体,与水混合后形成均一、稳定的溶液,选项正确;
C、花生油是一种不溶于水的液体,与水混合后形成乳浊液,选项错误;
D、辣椒粉是一种不溶于水的粉末,与水混合后形成悬浊液,选项错误;
故选B。
2.A
【详解】
A、溶液是均一、稳定的混合物,故A正确;
B、饱和溶液不一定是浓溶液,如氢氧化钙溶液达到饱和时也是稀溶液,故B错误;
C、溶液都不一定是无色的,有的溶液是有颜色的,如硫酸铜溶液是蓝色的,故C错误;
D、均一、稳定的液体不一定是溶液,如水,故D错误。故选A。
3.A
【详解】
A.溶液中的溶质可以是一种或多种,如食盐水中溶质只有食盐,海水中溶质有许多种,选项正确;
B.溶液是均一的,溶液上层的密度和下层的密度相同,选项错误;
C.长期放置不分层的液体混合物可能是溶液,选项错误;
D.溶液不一定是无色的,如硫酸铜溶液是蓝色的,选项错误。
故选A。
4.C
【详解】
A、溶液是均一稳定的混合物,溶液具有均一性和稳定性,故选项说法正确;B、物质的溶解过程通常会伴随着能量的变化,故选项说法正确;C、饱和溶液不一定是浓溶液,也可能是稀溶液,如氢氧化钙的饱和溶液为稀溶液,故选项说法错误;D、改变条件,能够使饱和溶液与不饱和溶液相互转化,故选项说法正确。故选C。
5.A
【详解】
A、元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,故选项说法正确;
B、核电荷数少于核外电子数的粒子带负电荷,一定是阴离子,故选项说法错误;
C、粗盐经溶解、过滤、蒸发提纯后的盐仍含有可溶性的化合物,如氯化钙、氯化镁等,属于混合物,故选项说法错误;
D、溶液的特点是均一稳定的混合物,均一、稳定的液体不一定是混合物,例如水不属于溶液,故选项说法错误。
故选A。
6.D
【详解】
A、升高温度,能加快分子运动速度,能加快固体物质与水的接触机会,从而加快了固体物质的溶解速度,故选项错误。
B、用玻璃棒不断搅拌,能加快分子运动速度,能加快固体物质与水的接触机会,从而加快了固体物质的溶解速度,故选项错误。
C、固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率,将固体研成粉末增加了蔗糖与水的接触面积,加快了固体物质的溶解速度,故选项错误。
D、多加蔗糖不能加快蔗糖在水中溶解速度,故选项正确。
故选D。
7.B
【详解】
由一种物质或几种物质分散到另一种物质中形成均一的、稳定的混合物为溶液,植物油、面粉都不溶于水中,不能形成溶液,木炭不溶于水,不能形成溶液。
8.B
【详解】
A、溶液通常是液体,溶质可以是固体、液体或气体,故选项说法错误;
B、溶液的本质特征是均一性、稳定性,属于混合物;故选项说法正确;
C、一种物质分散到另一种物质中,形成的液体不一定是均一的、稳定的,故不一定是溶液;故选项说法错误;
D、无色透明的液体不一定是溶液,如水是均一的、稳定的液体,但不是溶液;故选项说法错误。故选B。
9.D
【详解】
A、木炭具有吸附作用,可以用木炭可以除去冰箱中的异味,故A正确;
B、油污易溶于汽油,可以用汽油可以清洗衣服上的油污,故B正确;
C、明矾溶于水生成胶状物质,能够吸附水中的悬浮物,用明矾可以净化浑浊的生活用水,故C正确;
D、食盐主要成分是氯化钠,氯化钠溶液是中性物质,不能和水垢成分(碳酸钙、氢氧化镁等)反应,不能用食盐水不能除水瓶中的水垢,故D不正确。故选D。
10.A
【详解】
A、白糖易溶于水,形成均一、稳定的混合物,属于溶液,故选项正确;
B、牛奶是不溶性的小液滴等分散到液体中形成的,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
C、面粉不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
D、花生油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误。
11.B
【详解】
A、面粉不溶于水,不能形成溶液,故A不正确;
B、葡萄糖易溶于水,形成的均一的、稳定的葡萄糖溶液,故B正确;
C、山茶油不溶于水,不能形成溶液,故C不正确;
D、汽油是有机溶剂,不溶于水,不能形成溶液,故D不正确。故选B。
12.B
【详解】
A、碘能溶解在汽油中,属于溶解现象,因此可用汽油清洗沾有碘的试管;故选项错误;
B、利用洗洁精的乳化功能清洗餐具上的油污;故选项正确;
C、水能溶解蔗糖,用水冲洗杯子上的蔗糖属于溶解现象;故选项错误;
D、明矾溶于水后形成的胶状物能吸附水中的杂质从而达到净水的目的,不是乳化作用;故选项错误。
故选:B。
13.B
【详解】
A. 食盐,易溶于水,正确;B. 植物油,难溶于水,错误;C. 硝酸钾,易溶于水,正确;D. 白酒,易溶于水,正确。故选B。
14.A
【详解】
A、溶液②中溶质的质量为36g,④中溶质的质量为60g,故错误,符合题意;
B、溶液①的质量为:30g+100g=130g;溶液②的质量为:36g+100g=136g,溶液质量:①<②,故正确,不符合题意;
C、溶液①和③均是在100g水中溶解了30g溶质所得溶液中溶质的质量分数相等,故正确,不符合题意;
D、溶液⑤是在100g水中溶解了88g硝酸钠,所以⑤中溶质与溶剂的质量比为88:100=22:25,故正确,不符合题意。
故选A。
15.B
【详解】
溶液是均一稳定的混合物,在溶液中物质以分子或离子等微观粒子的的形式相互混合,因没有阻挡光线的微粒,所以溶液都是澄清透明的。面粉 、泥土 、乳胶漆和水混合否不能得到均一稳定的混合物,都不是溶液;氯化钠和水形成的是均一稳定的混合物,是溶液。选B
16.C
【详解】
A、水是由氢元素和氧元素组成的,故错误;
B、含可溶性钙、镁化合物较多的水叫做硬水,故错误;
C、冰和水都是水,是由一种物质组成的,故是纯净物,故正确;
D、油脂溶解在水中,不能形成溶液,形成的是乳浊液,故错误。故选C。
17. He C CaO NaCl 导电 吸附 略 CO B 氯化钠 葡萄糖 6:1:8 24 O 6.02 1023
【详解】
Ⅰ、①氦气的密度小且化学性质不活泼,不易的发生爆炸,故常用来充灌载人飞艇,化学式为:He;②金刚石用于切割玻璃,化学式为:C;③生石灰能与水反应生成氢氧化钙,可做干燥剂,化学式为:CaO;④食盐是常用的调味品,化学式为:NaCl;Ⅱ、①石墨能用于制作干电池电极,说明石墨具有导电性;②制糖工业中利用活性炭的吸附性脱色制白糖;③CO2通入汽水中可制作碳酸饮料,反应的化学方程式CO2+H2O=H2CO3;④炼铁时发生反应:3CO+Fe2O32Fe+3CO2,其中一氧化碳得到氧,发生了氧化反应,具有还原性;⑤在2Mg+CO22MgO+C中,碳元素由化合物转化为了单质,所以反应前后碳元素的存在形态由化合态到游离态;Ⅲ、该注射液中含有氯化钠和葡萄糖两种溶质;由葡萄糖的化学式可知,一个葡萄糖分子中含有6个碳原子、12个氢原子和6个氧原子,共24个原子;原子的物质的量之比为C:H:O=1:2:1;葡萄糖是由碳、氢、氧三种元素组成的,碳、氢、氧三种元素的质量比为:(12×6):(1×12):(16×6)=6:1:8,可见其中氧元素的质量分数最高;1mol 该葡萄糖中约含有6.02 1023个葡萄糖分子。
18. 一开始,液体分层,上层为无色,下层为红色,过一段时间后,溶液变为均匀的红色 气态、液态、固态 乳化作用 MnCl2 解:设至少需要氢氧化钠的质量是x
x=0.16g
答:至少需要氢氧化钠的质量是0.16g。
【详解】
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,乙醇的密度比水小,故一开始,液体分层,上层为无色,下层为红色,乙醇能与水以任意比例互溶,由于分子在不断运动,一定时间后,乙醇溶于水,形成均一、稳定的混合物,故最后溶液变为均匀的红色,故现象为:一开始,液体分层,上层为无色,下层为红色,过一段时间后,溶液变为均匀的红色;
(2)酒精溶于水,溶质是酒精,酒精是液态,高锰酸钾溶于水,溶质是高锰酸钾,高锰酸钾是固态,氯化氢溶于水,溶质是氯化氢,氯化氢是气态,故溶质状态可以是:气态、液态、固态;
(3)用洗涤剂清洗B试管,是因为洗涤剂中含有乳化剂,具有乳化作用,能将油污乳化为细小油滴,随水冲走,故填:乳化作用;
(4)根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含K、Mn、O、H、Cl的个数分别是2、2、8、16、16,生成物中含K、Mn、O、H、Cl的个数分别是2、0、8、16、12,故生成物中还应含2个Mn、4个Cl,故X的化学式为:MnCl2;
(5)见答案。
19. b a 溶剂种类 温度 吸附 蒸馏
【详解】
(1)在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物属于溶液,蔗糖易溶于水,形成均一、稳定的混合物,属于溶液;植物油不溶于水,与水混合形成乳浊液;(2)水和植物油属于溶剂种类不同,热水和冷水温度不同,这说明,物质的溶解能力与溶剂种类和温度有关;(3)活性炭的吸附性,所以活性炭在净水器中能起到过滤和吸附作用;从盐水中获得饮用水,可采取的方法是蒸馏。
20. 活性炭 混合物 C 验纯 氧气 20
【详解】
(1)活性炭具有吸附性,能除去水中的色素和异味,自来水净化天然水的主要步骤如图所示:试剂X可以用活性炭,净化后的水中含有可溶性物质,是混合物;
(2)冰糖能溶于水,形成溶液,而面粉、花生油都不能溶于水形成均一稳定的混合物,即不能形成溶液;冰块和水是同一种物质,不是溶液,故填:C;
(3)①可燃性气体在点燃前都要进行验纯,以防爆炸;氢气燃烧生成水,其化学方程式为:。
②接通直流电源一段时间后,玻璃管a与负极相连,是氢气,玻璃管b与正极相连,是氧气,氢气和氧气的体积比为2:1,该管内产生约10mL气体时,玻璃管a内产生约20mL气体。
21. CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 用燃着的木条放在集器瓶口,木条熄灭,证明集满。 过滤 漏斗 引流
【详解】
(1)实验室常用大理石主要成分是碳酸钙与稀盐酸反应制取二氧化碳,产物是氯化钙、水和二氧化碳,该反应的化学方程式CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,二氧化碳具有不支持燃烧,也不能燃烧的性质,常用燃着的小木条检验二氧化碳气体是否收集满,用燃着的木条放在集器瓶口,木条熄灭,证明集满;
(2)操作X实验固液分离,是过滤,过滤需要用到玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是引流,防止液体洒出。
22. KClO3、MnO2 C 用灯帽盖灭 B E NaOH、Na2CO3 产生白色沉淀 过滤,向滤液中加入少量的氢氧化钠溶液 通入二氧化碳的量的多少
【详解】
(1)装置A适用于固体加热反应制取氧气,且试管口没有棉花,适用于氯酸钾和二氧化锰制取氧气,故化学药品是:KClO3、MnO2;
氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,收集装置可选C;
实验结束,熄灭酒精灯,应用灯帽盖灭;
(2)石灰石的主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:;
该反应属于固液不加热反应,发生装置应选B,盐酸具有挥发性,制得的二氧化碳中会混有氯化氢气体,碳酸氢钠能与氯化氢反应生成氯化钠、二氧化碳和水,可用饱和碳酸氢钠溶液除去氯化氢,浓硫酸具有吸水性,且与二氧化碳不反应,可用浓硫酸干燥二氧化碳,故所选装置的连接顺序为:B→H→E→干燥、纯净CO2;
(3)猜想:氢氧化钠能与二氧化碳反应生成碳酸钠和水,如果二氧化碳过量,碳酸钠和二氧化碳、水反应生成碳酸氢钠,如果氢氧化钠不能完全转化为碳酸钠,则溶质为:氢氧化钠和碳酸钠,如果氢氧化钠恰好完全转化为碳酸钠,则溶质为:碳酸钠,如果碳酸钠部分转化为碳酸氢钠,则溶质为:碳酸钠和碳酸氢钠,如果碳酸钠完全转化为碳酸氢钠,则溶质为:碳酸氢钠,故猜想④:NaOH、Na2CO3;
实验:结论为猜想③正确,则溶质为碳酸钠和碳酸氢钠,取少量反应后的溶液,加入足量的CaCl2溶液,氯化钙与碳酸钠反应生成碳酸钙和氯化钠,现象为:产生白色沉淀,该反应的化学方程式为:;
现象为:产生白色沉淀,氢氧化钠能与碳酸氢钠反应生成碳酸钠,氯化钙与碳酸钠反应生成碳酸钙,产生白色沉淀,故步骤为:过滤,向滤液中加入少量氢氧化钠溶液;
讨论:由以上分析可知,二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素是:通入二氧化碳的量的多少。
答案第1页,共2页
一、选择题(共16题)
1.把少量下列物质分别放入水中充分搅拌,可以得到溶液的是
A.面粉 B.白糖 C.花生油 D.辣椒粉
2.下列关于溶液的说法正确的是
A.溶液一定是混合物 B.饱和溶液一定是浓溶液
C.溶液都是无色的 D.均一、稳定的液体一定是溶液
3.关于溶液的说法正确的是
A.溶液中的溶质可以是一种或多种
B.溶液上层的密度小,下层的密度大
C.长期放置不分层的液体就是溶液
D.溶液一定是无色、澄清的
4.下列有关溶液的说法中,错误的是( )
A.溶液具有均一性和稳定性
B.物质的溶解过程通常会伴随着能量的变化
C.饱和溶液一定是浓溶液
D.改变条件,能够使饱和溶液与不饱和溶液相互转化
5.下列叙述正确的是
A.不同种元素最本质的区别是质子数不同
B.核电荷数少于核外电子数的一定是阳离子
C.粗盐经溶解、过滤、蒸发提纯后的盐是纯净物
D.凡是均一、稳定的液体一定是溶液
6.下列措施中,不能加快蔗糖在水中溶解速度的是
A.升高温度 B.用玻璃棒搅拌
C.将颗粒磨碎 D.多加蔗糖
7.生活中的下列物质,溶于水形成溶液的是
A.面粉 B.蔗糖 C.植物油 D.木炭
8.下列有关溶液的说法,正确的是
A.溶液通常是液体,溶质一定是固体
B.凡是溶液一定是混合物
C.一种物质分散到另一种物质中,形成的液体是溶液
D.无色透明的液体是溶液
9.某学生利用身边常见的物质解决日常生活中的有关问题,下列方法中不正确的是( )
A.用木炭除去冰箱中的异味 B.用汽油清洗衣服上的油污
C.用明矾净化浑浊的生活用水 D.用食盐水除水瓶中的水垢
10.下列物质放入水中,能形成溶液的是
A.白糖 B.牛奶 C.面粉 D.花生油
11.下列物质分散到水中能形成溶液的是
A.面粉 B.葡萄糖 C.山茶油 D.汽油
12.下列方法中,利用了乳化功能的是
A.用汽油清洗沾有碘的试管
B.用洗洁精清洗餐具上的油污
C.用水冲洗杯子上的蔗糖
D.用明矾净化黄泥水
13.下列物质放入水中,不能形成溶液的是
A.食盐 B.植物油 C.硝酸钾 D.白酒
14.已知:20℃时,NaCl和NaNO3的溶解度分别为36 g和88 g。
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
上表是20℃时实验得出的数据,根据该数据,则下列关于①~⑤所得溶液的说法不正确的是A.溶质质量:②=④ B.溶液质量: ①<②
C.溶质质量分数:①=③ D.⑤中溶质与溶剂的质量比为22:25
15.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是
A.面粉 B.氯化钠 C.泥土 D.乳胶漆
16.2018年世界水日的主题是“借自然之力,护绿水青山”。下列有关水的说法,正确的是
A.水是由氢气和氧气组成的
B.含可溶性钙、镁化合物较多的水叫做软水
C.冰水混合物是纯净物
D.油脂在水中融化后形成溶液
二、综合题(共6题)
17.化学使世界更美好。请用所学化学知识回答下列问题。
Ⅰ.现有氢气、氦气、二氧化碳、食盐、金刚石、生石灰等物质,请按要求用化学式填写:
①飞艇中充入的气体是________; ②切割玻璃的是________;
③用作干燥剂的是_________; ④用作调味品的是_______。
Ⅱ.回答下列与含碳物质有关的问题
①石墨能用于制作干电池电极,说明石墨能__________;
②制糖工业中利用活性炭的__________性脱色制白糖;
③CO2通入汽水中可制作碳酸饮料,反应的化学方程式______________;
④炼铁时发生反应:,其中____做还原剂;
⑤在2Mg+CO22MgO+C中,反应前后碳元素的存在形态由_____(填编号)。
A.游离态到化合态 B. 化合态到游离态
Ⅲ. 某病人注射用的生理盐水(含0.85~0.90%的氯化钠)中添加了适量的葡萄糖(C6H12O6)以补充能量。该注射液中的溶质为_____;葡萄糖分子中碳,氢,氧元素的质量之比是______;1个葡萄糖分子中共含___________个原子;葡萄糖中质量分数最高是____元素;1mol 该葡萄糖中约含有___________个葡萄糖分子;
18.水是常用溶剂,某同学进行如图实验。
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是______。
(2)实验可知,溶质状态可以是______。
(3)实验结束后,用洗涤剂洗净B试管,原理是______。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知: ,X的化学式为______。
(5)询问老师得知用可处理Cl2,根据化学方程式计算,处理0.142gCl2至少需NaOH的质量是多少______?
19.水是人类宝贵的资源。
(1)下列物质加入水中能形成溶液的是________(填序号,下同),能形成乳浊液的是________。
a.植物油 b.蔗糖 c.粉笔灰
(2)NaCl能溶于水,难溶于植物油;NaCl在热水中溶解的质量比在等质量的冷水中溶解的质量大。这说明,物质的溶解能力与_____________________和__________有关。
(3)净化水常用方法有沉降、过滤、吸附和蒸馏,活性炭在净水器中起到过滤和______的作用,从盐水中获得饮用水,可采取的方法是______。
20.水是生命的源泉,是人类最宝贵的资源
(1)自来水净化天然水的主要步骤如图所示:试剂X可以用_____,净化后的水是_____(选填“纯净物”或“混合物”)
(2)水是一种最常用的溶剂,将下列生活中的物质分别放入水中,能形成溶液的是_____
A面粉 B冰块 C冰糖 D花生油
(3)某化学兴趣小组的同学利用以下两个实验验证水的组成
①实验Ⅰ:点燃氢气前,应先_____,请你写出氢气在空气中燃烧的化学方程式________
②实验Ⅱ:往水电解器中加入100g溶质质量分数为2%的硫酸钠溶液(碳酸钠不参与反应,仅起增加水的导电性的作用),接通直流电源一段时间后,玻璃管b内产生的气体是_____,该试管内产生约10mL气体时,玻璃管a内产生的气体约为_____mL
21.下图是实验室制取某些常见气体所使用的一些装置和仪器。
(1)实验室制取二氧化碳反应的化学方程式为______________,证明二氧化碳集满的方法是_____________________。
(2)某实验小组用氯酸钾和二氧化锰制取氧气,完全反应后从残余物中提纯KCl,进行以下操作:
(提示:MnO2不溶于水,含钾化合物均可溶于水)
操作X的名称是________,在实验室中进行该操作时用到的玻璃仪器有玻璃棒、烧杯、________,在该操作中玻璃棒的作用是________。
22.根据下列仪器装置,回答有关问题。
(1)制取氧气。实验室选用装置A制取氧气时,用到的化学药品是______(用化学式表示);收集氧气可以选用的装置是______填装置序号)。实验结束熄灭酒精灯的操作为______。
(2)制取二氧化碳。用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为______。为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为____→H→____→干燥、纯净CO2 (在括号内填装置序号)。
(3)进一步探究二氧化碳与氢氧化钠溶液的反应。
【提出问题】制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3。向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
【查阅资料】碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3=Na2CO3+H2O;Ca(HCO3)2溶于水。
【猜想】所得溶液中的溶质是:
①Na2CO3;②NaHCO3;③Na2CO3和NaHCO3;④______。
【实验】请你参与下列验证猜想③的实验,完成探究报告。
步骤和方法 现象 分析
取少量反应后的溶液,加入足量的CaCl2溶液 ______ 发生反应的方程式:______
______ 产生白色沉淀 结论:猜想③正确
【讨论】二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素是______。
试卷第1页,共3页
参考答案:
1.B
【详解】
A、面粉是一种不溶于水的粉末,与水混合后形成悬浊液,选项错误;
B、白糖是一种能够溶于水的固体,与水混合后形成均一、稳定的溶液,选项正确;
C、花生油是一种不溶于水的液体,与水混合后形成乳浊液,选项错误;
D、辣椒粉是一种不溶于水的粉末,与水混合后形成悬浊液,选项错误;
故选B。
2.A
【详解】
A、溶液是均一、稳定的混合物,故A正确;
B、饱和溶液不一定是浓溶液,如氢氧化钙溶液达到饱和时也是稀溶液,故B错误;
C、溶液都不一定是无色的,有的溶液是有颜色的,如硫酸铜溶液是蓝色的,故C错误;
D、均一、稳定的液体不一定是溶液,如水,故D错误。故选A。
3.A
【详解】
A.溶液中的溶质可以是一种或多种,如食盐水中溶质只有食盐,海水中溶质有许多种,选项正确;
B.溶液是均一的,溶液上层的密度和下层的密度相同,选项错误;
C.长期放置不分层的液体混合物可能是溶液,选项错误;
D.溶液不一定是无色的,如硫酸铜溶液是蓝色的,选项错误。
故选A。
4.C
【详解】
A、溶液是均一稳定的混合物,溶液具有均一性和稳定性,故选项说法正确;B、物质的溶解过程通常会伴随着能量的变化,故选项说法正确;C、饱和溶液不一定是浓溶液,也可能是稀溶液,如氢氧化钙的饱和溶液为稀溶液,故选项说法错误;D、改变条件,能够使饱和溶液与不饱和溶液相互转化,故选项说法正确。故选C。
5.A
【详解】
A、元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,故选项说法正确;
B、核电荷数少于核外电子数的粒子带负电荷,一定是阴离子,故选项说法错误;
C、粗盐经溶解、过滤、蒸发提纯后的盐仍含有可溶性的化合物,如氯化钙、氯化镁等,属于混合物,故选项说法错误;
D、溶液的特点是均一稳定的混合物,均一、稳定的液体不一定是混合物,例如水不属于溶液,故选项说法错误。
故选A。
6.D
【详解】
A、升高温度,能加快分子运动速度,能加快固体物质与水的接触机会,从而加快了固体物质的溶解速度,故选项错误。
B、用玻璃棒不断搅拌,能加快分子运动速度,能加快固体物质与水的接触机会,从而加快了固体物质的溶解速度,故选项错误。
C、固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率,将固体研成粉末增加了蔗糖与水的接触面积,加快了固体物质的溶解速度,故选项错误。
D、多加蔗糖不能加快蔗糖在水中溶解速度,故选项正确。
故选D。
7.B
【详解】
由一种物质或几种物质分散到另一种物质中形成均一的、稳定的混合物为溶液,植物油、面粉都不溶于水中,不能形成溶液,木炭不溶于水,不能形成溶液。
8.B
【详解】
A、溶液通常是液体,溶质可以是固体、液体或气体,故选项说法错误;
B、溶液的本质特征是均一性、稳定性,属于混合物;故选项说法正确;
C、一种物质分散到另一种物质中,形成的液体不一定是均一的、稳定的,故不一定是溶液;故选项说法错误;
D、无色透明的液体不一定是溶液,如水是均一的、稳定的液体,但不是溶液;故选项说法错误。故选B。
9.D
【详解】
A、木炭具有吸附作用,可以用木炭可以除去冰箱中的异味,故A正确;
B、油污易溶于汽油,可以用汽油可以清洗衣服上的油污,故B正确;
C、明矾溶于水生成胶状物质,能够吸附水中的悬浮物,用明矾可以净化浑浊的生活用水,故C正确;
D、食盐主要成分是氯化钠,氯化钠溶液是中性物质,不能和水垢成分(碳酸钙、氢氧化镁等)反应,不能用食盐水不能除水瓶中的水垢,故D不正确。故选D。
10.A
【详解】
A、白糖易溶于水,形成均一、稳定的混合物,属于溶液,故选项正确;
B、牛奶是不溶性的小液滴等分散到液体中形成的,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
C、面粉不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
D、花生油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误。
11.B
【详解】
A、面粉不溶于水,不能形成溶液,故A不正确;
B、葡萄糖易溶于水,形成的均一的、稳定的葡萄糖溶液,故B正确;
C、山茶油不溶于水,不能形成溶液,故C不正确;
D、汽油是有机溶剂,不溶于水,不能形成溶液,故D不正确。故选B。
12.B
【详解】
A、碘能溶解在汽油中,属于溶解现象,因此可用汽油清洗沾有碘的试管;故选项错误;
B、利用洗洁精的乳化功能清洗餐具上的油污;故选项正确;
C、水能溶解蔗糖,用水冲洗杯子上的蔗糖属于溶解现象;故选项错误;
D、明矾溶于水后形成的胶状物能吸附水中的杂质从而达到净水的目的,不是乳化作用;故选项错误。
故选:B。
13.B
【详解】
A. 食盐,易溶于水,正确;B. 植物油,难溶于水,错误;C. 硝酸钾,易溶于水,正确;D. 白酒,易溶于水,正确。故选B。
14.A
【详解】
A、溶液②中溶质的质量为36g,④中溶质的质量为60g,故错误,符合题意;
B、溶液①的质量为:30g+100g=130g;溶液②的质量为:36g+100g=136g,溶液质量:①<②,故正确,不符合题意;
C、溶液①和③均是在100g水中溶解了30g溶质所得溶液中溶质的质量分数相等,故正确,不符合题意;
D、溶液⑤是在100g水中溶解了88g硝酸钠,所以⑤中溶质与溶剂的质量比为88:100=22:25,故正确,不符合题意。
故选A。
15.B
【详解】
溶液是均一稳定的混合物,在溶液中物质以分子或离子等微观粒子的的形式相互混合,因没有阻挡光线的微粒,所以溶液都是澄清透明的。面粉 、泥土 、乳胶漆和水混合否不能得到均一稳定的混合物,都不是溶液;氯化钠和水形成的是均一稳定的混合物,是溶液。选B
16.C
【详解】
A、水是由氢元素和氧元素组成的,故错误;
B、含可溶性钙、镁化合物较多的水叫做硬水,故错误;
C、冰和水都是水,是由一种物质组成的,故是纯净物,故正确;
D、油脂溶解在水中,不能形成溶液,形成的是乳浊液,故错误。故选C。
17. He C CaO NaCl 导电 吸附 略 CO B 氯化钠 葡萄糖 6:1:8 24 O 6.02 1023
【详解】
Ⅰ、①氦气的密度小且化学性质不活泼,不易的发生爆炸,故常用来充灌载人飞艇,化学式为:He;②金刚石用于切割玻璃,化学式为:C;③生石灰能与水反应生成氢氧化钙,可做干燥剂,化学式为:CaO;④食盐是常用的调味品,化学式为:NaCl;Ⅱ、①石墨能用于制作干电池电极,说明石墨具有导电性;②制糖工业中利用活性炭的吸附性脱色制白糖;③CO2通入汽水中可制作碳酸饮料,反应的化学方程式CO2+H2O=H2CO3;④炼铁时发生反应:3CO+Fe2O32Fe+3CO2,其中一氧化碳得到氧,发生了氧化反应,具有还原性;⑤在2Mg+CO22MgO+C中,碳元素由化合物转化为了单质,所以反应前后碳元素的存在形态由化合态到游离态;Ⅲ、该注射液中含有氯化钠和葡萄糖两种溶质;由葡萄糖的化学式可知,一个葡萄糖分子中含有6个碳原子、12个氢原子和6个氧原子,共24个原子;原子的物质的量之比为C:H:O=1:2:1;葡萄糖是由碳、氢、氧三种元素组成的,碳、氢、氧三种元素的质量比为:(12×6):(1×12):(16×6)=6:1:8,可见其中氧元素的质量分数最高;1mol 该葡萄糖中约含有6.02 1023个葡萄糖分子。
18. 一开始,液体分层,上层为无色,下层为红色,过一段时间后,溶液变为均匀的红色 气态、液态、固态 乳化作用 MnCl2 解:设至少需要氢氧化钠的质量是x
x=0.16g
答:至少需要氢氧化钠的质量是0.16g。
【详解】
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,乙醇的密度比水小,故一开始,液体分层,上层为无色,下层为红色,乙醇能与水以任意比例互溶,由于分子在不断运动,一定时间后,乙醇溶于水,形成均一、稳定的混合物,故最后溶液变为均匀的红色,故现象为:一开始,液体分层,上层为无色,下层为红色,过一段时间后,溶液变为均匀的红色;
(2)酒精溶于水,溶质是酒精,酒精是液态,高锰酸钾溶于水,溶质是高锰酸钾,高锰酸钾是固态,氯化氢溶于水,溶质是氯化氢,氯化氢是气态,故溶质状态可以是:气态、液态、固态;
(3)用洗涤剂清洗B试管,是因为洗涤剂中含有乳化剂,具有乳化作用,能将油污乳化为细小油滴,随水冲走,故填:乳化作用;
(4)根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含K、Mn、O、H、Cl的个数分别是2、2、8、16、16,生成物中含K、Mn、O、H、Cl的个数分别是2、0、8、16、12,故生成物中还应含2个Mn、4个Cl,故X的化学式为:MnCl2;
(5)见答案。
19. b a 溶剂种类 温度 吸附 蒸馏
【详解】
(1)在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物属于溶液,蔗糖易溶于水,形成均一、稳定的混合物,属于溶液;植物油不溶于水,与水混合形成乳浊液;(2)水和植物油属于溶剂种类不同,热水和冷水温度不同,这说明,物质的溶解能力与溶剂种类和温度有关;(3)活性炭的吸附性,所以活性炭在净水器中能起到过滤和吸附作用;从盐水中获得饮用水,可采取的方法是蒸馏。
20. 活性炭 混合物 C 验纯 氧气 20
【详解】
(1)活性炭具有吸附性,能除去水中的色素和异味,自来水净化天然水的主要步骤如图所示:试剂X可以用活性炭,净化后的水中含有可溶性物质,是混合物;
(2)冰糖能溶于水,形成溶液,而面粉、花生油都不能溶于水形成均一稳定的混合物,即不能形成溶液;冰块和水是同一种物质,不是溶液,故填:C;
(3)①可燃性气体在点燃前都要进行验纯,以防爆炸;氢气燃烧生成水,其化学方程式为:。
②接通直流电源一段时间后,玻璃管a与负极相连,是氢气,玻璃管b与正极相连,是氧气,氢气和氧气的体积比为2:1,该管内产生约10mL气体时,玻璃管a内产生约20mL气体。
21. CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 用燃着的木条放在集器瓶口,木条熄灭,证明集满。 过滤 漏斗 引流
【详解】
(1)实验室常用大理石主要成分是碳酸钙与稀盐酸反应制取二氧化碳,产物是氯化钙、水和二氧化碳,该反应的化学方程式CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,二氧化碳具有不支持燃烧,也不能燃烧的性质,常用燃着的小木条检验二氧化碳气体是否收集满,用燃着的木条放在集器瓶口,木条熄灭,证明集满;
(2)操作X实验固液分离,是过滤,过滤需要用到玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是引流,防止液体洒出。
22. KClO3、MnO2 C 用灯帽盖灭 B E NaOH、Na2CO3 产生白色沉淀 过滤,向滤液中加入少量的氢氧化钠溶液 通入二氧化碳的量的多少
【详解】
(1)装置A适用于固体加热反应制取氧气,且试管口没有棉花,适用于氯酸钾和二氧化锰制取氧气,故化学药品是:KClO3、MnO2;
氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,收集装置可选C;
实验结束,熄灭酒精灯,应用灯帽盖灭;
(2)石灰石的主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:;
该反应属于固液不加热反应,发生装置应选B,盐酸具有挥发性,制得的二氧化碳中会混有氯化氢气体,碳酸氢钠能与氯化氢反应生成氯化钠、二氧化碳和水,可用饱和碳酸氢钠溶液除去氯化氢,浓硫酸具有吸水性,且与二氧化碳不反应,可用浓硫酸干燥二氧化碳,故所选装置的连接顺序为:B→H→E→干燥、纯净CO2;
(3)猜想:氢氧化钠能与二氧化碳反应生成碳酸钠和水,如果二氧化碳过量,碳酸钠和二氧化碳、水反应生成碳酸氢钠,如果氢氧化钠不能完全转化为碳酸钠,则溶质为:氢氧化钠和碳酸钠,如果氢氧化钠恰好完全转化为碳酸钠,则溶质为:碳酸钠,如果碳酸钠部分转化为碳酸氢钠,则溶质为:碳酸钠和碳酸氢钠,如果碳酸钠完全转化为碳酸氢钠,则溶质为:碳酸氢钠,故猜想④:NaOH、Na2CO3;
实验:结论为猜想③正确,则溶质为碳酸钠和碳酸氢钠,取少量反应后的溶液,加入足量的CaCl2溶液,氯化钙与碳酸钠反应生成碳酸钙和氯化钠,现象为:产生白色沉淀,该反应的化学方程式为:;
现象为:产生白色沉淀,氢氧化钠能与碳酸氢钠反应生成碳酸钠,氯化钙与碳酸钠反应生成碳酸钙,产生白色沉淀,故步骤为:过滤,向滤液中加入少量氢氧化钠溶液;
讨论:由以上分析可知,二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素是:通入二氧化碳的量的多少。
答案第1页,共2页
