科粤版九年级化学下册9.1有机物的常识同步练习(word版 含答案)
文档属性
| 名称 | 科粤版九年级化学下册9.1有机物的常识同步练习(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 146.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-30 00:00:00 | ||
图片预览



文档简介
科粤版九年级化学下册 9.1 有机物的常识 同步练习
一、单选题
1.学习化学,提高学科核心素养,学会从化学的角度分析问题。下列说法错误的是( )
A.氮气可用于填充灯泡是因为其化学性质不活泼
B.酸碱中和反应都会放出热量,因此放热反应都是中和反应
C.点燃甲烷前,一定要先检验甲烷的纯度,可防止发生爆炸
D.物体热胀冷缩现象,是因为物质的微粒间距离发生了变化
2.下列物质是某食品配料中的主要成分,其中属于无机化合物的是
A.淀粉 B.食盐 C.食用油 D.白砂糖
3.分类学习是化学学习的重要思想方法,下列物质分类错误的一组是( )
A.S、P、C
B.H2O、H2SO4、HCl
C.NaCl、CaCO3、Na2CO3
D.CH4、C2H5OH、C6H12O6
4.据《易经》记载:“泽中有火”,“上火下泽”。泽,指湖泊池沼。“泽中有火”是对“X气体”在湖泊池沼水面上起火现象的描述。这里“X气体”是指
A.一氧化碳 B.甲烷 C.氧气 D.氢气
5.下列生活生产中常见的物质里含有的有机物属于高分子化合物的是( )
A.蜂蜜中含有的葡萄糖
B.石油中含有的C16H34
C.芹菜中含有的纤维素
D.植物油中含有的油脂
6.下列物质分别在空气中燃烧,同时有二氧化碳和水生成的是
①甲烷 ②木炭 ③氢气 ④石蜡 ⑤酒精 ⑥一氧化碳
A.①④⑤ B.①③④⑤
C.②④⑤⑥ D.①②③④⑤⑥
7.下列物质不属于有机物的是
A.葡萄糖(C6H12O6) B.乙醇(C2H5OH) C.乙酸(CH3COOH) D.水(H2O)
8.下列物质按照单质、化合物、混合物的顺序排列的是
A.汞、乙醇、石油
B.干冰、氧化铜、赤铁矿
C.铁、五氧化二磷、冰水混合物
D.C60、天然气、煤
9.小军同学来到他家厨房,他不可能找到的调味品是
A.食盐(氯化钠) B.醋(醋酸) C.酒(乙醇) D.胆矾(硫酸铜晶体)
10.下列物质中均含有碳元素,其中不属于有机物的是
A.酒精 B.醋酸 C.碳酸 D.甲烷
11.下列物质的俗称与化学式,不对应的是
A.水银——Hg B.酒精——C2H5OH
C.生石灰——CaO D.熟石灰——CaCO3
12.2020年3月26日,科技部长徐南平指出,我国已经筛选出磷酸氯喹、法匹拉韦、可利霉素等药物,在临床中显示这些药物治疗新冠肺炎有一定的疗效。其中磷酸氯喹的化学式为,下列有关磷酸氯喹的说法错误的是( )
A.磷酸氯喹是一种有机物
B.一个磷酸氯喹分子含有64个原子
C.磷酸氯喹由碳、氢、氯、氮、氧、磷六种元素组成
D.磷酸氯喹中碳、氢、氮三种元素的质量比为18:32:3
13.下列不属于有机物的是( )
A.碳酸 B.乙醇 C.乙酸 D.蔗糖
14.下列物质属于有机化合物的是
A.NaCl B.NaOH C.HCl D.CH4
15.对CO2、C2H2、H2CO3、Ca(HCO3)2、Na2CO3五种物质的判断,正确的是
A.C2H2、H2CO3都是有机物
B.CO2、H2CO3都属于氧化物
C.Ca(HCO3)2、Na2CO3都属于盐
D.H2CO3、Na2CO3溶液都显酸性
16.烈性炸药TNT(化学式为C7H5N3O6)广泛用于开矿、修路、兴修水利等,下列关于TNT的说法错误的是
A.TNT是一种有机物
B.TNT爆炸后会产生二氧化硫
C.TNT由四种元素组成
D.每个TNT分子含有21个原子
二、综合应用题
17.为了确定CH4、H2和CO (以下简称试验气)三种可燃性气体,分别将它们在氧气中燃烧,把燃烧后生成的气体依次通过如图所示的装置.回答以下问题.
(1)若装置A的质量增加,B的质量不变,则试验气是________,燃烧的化学方程式为__________________.
(2)若装置A的质量不变,B的质量增加,则试验气是_________,在B瓶中的反应方程式是_________________.
(3)若装置A、B的质量都增加,则试验气是___________;若B的质量增加2.2g,则A的质量增加__________g.
18.物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序。
规律 排序
示例:标准状况下,密度由大到小 CO2、C2H4(乙烯)、C2H2(乙炔)、CH4
_________ _________
_________ _________
(2)由CH4、CO、H2中的一种、两种或三种组成的气体,完全燃烧后,生成的CO2和H2O的质量之比是11︰9,下列判断中正确的是_________。
A.原气体可能是H2和CH4 的混合物
B.原气体中一定含有CH4
C.原气体中若含有CO,则一定含有H2
D.气体中若同时含有CH4、CO和H2,则CO与H2的质量之比为7︰1
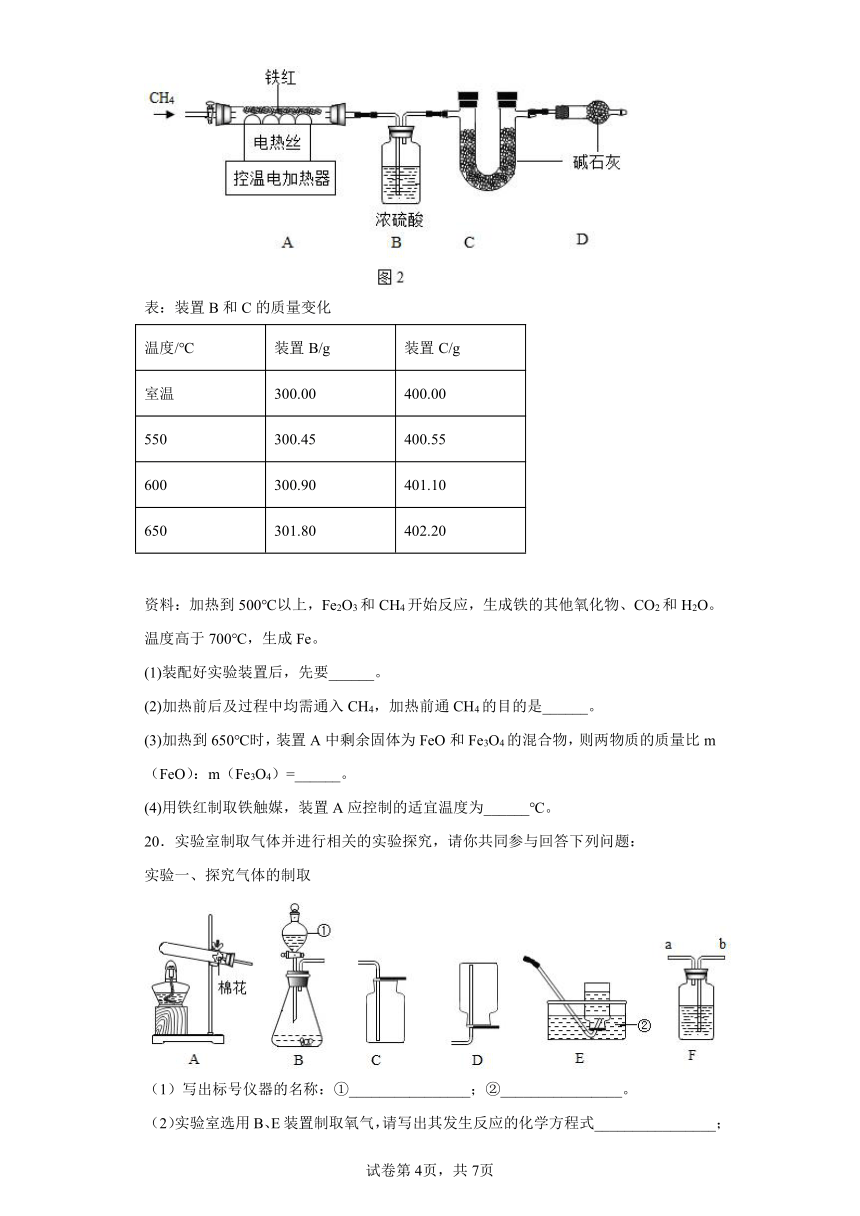
19.铁触媒是工业合成氨的催化剂,主要成分为Fe3O4。用下列装置对铁触媒的制备进行研究。取48.00g铁红置于装置A中,控制不同的温度对其加热,测得装置B和C的质量变化如表。
表:装置B和C的质量变化
温度/℃ 装置B/g 装置C/g
室温 300.00 400.00
550 300.45 400.55
600 300.90 401.10
650 301.80 402.20
资料:加热到500℃以上,Fe2O3和CH4开始反应,生成铁的其他氧化物、CO2和H2O。温度高于700℃,生成Fe。
(1)装配好实验装置后,先要______。
(2)加热前后及过程中均需通入CH4,加热前通CH4的目的是______。
(3)加热到650℃时,装置A中剩余固体为FeO和Fe3O4的混合物,则两物质的质量比m(FeO):m(Fe3O4)=______。
(4)用铁红制取铁触媒,装置A应控制的适宜温度为______℃。
20.实验室制取气体并进行相关的实验探究,请你共同参与回答下列问题:
实验一、探究气体的制取
(1)写出标号仪器的名称:①________________;②________________。
(2)实验室选用B、E装置制取氧气,请写出其发生反应的化学方程式________________;若实验中始终未能集满氧气,可能的原因是________________________(填字母序号);
A 装置可能漏气 B 药品用量可能不足 C 导气管未伸到集气瓶底部
(3)实验室常用来制取氢气的化学方程式________________,该反应获得的氢气中常混有少量水蒸气,可通过盛有________________(填一种物质的名称)的F装置除去水蒸气,混合气体应从F装置的________(填“a”或“b”)口通入。
实验二、回收反应后的剩余物
用高锰酸钾制取氧气的实验中,欲从完全反应后的剩余物中回收某些物质,根据查阅的资料设计了如图所示实验方案:
【查阅资料】
①滤纸的主要成分是纤维素,能和纤维素反应;
②在中性溶液中比较稳定,在碱性加热条件下,溶液中会有部分和反应生成;
③锰酸钾溶于水为墨绿色,不稳定,在水溶液中能全都转化为、和KOH,反应的化学方程式为:。
【实验方案】
(1)滤纸的主要成分纤维素属于________________(填“有机物”或“无机物”);
(2)回收物甲是________________________(填化学式);
(3)滤液B中一定含有的溶质是________________________;
(4)静置后过滤时,发现滤液浑浊,在所用仪器洁净、操作均正确的情况下(过滤前滤纸完好无损),原因是________________________________________________;
(5)降温结晶、过滤后,低温烘干高锰酸钾晶体其目的是________________________;
(6)请你对溶液B的颜色提出设想并说明依据:________________________________。
21.可燃冰是一种在海底储量巨大的清洁能源,对可燃冰的研究方兴未艾。
(1)探究可燃冰的组成。
将可燃冰加热到20℃以上,发生分解,生成甲烷气和水。
①已知甲烷分子中只含有碳和氢两种元素,且碳和氢的原子比为1:4。则甲烷的分子式是_____;甲烷分子中氢元素的质量分数为________。
②可燃冰可以看作是1个分子的甲烷和8个分子的水结合而成。计算可燃冰中甲烷所占的质量分数________。
(2)开采和利用可燃冰。
方法一:热解法
将可燃冰在海底加热,使其分解成甲烷,再通过管道将甲烷气输送到海面上。
①热解法是一种高能耗的开采方式,原因是_______。
②甲烷的温室效应是二氧化碳的13倍。热解法开采可能对大气环境造成的危害是_______。
方法二:置换法
将二氧化碳通入海底可燃冰层中,在海水的高压下,二氧化碳和可燃冰中的水结合,形成水合二氧化碳,同时释放出甲烷气。
③水和二氧化碳在常温下即可反应生成水合二氧化碳。反应如上图所示。该反应的反应类型为_______。
④甲烷是清洁燃料和化工原料。高温下甲烷分解为两种单质,单质的化学式是_______。
22.化学就在我们身边,它与我们生活息息相关。
(1)目前,城镇居民的生活燃料主要是天然气,天然气的主要成分是______。
(2)家庭厨房中的食盐、醋酸、味精、花椒面等调味品分别与水混合搅拌,其中不能形成溶液的物质是______;用洗洁精和水可以轻松洗掉餐具上的的油渍,这是利用了洗洁精的______功能。
(3)遂宁是四川省第一个获得“森林城市”的地级市,“森林遂宁”的实施有助于改善我们的居住环境,因为绿色植物能吸收二氧化碳,并释放出氧气,其反应原理为:6CO2+6H2OX+6O2,其中X的化学式为______。
(4)“酒驾”是近年来热门话题之一,交警检查驾驶员是否酒后驾车,可用一种装有重铬酸钾(K2Cr2O7)的仪器,重铬酸钾中铬元素(Cr)的化合价为______。
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.B
2.B
3.B
4.B
5.C
6.A
7.D
8.A
9.D
10.C
11.D
12.D
13.A
14.D
15.C
16.B
17. H2 2H2+O2 2H2O CO CO2+Ca(OH) 2===CaCO3↓+H2O CH4 1.8
18. 相对分子质量由大到小 CO2、C2H4、C2H2、CH4 一个分子中原子个数由多到少 C2H4、CH4、C2H2、CO2(其他合理的均可) CD
19.(1)检查装置的气密性
(2)排尽装置内的空气,防止加热时发生爆炸(或排尽装置内的空气,防止甲烷和氧气发生反应生成二氧化碳和水,影响测定结果)
(3)27:29
(4)600℃
20. 分液漏斗 水槽 AB 浓硫酸 b 有机物 、KOH 与滤纸的主要成分纤维素反应,使滤纸破损。 溶液B中含有氢氧化钾,显碱性,在温度较高时,会与水反应而被消耗,故虚低温烘干。 紫红色;因为锰酸钾在水溶液中不稳定,会全部分解为紫红色的高锰酸钾溶液和二氧化锰固体以及无色的氢氧化钾,故溶液呈现紫红色。
21.(1) CH4 25% 10%
(2) 海底温度较低,在海底加热可燃冰,使其分解成甲烷,消耗能量高 温室效应加剧 化合反应 C、H2
22.(1)CH4
(2) 花椒面 乳化
(3)C6H12O6
(4)+6
答案第1页,共2页
答案第1页,共2页
一、单选题
1.学习化学,提高学科核心素养,学会从化学的角度分析问题。下列说法错误的是( )
A.氮气可用于填充灯泡是因为其化学性质不活泼
B.酸碱中和反应都会放出热量,因此放热反应都是中和反应
C.点燃甲烷前,一定要先检验甲烷的纯度,可防止发生爆炸
D.物体热胀冷缩现象,是因为物质的微粒间距离发生了变化
2.下列物质是某食品配料中的主要成分,其中属于无机化合物的是
A.淀粉 B.食盐 C.食用油 D.白砂糖
3.分类学习是化学学习的重要思想方法,下列物质分类错误的一组是( )
A.S、P、C
B.H2O、H2SO4、HCl
C.NaCl、CaCO3、Na2CO3
D.CH4、C2H5OH、C6H12O6
4.据《易经》记载:“泽中有火”,“上火下泽”。泽,指湖泊池沼。“泽中有火”是对“X气体”在湖泊池沼水面上起火现象的描述。这里“X气体”是指
A.一氧化碳 B.甲烷 C.氧气 D.氢气
5.下列生活生产中常见的物质里含有的有机物属于高分子化合物的是( )
A.蜂蜜中含有的葡萄糖
B.石油中含有的C16H34
C.芹菜中含有的纤维素
D.植物油中含有的油脂
6.下列物质分别在空气中燃烧,同时有二氧化碳和水生成的是
①甲烷 ②木炭 ③氢气 ④石蜡 ⑤酒精 ⑥一氧化碳
A.①④⑤ B.①③④⑤
C.②④⑤⑥ D.①②③④⑤⑥
7.下列物质不属于有机物的是
A.葡萄糖(C6H12O6) B.乙醇(C2H5OH) C.乙酸(CH3COOH) D.水(H2O)
8.下列物质按照单质、化合物、混合物的顺序排列的是
A.汞、乙醇、石油
B.干冰、氧化铜、赤铁矿
C.铁、五氧化二磷、冰水混合物
D.C60、天然气、煤
9.小军同学来到他家厨房,他不可能找到的调味品是
A.食盐(氯化钠) B.醋(醋酸) C.酒(乙醇) D.胆矾(硫酸铜晶体)
10.下列物质中均含有碳元素,其中不属于有机物的是
A.酒精 B.醋酸 C.碳酸 D.甲烷
11.下列物质的俗称与化学式,不对应的是
A.水银——Hg B.酒精——C2H5OH
C.生石灰——CaO D.熟石灰——CaCO3
12.2020年3月26日,科技部长徐南平指出,我国已经筛选出磷酸氯喹、法匹拉韦、可利霉素等药物,在临床中显示这些药物治疗新冠肺炎有一定的疗效。其中磷酸氯喹的化学式为,下列有关磷酸氯喹的说法错误的是( )
A.磷酸氯喹是一种有机物
B.一个磷酸氯喹分子含有64个原子
C.磷酸氯喹由碳、氢、氯、氮、氧、磷六种元素组成
D.磷酸氯喹中碳、氢、氮三种元素的质量比为18:32:3
13.下列不属于有机物的是( )
A.碳酸 B.乙醇 C.乙酸 D.蔗糖
14.下列物质属于有机化合物的是
A.NaCl B.NaOH C.HCl D.CH4
15.对CO2、C2H2、H2CO3、Ca(HCO3)2、Na2CO3五种物质的判断,正确的是
A.C2H2、H2CO3都是有机物
B.CO2、H2CO3都属于氧化物
C.Ca(HCO3)2、Na2CO3都属于盐
D.H2CO3、Na2CO3溶液都显酸性
16.烈性炸药TNT(化学式为C7H5N3O6)广泛用于开矿、修路、兴修水利等,下列关于TNT的说法错误的是
A.TNT是一种有机物
B.TNT爆炸后会产生二氧化硫
C.TNT由四种元素组成
D.每个TNT分子含有21个原子
二、综合应用题
17.为了确定CH4、H2和CO (以下简称试验气)三种可燃性气体,分别将它们在氧气中燃烧,把燃烧后生成的气体依次通过如图所示的装置.回答以下问题.
(1)若装置A的质量增加,B的质量不变,则试验气是________,燃烧的化学方程式为__________________.
(2)若装置A的质量不变,B的质量增加,则试验气是_________,在B瓶中的反应方程式是_________________.
(3)若装置A、B的质量都增加,则试验气是___________;若B的质量增加2.2g,则A的质量增加__________g.
18.物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序。
规律 排序
示例:标准状况下,密度由大到小 CO2、C2H4(乙烯)、C2H2(乙炔)、CH4
_________ _________
_________ _________
(2)由CH4、CO、H2中的一种、两种或三种组成的气体,完全燃烧后,生成的CO2和H2O的质量之比是11︰9,下列判断中正确的是_________。
A.原气体可能是H2和CH4 的混合物
B.原气体中一定含有CH4
C.原气体中若含有CO,则一定含有H2
D.气体中若同时含有CH4、CO和H2,则CO与H2的质量之比为7︰1
19.铁触媒是工业合成氨的催化剂,主要成分为Fe3O4。用下列装置对铁触媒的制备进行研究。取48.00g铁红置于装置A中,控制不同的温度对其加热,测得装置B和C的质量变化如表。
表:装置B和C的质量变化
温度/℃ 装置B/g 装置C/g
室温 300.00 400.00
550 300.45 400.55
600 300.90 401.10
650 301.80 402.20
资料:加热到500℃以上,Fe2O3和CH4开始反应,生成铁的其他氧化物、CO2和H2O。温度高于700℃,生成Fe。
(1)装配好实验装置后,先要______。
(2)加热前后及过程中均需通入CH4,加热前通CH4的目的是______。
(3)加热到650℃时,装置A中剩余固体为FeO和Fe3O4的混合物,则两物质的质量比m(FeO):m(Fe3O4)=______。
(4)用铁红制取铁触媒,装置A应控制的适宜温度为______℃。
20.实验室制取气体并进行相关的实验探究,请你共同参与回答下列问题:
实验一、探究气体的制取
(1)写出标号仪器的名称:①________________;②________________。
(2)实验室选用B、E装置制取氧气,请写出其发生反应的化学方程式________________;若实验中始终未能集满氧气,可能的原因是________________________(填字母序号);
A 装置可能漏气 B 药品用量可能不足 C 导气管未伸到集气瓶底部
(3)实验室常用来制取氢气的化学方程式________________,该反应获得的氢气中常混有少量水蒸气,可通过盛有________________(填一种物质的名称)的F装置除去水蒸气,混合气体应从F装置的________(填“a”或“b”)口通入。
实验二、回收反应后的剩余物
用高锰酸钾制取氧气的实验中,欲从完全反应后的剩余物中回收某些物质,根据查阅的资料设计了如图所示实验方案:
【查阅资料】
①滤纸的主要成分是纤维素,能和纤维素反应;
②在中性溶液中比较稳定,在碱性加热条件下,溶液中会有部分和反应生成;
③锰酸钾溶于水为墨绿色,不稳定,在水溶液中能全都转化为、和KOH,反应的化学方程式为:。
【实验方案】
(1)滤纸的主要成分纤维素属于________________(填“有机物”或“无机物”);
(2)回收物甲是________________________(填化学式);
(3)滤液B中一定含有的溶质是________________________;
(4)静置后过滤时,发现滤液浑浊,在所用仪器洁净、操作均正确的情况下(过滤前滤纸完好无损),原因是________________________________________________;
(5)降温结晶、过滤后,低温烘干高锰酸钾晶体其目的是________________________;
(6)请你对溶液B的颜色提出设想并说明依据:________________________________。
21.可燃冰是一种在海底储量巨大的清洁能源,对可燃冰的研究方兴未艾。
(1)探究可燃冰的组成。
将可燃冰加热到20℃以上,发生分解,生成甲烷气和水。
①已知甲烷分子中只含有碳和氢两种元素,且碳和氢的原子比为1:4。则甲烷的分子式是_____;甲烷分子中氢元素的质量分数为________。
②可燃冰可以看作是1个分子的甲烷和8个分子的水结合而成。计算可燃冰中甲烷所占的质量分数________。
(2)开采和利用可燃冰。
方法一:热解法
将可燃冰在海底加热,使其分解成甲烷,再通过管道将甲烷气输送到海面上。
①热解法是一种高能耗的开采方式,原因是_______。
②甲烷的温室效应是二氧化碳的13倍。热解法开采可能对大气环境造成的危害是_______。
方法二:置换法
将二氧化碳通入海底可燃冰层中,在海水的高压下,二氧化碳和可燃冰中的水结合,形成水合二氧化碳,同时释放出甲烷气。
③水和二氧化碳在常温下即可反应生成水合二氧化碳。反应如上图所示。该反应的反应类型为_______。
④甲烷是清洁燃料和化工原料。高温下甲烷分解为两种单质,单质的化学式是_______。
22.化学就在我们身边,它与我们生活息息相关。
(1)目前,城镇居民的生活燃料主要是天然气,天然气的主要成分是______。
(2)家庭厨房中的食盐、醋酸、味精、花椒面等调味品分别与水混合搅拌,其中不能形成溶液的物质是______;用洗洁精和水可以轻松洗掉餐具上的的油渍,这是利用了洗洁精的______功能。
(3)遂宁是四川省第一个获得“森林城市”的地级市,“森林遂宁”的实施有助于改善我们的居住环境,因为绿色植物能吸收二氧化碳,并释放出氧气,其反应原理为:6CO2+6H2OX+6O2,其中X的化学式为______。
(4)“酒驾”是近年来热门话题之一,交警检查驾驶员是否酒后驾车,可用一种装有重铬酸钾(K2Cr2O7)的仪器,重铬酸钾中铬元素(Cr)的化合价为______。
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.B
2.B
3.B
4.B
5.C
6.A
7.D
8.A
9.D
10.C
11.D
12.D
13.A
14.D
15.C
16.B
17. H2 2H2+O2 2H2O CO CO2+Ca(OH) 2===CaCO3↓+H2O CH4 1.8
18. 相对分子质量由大到小 CO2、C2H4、C2H2、CH4 一个分子中原子个数由多到少 C2H4、CH4、C2H2、CO2(其他合理的均可) CD
19.(1)检查装置的气密性
(2)排尽装置内的空气,防止加热时发生爆炸(或排尽装置内的空气,防止甲烷和氧气发生反应生成二氧化碳和水,影响测定结果)
(3)27:29
(4)600℃
20. 分液漏斗 水槽 AB 浓硫酸 b 有机物 、KOH 与滤纸的主要成分纤维素反应,使滤纸破损。 溶液B中含有氢氧化钾,显碱性,在温度较高时,会与水反应而被消耗,故虚低温烘干。 紫红色;因为锰酸钾在水溶液中不稳定,会全部分解为紫红色的高锰酸钾溶液和二氧化锰固体以及无色的氢氧化钾,故溶液呈现紫红色。
21.(1) CH4 25% 10%
(2) 海底温度较低,在海底加热可燃冰,使其分解成甲烷,消耗能量高 温室效应加剧 化合反应 C、H2
22.(1)CH4
(2) 花椒面 乳化
(3)C6H12O6
(4)+6
答案第1页,共2页
答案第1页,共2页
