第四单元盐化肥巩固练习-2021-2022学年九年级化学人教版(五四学制)全一册(word版有答案)
文档属性
| 名称 | 第四单元盐化肥巩固练习-2021-2022学年九年级化学人教版(五四学制)全一册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 127.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-30 00:00:00 | ||
图片预览



文档简介
第四单元盐化肥巩固练习2021-2022学年九年级化学人教版(五四学制)全一册
一、单选题
1.草木灰能促进作物生长、增强抗病虫害和抗倒伏能力,其主要成分是K2CO3。K2CO3属于
A.钾肥 B.磷肥 C.氮肥 D.复合肥
2.科学地施用化肥是农业增产的重要手段。下列属于氮肥的是
A.K2CO3 B.Ca(H2PO4)2
C.NH4HCO3 D.K2SO4
3.下列实验现象的描述,正确的是
A.铜绿中加入盐酸,生成气泡,溶液最终变成无色
B.燃着的蜡烛熄灭时产生白雾
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.红磷在空气中燃烧产生大量白烟,放热
4.兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。应选用的药品是
A.铁粉和稀盐酸液体中
B.硝酸钾晶体和水
C.碳酸钡粉末和稀硫酸
D.铜粉和硝酸银溶液
5.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是( )
A.NH4NO3 B.KNO3 C.K3PO4 D.KCl
6.下列化学方程式中符合题意且书写正确的是
A.正常雨水偏弱酸性原因:SO3+H2O=H2SO4
B.生活中用天然气作燃料:C2H5OH+3O22CO2+3H2O
C.用小苏打治疗胃酸过多症:NaHCO3+HCl=NaCl+CO2↑+H2O
D.工业上用熟石灰制烧碱:Ca(OH)2+2NaNO3=Ca(NO3)2+2NaOH
7.下列各组物质用稀硫酸不能区分开的是( )
A.镁粉、氧化铜粉 B.NaOH溶液、KOH溶液
C.铁片、铜片 D.Na2CO3溶液、NaCl溶液
8.化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
选项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
A.A B.B C.C D.D
9.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是
A.分离CO2和CO,先用NaOH溶液吸收CO2,再向该溶液中加足量稀盐酸
B.只用一种试剂无法把稀盐酸、氯化钡溶液和硝酸钾三种溶液区别开
C.除去氯化钙溶液中混有的少量稀盐酸,可加入过量碳酸钙,充分反应后过滤
D.只用组内溶液相互混合方法,能将KOH、Na2SO4、CuSO4、MgCl2鉴别开
10.以下归纳和总结完全正确的一组是
A.对酸的认识:①酸溶液中都存在H+②pH小于7的雨水为酸雨
B.对碱的认识:①碱溶液中都存在OH﹣②氨水可以作为氮肥使用
C.对盐的认识:①盐溶液都是中性的②盐类物质就是食盐可食用
D.对氧化物的认识:①氧化物都含有氧元素②氯酸钾是氧化物
11.要鉴别NaCl、MgCl2、酚酞三瓶无色溶液,可选用下列试剂中的
A.AgNO3溶液 B.HCl溶液 C.石蕊试液 D.NaOH溶液
12.某兴趣小组同学在化学老师的指导下,用一定比例的生石灰、纯碱、氯化钠加水调成糊状敷料,涂在鸡蛋外面,制成松花蛋,并对剩余敷料成分进行探究,过程如下:下列说法正确的是( )
A.步骤②中的现象说明滤渣中存在纯碱
B.步骤③的现象说明滤液中一定有氢氧化钙
C.滤液中含有的溶质为氢氧化钠、纯碱
D.上述过程没有涉及到的基本反应类型为分解反应、置换反应
二、简答题
13.过滤后的滤液若出现浑浊,原因可能是什么?浑浊滤液如何处理?
14.为了提高农作物的产量,需要庄稼施肥.以玉米为例,每公顷需施用约1吨尿素,其中只有约20%被玉米吸收,其余会随水流入江中.请回答:
(1)说说你对此现象的看法_____;
(2)对此情况你的建议是_____.
15.小明周末放假回家告诉爸爸学习有关化肥的知识了,爸爸拿出家里的几种化肥分别是氯化铵、碳酸氢铵、硫酸钾、磷矿粉,决定考考他:
(1)各取上述四种化肥进行观察,从外观上即可与其它化肥区别出来的是________________。
(2)给农作物施用碳酸氢铵后要立即盖上,其原因是_____________,铵态氮肥也不能跟草木灰混合使用,其原因是_____________。
(3)为了增强农作物的抗病虫害和抗倒伏能力,应使用上述化肥中的______________。
三、推断题
16.有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是:Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“﹣”表示观察不到明显变化。试回答下面问题:
A B C D E F G
A ﹣ ﹣ ﹣ ﹣ ﹣ ﹣ ↓
B ﹣ ﹣ ﹣ ﹣ ↓ ↓ ↓
C ﹣ ﹣ ﹣ ↓ ﹣ ↓ ↓
D ﹣ ﹣ ↓ ﹣ ↓ ↓ ↓
E ﹣ ↓ ﹣ ↓ ﹣ ↓ ﹣
F ﹣ ↓ ↓ ↓ ↓ ﹣ ↓
G ↓ ↓ ↓ ↓ ﹣ ↓ ﹣
(1)A、G的化学式分别是_______,判断的理由是_______。
(2)写出下列物质间的反应方程式。B和F_______;D和E_______。
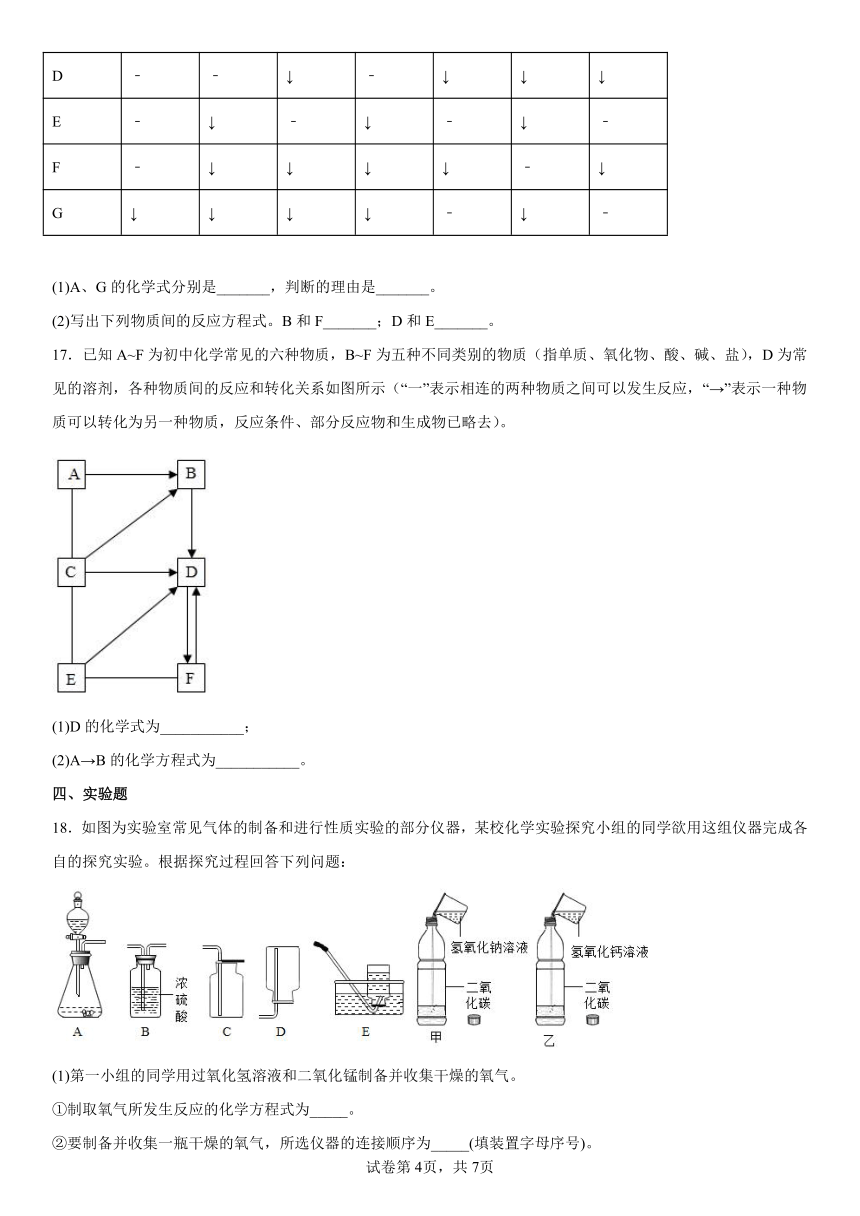
17.已知A~F为初中化学常见的六种物质,B~F为五种不同类别的物质(指单质、氧化物、酸、碱、盐),D为常见的溶剂,各种物质间的反应和转化关系如图所示(“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
(1)D的化学式为___________;
(2)A→B的化学方程式为___________。
四、实验题
18.如图为实验室常见气体的制备和进行性质实验的部分仪器,某校化学实验探究小组的同学欲用这组仪器完成各自的探究实验。根据探究过程回答下列问题:
(1)第一小组的同学用过氧化氢溶液和二氧化锰制备并收集干燥的氧气。
①制取氧气所发生反应的化学方程式为_____。
②要制备并收集一瓶干燥的氧气,所选仪器的连接顺序为_____(填装置字母序号)。
③向气体发生装置内加入药品前,应该进行的操作是_____。
(2)第二小组的同学探究碱溶液与二氧化碳的反应。如图甲、乙所示,分别向盛满二氧化碳的两个塑料瓶中,倒入等体积的氢氧化钠溶液和氢氧化钙溶液,盖紧瓶塞,充分振荡,发现两个塑料瓶变瘪的程度为甲>乙。
①同学们发现乙瓶内液体出现白色浑浊,请写出该反应的化学方程式_____。
②同学们看到甲瓶内的液体没有明显变化,小明同学想检验氢氧化钠溶液是否与二氧化碳发生了反应,他所想到的下列试剂中,不能得到结果的是_____。
A.稀盐酸
B.氯化钡溶液
C.石蕊试液
D.硝酸钙溶液
19.根据下列实验装置图,回答有关问题。
(1)仪器①的名称是__________。
(2)用高锰酸钾制取氧气的化学方程式是__________,应选择的发生装置是_________(填序号)。如需收集较纯净的氧气最好用__________法收集。
(3)如需制取干燥的CO2,装置合理的连接顺序为:__________→C→_________(填序号)。连接装置时,发生装置的出气口应与装置C的__________(填“a”或“b”)端相连。
(4)小东同学在查阅资料时发现:某浓度的Na2CO3溶液和NaHCO3溶液的pH分别为11.0和8.5。由此他得出结论:__________(填“Na2CO3”或“NaHCO3”)的碱性更强。
(5)为了探究CO2和NaOH溶液发生的反应,他将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测得反应过程中温度和pH的变化的结果如图1和图2所示。
①图1中PQ段温度变化的原因可能是_________。
②图2中XY段发生反应的化学方程式为__________,YZ段发生反应的化学方程式为__________。
20.补全实验方案。
实验 实验目的 实验操作
1 检验钙片中含有碳酸钙 ______
2 ______ 先将粗盐放入烧杯中加水溶解,再将浑浊液过滤,最后将澄清滤液蒸发
五、计算题
21.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
22.菱铁矿(主要成分是碳酸亚铁)是炼铁的原料之一,现取20.0 g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中的杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示。
(1)20.0 g菱铁矿中FeCO3的质量分数为________%。
(2)列式计算,恰好完全反应时所得溶液的质量。
(3)向上述所得溶液中加入____________g水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。
23.下图是某种化肥广告内容,请根据相关信息回答下列问题。
(1)硝酸铵的相对分子质量为 。
(2)硝酸铵中氮、氢元素的质量比为 。
(3)通过计算判断该广告是否属于虚假广告?(写出计算过程)结论:该广告_____(“是”或“不是”)虚假广告。
(4)40千克NH4NO3与多少千克NH4HCO3(碳酸氢铵)的肥效相同(即含氮元素质量相等)?(写出计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.D
4.D
5.B
6.C
7.B
8.C
9.B
10.B
11.D
12.D
13.原因可能是滤纸破损或液面高于滤纸边缘。浑浊滤液应重新过滤。
14. 化肥的过量使用会造成水污染 应合理使用化肥,最好与农家肥混合使用
15. 磷矿粉 碳酸氢铵性质很不稳定,受热时容易分解,温度越高,分解越快 碱性的草木灰跟铵态氮肥混合使用后,会产生氨气,氨气易挥发,会降低肥效 硫酸钾
16. KCl,AgNO3 物质间混合时只生成一种沉淀的是KCl,生成AgCl为沉淀 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3
17.(1)H2O
(2)Fe+2HCl=FeCl2+H2↑(其他答案合理即可)
18. A、B、C 检查装置气密性 Ca(OH)2+CO2═CaCO3↓+H2O C
19. 试管 A 排水法 B F a Na2CO3(或碳酸钠) 二氧化碳和氢氧化钠反应放出热量
20. 取一片钙片放入试管中,再加入稀盐酸,并将生成的气体导入澄清石灰水中 去除粗盐中难溶性杂质
21.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
22.(1)58(2)解:设生成FeSO4质量为x,CO2质量为y,
FeCO3+H2SO4=FeSO4+CO2+H2O
116 142 44
11.6g x y
,x=15.2g
,y=4.4g
恰好完全反应时,所得溶液的质量为20.0 g-8.4 g+50.0 g-4.4 g=57.2 g
答:恰好完全反应时,所得溶液的质量为57.2 g。
(3)94.8
23.(1)硝酸铵的相对分子质量为:14×2+1×4+16×3=80;
答:硝酸铵的相对分子质量为80。
(2)硝酸铵中氮、氢元素的质量比为(14×2):(1×4)=7:1;
答:硝酸铵中氮、氢元素的质量比为7:1。
(3)纯净硝酸铵中氮元素的质量分数为×100%=35%,35%<38%,
答:该广告属于虚假广告。
(4)40千克NH4NO3与79千克NH4HCO3(碳酸氢铵)的肥效相同。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.草木灰能促进作物生长、增强抗病虫害和抗倒伏能力,其主要成分是K2CO3。K2CO3属于
A.钾肥 B.磷肥 C.氮肥 D.复合肥
2.科学地施用化肥是农业增产的重要手段。下列属于氮肥的是
A.K2CO3 B.Ca(H2PO4)2
C.NH4HCO3 D.K2SO4
3.下列实验现象的描述,正确的是
A.铜绿中加入盐酸,生成气泡,溶液最终变成无色
B.燃着的蜡烛熄灭时产生白雾
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.红磷在空气中燃烧产生大量白烟,放热
4.兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。应选用的药品是
A.铁粉和稀盐酸液体中
B.硝酸钾晶体和水
C.碳酸钡粉末和稀硫酸
D.铜粉和硝酸银溶液
5.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是( )
A.NH4NO3 B.KNO3 C.K3PO4 D.KCl
6.下列化学方程式中符合题意且书写正确的是
A.正常雨水偏弱酸性原因:SO3+H2O=H2SO4
B.生活中用天然气作燃料:C2H5OH+3O22CO2+3H2O
C.用小苏打治疗胃酸过多症:NaHCO3+HCl=NaCl+CO2↑+H2O
D.工业上用熟石灰制烧碱:Ca(OH)2+2NaNO3=Ca(NO3)2+2NaOH
7.下列各组物质用稀硫酸不能区分开的是( )
A.镁粉、氧化铜粉 B.NaOH溶液、KOH溶液
C.铁片、铜片 D.Na2CO3溶液、NaCl溶液
8.化肥对提高农作物的产量具有重要作用。某同学设计了如图实验对几种化肥进行简易鉴别:
取少量固体分别进行实验,如表方案中不合理的是( )
选项 实验① 实验②
A 观察固体颜色 与熟石灰粉末混合研磨
B 观察固体颜色 加入Ba(NO3)2溶液中
C 加入足量水中 加入AgNO3溶液中
D 加入足量水中 加入Ba(OH)2溶液中
A.A B.B C.C D.D
9.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是
A.分离CO2和CO,先用NaOH溶液吸收CO2,再向该溶液中加足量稀盐酸
B.只用一种试剂无法把稀盐酸、氯化钡溶液和硝酸钾三种溶液区别开
C.除去氯化钙溶液中混有的少量稀盐酸,可加入过量碳酸钙,充分反应后过滤
D.只用组内溶液相互混合方法,能将KOH、Na2SO4、CuSO4、MgCl2鉴别开
10.以下归纳和总结完全正确的一组是
A.对酸的认识:①酸溶液中都存在H+②pH小于7的雨水为酸雨
B.对碱的认识:①碱溶液中都存在OH﹣②氨水可以作为氮肥使用
C.对盐的认识:①盐溶液都是中性的②盐类物质就是食盐可食用
D.对氧化物的认识:①氧化物都含有氧元素②氯酸钾是氧化物
11.要鉴别NaCl、MgCl2、酚酞三瓶无色溶液,可选用下列试剂中的
A.AgNO3溶液 B.HCl溶液 C.石蕊试液 D.NaOH溶液
12.某兴趣小组同学在化学老师的指导下,用一定比例的生石灰、纯碱、氯化钠加水调成糊状敷料,涂在鸡蛋外面,制成松花蛋,并对剩余敷料成分进行探究,过程如下:下列说法正确的是( )
A.步骤②中的现象说明滤渣中存在纯碱
B.步骤③的现象说明滤液中一定有氢氧化钙
C.滤液中含有的溶质为氢氧化钠、纯碱
D.上述过程没有涉及到的基本反应类型为分解反应、置换反应
二、简答题
13.过滤后的滤液若出现浑浊,原因可能是什么?浑浊滤液如何处理?
14.为了提高农作物的产量,需要庄稼施肥.以玉米为例,每公顷需施用约1吨尿素,其中只有约20%被玉米吸收,其余会随水流入江中.请回答:
(1)说说你对此现象的看法_____;
(2)对此情况你的建议是_____.
15.小明周末放假回家告诉爸爸学习有关化肥的知识了,爸爸拿出家里的几种化肥分别是氯化铵、碳酸氢铵、硫酸钾、磷矿粉,决定考考他:
(1)各取上述四种化肥进行观察,从外观上即可与其它化肥区别出来的是________________。
(2)给农作物施用碳酸氢铵后要立即盖上,其原因是_____________,铵态氮肥也不能跟草木灰混合使用,其原因是_____________。
(3)为了增强农作物的抗病虫害和抗倒伏能力,应使用上述化肥中的______________。
三、推断题
16.有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是:Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“﹣”表示观察不到明显变化。试回答下面问题:
A B C D E F G
A ﹣ ﹣ ﹣ ﹣ ﹣ ﹣ ↓
B ﹣ ﹣ ﹣ ﹣ ↓ ↓ ↓
C ﹣ ﹣ ﹣ ↓ ﹣ ↓ ↓
D ﹣ ﹣ ↓ ﹣ ↓ ↓ ↓
E ﹣ ↓ ﹣ ↓ ﹣ ↓ ﹣
F ﹣ ↓ ↓ ↓ ↓ ﹣ ↓
G ↓ ↓ ↓ ↓ ﹣ ↓ ﹣
(1)A、G的化学式分别是_______,判断的理由是_______。
(2)写出下列物质间的反应方程式。B和F_______;D和E_______。
17.已知A~F为初中化学常见的六种物质,B~F为五种不同类别的物质(指单质、氧化物、酸、碱、盐),D为常见的溶剂,各种物质间的反应和转化关系如图所示(“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
(1)D的化学式为___________;
(2)A→B的化学方程式为___________。
四、实验题
18.如图为实验室常见气体的制备和进行性质实验的部分仪器,某校化学实验探究小组的同学欲用这组仪器完成各自的探究实验。根据探究过程回答下列问题:
(1)第一小组的同学用过氧化氢溶液和二氧化锰制备并收集干燥的氧气。
①制取氧气所发生反应的化学方程式为_____。
②要制备并收集一瓶干燥的氧气,所选仪器的连接顺序为_____(填装置字母序号)。
③向气体发生装置内加入药品前,应该进行的操作是_____。
(2)第二小组的同学探究碱溶液与二氧化碳的反应。如图甲、乙所示,分别向盛满二氧化碳的两个塑料瓶中,倒入等体积的氢氧化钠溶液和氢氧化钙溶液,盖紧瓶塞,充分振荡,发现两个塑料瓶变瘪的程度为甲>乙。
①同学们发现乙瓶内液体出现白色浑浊,请写出该反应的化学方程式_____。
②同学们看到甲瓶内的液体没有明显变化,小明同学想检验氢氧化钠溶液是否与二氧化碳发生了反应,他所想到的下列试剂中,不能得到结果的是_____。
A.稀盐酸
B.氯化钡溶液
C.石蕊试液
D.硝酸钙溶液
19.根据下列实验装置图,回答有关问题。
(1)仪器①的名称是__________。
(2)用高锰酸钾制取氧气的化学方程式是__________,应选择的发生装置是_________(填序号)。如需收集较纯净的氧气最好用__________法收集。
(3)如需制取干燥的CO2,装置合理的连接顺序为:__________→C→_________(填序号)。连接装置时,发生装置的出气口应与装置C的__________(填“a”或“b”)端相连。
(4)小东同学在查阅资料时发现:某浓度的Na2CO3溶液和NaHCO3溶液的pH分别为11.0和8.5。由此他得出结论:__________(填“Na2CO3”或“NaHCO3”)的碱性更强。
(5)为了探究CO2和NaOH溶液发生的反应,他将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测得反应过程中温度和pH的变化的结果如图1和图2所示。
①图1中PQ段温度变化的原因可能是_________。
②图2中XY段发生反应的化学方程式为__________,YZ段发生反应的化学方程式为__________。
20.补全实验方案。
实验 实验目的 实验操作
1 检验钙片中含有碳酸钙 ______
2 ______ 先将粗盐放入烧杯中加水溶解,再将浑浊液过滤,最后将澄清滤液蒸发
五、计算题
21.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
22.菱铁矿(主要成分是碳酸亚铁)是炼铁的原料之一,现取20.0 g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中的杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示。
(1)20.0 g菱铁矿中FeCO3的质量分数为________%。
(2)列式计算,恰好完全反应时所得溶液的质量。
(3)向上述所得溶液中加入____________g水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。
23.下图是某种化肥广告内容,请根据相关信息回答下列问题。
(1)硝酸铵的相对分子质量为 。
(2)硝酸铵中氮、氢元素的质量比为 。
(3)通过计算判断该广告是否属于虚假广告?(写出计算过程)结论:该广告_____(“是”或“不是”)虚假广告。
(4)40千克NH4NO3与多少千克NH4HCO3(碳酸氢铵)的肥效相同(即含氮元素质量相等)?(写出计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.D
4.D
5.B
6.C
7.B
8.C
9.B
10.B
11.D
12.D
13.原因可能是滤纸破损或液面高于滤纸边缘。浑浊滤液应重新过滤。
14. 化肥的过量使用会造成水污染 应合理使用化肥,最好与农家肥混合使用
15. 磷矿粉 碳酸氢铵性质很不稳定,受热时容易分解,温度越高,分解越快 碱性的草木灰跟铵态氮肥混合使用后,会产生氨气,氨气易挥发,会降低肥效 硫酸钾
16. KCl,AgNO3 物质间混合时只生成一种沉淀的是KCl,生成AgCl为沉淀 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3
17.(1)H2O
(2)Fe+2HCl=FeCl2+H2↑(其他答案合理即可)
18. A、B、C 检查装置气密性 Ca(OH)2+CO2═CaCO3↓+H2O C
19. 试管 A 排水法 B F a Na2CO3(或碳酸钠) 二氧化碳和氢氧化钠反应放出热量
20. 取一片钙片放入试管中,再加入稀盐酸,并将生成的气体导入澄清石灰水中 去除粗盐中难溶性杂质
21.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
22.(1)58(2)解:设生成FeSO4质量为x,CO2质量为y,
FeCO3+H2SO4=FeSO4+CO2+H2O
116 142 44
11.6g x y
,x=15.2g
,y=4.4g
恰好完全反应时,所得溶液的质量为20.0 g-8.4 g+50.0 g-4.4 g=57.2 g
答:恰好完全反应时,所得溶液的质量为57.2 g。
(3)94.8
23.(1)硝酸铵的相对分子质量为:14×2+1×4+16×3=80;
答:硝酸铵的相对分子质量为80。
(2)硝酸铵中氮、氢元素的质量比为(14×2):(1×4)=7:1;
答:硝酸铵中氮、氢元素的质量比为7:1。
(3)纯净硝酸铵中氮元素的质量分数为×100%=35%,35%<38%,
答:该广告属于虚假广告。
(4)40千克NH4NO3与79千克NH4HCO3(碳酸氢铵)的肥效相同。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
