6.4珍惜和保护金属资源-2021-2022学年九年级化学科粤版(2012)下册(word版有答案)
文档属性
| 名称 | 6.4珍惜和保护金属资源-2021-2022学年九年级化学科粤版(2012)下册(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 268.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-31 00:00:00 | ||
图片预览




文档简介
科粤版九年级化学下册 6.4 珍惜和保护金属资源
一、单选题
1.保护资源、合理利用资源是每个公民的责任,下列做法不利于保护金属资源的是
A.铸铁暖气片金属表面刷银粉形成保护层
B.国家加大开采矿物的力度,并鼓励私人到处开采
C.及时除去铁制品表面的铁锈
D.回收废旧易拉罐
2.下列有关金属的说法正确的是( )
A.钢的含碳量比生铁的含碳量高
B.防止金属锈蚀是保护金属资源的有效途径
C.镁带在空气中燃烧,发出耀眼白光,生成黑色固体
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝不与氧气反应
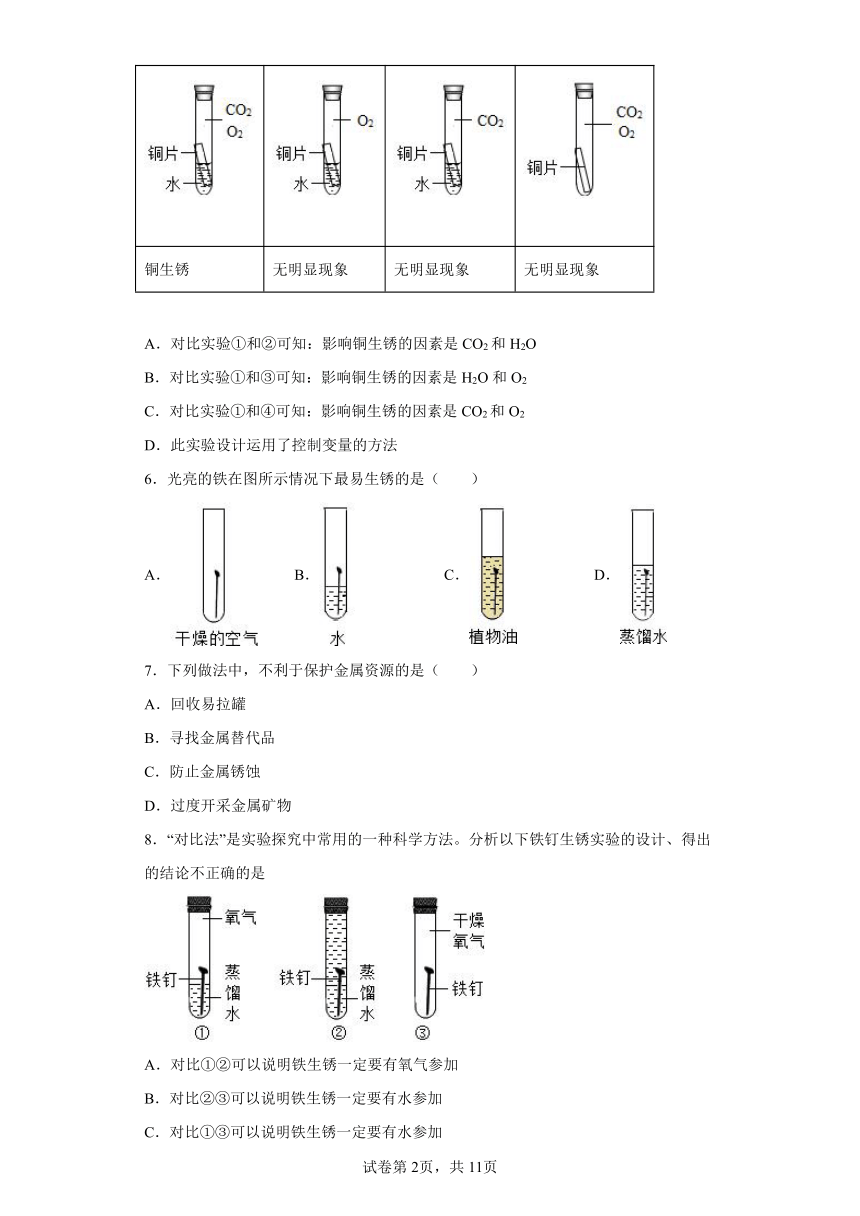
3.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
4.根据你所具备的化学知识和生活经验,指出铁钉在下列哪种情况下最容易生锈
A. B. C. D.
5.为了探究影响铜生锈的因素,设计如下实验,有关分析正确的是
实验① 实验② 实验③ 实验④
铜生锈 无明显现象 无明显现象 无明显现象
A.对比实验①和②可知:影响铜生锈的因素是CO2和H2O
B.对比实验①和③可知:影响铜生锈的因素是H2O和O2
C.对比实验①和④可知:影响铜生锈的因素是CO2和O2
D.此实验设计运用了控制变量的方法
6.光亮的铁在图所示情况下最易生锈的是( )
A. B. C. D.
7.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐
B.寻找金属替代品
C.防止金属锈蚀
D.过度开采金属矿物
8.“对比法”是实验探究中常用的一种科学方法。分析以下铁钉生锈实验的设计、得出的结论不正确的是
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.对比①②③可以说明铁生锈必须水和氧气同时参加
9.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
10.下列关于回收铝饮料罐说法不正确的是
A.回收铝饮料罐可以节约金属资源
B.回收铝饮料罐可以节约能源
C.回收铝饮料罐可以减少对环境的污染
D.回收一个铝饮料罐比制造一个铝饮料罐要贵
11.如图是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )
A.丁中铁钉生锈最严重
B.丙中的铁钉不生锈
C.铁生锈的主要条件是与空气、水直接接触
D.甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊
12.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
13.下列铁制品在使用和保存时的注意事项,不正确的是
A.避免铁制品长期接触潮湿空气
B.用铁制容器盛装食醋
C.应保持铁制品表面洁净、干燥
D.为防止机床生锈,在机床表面上涂油
14.下列措施中,不能防止铁制品锈蚀的是( )
A.喷漆
B.镀一层耐腐蚀的金属
C.制成不锈钢
D.存放在潮湿的空气中
15.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐
B.寻找金属替代品
C.防止金属锈蚀
D.过度开采金属矿物
16.下列所举措施,不能有效保护金属资源的是
A.寻找、开发金属的替代品
B.加速国内矿产资源的开采
C.对易生锈的铁制品采取涂油、喷漆、搪瓷、镀金等措施
D.加强废旧金属的回收利用
二、综合应用题
17.人类文明的发展和社会的进步与材料密切相关。请根据相关信息回答下列问题:
(1)解码智慧冬奥:
①2022年北京冬奥会,碲化镉发电玻璃成为绿色和科技办奥交汇的创新点。如图是碲的原子结构示意图,有关信息正确的是______。
A.碲是金属元素 B.碲的核电荷数为52
C.相对原子质量为127.6g D.蹄元素位于第六周期
②氢能“黑科技”将亮相北京冬奥会。冬奥会“飞扬”火炬科技亮点之一是采用氢气作为燃料,其优点是什么______(答出一点);写出氢气燃烧的化学方程式______。
③冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。金属资源储量有限,钢铁生锈是世界面临的难题。铁生锈的主要条件是什么______。
(2)近年来,我国高铁建设飞速发展,建造高铁需要大量的钢铁。图为模拟炼铁的装置,写出a中发生反应的化学方程式______;描述b处反应的现象______。
(3)2021年12月8日,我国首座大型二氧化碳循环发电机组投入运行。实验室若用500g含碳酸钙80%的石灰石与足量的稀盐酸反应,可制得二氧化碳多少g?
18.铁及其化合物在生产生活中发挥着重要作用。
(1)我国早在春秋战国时期就开始生产和使用铁器。
①深埋的古墓中有些铁器保存至今是因为______(选填序号)。
a.铁不活泼 b.密封少氧 c.干燥少水
②钢铁露置在空气中易生锈,请提出防止其生锈的一种措施_______。
(2)生活中我们常用铁锅炒菜,主要利用了铁良好的______性。
(3)高铁酸钠(Na2FeO4)是一种新型高效的净水剂,其中铁元素的化合价为______。
(4)“暖宝宝”使用时,铁、氧气和水反应生成Fe(OH)3,该反应的化学方程式为______。
二、铁红(Fe2O3)的制备
用硫酸厂的炉渣(含有Fe2O3、FeO、SiO2、CaSO4)制备化工原料铁红的实验流程如下。
(5)酸溶前,将炉渣粉碎的主要目的是_______。
(6)滤液中含有H2SO4、FeSO4和Fe2(SO4)3,加入Fe粉后全部转化为FeSO4,转化时除Fe与Fe2(SO4)3反应外,还发生反应的化学方程式为______。
(7)写出空气中煅烧FeCO3生成Fe2O3和CO2的化学方程式______。
三、CO还原铁红的探究
上述流程中得到的铁红混有少量的FeCO3,用下图装置进行实验,测定Fe2O3的含量并对反应及产物进行探究。取25.00g样品置于装置A中,控制不同的温度对其加热,测得装置B质量变化如下表。
表:装置B的质量变化
温度/℃ 装置B/g
室温 400.00
290 402.20
600 403.96
资料:①FeCO3隔绝空气加热至282℃开始分解,290℃分解完全,生成FeO和CO2。
②500℃时Fe2O3才开始被还原,且温度不同时产物可能是Fe3O4、FeO、Fe。
③碱石灰吸收H2O和CO2。
(8)装配好实验装置后,先要_______,再加药品。
(9)加热前后及过程中均需通入CO,加热后通CO的目的是______。
(10)装置C的作用是______。
(11)样品中Fe2O3的质量分数为_______。
(12)加热到600℃时,装置A中剩余固体的质量为_______g,继续加热至充分反应,最终得到单质铁的质量为______g。
19.(1)地铁是以地下运行为主的城市轨道交通系统。对于济南来讲,地铁承载着城市迭代升级的厚望,当轨道贯穿了这座城市,它代表的不再仅仅是交通,更是一座城市的血脉。地铁建设中各种材料被广泛应用。请你根据学过的知识回答以下问题:
①锰钢主要成分是铁、锰、碳,主要用于制造钢轨、挖掘机铲斗等,锰钢属于__________(填“纯净物”、“混合物”“金属材料”、“有机高分子材料”中的两项)。
②在钢轨上喷涂防锈涂料,可防止钢轨生锈。该防锈方法的原理是________。
③地铁中常用氢氧化镁作为阻燃材料,氢氧化镁不溶于水,可用海水中提取的氯化镁与熟石灰在溶液中反应制取,该制取反应的化学方程式是_________。
(2)从海水中提取食盐的方法主要为盐田法,这是一种古老而至 今仍广泛沿用的方法。海水晒盐的流程如下:
①海水晒盐后得到的母液是当时温度下氯化钠的_______(填“饱和”或“不饱和”)溶液。
②如图是NaCl、Na2CO3两种物质的溶解度曲线,t1°C时,Na2CO3的溶解度________NaCl的溶解度(填“大度于”“等于”“小于”之一);该温度时,将20gNa2CO3粉末放入盛有150g水的烧杯中,充分溶解后,所得溶液的质量是________g;若Na2CO3中混有少量的NaCl,可采用____结晶的方法提纯Na2CO3。
20.金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)在铁制品表面覆盖保护膜可防锈的原理是_____;金属制成合金后其抗腐蚀性增强,合金的硬度比组成它的纯金属的硬度_____(填“大”或“小”)。
(2)如图是实验室炼铁的示意图,某学校采用“问题探究式”课堂教学,从而解决问题:请你参与完成下列问题。
①A处的现象是_____;C处进行尾气处理的原因是_____。
②请从微观角度分析,CO、CO2性质不同原因_____;
③小明同学认为尾气可先储存在瓶内,然后再处理,如图是他设计的贮气瓶,a、b两管应如何伸入,请将图补充完整(尾气从a管通入)_____。
(3)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①判断X、Y、Z和银四种金属的活动性由强到弱的顺序_____。
②依据常见金属的活动性顺序能具体确定X物质为_____,写出X与硝酸银溶液反应的化学方程式_____。
(4)若将一定质量的Al放入Cu(NO3)2和Mg(NO3)2的混合溶液中,充分反应后过滤,所得滤液一定含有的溶质是_____(写化学式),写出上述过程中发生反应的化学方程式_____,反应后溶液的质量比反应前_____(填“大”或“小”)。
(5)如图是工业炼铁示意图,请写出符合以下要求的两个化学方程式:分解反应_____,有铁生成的反应_____。
21.多角度认识物质能帮助我们更全面地了解物质世界。以金属为例回答列问题:
(1)认识金属的性质
如图,用粗木棍在涂有蜡的锌板上写“福”、“州”两个字,露出下面的锌板。向“福”字上滴加稀盐酸,向“州”字上滴加CuSO4溶液。
①“福”字上的现象是______;
②“州”字上有红色物质析出,用化学方程式解释:______。
(2)认识金属的制备
工业上,金属钨(W)可由氢气和三氧化钨(WO3)在高温下发生置换反应制得。写出该反应的化学方程式______。
(3)如下图,利用W形管完成一氧化碳还原氧化铁实验。已知一氧化碳还原氧化铁的反应是分步进行:
;;
①实验中,B处酒精灯火焰外围加装防风罩的原因是______。
②为得到纯铁,当红棕色粉末全部变黑时,不能立刻停止加热,应再加热一段时间,原因是______。
③实验一段时间,如何证明黑色粉末中会含有铁粉______(写出具体实验过程)。
(4)铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象
【实验结论】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小,
【实验结论】铁生锈实际上是铁与空气中的______(填名称)发生反应的结果。
【实验思考】
①当铁丝足量,时间足够长:实验③进入试管内的水的体积约占试管体积的______。
②该实验创新之处在于:可根据铁丝表面的铁锈和______两种现象来判断铁丝反应进行的情况。
③铝比铁活泼,但铝难腐蚀,原因是______(用化学方程式表示)
④要防止铁生锈,可采用______(写一种方法):
22.暖贴发热是利用了铁粉生锈放出热量的原理,某校学习小组在实验室验证铁生锈的条件并探究影响铁生锈速率的因素。
【实验1】验证铁生锈的条件
(1)如图进行实验A和B,得出铁生锈需要与氧气接触的结论,实验现象是________。
(2)请设计实验C与实验B对比,证明铁生锈需要与水接触:在图C框内画出实验装置图______。
【实验2】探究影响铁生锈速率的因素
【查阅资料】暖贴发热是利用了铁粉生锈放出热量的原理,暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
【猜想假设】猜想一:活性炭能加快铁粉生锈的速率。
猜想二:食盐能加快铁粉生锈的速率。
【进行实验】表中是2 g铁粉、5 g水与不同量活性炭、食盐均匀混合后,在10分钟内温度上升的实验记录。
实验编号 活性炭/g 食盐/g 温度上升值/℃
① 0 0 0.1
② 0.2 0 22.0
③ x 0.1 3.1
④ 0.2 0.1 56.3
【解释与结论】
(3)表中x的值为________。
(4)对比实验①和③,得出的结论是________。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,最少需要对比实验________ (填实验编号)。
【拓展应用】同学们通过测量下表实验装置中氧气含量的变化也可验证铁生锈需要与水接触以及活性炭与食盐同时存在会大幅度加快铁生锈速率。
实验装置 序号 其他试剂 200 s时O2的含量
Ⅰ 干燥剂 21%
Ⅱ 10滴水 X
Ⅲ 10滴水和1.0 g食盐 8%
(6)对比实验Ⅰ和Ⅱ,可知铁生锈需要与_______________,测得X的数值范围是________试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.A
4.C
5.D
6.B
7.D
8.B
9.D
10.D
11.A
12.D
13.B
14.D
15.D
16.B
17.(1) B 燃烧产物是水,无污染 铁与O2、H2O等同时接触
(2) 澄清石灰水变浑浊
(3)176g
解:设:可制得二氧化碳的质量为x,
答:可制得二氧化碳176g。
18.(1) bc##cb 喷漆
(2)导热
(3)+6
(4)
(5)增大接触面积,加快反应速率
(6)
(7)
(8)检查装置的气密性
(9)作还原剂
(10)防止空气中的CO2和H2O进入B装置
(11)76.8%
(12) 22.16 16.24
19. 混合物、金属材料 隔绝氧气和水 饱和 小于 165 降温
20. 隔绝氧气和水蒸气 大 红棕色粉末变为黑色 一氧化碳有毒,排放到空气中会污染空气(意思对即可) 分子的构成不同 Y、X、Ag、Z Cu或铜 Al(NO3)3、Mg(NO3)2 小
21.(1) 产生气泡
(2)
(3) 集中火焰、提高温度 黑色粉末中可能混有四氧化三铁、氧化亚铁 取样,加入适量稀盐酸,产生气泡,说明黑色粉末中含有铁粉
(4) 氧气和水 五分之一##1/5 试管内液面上升
刷漆
22.(1)A中铁钉不生锈,B中铁钉生锈
(2)
(3)0
(4)食盐能加快铁粉生锈的速率
(5)②③④
(6) 水接触 8% 21%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.保护资源、合理利用资源是每个公民的责任,下列做法不利于保护金属资源的是
A.铸铁暖气片金属表面刷银粉形成保护层
B.国家加大开采矿物的力度,并鼓励私人到处开采
C.及时除去铁制品表面的铁锈
D.回收废旧易拉罐
2.下列有关金属的说法正确的是( )
A.钢的含碳量比生铁的含碳量高
B.防止金属锈蚀是保护金属资源的有效途径
C.镁带在空气中燃烧,发出耀眼白光,生成黑色固体
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝不与氧气反应
3.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
4.根据你所具备的化学知识和生活经验,指出铁钉在下列哪种情况下最容易生锈
A. B. C. D.
5.为了探究影响铜生锈的因素,设计如下实验,有关分析正确的是
实验① 实验② 实验③ 实验④
铜生锈 无明显现象 无明显现象 无明显现象
A.对比实验①和②可知:影响铜生锈的因素是CO2和H2O
B.对比实验①和③可知:影响铜生锈的因素是H2O和O2
C.对比实验①和④可知:影响铜生锈的因素是CO2和O2
D.此实验设计运用了控制变量的方法
6.光亮的铁在图所示情况下最易生锈的是( )
A. B. C. D.
7.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐
B.寻找金属替代品
C.防止金属锈蚀
D.过度开采金属矿物
8.“对比法”是实验探究中常用的一种科学方法。分析以下铁钉生锈实验的设计、得出的结论不正确的是
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.对比①②③可以说明铁生锈必须水和氧气同时参加
9.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
10.下列关于回收铝饮料罐说法不正确的是
A.回收铝饮料罐可以节约金属资源
B.回收铝饮料罐可以节约能源
C.回收铝饮料罐可以减少对环境的污染
D.回收一个铝饮料罐比制造一个铝饮料罐要贵
11.如图是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )
A.丁中铁钉生锈最严重
B.丙中的铁钉不生锈
C.铁生锈的主要条件是与空气、水直接接触
D.甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊
12.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
13.下列铁制品在使用和保存时的注意事项,不正确的是
A.避免铁制品长期接触潮湿空气
B.用铁制容器盛装食醋
C.应保持铁制品表面洁净、干燥
D.为防止机床生锈,在机床表面上涂油
14.下列措施中,不能防止铁制品锈蚀的是( )
A.喷漆
B.镀一层耐腐蚀的金属
C.制成不锈钢
D.存放在潮湿的空气中
15.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐
B.寻找金属替代品
C.防止金属锈蚀
D.过度开采金属矿物
16.下列所举措施,不能有效保护金属资源的是
A.寻找、开发金属的替代品
B.加速国内矿产资源的开采
C.对易生锈的铁制品采取涂油、喷漆、搪瓷、镀金等措施
D.加强废旧金属的回收利用
二、综合应用题
17.人类文明的发展和社会的进步与材料密切相关。请根据相关信息回答下列问题:
(1)解码智慧冬奥:
①2022年北京冬奥会,碲化镉发电玻璃成为绿色和科技办奥交汇的创新点。如图是碲的原子结构示意图,有关信息正确的是______。
A.碲是金属元素 B.碲的核电荷数为52
C.相对原子质量为127.6g D.蹄元素位于第六周期
②氢能“黑科技”将亮相北京冬奥会。冬奥会“飞扬”火炬科技亮点之一是采用氢气作为燃料,其优点是什么______(答出一点);写出氢气燃烧的化学方程式______。
③冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。金属资源储量有限,钢铁生锈是世界面临的难题。铁生锈的主要条件是什么______。
(2)近年来,我国高铁建设飞速发展,建造高铁需要大量的钢铁。图为模拟炼铁的装置,写出a中发生反应的化学方程式______;描述b处反应的现象______。
(3)2021年12月8日,我国首座大型二氧化碳循环发电机组投入运行。实验室若用500g含碳酸钙80%的石灰石与足量的稀盐酸反应,可制得二氧化碳多少g?
18.铁及其化合物在生产生活中发挥着重要作用。
(1)我国早在春秋战国时期就开始生产和使用铁器。
①深埋的古墓中有些铁器保存至今是因为______(选填序号)。
a.铁不活泼 b.密封少氧 c.干燥少水
②钢铁露置在空气中易生锈,请提出防止其生锈的一种措施_______。
(2)生活中我们常用铁锅炒菜,主要利用了铁良好的______性。
(3)高铁酸钠(Na2FeO4)是一种新型高效的净水剂,其中铁元素的化合价为______。
(4)“暖宝宝”使用时,铁、氧气和水反应生成Fe(OH)3,该反应的化学方程式为______。
二、铁红(Fe2O3)的制备
用硫酸厂的炉渣(含有Fe2O3、FeO、SiO2、CaSO4)制备化工原料铁红的实验流程如下。
(5)酸溶前,将炉渣粉碎的主要目的是_______。
(6)滤液中含有H2SO4、FeSO4和Fe2(SO4)3,加入Fe粉后全部转化为FeSO4,转化时除Fe与Fe2(SO4)3反应外,还发生反应的化学方程式为______。
(7)写出空气中煅烧FeCO3生成Fe2O3和CO2的化学方程式______。
三、CO还原铁红的探究
上述流程中得到的铁红混有少量的FeCO3,用下图装置进行实验,测定Fe2O3的含量并对反应及产物进行探究。取25.00g样品置于装置A中,控制不同的温度对其加热,测得装置B质量变化如下表。
表:装置B的质量变化
温度/℃ 装置B/g
室温 400.00
290 402.20
600 403.96
资料:①FeCO3隔绝空气加热至282℃开始分解,290℃分解完全,生成FeO和CO2。
②500℃时Fe2O3才开始被还原,且温度不同时产物可能是Fe3O4、FeO、Fe。
③碱石灰吸收H2O和CO2。
(8)装配好实验装置后,先要_______,再加药品。
(9)加热前后及过程中均需通入CO,加热后通CO的目的是______。
(10)装置C的作用是______。
(11)样品中Fe2O3的质量分数为_______。
(12)加热到600℃时,装置A中剩余固体的质量为_______g,继续加热至充分反应,最终得到单质铁的质量为______g。
19.(1)地铁是以地下运行为主的城市轨道交通系统。对于济南来讲,地铁承载着城市迭代升级的厚望,当轨道贯穿了这座城市,它代表的不再仅仅是交通,更是一座城市的血脉。地铁建设中各种材料被广泛应用。请你根据学过的知识回答以下问题:
①锰钢主要成分是铁、锰、碳,主要用于制造钢轨、挖掘机铲斗等,锰钢属于__________(填“纯净物”、“混合物”“金属材料”、“有机高分子材料”中的两项)。
②在钢轨上喷涂防锈涂料,可防止钢轨生锈。该防锈方法的原理是________。
③地铁中常用氢氧化镁作为阻燃材料,氢氧化镁不溶于水,可用海水中提取的氯化镁与熟石灰在溶液中反应制取,该制取反应的化学方程式是_________。
(2)从海水中提取食盐的方法主要为盐田法,这是一种古老而至 今仍广泛沿用的方法。海水晒盐的流程如下:
①海水晒盐后得到的母液是当时温度下氯化钠的_______(填“饱和”或“不饱和”)溶液。
②如图是NaCl、Na2CO3两种物质的溶解度曲线,t1°C时,Na2CO3的溶解度________NaCl的溶解度(填“大度于”“等于”“小于”之一);该温度时,将20gNa2CO3粉末放入盛有150g水的烧杯中,充分溶解后,所得溶液的质量是________g;若Na2CO3中混有少量的NaCl,可采用____结晶的方法提纯Na2CO3。
20.金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)在铁制品表面覆盖保护膜可防锈的原理是_____;金属制成合金后其抗腐蚀性增强,合金的硬度比组成它的纯金属的硬度_____(填“大”或“小”)。
(2)如图是实验室炼铁的示意图,某学校采用“问题探究式”课堂教学,从而解决问题:请你参与完成下列问题。
①A处的现象是_____;C处进行尾气处理的原因是_____。
②请从微观角度分析,CO、CO2性质不同原因_____;
③小明同学认为尾气可先储存在瓶内,然后再处理,如图是他设计的贮气瓶,a、b两管应如何伸入,请将图补充完整(尾气从a管通入)_____。
(3)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①判断X、Y、Z和银四种金属的活动性由强到弱的顺序_____。
②依据常见金属的活动性顺序能具体确定X物质为_____,写出X与硝酸银溶液反应的化学方程式_____。
(4)若将一定质量的Al放入Cu(NO3)2和Mg(NO3)2的混合溶液中,充分反应后过滤,所得滤液一定含有的溶质是_____(写化学式),写出上述过程中发生反应的化学方程式_____,反应后溶液的质量比反应前_____(填“大”或“小”)。
(5)如图是工业炼铁示意图,请写出符合以下要求的两个化学方程式:分解反应_____,有铁生成的反应_____。
21.多角度认识物质能帮助我们更全面地了解物质世界。以金属为例回答列问题:
(1)认识金属的性质
如图,用粗木棍在涂有蜡的锌板上写“福”、“州”两个字,露出下面的锌板。向“福”字上滴加稀盐酸,向“州”字上滴加CuSO4溶液。
①“福”字上的现象是______;
②“州”字上有红色物质析出,用化学方程式解释:______。
(2)认识金属的制备
工业上,金属钨(W)可由氢气和三氧化钨(WO3)在高温下发生置换反应制得。写出该反应的化学方程式______。
(3)如下图,利用W形管完成一氧化碳还原氧化铁实验。已知一氧化碳还原氧化铁的反应是分步进行:
;;
①实验中,B处酒精灯火焰外围加装防风罩的原因是______。
②为得到纯铁,当红棕色粉末全部变黑时,不能立刻停止加热,应再加热一段时间,原因是______。
③实验一段时间,如何证明黑色粉末中会含有铁粉______(写出具体实验过程)。
(4)铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象
【实验结论】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小,
【实验结论】铁生锈实际上是铁与空气中的______(填名称)发生反应的结果。
【实验思考】
①当铁丝足量,时间足够长:实验③进入试管内的水的体积约占试管体积的______。
②该实验创新之处在于:可根据铁丝表面的铁锈和______两种现象来判断铁丝反应进行的情况。
③铝比铁活泼,但铝难腐蚀,原因是______(用化学方程式表示)
④要防止铁生锈,可采用______(写一种方法):
22.暖贴发热是利用了铁粉生锈放出热量的原理,某校学习小组在实验室验证铁生锈的条件并探究影响铁生锈速率的因素。
【实验1】验证铁生锈的条件
(1)如图进行实验A和B,得出铁生锈需要与氧气接触的结论,实验现象是________。
(2)请设计实验C与实验B对比,证明铁生锈需要与水接触:在图C框内画出实验装置图______。
【实验2】探究影响铁生锈速率的因素
【查阅资料】暖贴发热是利用了铁粉生锈放出热量的原理,暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
【猜想假设】猜想一:活性炭能加快铁粉生锈的速率。
猜想二:食盐能加快铁粉生锈的速率。
【进行实验】表中是2 g铁粉、5 g水与不同量活性炭、食盐均匀混合后,在10分钟内温度上升的实验记录。
实验编号 活性炭/g 食盐/g 温度上升值/℃
① 0 0 0.1
② 0.2 0 22.0
③ x 0.1 3.1
④ 0.2 0.1 56.3
【解释与结论】
(3)表中x的值为________。
(4)对比实验①和③,得出的结论是________。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,最少需要对比实验________ (填实验编号)。
【拓展应用】同学们通过测量下表实验装置中氧气含量的变化也可验证铁生锈需要与水接触以及活性炭与食盐同时存在会大幅度加快铁生锈速率。
实验装置 序号 其他试剂 200 s时O2的含量
Ⅰ 干燥剂 21%
Ⅱ 10滴水 X
Ⅲ 10滴水和1.0 g食盐 8%
(6)对比实验Ⅰ和Ⅱ,可知铁生锈需要与_______________,测得X的数值范围是________
试卷第1页,共3页
参考答案:
1.B
2.B
3.A
4.C
5.D
6.B
7.D
8.B
9.D
10.D
11.A
12.D
13.B
14.D
15.D
16.B
17.(1) B 燃烧产物是水,无污染 铁与O2、H2O等同时接触
(2) 澄清石灰水变浑浊
(3)176g
解:设:可制得二氧化碳的质量为x,
答:可制得二氧化碳176g。
18.(1) bc##cb 喷漆
(2)导热
(3)+6
(4)
(5)增大接触面积,加快反应速率
(6)
(7)
(8)检查装置的气密性
(9)作还原剂
(10)防止空气中的CO2和H2O进入B装置
(11)76.8%
(12) 22.16 16.24
19. 混合物、金属材料 隔绝氧气和水 饱和 小于 165 降温
20. 隔绝氧气和水蒸气 大 红棕色粉末变为黑色 一氧化碳有毒,排放到空气中会污染空气(意思对即可) 分子的构成不同 Y、X、Ag、Z Cu或铜 Al(NO3)3、Mg(NO3)2 小
21.(1) 产生气泡
(2)
(3) 集中火焰、提高温度 黑色粉末中可能混有四氧化三铁、氧化亚铁 取样,加入适量稀盐酸,产生气泡,说明黑色粉末中含有铁粉
(4) 氧气和水 五分之一##1/5 试管内液面上升
刷漆
22.(1)A中铁钉不生锈,B中铁钉生锈
(2)
(3)0
(4)食盐能加快铁粉生锈的速率
(5)②③④
(6) 水接触 8% 21%
答案第1页,共2页
答案第1页,共2页
