粤教版化学九年级下册同步提优训练 8.2 第4课时 碱溶液的化学性质(word版有答案)
文档属性
| 名称 | 粤教版化学九年级下册同步提优训练 8.2 第4课时 碱溶液的化学性质(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 164.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-31 00:00:00 | ||
图片预览

文档简介
数学
化学
8.2 常见的酸和碱
第4课时 碱溶液的化学性质
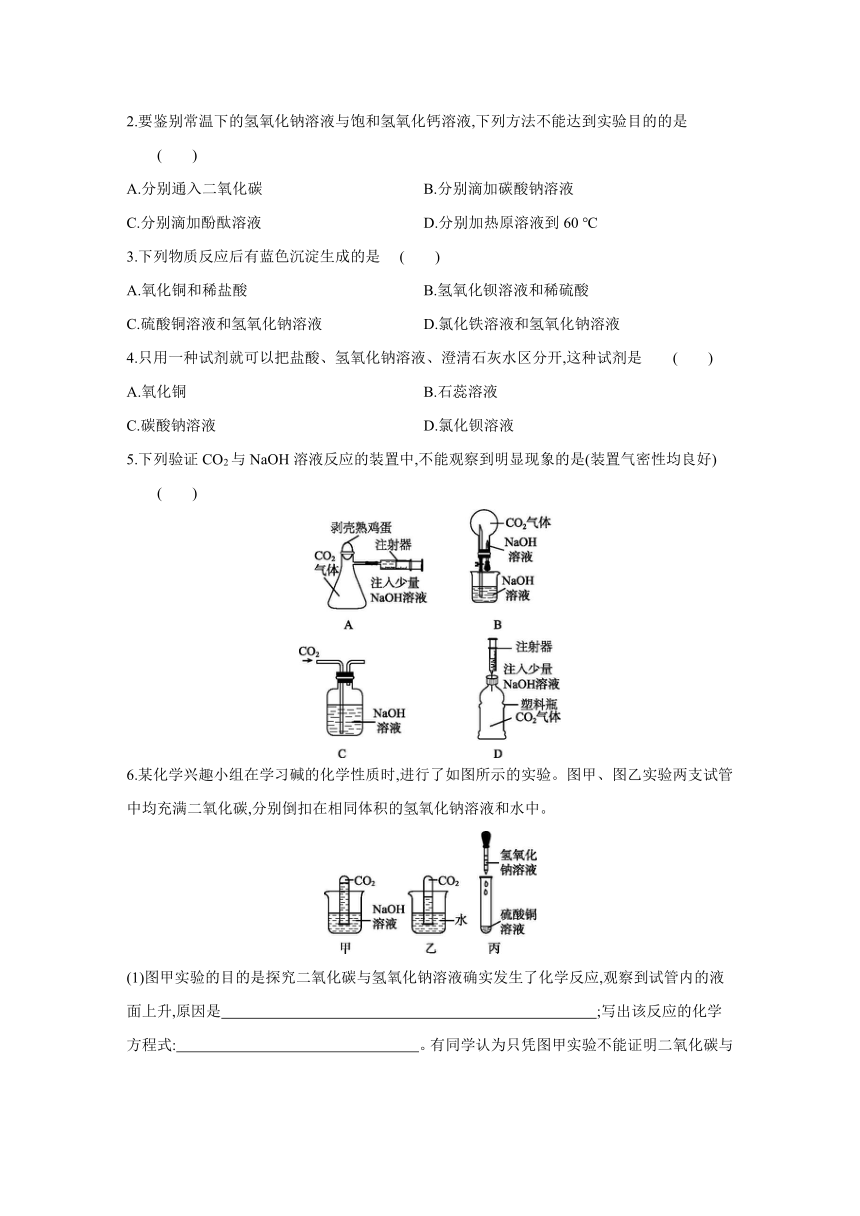
小明同学以NaOH溶液为例用图甲总结了碱溶液的四条化学性质(即NaOH能够与四类物质发生化学变化)。
(1)为了验证反应①,小明将无色酚酞溶液滴入NaOH溶液中,溶液变成 色。
(2)依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为 。
(3)小明用微观示意图(如图乙)来说明反应③的发生,其化学方程式为 。从该图中可以看出,反应后的溶液pH (填“>”“<”或“=”)7。
(4)为了验证反应④能够发生,你选择的物质是 (填字母),该反应的现象是 ,化学方程式为 。
A.Na2CO3 B.HCl C.CuSO4 D.NaCl
[核心知识] 碱溶液具有一些相似的化学性质:
(1)碱溶液能使紫色石蕊溶液变蓝,使无色酚酞溶液变红。
(2)碱溶液能和某些非金属氧化物反应生成盐和水。
(3)碱溶液能和某些盐溶液反应生成新碱和新盐。
[易错点拨]
1.只有碱溶液才具备相似的化学性质,难溶性的碱不具备。
2. 碱与盐的反应中两种反应物都必须可溶。
1.某无色溶液具有如下性质:能使无色酚酞溶液变红;能与CuSO4溶液反应产生蓝色沉淀;能与Na2CO3溶液反应产生白色沉淀。此溶液是 ( )
A.氢氧化钠溶液 B.氯化钙溶液 C.澄清石灰水 D.盐酸
2.要鉴别常温下的氢氧化钠溶液与饱和氢氧化钙溶液,下列方法不能达到实验目的的是 ( )
A.分别通入二氧化碳 B.分别滴加碳酸钠溶液
C.分别滴加酚酞溶液 D.分别加热原溶液到60 ℃
3.下列物质反应后有蓝色沉淀生成的是 ( )
A.氧化铜和稀盐酸 B.氢氧化钡溶液和稀硫酸
C.硫酸铜溶液和氢氧化钠溶液 D.氯化铁溶液和氢氧化钠溶液
4.只用一种试剂就可以把盐酸、氢氧化钠溶液、澄清石灰水区分开,这种试剂是 ( )
A.氧化铜 B.石蕊溶液
C.碳酸钠溶液 D.氯化钡溶液
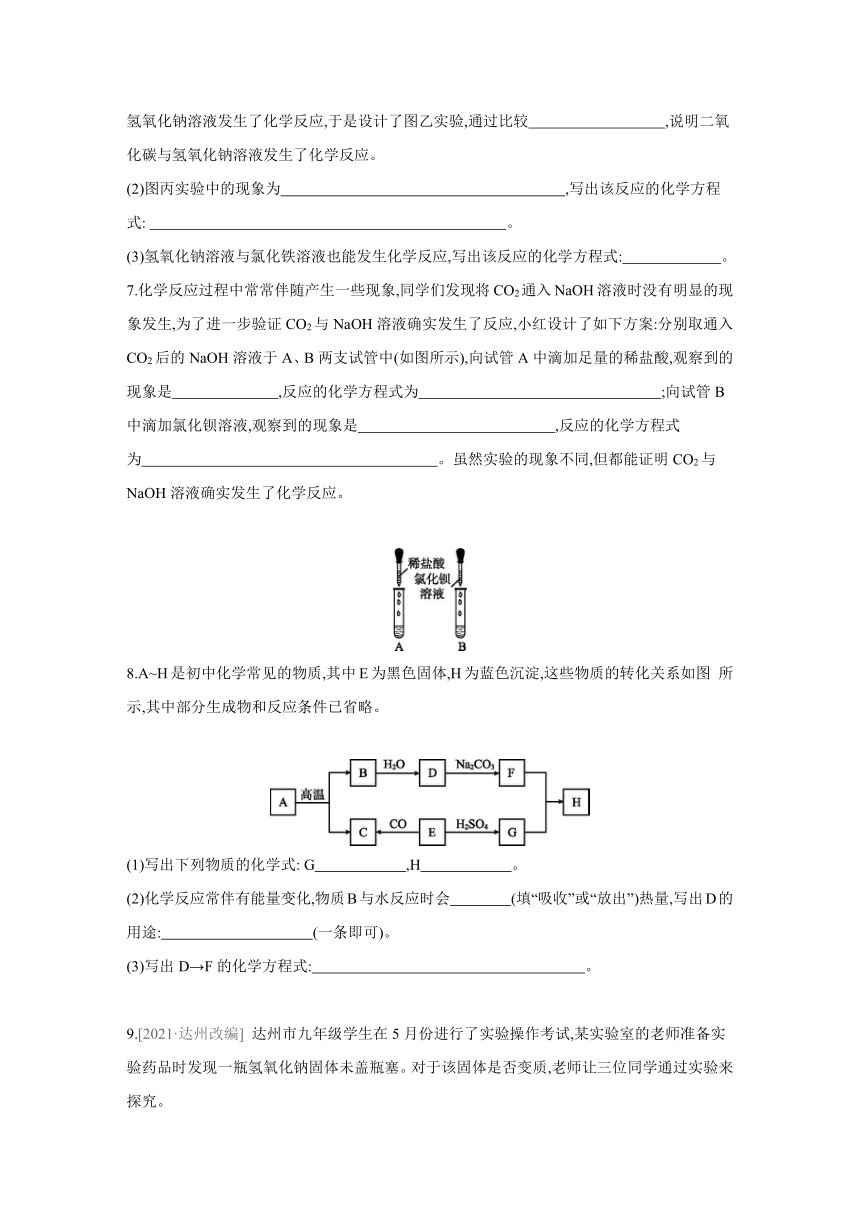
5.下列验证CO2与NaOH溶液反应的装置中,不能观察到明显现象的是(装置气密性均良好) ( )
6.某化学兴趣小组在学习碱的化学性质时,进行了如图所示的实验。图甲、图乙实验两支试管中均充满二氧化碳,分别倒扣在相同体积的氢氧化钠溶液和水中。
(1)图甲实验的目的是探究二氧化碳与氢氧化钠溶液确实发生了化学反应,观察到试管内的液面上升,原因是 ;写出该反应的化学方程式: 。有同学认为只凭图甲实验不能证明二氧化碳与氢氧化钠溶液发生了化学反应,于是设计了图乙实验,通过比较 ,说明二氧化碳与氢氧化钠溶液发生了化学反应。
(2)图丙实验中的现象为 ,写出该反应的化学方程式: 。
(3)氢氧化钠溶液与氯化铁溶液也能发生化学反应,写出该反应的化学方程式: 。
7.化学反应过程中常常伴随产生一些现象,同学们发现将CO2通入NaOH溶液时没有明显的现象发生,为了进一步验证CO2与NaOH溶液确实发生了反应,小红设计了如下方案:分别取通入CO2后的NaOH溶液于A、B两支试管中(如图所示),向试管A中滴加足量的稀盐酸,观察到的现象是 ,反应的化学方程式为 ;向试管B中滴加氯化钡溶液,观察到的现象是 ,反应的化学方程式为 。虽然实验的现象不同,但都能证明CO2与NaOH溶液确实发生了化学反应。
8.A~H是初中化学常见的物质,其中E为黑色固体,H为蓝色沉淀,这些物质的转化关系如图 所示,其中部分生成物和反应条件已省略。
(1)写出下列物质的化学式: G ,H 。
(2)化学反应常伴有能量变化,物质B与水反应时会 (填“吸收”或“放出”)热量,写出D的用途: (一条即可)。
(3)写出D→F的化学方程式: 。
9.[2021·达州改编] 达州市九年级学生在5月份进行了实验操作考试,某实验室的老师准备实验药品时发现一瓶氢氧化钠固体未盖瓶塞。对于该固体是否变质,老师让三位同学通过实验来探究。
[提出问题] 氢氧化钠是否变质 变质程度如何
[猜想与假设]
猜想Ⅰ:没有变质,全部是NaOH;
猜想Ⅱ:部分变质,固体是NaOH和Na2CO3;
猜想Ⅲ:全部变质,全部是Na2CO3。
氢氧化钠变质的原因是 (用化学方程式表示)。
[设计并进行实验] 取一定量的固体溶于水配制成溶液,分成三份,三位同学按照自己的方案进行以下实验:
实验操作 实验现象 实验结论
小李 向第一份溶液中加入无色酚酞溶液 溶液变红 猜想Ⅰ成立
小王 向第二份溶液中滴加几滴稀盐酸 无明显现象 猜想Ⅰ成立
小陈 向第三份溶液中加入CaCl2溶液 猜想Ⅲ成立
[分析讨论]
①小王和小陈认为碳酸钠溶液也能使无色酚酞溶液变红,因此小李的结论不正确。
②经过讨论他们认为通过小王的实验不能得出样品中一定不含Na2CO3的结论,原因是
。
[得出结论] 综合三位同学的实验操作和现象可以得出猜想 成立。
实验结束后大家将废液倒入同一个废液缸内,观察到废液呈红色,且有白色沉淀。他们向废液缸里加入一定量的稀盐酸后得到无色澄清溶液,所得溶液中溶质(酚酞除外)种类最多时,溶液中所含离子有 (填离子符号)。
答案
(1)红 (2)2NaOH+CO2 Na2CO3+H2O
(3)2NaOH+H2SO4Na2SO4+2H2O >
(4)C 有蓝色沉淀生成
2NaOH+CuSO4Na2SO4+Cu(OH)2↓
[应考能力提升练]
1.C 2.C 3.C
4.C 氧化铜只能溶于盐酸,与氢氧化钠和石灰水都不反应;盐酸能使石蕊溶液变红,氢氧化钠和石灰水都能使石蕊溶液变蓝;盐酸与碳酸钠反应产生气泡,氢氧化钠与碳酸钠不反应,石灰水与碳酸钠反应产生白色沉淀,可以区分三者;氯化钡与三者都不反应。
5.C 二氧化碳与氢氧化钠反应后,生成碳酸钠和水,A、B、D装置中的气压由于二氧化碳减少而减小。A中鸡蛋进入容器中;B中打开止水夹,烧瓶中导管有液体喷出; D中塑料瓶变瘪。C中气压不变,无现象。
6.(1)二氧化碳与氢氧化钠溶液发生化学反应,试管内的压强减小,在大气压的作用下液体被压入试管中
2NaOH+CO2Na2CO3+H2O 试管内液面上升的高度
(2)有蓝色沉淀产生,溶液由蓝色变为无色
2NaOH+CuSO4Cu(OH)2↓+Na2SO4
(3)3NaOH+FeCl3Fe(OH)3↓+3NaCl
7.有气泡产生 Na2CO3+2HCl2NaCl+H2O+CO2↑
有白色沉淀产生 Na2CO3+BaCl2BaCO3↓+2NaCl
氢氧化钠和二氧化碳反应后生成碳酸钠,碳酸钠能和盐酸反应生成二氧化碳气体,因此加入足量稀盐酸后会观察到有气泡产生;碳酸钠能和氯化钡反应生成碳酸钡白色沉淀,因此加入氯化钡溶液后会观察到有白色沉淀产生。
8.(1)CuSO4 Cu(OH)2
(2)放出 改良酸性土壤(合理即可)
(3)Ca(OH)2+Na2CO32NaOH+CaCO3↓
9.[猜想与假设] 2NaOH+CO2Na2CO3+H2O
[设计并进行实验] 产生白色沉淀
[分析讨论] ②当氢氧化钠和碳酸钠同时存在时,少量稀盐酸先与氢氧化钠反应,也无明显现象
[得出结论] Ⅱ Na+、Cl-、Ca2+、H+
[猜想与假设] 氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳发生反应生成了碳酸钠和水,化学方程式为2NaOH+CO2Na2CO3+H2O。[设计并进行实验] 猜想Ⅲ是全部变质为碳酸钠,氯化钙与碳酸钠反应生成碳酸钙白色沉淀,故现象为产生白色沉淀。[分析讨论] ②如果样品中含有氢氧化钠,则盐酸应该先和氢氧化钠反应,再和碳酸钠反应。[得出结论] 向溶液中加入无色酚酞,溶液变红,说明溶液呈碱性;滴加几滴稀盐酸,无明显现象,故含有氢氧化钠;加入氯化钙产生白色沉淀,说明含有碳酸根离子,因此两种固体同时存在。加入稀盐酸后得到无色澄清溶液,说明此时的溶液为中性或酸性,白色碳酸钙沉淀与稀盐酸反应生成氯化钙、水和二氧化碳,此时溶液中最多含有Na+、Cl-、Ca2+、H+四种离子。
化学
8.2 常见的酸和碱
第4课时 碱溶液的化学性质
小明同学以NaOH溶液为例用图甲总结了碱溶液的四条化学性质(即NaOH能够与四类物质发生化学变化)。
(1)为了验证反应①,小明将无色酚酞溶液滴入NaOH溶液中,溶液变成 色。
(2)依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为 。
(3)小明用微观示意图(如图乙)来说明反应③的发生,其化学方程式为 。从该图中可以看出,反应后的溶液pH (填“>”“<”或“=”)7。
(4)为了验证反应④能够发生,你选择的物质是 (填字母),该反应的现象是 ,化学方程式为 。
A.Na2CO3 B.HCl C.CuSO4 D.NaCl
[核心知识] 碱溶液具有一些相似的化学性质:
(1)碱溶液能使紫色石蕊溶液变蓝,使无色酚酞溶液变红。
(2)碱溶液能和某些非金属氧化物反应生成盐和水。
(3)碱溶液能和某些盐溶液反应生成新碱和新盐。
[易错点拨]
1.只有碱溶液才具备相似的化学性质,难溶性的碱不具备。
2. 碱与盐的反应中两种反应物都必须可溶。
1.某无色溶液具有如下性质:能使无色酚酞溶液变红;能与CuSO4溶液反应产生蓝色沉淀;能与Na2CO3溶液反应产生白色沉淀。此溶液是 ( )
A.氢氧化钠溶液 B.氯化钙溶液 C.澄清石灰水 D.盐酸
2.要鉴别常温下的氢氧化钠溶液与饱和氢氧化钙溶液,下列方法不能达到实验目的的是 ( )
A.分别通入二氧化碳 B.分别滴加碳酸钠溶液
C.分别滴加酚酞溶液 D.分别加热原溶液到60 ℃
3.下列物质反应后有蓝色沉淀生成的是 ( )
A.氧化铜和稀盐酸 B.氢氧化钡溶液和稀硫酸
C.硫酸铜溶液和氢氧化钠溶液 D.氯化铁溶液和氢氧化钠溶液
4.只用一种试剂就可以把盐酸、氢氧化钠溶液、澄清石灰水区分开,这种试剂是 ( )
A.氧化铜 B.石蕊溶液
C.碳酸钠溶液 D.氯化钡溶液
5.下列验证CO2与NaOH溶液反应的装置中,不能观察到明显现象的是(装置气密性均良好) ( )
6.某化学兴趣小组在学习碱的化学性质时,进行了如图所示的实验。图甲、图乙实验两支试管中均充满二氧化碳,分别倒扣在相同体积的氢氧化钠溶液和水中。
(1)图甲实验的目的是探究二氧化碳与氢氧化钠溶液确实发生了化学反应,观察到试管内的液面上升,原因是 ;写出该反应的化学方程式: 。有同学认为只凭图甲实验不能证明二氧化碳与氢氧化钠溶液发生了化学反应,于是设计了图乙实验,通过比较 ,说明二氧化碳与氢氧化钠溶液发生了化学反应。
(2)图丙实验中的现象为 ,写出该反应的化学方程式: 。
(3)氢氧化钠溶液与氯化铁溶液也能发生化学反应,写出该反应的化学方程式: 。
7.化学反应过程中常常伴随产生一些现象,同学们发现将CO2通入NaOH溶液时没有明显的现象发生,为了进一步验证CO2与NaOH溶液确实发生了反应,小红设计了如下方案:分别取通入CO2后的NaOH溶液于A、B两支试管中(如图所示),向试管A中滴加足量的稀盐酸,观察到的现象是 ,反应的化学方程式为 ;向试管B中滴加氯化钡溶液,观察到的现象是 ,反应的化学方程式为 。虽然实验的现象不同,但都能证明CO2与NaOH溶液确实发生了化学反应。
8.A~H是初中化学常见的物质,其中E为黑色固体,H为蓝色沉淀,这些物质的转化关系如图 所示,其中部分生成物和反应条件已省略。
(1)写出下列物质的化学式: G ,H 。
(2)化学反应常伴有能量变化,物质B与水反应时会 (填“吸收”或“放出”)热量,写出D的用途: (一条即可)。
(3)写出D→F的化学方程式: 。
9.[2021·达州改编] 达州市九年级学生在5月份进行了实验操作考试,某实验室的老师准备实验药品时发现一瓶氢氧化钠固体未盖瓶塞。对于该固体是否变质,老师让三位同学通过实验来探究。
[提出问题] 氢氧化钠是否变质 变质程度如何
[猜想与假设]
猜想Ⅰ:没有变质,全部是NaOH;
猜想Ⅱ:部分变质,固体是NaOH和Na2CO3;
猜想Ⅲ:全部变质,全部是Na2CO3。
氢氧化钠变质的原因是 (用化学方程式表示)。
[设计并进行实验] 取一定量的固体溶于水配制成溶液,分成三份,三位同学按照自己的方案进行以下实验:
实验操作 实验现象 实验结论
小李 向第一份溶液中加入无色酚酞溶液 溶液变红 猜想Ⅰ成立
小王 向第二份溶液中滴加几滴稀盐酸 无明显现象 猜想Ⅰ成立
小陈 向第三份溶液中加入CaCl2溶液 猜想Ⅲ成立
[分析讨论]
①小王和小陈认为碳酸钠溶液也能使无色酚酞溶液变红,因此小李的结论不正确。
②经过讨论他们认为通过小王的实验不能得出样品中一定不含Na2CO3的结论,原因是
。
[得出结论] 综合三位同学的实验操作和现象可以得出猜想 成立。
实验结束后大家将废液倒入同一个废液缸内,观察到废液呈红色,且有白色沉淀。他们向废液缸里加入一定量的稀盐酸后得到无色澄清溶液,所得溶液中溶质(酚酞除外)种类最多时,溶液中所含离子有 (填离子符号)。
答案
(1)红 (2)2NaOH+CO2 Na2CO3+H2O
(3)2NaOH+H2SO4Na2SO4+2H2O >
(4)C 有蓝色沉淀生成
2NaOH+CuSO4Na2SO4+Cu(OH)2↓
[应考能力提升练]
1.C 2.C 3.C
4.C 氧化铜只能溶于盐酸,与氢氧化钠和石灰水都不反应;盐酸能使石蕊溶液变红,氢氧化钠和石灰水都能使石蕊溶液变蓝;盐酸与碳酸钠反应产生气泡,氢氧化钠与碳酸钠不反应,石灰水与碳酸钠反应产生白色沉淀,可以区分三者;氯化钡与三者都不反应。
5.C 二氧化碳与氢氧化钠反应后,生成碳酸钠和水,A、B、D装置中的气压由于二氧化碳减少而减小。A中鸡蛋进入容器中;B中打开止水夹,烧瓶中导管有液体喷出; D中塑料瓶变瘪。C中气压不变,无现象。
6.(1)二氧化碳与氢氧化钠溶液发生化学反应,试管内的压强减小,在大气压的作用下液体被压入试管中
2NaOH+CO2Na2CO3+H2O 试管内液面上升的高度
(2)有蓝色沉淀产生,溶液由蓝色变为无色
2NaOH+CuSO4Cu(OH)2↓+Na2SO4
(3)3NaOH+FeCl3Fe(OH)3↓+3NaCl
7.有气泡产生 Na2CO3+2HCl2NaCl+H2O+CO2↑
有白色沉淀产生 Na2CO3+BaCl2BaCO3↓+2NaCl
氢氧化钠和二氧化碳反应后生成碳酸钠,碳酸钠能和盐酸反应生成二氧化碳气体,因此加入足量稀盐酸后会观察到有气泡产生;碳酸钠能和氯化钡反应生成碳酸钡白色沉淀,因此加入氯化钡溶液后会观察到有白色沉淀产生。
8.(1)CuSO4 Cu(OH)2
(2)放出 改良酸性土壤(合理即可)
(3)Ca(OH)2+Na2CO32NaOH+CaCO3↓
9.[猜想与假设] 2NaOH+CO2Na2CO3+H2O
[设计并进行实验] 产生白色沉淀
[分析讨论] ②当氢氧化钠和碳酸钠同时存在时,少量稀盐酸先与氢氧化钠反应,也无明显现象
[得出结论] Ⅱ Na+、Cl-、Ca2+、H+
[猜想与假设] 氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳发生反应生成了碳酸钠和水,化学方程式为2NaOH+CO2Na2CO3+H2O。[设计并进行实验] 猜想Ⅲ是全部变质为碳酸钠,氯化钙与碳酸钠反应生成碳酸钙白色沉淀,故现象为产生白色沉淀。[分析讨论] ②如果样品中含有氢氧化钠,则盐酸应该先和氢氧化钠反应,再和碳酸钠反应。[得出结论] 向溶液中加入无色酚酞,溶液变红,说明溶液呈碱性;滴加几滴稀盐酸,无明显现象,故含有氢氧化钠;加入氯化钙产生白色沉淀,说明含有碳酸根离子,因此两种固体同时存在。加入稀盐酸后得到无色澄清溶液,说明此时的溶液为中性或酸性,白色碳酸钙沉淀与稀盐酸反应生成氯化钙、水和二氧化碳,此时溶液中最多含有Na+、Cl-、Ca2+、H+四种离子。
