第12章 盐单元练习—2021-2022学年九年级化学京改版(2013)下册(word版 含答案)
文档属性
| 名称 | 第12章 盐单元练习—2021-2022学年九年级化学京改版(2013)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 86.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 00:00:00 | ||
图片预览


文档简介
第12章《盐》2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.蒸馒头、炸油条时常用到一种白色物质,它既能中和发酵过程中产生的酸,又能起发泡作用,这种物质是
A.NaOH B.NaHCO3 C.Ca(OH)2 D.NaCl
2.施用钾肥能增强农作物的抗倒伏能力。下列物质可用作钾肥的是
A.NH4HCO3 B.K2CO3 C.CO(NH2)2 D.Ca(H2PO4)2
3.下列物质的的俗称和化学式一致的是( )
A.NaCl ——盐 B.NaHCO3——苏打
C.NaOH——纯碱、烧碱 D.Ca(OH)2——消石灰、熟石灰
4.小玲家的水稻出现了倒伏现象,急需施用的化肥是( )
A.CO(NH2)2 B.Ca3(PO4)2 C.K2SO4 D.NH4Cl
5.2020年世界水日的主题是“水与气候变化”。下列关于水的说法正确的是
A.生活中硬水转化为软水的方法是煮沸
B.电解水实验中产生氢气和氧气的体积比为1:8
C.化合物之间有水生成的反应一定是复分解反应
D.过滤后的河水为纯净水
6.若利用碱的性质进行下列实验,不能达到相应目的的是
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
7.下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是
A.NaCl
B.NaOH
C.NaHCO3
D.Na2SO4
8.如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是
A.水、硝酸铵
B.水、烧碱
C.稀硫酸、铁粉
D.稀盐酸、小苏打
9.下列各组离子在水中能大量共存且形成无色溶液的是
A.Na+、、 B.H+、K+、
C.Cu2+、H+、 D.Cl-、、OH-
10.下列除杂方法正确的是
选项 物质(括号内为杂质) 方法
A K2CO3溶液(K2SO4) 加BaCl2溶液,过滤
B N2(O2) 将气体通过灼热的铜网
C NaOH溶液(Na2CO3) 加入稀硫酸
D ZnSO4溶液(CuSO4) 加入过量的铁粉,过滤
A.A B.B C.C D.D
二、简答题
11.化学与生活、生产密切相关。请用学过的化学知识解决下列问题:
(1)家庭中使用松花蛋时,为消除皮蛋中碱性物质的涩味,可加入厨房中的_____调味品使味道更加。
(2)人体胃液中含有适量的盐酸,在医学中可用碳酸氢钠中和胃酸过多症,是因为_____(用化学方程时表示),同时,医生建议患有胃溃疡的患者不宜过多服用。
(3)锅炉水垢会降低燃料利用率,某锅炉水垢的主要成分有CaCO3、Mg(OH)2等,用“酸洗”法可除去水垢
①“酸洗”时,一般不选用稀硫酸的原因是_____。
②写出稀盐酸与CaCO3反应化学方程式_____。
(4)为除去SO2气体污染火力发电厂常用石灰浆喷雾处理,写出该反应的化学方程式_____。
12.生活中处处有化学,请同学们用所学的化学知识来解决下列生活中的问题:
(1)小明同学晚餐后和妈妈一起清洗玻璃杯,他如何判断玻璃杯已经洗干净了?______
(2)写出一种用于治疗胃酸过多的药物中有效成分的化学式。______
(3)喝了冰镇汽水以后,常常会打嗝,这是什么原因?______
13.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性]
(1)以上操作中所发生的复分解反应共有________个。
(2)操作①、③、⑤要用到同一种玻璃仪器,请写出该仪器的名称和该仪器在操作⑤中的作用。
______________________________________
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象)
______________________________________
三、推断题
14.现有三种固体:铁粉、铜粉、Cu(OH)2。五种溶液:CuSO4,NaOH,FeSO4,,Na2SO4,稀硫酸。它们之间存在如下关系:
(1)A溶液+C溶液→固体甲+D溶液。
(2)固体乙+B溶液→E溶液+H2↑。
(3)固体甲+B溶液→C溶液+H2O。
试写出上述三个反应的化学方程式。
(1)_______;
(2)_______;
(3)_______。
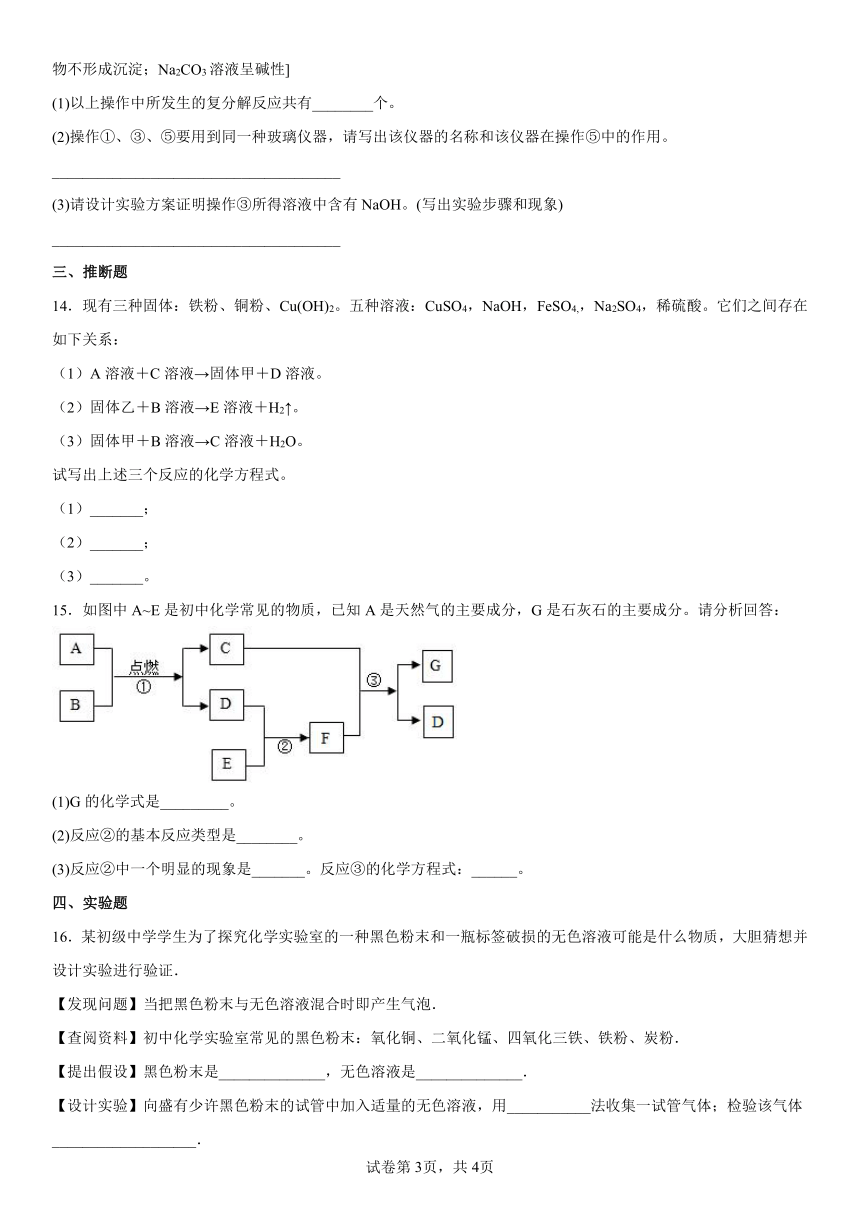
15.如图中A~E是初中化学常见的物质,已知A是天然气的主要成分,G是石灰石的主要成分。请分析回答:
(1)G的化学式是_________。
(2)反应②的基本反应类型是________。
(3)反应②中一个明显的现象是_______。反应③的化学方程式:______。
四、实验题
16.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
17.实验小组用下图装置进行实验。
已知:甲瓶中充满二氧化碳,乙中液体是水,实验前K关闭。
(1)将胶头滴管中的浓NaOH溶液挤入瓶中,振荡,该反应的化学方程式为___________。
(2)打开K,观察到乙中导管口有气泡冒出,原因是____________。
(3)将分液漏斗中的稀盐酸注入甲中,观察到乙中的现象是____________。
五、计算题
18.小明用某纯碱样品(含少量氯化钠)进行了下图所示的实验。请计算:
(1)生成二氧化碳的总重量为_____g。
(2)所用稀盐酸的溶质质量分数为___________。
19.纯碱(主要成分为碳酸钠)中常含有少量氯化钠。化学兴趣小组的同学为了测定实验室中某盐酸的溶质质量分数,称取了某品牌纯碱样品12g进行了以下实验:将样品置于烧杯中,取50g此稀盐酸分五次加入其中,测得的有关数据如下表所示。
第一次 第二次 第三次 第四次 第五次
加入稀盐酸质量/ 10 10 10 10 10
烧杯中剩余物的质量/ 20.9 29.8 47.6 57.6
试计算:
(1)表中a的值为______。
(2)实验中产生二氧化碳的总质量为______。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程,计算结果保留一位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.C
5.A
6.C
7.C
8.A
9.A
10.B
11. 食醋 NaHCO3+HCl═NaCl+H2O+CO2↑ 稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,会阻止反应的进行 CaCO3+2HCl═CaCl2+H2O+CO2↑ Ca(OH)2+SO2═CaSO3↓+H2O
12. 上面附着的水既不聚成水滴也不成股流下 Al(OH)3或Mg(OH)2或NaHCO3 气体的溶解度随温度和升高而减小,二氧化碳从汽水中散逸出来
13. 6 玻璃棒;搅拌,使液体受热均匀,防止液滴飞溅 取③所得溶液,加入足量的BaCl2溶液,静置,向上层清液中滴加无色酚酞溶液,溶液变红色,说明溶液中含有氢氧化钠
14.
15.(1)CaCO3
(2)化合反应
(3) 放出热量
16. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
17. 2NaOH+CO2====Na2CO3+H2O 甲中二氧化碳被消耗,压强减小,乙中气体进入甲,压强减小,空气进入乙 长玻璃管内液面上升
18.(1)4.4(2)7.3%
19.(1)38.7;(2)4.4g
(3)根据反应生成二氧化碳的质量,可求出稀盐酸中溶质的质量,根据溶质质量分数的计算公式计算稀盐酸中溶质的质量分数。
设参加反应的HCl的总质量为x。
x=7.3g
稀盐酸中溶质的质量分数为(其他解法合理即可)
答:所用稀盐酸中溶质的质量分数为。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.蒸馒头、炸油条时常用到一种白色物质,它既能中和发酵过程中产生的酸,又能起发泡作用,这种物质是
A.NaOH B.NaHCO3 C.Ca(OH)2 D.NaCl
2.施用钾肥能增强农作物的抗倒伏能力。下列物质可用作钾肥的是
A.NH4HCO3 B.K2CO3 C.CO(NH2)2 D.Ca(H2PO4)2
3.下列物质的的俗称和化学式一致的是( )
A.NaCl ——盐 B.NaHCO3——苏打
C.NaOH——纯碱、烧碱 D.Ca(OH)2——消石灰、熟石灰
4.小玲家的水稻出现了倒伏现象,急需施用的化肥是( )
A.CO(NH2)2 B.Ca3(PO4)2 C.K2SO4 D.NH4Cl
5.2020年世界水日的主题是“水与气候变化”。下列关于水的说法正确的是
A.生活中硬水转化为软水的方法是煮沸
B.电解水实验中产生氢气和氧气的体积比为1:8
C.化合物之间有水生成的反应一定是复分解反应
D.过滤后的河水为纯净水
6.若利用碱的性质进行下列实验,不能达到相应目的的是
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
7.下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是
A.NaCl
B.NaOH
C.NaHCO3
D.Na2SO4
8.如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是
A.水、硝酸铵
B.水、烧碱
C.稀硫酸、铁粉
D.稀盐酸、小苏打
9.下列各组离子在水中能大量共存且形成无色溶液的是
A.Na+、、 B.H+、K+、
C.Cu2+、H+、 D.Cl-、、OH-
10.下列除杂方法正确的是
选项 物质(括号内为杂质) 方法
A K2CO3溶液(K2SO4) 加BaCl2溶液,过滤
B N2(O2) 将气体通过灼热的铜网
C NaOH溶液(Na2CO3) 加入稀硫酸
D ZnSO4溶液(CuSO4) 加入过量的铁粉,过滤
A.A B.B C.C D.D
二、简答题
11.化学与生活、生产密切相关。请用学过的化学知识解决下列问题:
(1)家庭中使用松花蛋时,为消除皮蛋中碱性物质的涩味,可加入厨房中的_____调味品使味道更加。
(2)人体胃液中含有适量的盐酸,在医学中可用碳酸氢钠中和胃酸过多症,是因为_____(用化学方程时表示),同时,医生建议患有胃溃疡的患者不宜过多服用。
(3)锅炉水垢会降低燃料利用率,某锅炉水垢的主要成分有CaCO3、Mg(OH)2等,用“酸洗”法可除去水垢
①“酸洗”时,一般不选用稀硫酸的原因是_____。
②写出稀盐酸与CaCO3反应化学方程式_____。
(4)为除去SO2气体污染火力发电厂常用石灰浆喷雾处理,写出该反应的化学方程式_____。
12.生活中处处有化学,请同学们用所学的化学知识来解决下列生活中的问题:
(1)小明同学晚餐后和妈妈一起清洗玻璃杯,他如何判断玻璃杯已经洗干净了?______
(2)写出一种用于治疗胃酸过多的药物中有效成分的化学式。______
(3)喝了冰镇汽水以后,常常会打嗝,这是什么原因?______
13.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性]
(1)以上操作中所发生的复分解反应共有________个。
(2)操作①、③、⑤要用到同一种玻璃仪器,请写出该仪器的名称和该仪器在操作⑤中的作用。
______________________________________
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象)
______________________________________
三、推断题
14.现有三种固体:铁粉、铜粉、Cu(OH)2。五种溶液:CuSO4,NaOH,FeSO4,,Na2SO4,稀硫酸。它们之间存在如下关系:
(1)A溶液+C溶液→固体甲+D溶液。
(2)固体乙+B溶液→E溶液+H2↑。
(3)固体甲+B溶液→C溶液+H2O。
试写出上述三个反应的化学方程式。
(1)_______;
(2)_______;
(3)_______。
15.如图中A~E是初中化学常见的物质,已知A是天然气的主要成分,G是石灰石的主要成分。请分析回答:
(1)G的化学式是_________。
(2)反应②的基本反应类型是________。
(3)反应②中一个明显的现象是_______。反应③的化学方程式:______。
四、实验题
16.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
17.实验小组用下图装置进行实验。
已知:甲瓶中充满二氧化碳,乙中液体是水,实验前K关闭。
(1)将胶头滴管中的浓NaOH溶液挤入瓶中,振荡,该反应的化学方程式为___________。
(2)打开K,观察到乙中导管口有气泡冒出,原因是____________。
(3)将分液漏斗中的稀盐酸注入甲中,观察到乙中的现象是____________。
五、计算题
18.小明用某纯碱样品(含少量氯化钠)进行了下图所示的实验。请计算:
(1)生成二氧化碳的总重量为_____g。
(2)所用稀盐酸的溶质质量分数为___________。
19.纯碱(主要成分为碳酸钠)中常含有少量氯化钠。化学兴趣小组的同学为了测定实验室中某盐酸的溶质质量分数,称取了某品牌纯碱样品12g进行了以下实验:将样品置于烧杯中,取50g此稀盐酸分五次加入其中,测得的有关数据如下表所示。
第一次 第二次 第三次 第四次 第五次
加入稀盐酸质量/ 10 10 10 10 10
烧杯中剩余物的质量/ 20.9 29.8 47.6 57.6
试计算:
(1)表中a的值为______。
(2)实验中产生二氧化碳的总质量为______。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程,计算结果保留一位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.C
5.A
6.C
7.C
8.A
9.A
10.B
11. 食醋 NaHCO3+HCl═NaCl+H2O+CO2↑ 稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,会阻止反应的进行 CaCO3+2HCl═CaCl2+H2O+CO2↑ Ca(OH)2+SO2═CaSO3↓+H2O
12. 上面附着的水既不聚成水滴也不成股流下 Al(OH)3或Mg(OH)2或NaHCO3 气体的溶解度随温度和升高而减小,二氧化碳从汽水中散逸出来
13. 6 玻璃棒;搅拌,使液体受热均匀,防止液滴飞溅 取③所得溶液,加入足量的BaCl2溶液,静置,向上层清液中滴加无色酚酞溶液,溶液变红色,说明溶液中含有氢氧化钠
14.
15.(1)CaCO3
(2)化合反应
(3) 放出热量
16. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
17. 2NaOH+CO2====Na2CO3+H2O 甲中二氧化碳被消耗,压强减小,乙中气体进入甲,压强减小,空气进入乙 长玻璃管内液面上升
18.(1)4.4(2)7.3%
19.(1)38.7;(2)4.4g
(3)根据反应生成二氧化碳的质量,可求出稀盐酸中溶质的质量,根据溶质质量分数的计算公式计算稀盐酸中溶质的质量分数。
设参加反应的HCl的总质量为x。
x=7.3g
稀盐酸中溶质的质量分数为(其他解法合理即可)
答:所用稀盐酸中溶质的质量分数为。
答案第1页,共2页
答案第1页,共2页
